目前研究人员开发了两种新的给药策略,通过改变药物的药代动力学特性实现其组织分布的优化。第一种是被动靶向递送,采用纳微颗粒或强亲水性高分子作为运载工具,借助此类大尺寸分子特有的EPR效应,将包埋或吸附的化疗药物运输至具有特殊血管结构的肿瘤部位;第二种是主动靶向递送,以肿瘤组织中过度表达的受体作为靶点,将特异性识别并结合受体的配体作为弹头与药物共价结合,到达肿瘤部位后经过肿瘤微环境激活,重新释放药物恢复其生物活性(即“前药”策略)。与第一种方法相比,“前药”策略不仅能够将药物精准递送至肿瘤部位,并且在递送过程中借助配体的稳定偶联结构有效掩盖或限制药物活性,具有生物安全性更高、非靶点部位释放量较低和非药理成分含量较少等优势。其中最令人瞩目的是将主动靶向性的弹头(抗体或靶向肽)与高细胞毒性药物共价偶联得到的高特异性肿瘤杀伤药物,即抗体偶联药物(Antibody-drug Conjugate, ADC) 和 多 肽 偶 联 药 物(Peptide-drug Conjugate, PDC)
截至2020年5月,已有Trodelvy等8款ADC药物获得美国FDA批准用于三阴性乳腺癌、复发或难治性淋巴瘤等多种临床棘手肿瘤的治疗,其中 Kadcyla, Adcetris已于2019年成功跻身“重磅炸弹”行列,在全球范围获得广泛认可。尽管如此,ADC 的发展之路仍是困难重重,而且这些障碍大多是由抗体大分子所固有的如下结构特征带来的:
(1) ADC的大分子体积(15~16 kDa)、肿瘤组织的高间质压和异常血管结构直接导致其肿瘤渗透性极低,每 克 肿 瘤 组 织 仅 能 聚 集 抗 体 注 射 剂 量 的 0.003%~0.08%,当肿瘤细胞内药物远未达到有效药理浓度时,ADC所负载毒素分子就已产生严重的系统毒性。因此,目前ADC药物适应症大多针对血液恶性肿瘤,对实体瘤的治疗效果不明显。
(2) ADC基于多种机制在非靶点部位被大量清除,不仅严重降低药效,更直接激发预期外的高毒副作用:一类是通过抗体Fc区与体内广泛表达的FcR受体(Fcγ和FcRn)非特异性结合,被网状内皮系统(RES)内化及消除,并在此过程中造成肝脏、脾脏和骨髓剂量限制性毒性;另一类则是高免疫原性抗体与其诱导产生的抗药物抗体ADA (Anti Drug Antibody)特异性结合亦触发RES消除;再则化学偶联的高效力细胞毒性分子在体内复杂血浆环境极易脱落,造成严重的脱靶毒性。
(3) 抗体大分子序列的复杂性和残基重复性,使现行ADC偶联策略缺乏反应选择性,获得的“异质性”产物,其药物载量及负载结构均不可控,对ADC的药代动力学、药效和安全性均造成不良影响,直接导致大量ADC临床研究的失败,乃至上市药品的撤市。
(4) 基于抗体分子的引入,ADC在药物分子外排泵的基础上,更激发了内化效率低、细胞周期蛋白沉默、下游信号通路激活和凋亡失调等更多耐药机制,进一步增加了治疗失败的机率。
而且,除上述问题外,制造困难和成本高昂亦是ADC应用中不可忽视的现实问题。出于对简单性、模块化、更好生物物理性质和生产便利性的需求,研究者们提出了利用同样具有肿瘤靶向性,但肿瘤渗透性更高、免疫原性更小的小分子多肽代替抗体大分子,通过与毒素分子共价结合形成新的偶联物PDC,有望从多个方面共同提高其靶向治疗效果。多项研究表明,相较于抗体大分子,靶向肽与毒素分子结合的优势主要体现在以下5个方面:
(1) 分子体积小(2~20 kDa),更容易穿透肿瘤基质,进入肿瘤细胞;
(2) 结合物无FcR途径、RES途径及ADA途径介导的非药理消除,有效提高药物利用率;
(3) 可原核表达或化学合成,生产过程简便且易于规模放大;
(4) 可与阿霉素、紫杉醇多种已获临床验证的细胞毒性分子偶联制备靶向制剂,无须局限于 ADC 领域中MMAE, DM-1 等极少数高毒候选品种,显著降低脱靶毒性影响,可极大地提高PDC制剂平台技术的可行性;
(5) 部分靶向肽可通过改变入胞机制克服肿瘤细胞的耐药性,实现耐药肿瘤的有效杀伤,打破传统化疗中普遍存在的耐药导致治疗无效的困境。
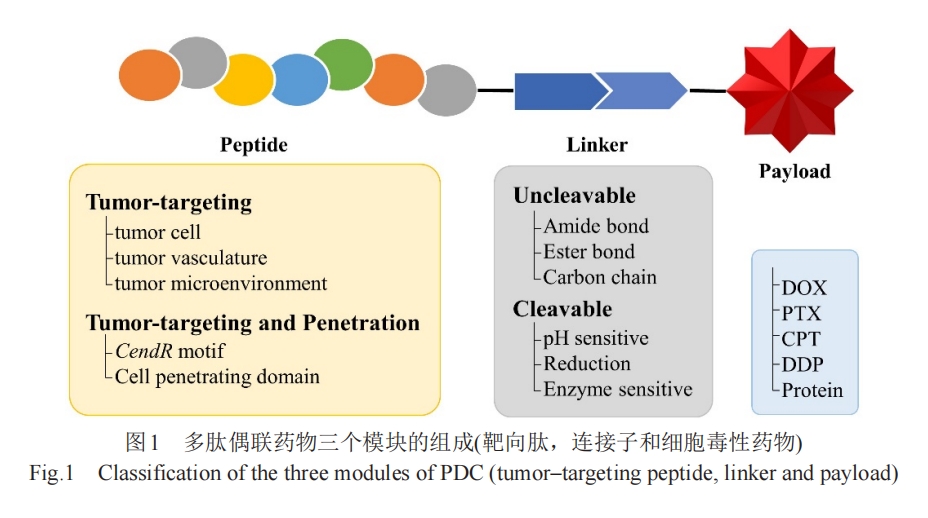
大量研究表明,肿瘤细胞和肿瘤血管内皮细胞表面的分子表达状态与正常细胞存在较大差别,使区分肿瘤组织与正常组织成为可能。研究者们采用噬菌体展示组合文库、OBOC (One-bead One-compound)组合文库和 PSSPCLs (Positional Scanning-synthetic PeptideCombinatorial Libraries)等技术获得大量靶向肽,以此为载体,通过化学连接与细胞毒素形成 PDC,利用这些肽特异性靶向肿瘤细胞,在肿瘤细胞或组织的特异生理环境中(如低pH、高表达蛋白酶、高还原性)释放出携载的抗癌药物分子。基于上述机制获得的受体靶向PDC在乳腺癌、前列腺癌、黑色素瘤等多种肿瘤模型中,均已表现出比未偶联多肽的游离化学药物分子更有效的肿瘤治疗效果。


肽库生物可依据客户要求,生产合成多肽序列,并评估偶联药物小分子化合物技术路线,目前已经为客户提供了阿霉素(DOX)、喜树碱(CPT)、紫杉醇(PTX)等等药物分子的偶联产物并提供原始数据及技术路线。

