质膜对于细胞信号转导尤为重要,许多具有治疗价值的蛋白质通常定位于这一区域。通过脂质介导的亲和力或蛋白质相关偶联实现的膜锚定,为有前景的亚细胞靶向提供了大量可能性。如上所述,肿瘤细胞中特定质膜过表达的蛋白质(如 NRP-1、EGFR、整合素 αvβ6 等)可通过配体-受体偶联成为极佳的靶点。然而,这种蛋白质相关偶联策略无法维持长期的细胞膜锚定效果,最终会导致细胞内吞。因此,脂质介导的细胞膜亲和力更适合基于亚细胞器的靶向和治疗。
C16-K(TPE)-GGGH-GFLGK-PEG8
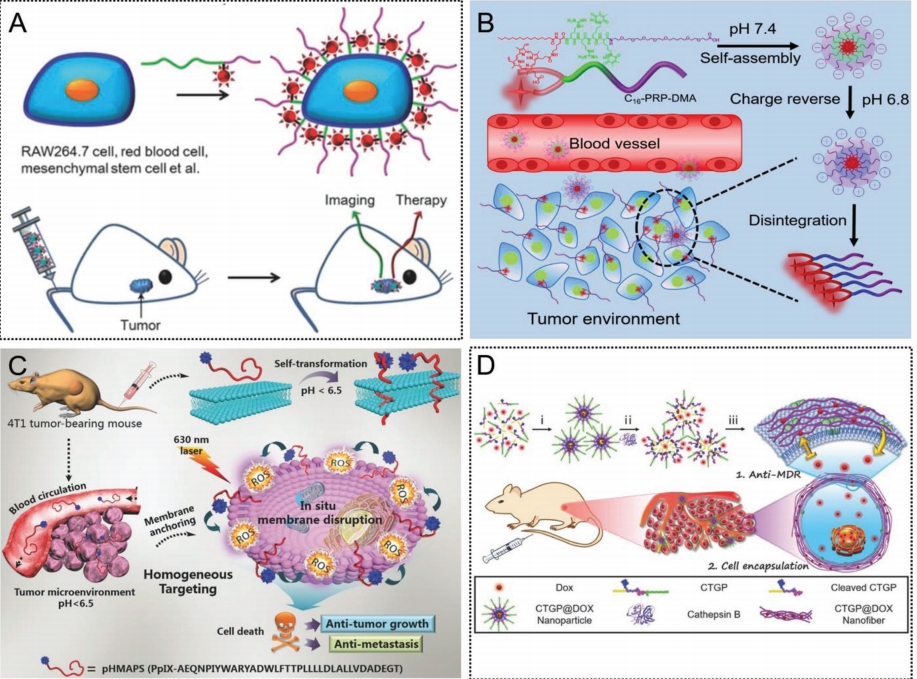
图 1. A) 两亲性肽用于肿瘤成像和治疗的多功能细胞膜靶向策略。B) 两亲性嵌合肽自组装纳米粒子用于酸激活解离、肿瘤细胞膜靶向和光动力治疗的示意图。C) pH 驱动的自转换膜锚定嵌合肽用于高效膜靶向和光动力治疗,具有出色的抗肿瘤和抗转移效果的示意图。D) 建议的组织蛋白酶 B 激活嵌合肽 CTGP 的细胞膜靶向、自组装和抗多药耐药机制示意图。
一般来说,脂质介导的细胞膜靶向是通过疏水烷基链或特定肽介导的膜插入来实现的。这种质膜工程方法具有许多优点,包括出色的膜靶向效果、长期的膜锚定能力、易于修饰、广泛应用于各种细胞的质膜以及良好的生物相容性和极小的副作用。鉴于这种有前景的方法,我们团队开发了一系列用于精准肿瘤治疗的质膜锚定方法。例如,构建了一种用于肿瘤靶向药物递送和接触细胞增强光动力治疗的多功能质膜工程细胞载体(称为“CONCEPT”),如图1A所示。该细胞载体是通过将多功能两亲性肽锚定在巨噬细胞膜上制备而成。两亲性肽由带正电荷的亲水肽序列Arg-Arg-Arg-Arg、疏水膜插入分子棕榈酸以及它们之间的Lys连接子组成,以便进一步修饰功能基团。由于带正电荷的四精氨酸肽与带负电荷的细胞膜之间的静电相互作用以及烷基链的膜插入功能,这些肽能够锚定在各种细胞表面。随后,这些肽被光敏剂原卟啉IX(PpIX)修饰,并进一步锚定在RAW264.7细胞表面,以实现精确的肿瘤靶向和增强的光动力治疗。这种接触细胞增强型光动力治疗策略首次被提出,作为肿瘤治疗的一个全新概念。基于此,我们继续研究细胞膜靶向策略,以最大限度地提高光动力治疗效果。如图1B所示,开发了一种新型电荷可逆自递送嵌合肽C16-PRP-DMA,用于长期细胞膜靶向光动力治疗。这种嵌合肽能够有效地、特异性地插入肿瘤细胞膜,并在超过14小时内保持长时间的锚定。一旦用630纳米的光照射,肿瘤细胞膜会因过量产生的活性氧(ROS)而直接被破坏,进而导致细胞坏死。随后,基于新发现的pH低插入肽(pHLIP),设计了一种自转换型pH驱动膜锚定光敏剂用于抗肿瘤和抗转移,如图1C所示。此外,还提出了一种通过设计可转换型细胞膜锚定嵌合肽的细胞封装策略来捕获肿瘤细胞并增强药物滞留,以克服肿瘤多药耐药性(图1D)。这种细胞封装策略将拓展细胞膜靶向的应用,并在生物医学领域展现出巨大的潜力。

电话:0551-65177703 邮箱:pb@peptidesbank.com 地址:安徽省合肥市四川路868号云谷创新园A6栋3层
合肥肽库生物(Taikubio)只为有资质的科研机构、医药企业基于科学研究或药证申报的用途提供医药研发服务, 不为任何个人或者非科研性质的、非用于药证申报使用等其他用途提供服务。