多重耐药菌的出现对全球公共卫生产生了直接影响,因为现有抗生素对病原体的效力降低。因此,迫切需要具有不同作用机制的新药来杀灭微生物。抗菌肽(AMPs)可以被视为实现这一目标的替代工具,因为它们已被证明具有广谱活性的治疗效果。将抗菌肽作为临床候选药物存在一些障碍,例如毒性、缺乏稳定性和生产所需的高昂成本。这可以通过开发更短且更容易获得的抗菌肽来克服,即所谓的短抗菌肽(SAMPs),其包含 2 至 10 个氨基酸残基。这些短抗菌肽正逐渐成为一类具有临床应用潜力和多功能活性的有吸引力的治疗剂。在这篇综述中,我们试图汇总那些已展现出被认为有望在未来取得成功的生物学特性的短抗菌肽。
本综述的重点在于展示多种较短的抗菌肽,它们对多种病原体具有广谱活性(表 1,来自 44 项研究的约 450 种生物活性短抗菌肽)。头到侧链环肽,如多粘菌素、达托霉素或泰斯巴汀,通常不被视为短抗菌肽,因此不在本综述的讨论范围内。最终,这一集合应成为研究人员识别肽并根据特定需求对其进行微调的平台。
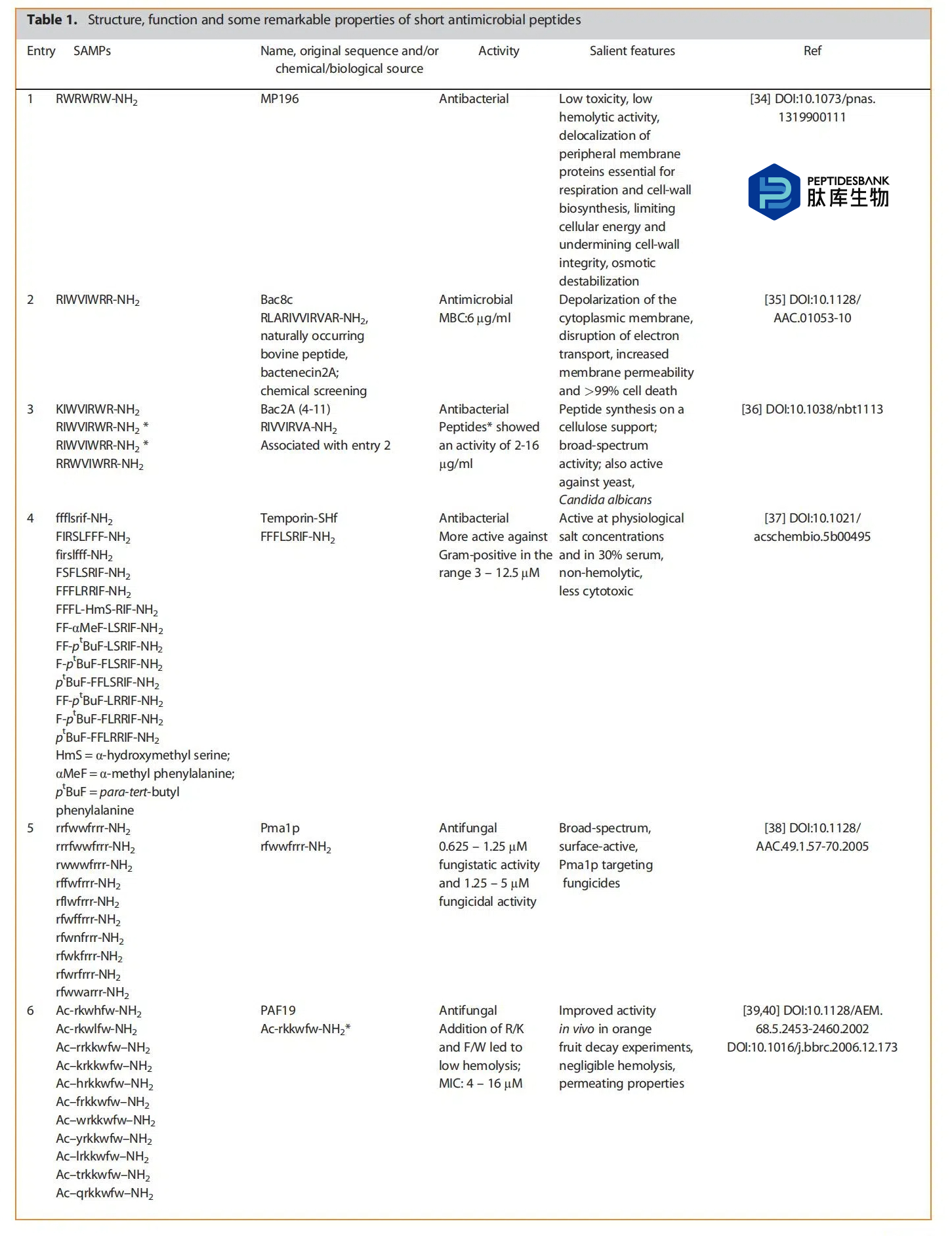
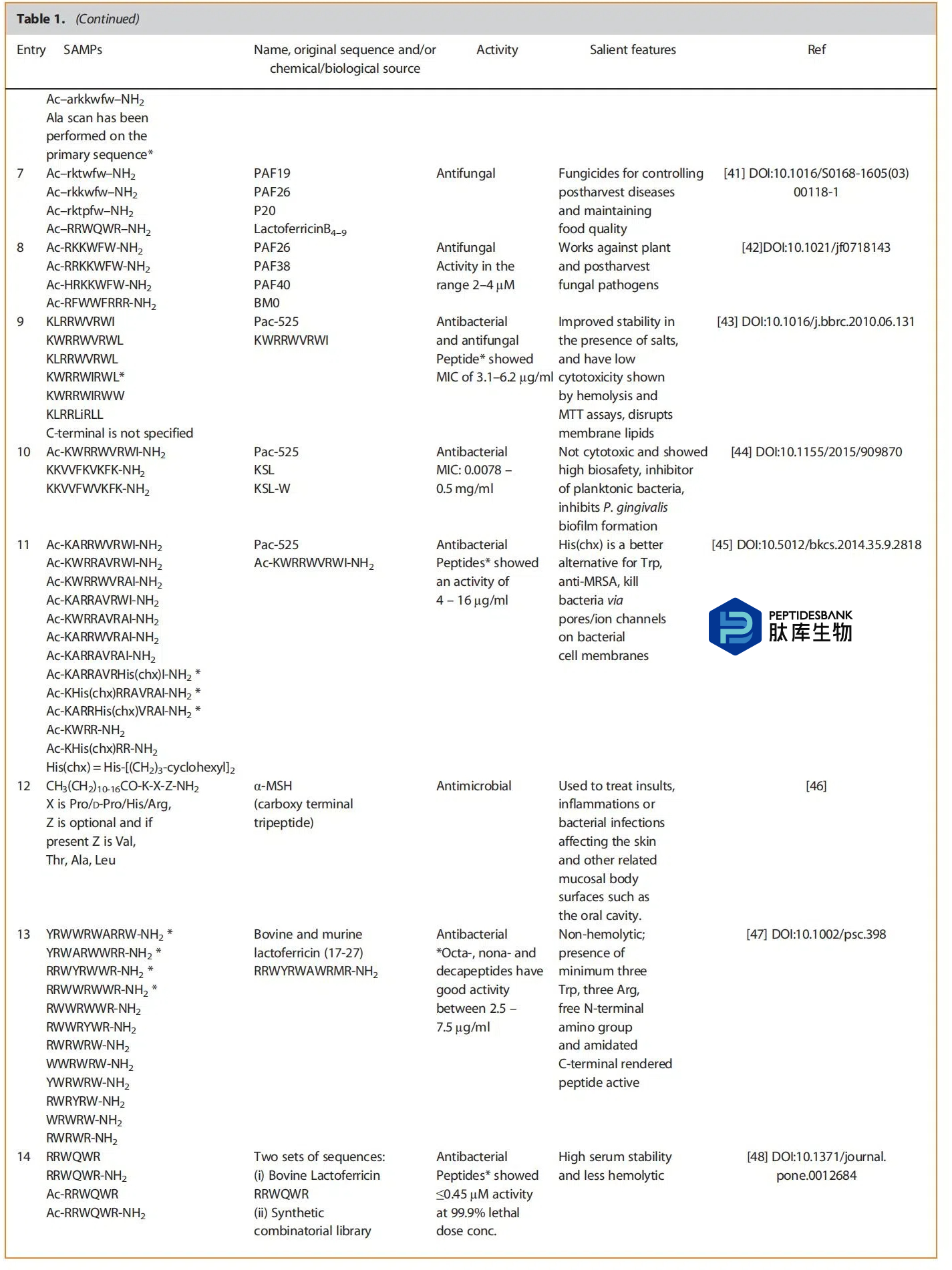
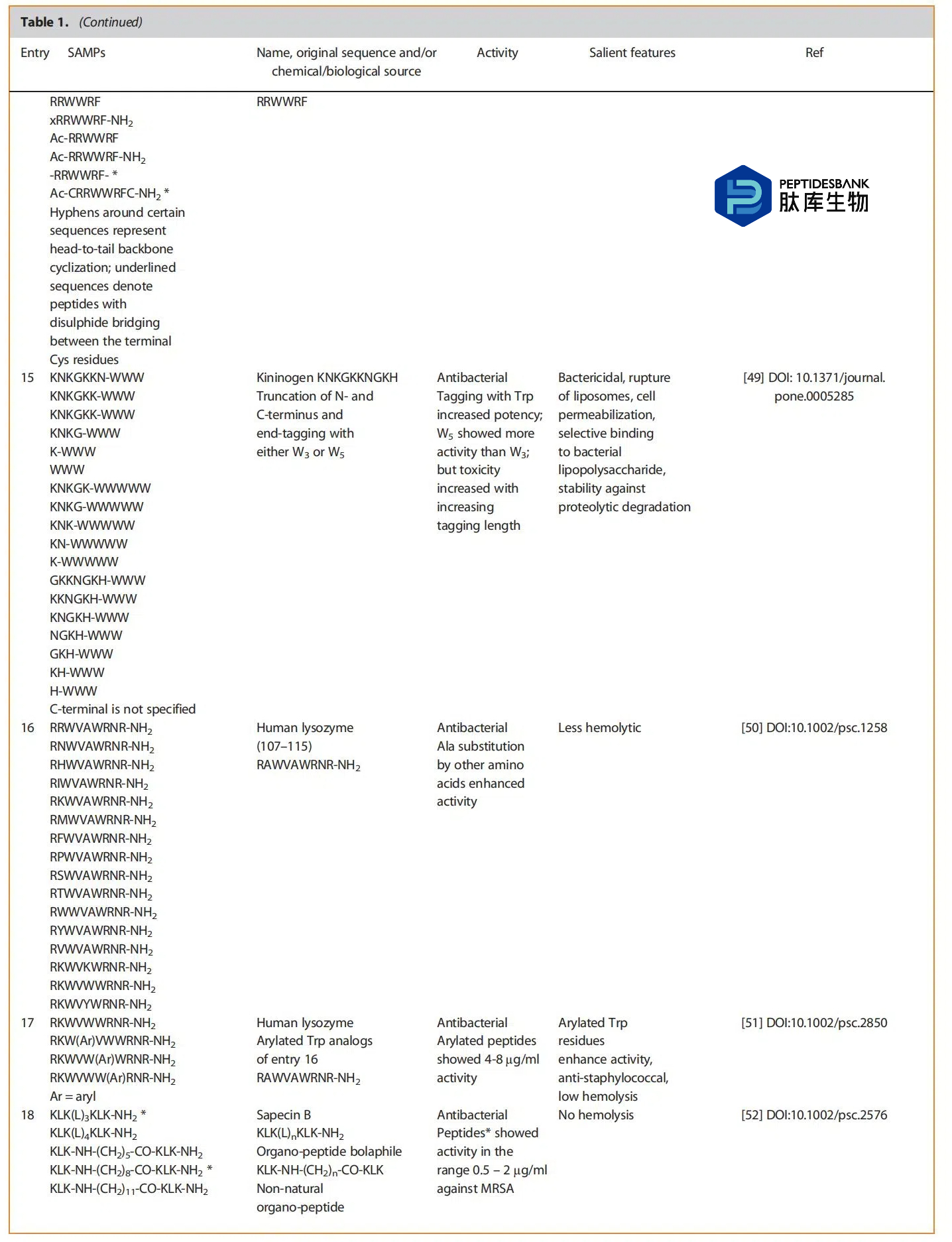
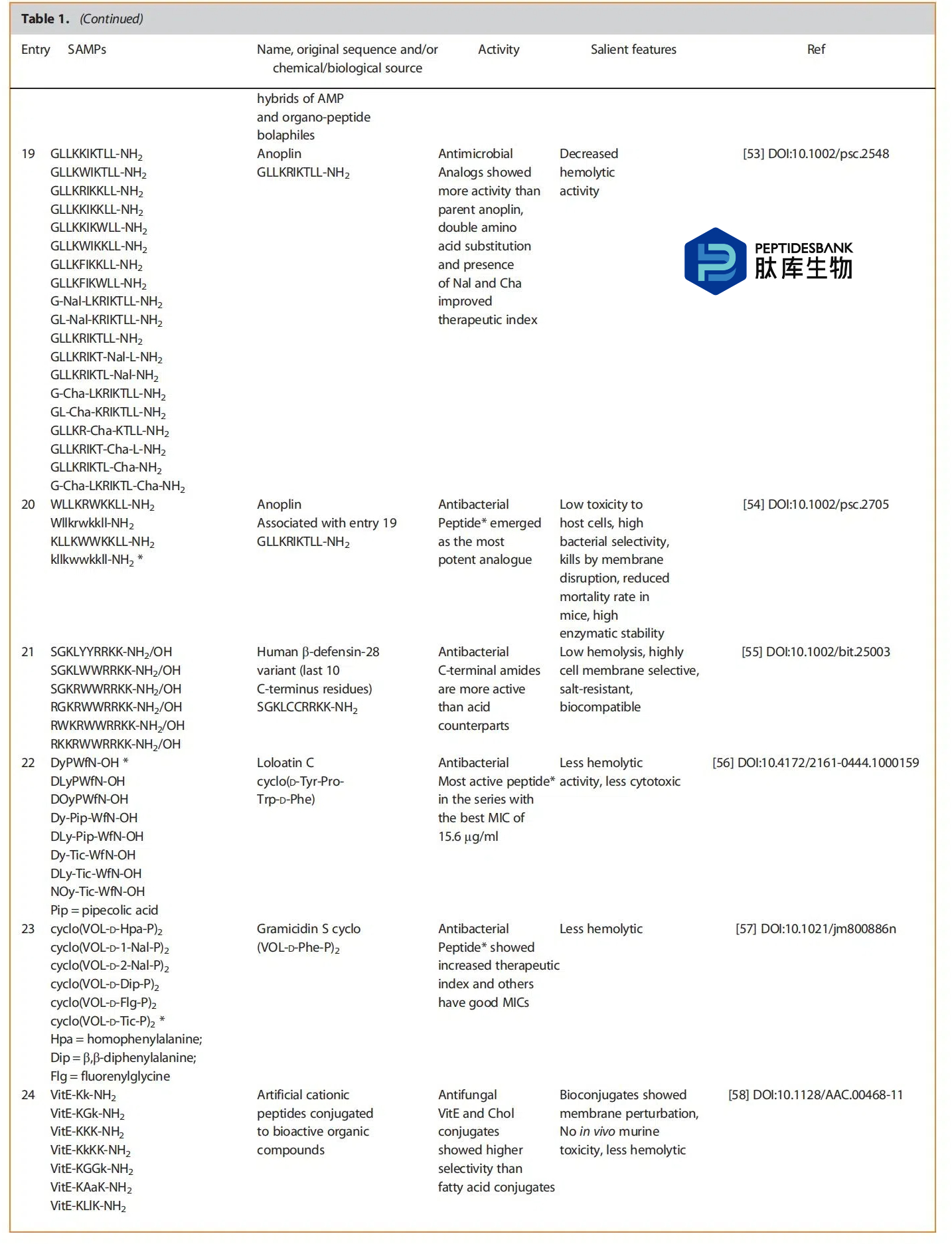

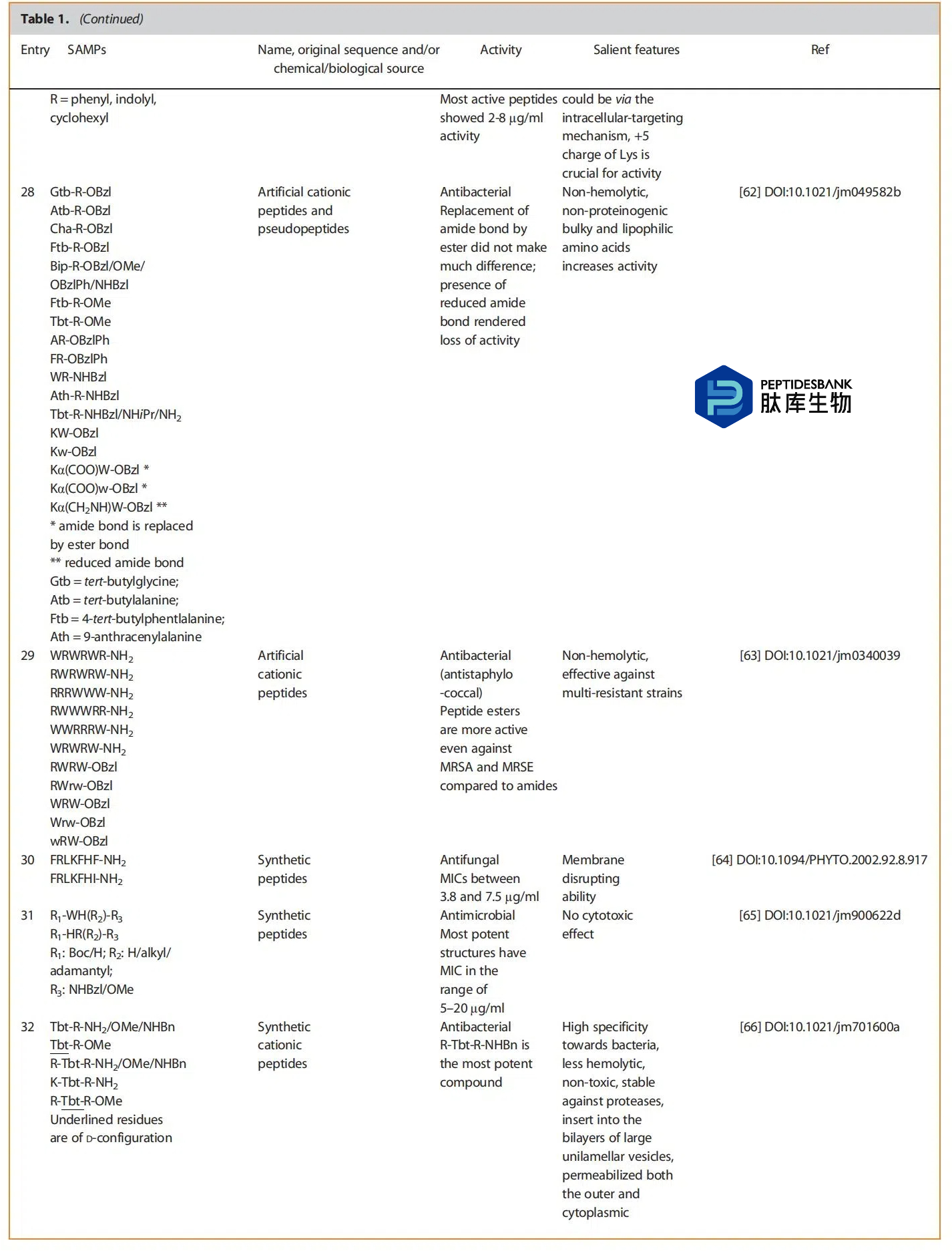
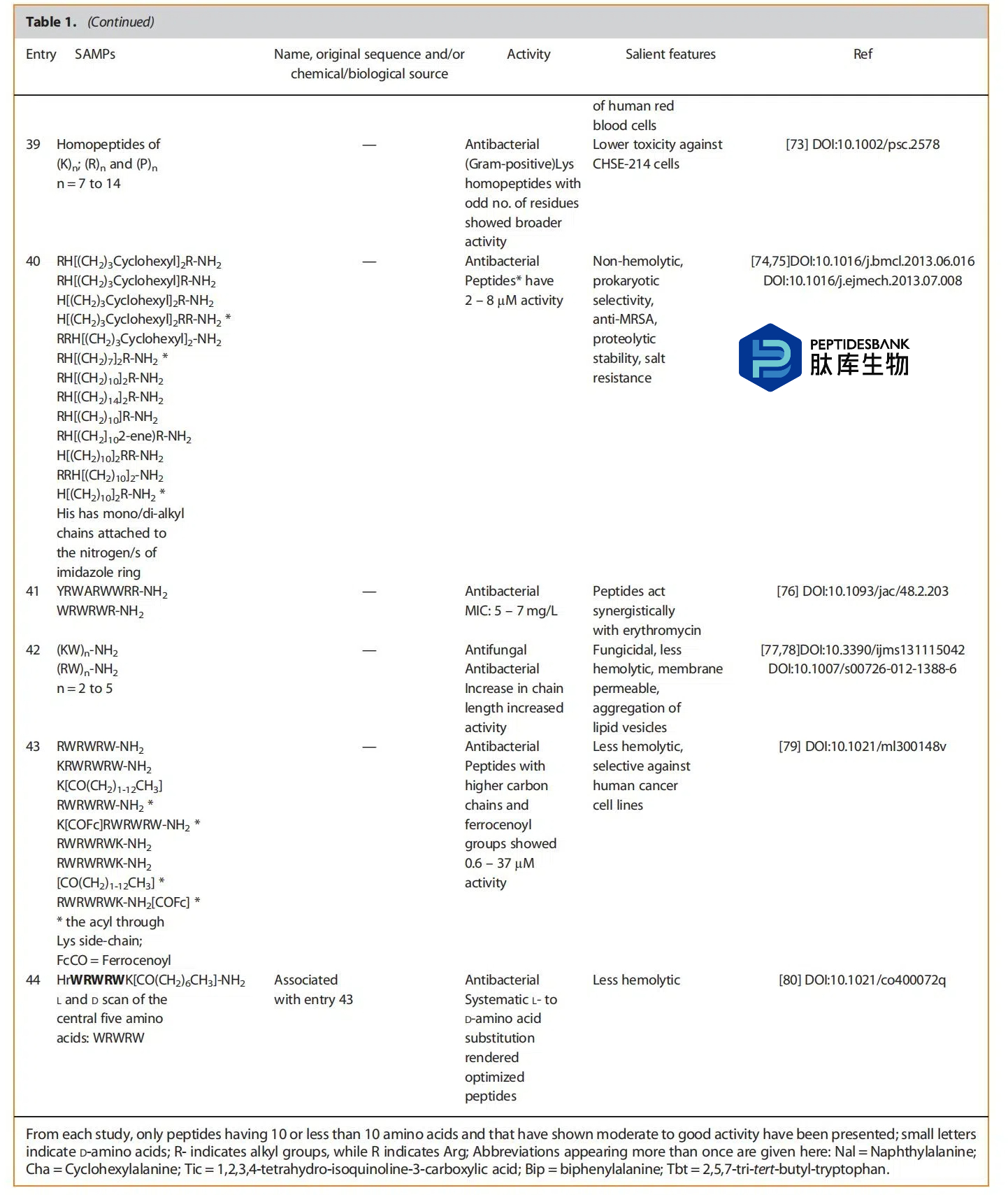
以上是汇总表,展示了来自四十多项研究中最活跃的肽类物质。该表分为几个子标题:(i)天然存在的肽(将属于相似家族的肽归为一组)――第1至22项,(ii)环肽――第23项,(iii)人工或合成肽,可能是天然肽的衍生物或任意设计或打乱的――第24至44项。在最后一类中,我们可以看到一些非蛋白质氨基酸、有机部分、金属等的存在。这表明肽类物质在与其他部分结合方面仍具有开放性,从而也能提高活性。有一些文章从文献中筛选出几种活性肽,并进一步研究它们作为针对不同靶点的治疗药物的潜力。似乎有些出版物是之前研究的延续部分或相关部分,这表明SAMPs是药物研发中作为先导化合物的热门分子。大多数肽在0.5至16微克/毫升或微摩尔的浓度范围内表现出活性,这是药物研发的一个先决条件。这些化合物将进入临床试验。这一数值非常有前景,这使得肽类药物的研发成为可能。一些研究表明,电荷数量的增加会提高活性。值得注意的是,某些氨基酸被色氨酸取代,这无疑提高了活性,但当色氨酸的数量增加时,又会表现出溶血性。因此,对色氨酸残基的数量进行微调和适当引入将是获得强效肽类药物的明智策略。上述部分对来自表格的肽类/序列/结构/活性/替代等进行了更深入的分析。
总的来说,一些SAMP是通过较长肽段的修饰获得的,例如乳铁蛋白肽(表1中的#13),而有些则是原始肽的修饰版本(表1中的#6、#9、#16、#42、#26),还有一些则是随意设计的(表1中的#18、#19、#22、#25、#27、#28、#29、#31、#34、#35、#39、#40、#41、#42)。上述所有策略的主要目的是获得具有强大生物活性的合适候选肽。一些SAMP的活性优于其亲本肽,这表明它们需要进一步优化。大多数肽都含有精氨酸、赖氨酸以及色氨酸等氨基酸(表1中的#2、#9、#13、#14、#27、#34、#38、#39等)。这表明碱性和芳香族氨基酸的存在有助于提高肽对革兰氏阴性菌膜的活性。上述部分肽(表1中的#4、#17、#29、#38、#39)对革兰氏阳性菌(包括葡萄球菌)的活性优于对革兰氏阴性菌的活性。因此,值得注意的是,#29、#38和#39是主要含色氨酸、精氨酸和赖氨酸的合成肽,对革兰氏阳性菌具有活性。另一项重要的改进包括引入了Nal,这是一种体积较大且非蛋白质生成的氨基酸(#19,23,表1),有助于提高肽在血清中的蛋白水解稳定性,同时还能增强耐盐性。这可被视为肽化学领域的一项进步。通常,母肽中的某些L-氨基酸会被替换为其D-异构体,例如在Temporin-SHf、Bac8c、cathelicidin等中(#4,20,28,29,37,44,表1)。这些观察结果表明,构型上的微小变化可能会影响分子相对于其靶点的特性。相反,在某些情况下,这种替换策略并未取得太多积极成果。另一种变化是在N-端、C-端或侧链处连接不同碳原子数的脂肪酸尾或烷基链(#12,33,34,40,表1),这进一步提高了此类修饰的SAMPs的生物活性。序列中存在一些重复单元或同聚肽,还观察到不同链长也会诱导活性增强(#1、4、5、15、18、19、20、33、35、38、36、39、41,表1)。此外,添加/结合某些有机基团,如Ac、Tbt、Ath、Gtb、Bip、Ind、Flg、Chx、Vit、Chol、Bz、Tic等(#4、11、20、22、23、24、25、28、29、32、40,表1),确实有助于提高治疗活性。上述大多数SAMPs具有抗菌和抗真菌作用,但无抗病毒作用,这为新发展带来了令人兴奋的挑战。一些SAMPs已显示出抗结核作用(#26,表1),这是该研究领域的一个里程碑。抗真菌SAMPs的一个共同特点是大多数肽都含有D-氨基酸(#5、6、7、24,表1),这有利于分子穿透真菌细胞壁。仅在一些任意的SAMPs中(#9、33、42,表1)观察到同时具有抗菌和抗真菌的特性。同样,仅有一个环肽(gramicidinS,#23,表1)源自SAMPs,这与大量环AMPs形成对比。这可能是由于合成困难和聚集所致。为该领域的更多研究铺平道路。据我们所知,这是上述SAMPs中带电荷最少的肽,这表明带电荷较少的肽也具有良好的活性特征。几乎所有SAMPs(无论是否含有天然或非天然氨基酸)都表现出比相应AMPs更低的细胞毒性和溶血性特征,这是将肽开发为候选药物的重要前提条件。在某些情况下,已表明肽的金属化(表1中的#38、43)会导致人类红细胞有限的溶解,这应作为设计新肽药物的一种新策略加以探索。一些SAMPs,如Pac-525、Anoplin、MP196等(表1中的#1、19、21、32),除了具有高度特异性外,还显示出能够渗透细菌膜(内膜和外膜)的能力。文献中已报道在AMPs中存在芳基化氨基酸。从这个意义上说,最近合成了含芳基化色氨酸的肽(表1中的#17),并显示出比其母体肽(非芳基化)具有更优的活性和更低的溶血性。这为该领域的进一步研究留出了空间。总的来说,天然肽和合成肽的活性之间没有明显区别,因为两者都展现出了令人鼓舞的结果。这为研究人员同时研究天然和合成版本的肽铺平了道路。上述大多数肽的C末端都进行了酰胺化处理,只有少数序列的C末端为羧酸。通常,C末端酰胺化的肽表现出更优的活性。
观点与未来展望
尽管抗菌肽(AMPs)展现出多种应用,但诸如毒性问题、蛋白酶稳定性以及高昂的生产成本等挑战,阻碍了其在生物活性应用方面的进一步发展。因此,为了推动该领域肽类研究的发展,人们采用了多种策略来促使微生物将短抗菌肽(SAMPs)视为“候选药物”。其中一种方法是识别天然长肽的较短活性类似物,这些类似物实际上具有与前者相同或更高的活性。例如:(i)对长序列进行定制的短版本;(ii)简单的修饰,如氨基酸替换或N/C端变化,或改变氨基酸构型;(iii)连接烷基/芳基/芳香基团;(iv)脂化;(v)包含大量碱性氨基酸,如赖氨酸、精氨酸、色氨酸,包括鸟氨酸;(vi)金属环肽;(vii)环状版本;(viii)引入非蛋白氨基酸,如Nal;(ix)芳基化残基等。所有这些策略都提高了SAMPs的活性。其中一些结构变化还导致了提高蛋白酶的稳定性、特异性和降低毒性,这些都是潜在药物进入市场所必需的。此外,较短的肽段在合成过程中具有快速扫描Ala/Trp/Lys的优势,以确定哪些氨基酸是必需的;对于较短的序列,这一过程比长序列要快得多。另一个值得一提的方面是,尽管抗菌肽在体外具有活性,但在动物模型中只有在非常高的剂量下才有效,这反映了不可接受的安全性余量,而短抗菌肽似乎已经克服了这一障碍,因为其活性得到了增强。此外,短抗菌肽还允许快速且经济高效地合成“反式”和“反式-反式”肽,即分别将L转换为D以及序列反转,这使它们成为制药领域的有吸引力的候选药物。结合这些优势,这些较短的类似物还可以通过微波技术生产,从而满足在“更短时间和更少浪费”的情况下对更高质量肽的需求,这是任何行业的底线。计算机技术也被用于设计和筛选具有抗菌作用的小肽。显然,有许多短肽具有广泛的应用前景,正处于不同阶段的临床试验中,有望用于药物开发。在大多数情况下,我们发现这些短肽是天然肽的衍生物。
参考文献:DOI 10.1002/psc.2894
免责声明:本文为行业交流学习,版权归原作者所有,如有侵权,可联系删除

电话:0551-65177703 邮箱:pb@peptidesbank.com 地址:安徽省合肥市四川路868号云谷创新园A6栋3层
合肥肽库生物(Taikubio)只为有资质的科研机构、医药企业基于科学研究或药证申报的用途提供医药研发服务, 不为任何个人或者非科研性质的、非用于药证申报使用等其他用途提供服务。