���������ѱ����Ľ��Խ�˷�֦�˾�����Ⱥ���л��ԵĿ����Ľ����������Է�����Ȼ����������Щ������ģ�ֻҪ���Ͽɵã�Ҳ�ʵ���������Էǽ�˷�֦�˾����꣨�����֦�˾��Ͱ��ڷ�֦�˾����Ļ�����������Ľ����˶������е���Ȼ�ͺϳɿ����ļ��仯ѧ�ṹ�������俹��֦�˾����Խ��������ۺ������Խṹ�뿹��֦�˾����Ե��������ʹ�����ܹ��ó���Ҫ���ۣ���Ϊ��Щ��ǰ���ķ��ӵ��о��Ϳ����ṩ˼·���Գ�ַ�����DZ�������ܱ�������Ҫ��ע�������ʣ������ǻ���Ҫ�ܽ���Ŀǰ���ú������з��ĸ���С����ҩ��Ľṹ��Ч������Щҩ�����ڽ�˲������ơ�
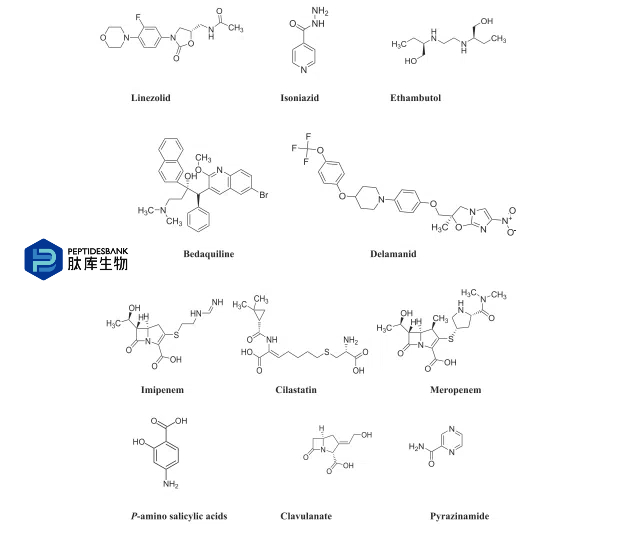
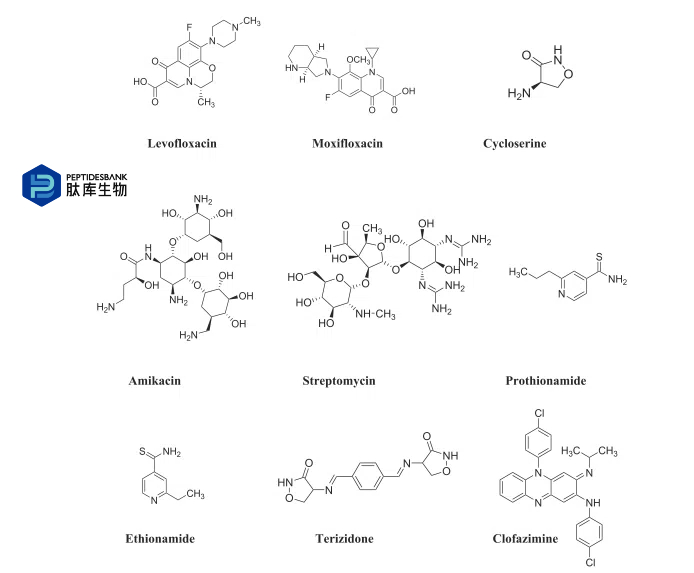
ͼ1 Ŀǰʹ�õĿ����ҩ��Ļ�ѧ�ṹ
2 | ��ҩ̽��������ҩ��
��Ѱ�Ҿ���DZ�ڿ���֦�˾����Ե�С���ӵĹ����У��о��ѷ��ּ��ֿ����ģ�AMPs����������������Ƭ�μ���Ƭ�Ρ� ������ͨ���̣ܶ����� 50 ��������л���������������Ҿ��������ԡ��������ǶԶ����������ֱ����Ѹ�ٵ�ɱ�����ã��Լ���������ҩ�ԵĿ����Խϵͣ����������Ϊ���Ϳ���֦�˾�ҩ�����������Ͷ�ҩ��˷�֦�˾����꣬���кܴ��ǰ�������ǿ���ͨ�����ֲ�ͬ�Ļ�������ϸ������������ϸ��Ĥ������ϸ��������ϳɡ����Ƶ����ʻ� RNA �ϳɣ�����ֱ����ϸ������á������Ŀ��Ե���ʹ�ã����������ͳ�Ļ���������ʹ�����ڽ�˲����ơ� ������Ȼ�ͺϳɿ����Ŀ���֦�˾����ԵĶ����о��ٽ��˶�DZ�ڿ���˲������ĵ�ʶ������⣨�� 3����
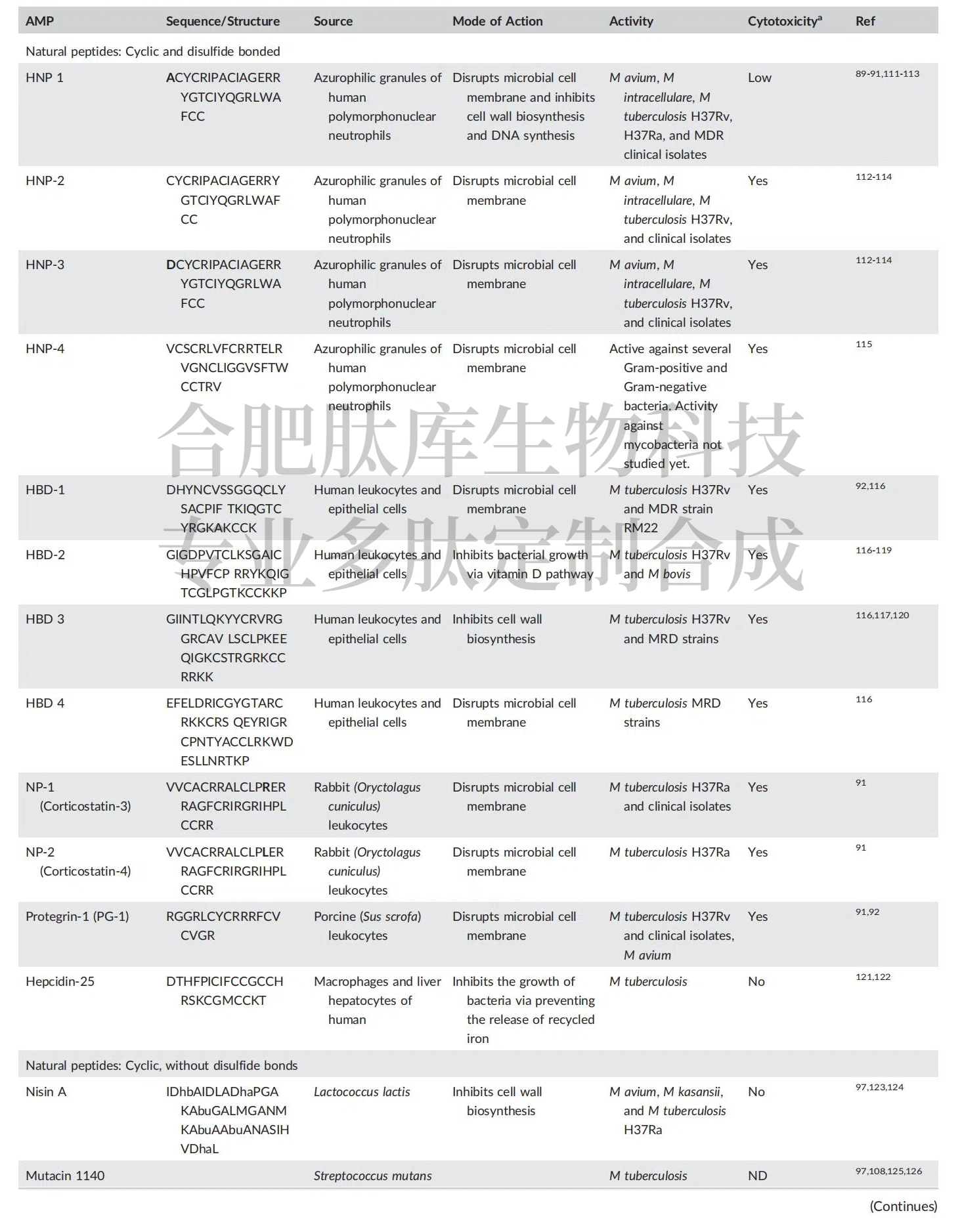
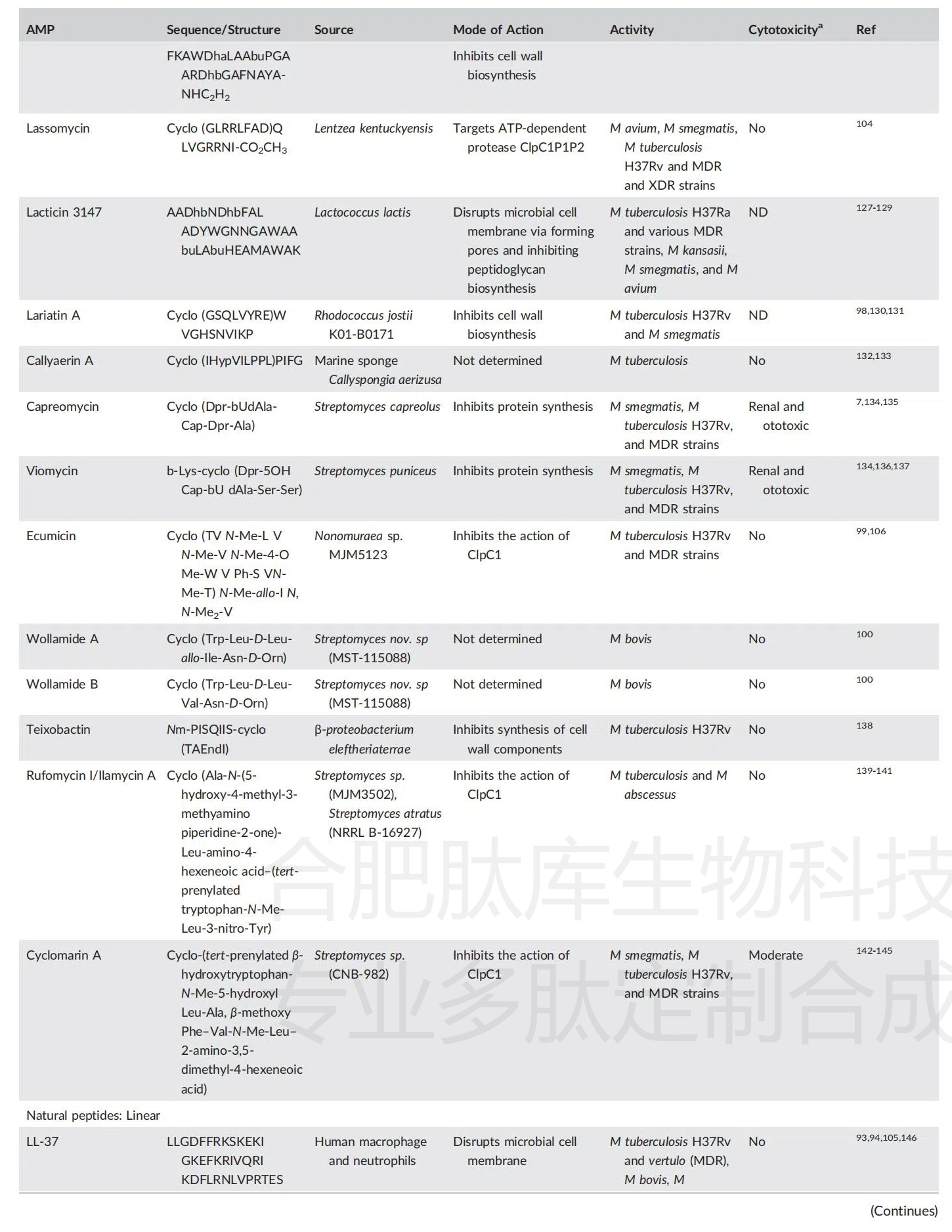
��3������֦�˾��ĺ���ģ��������
�������������Ը��ּ������簩֢����֢�Լ�ϸ���Ͳ�����Ⱦ�������ٴ����顣�ϳɵ�Ĥ�ѽ��� LTX-109 ���ڽ��������ͼ������ֽ��ɫ��������Dz���Ⱦ�� II ���ٴ����飬�� NZ2114��plectasin �������������� MRSA.171-173 ��ҩ�Ը�Ⱦ���ڵ�ȫ������ҩ��Ⱦ�����ٴ�ǰ������һ��ģ������ص��� PMX-30063 �Ѿ������������ʵ���У������ʶԶ��ָ��������Ծ����������Ծ������ֳ������Ŀ������ԣ�������һ���ٴ�������ϵͳ���������á�Ȼ�������ڶ��ԡ���Ч�����Լ��������ȶ��Բ��ԭ���������ٴ�������ȡ�õijɹ����ޡ����������������������ҩ�� pexiganan ����������������������ٴ�����������Ч���ѣ��봫ͳ���ŵͪ�������ȣ�������ֹ��RNA �������ҩ��ά��ù������Ϊ����ҩ�����ڽ�˲����ƣ������������Խ�С������ҩ�����ù����ȡ������������������֯�����ָ�ϣ����ڻ�������Ч�����ѣ�����ù��Ҳ���ٱ��Ƽ���Ϊ��˲�����ҩ�ʹ������ҩ�����Ҫ���������������ȶ��Բ��ˣ�ͨ����ѧ��������������������ģ�������������ҩ�ﻯѧ�о�����������
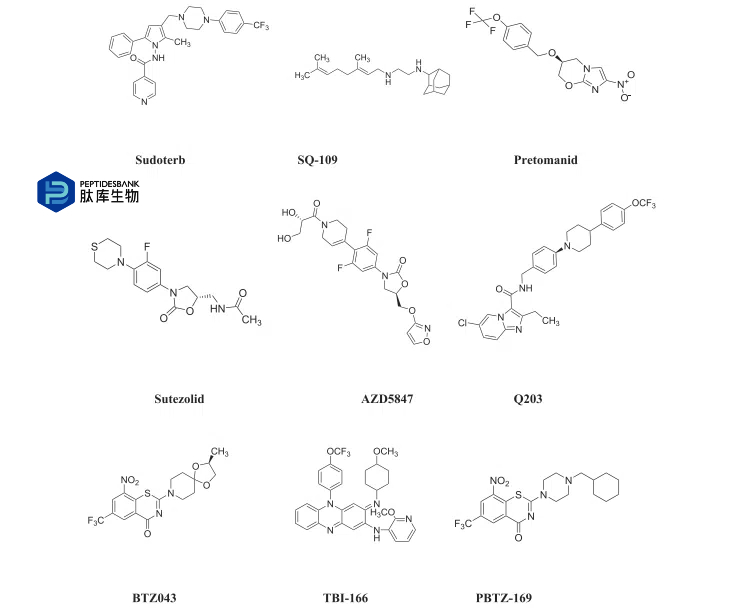
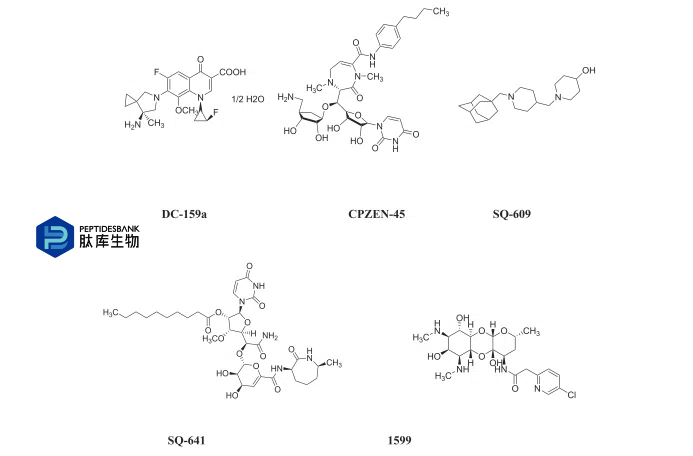
Ŀǰ�����ٴ�����εĽ�˲�ҩ��Ļ�ѧ�ṹ
�ڱ������У������ص��ע����DZ�ڿ���˻��Ե�����ͻ����ĵķ��ӡ���������ʾ������˻��Ե����࣬�������������ʱ��������Էǽ�˾���Ļ��ԡ����⣬������ͼ���ʵ������ݿ��õ�����£�̽������˻��������ఱ��������֮��Ĺ�ϵ������Ϊ��ƺͿ�������Ч�Ŀ�������ṩ֧�֡�
���¸��ڽ���ϸ������Щ�������ʵĿ���֦�˾����Ե����ʣ������ҳ���Щ�������ʵĽṹ���俹��˻���֮��Ĺ�ϵ��
2.1| ���ж��������Ȼ��
һЩ��Ȼ���ڵĿ���֦�˾��ĸ������װ���л�����Щ�л����γɷ����ڵĶ���������У���������������ϸ����HNP1-4���Լ�������������ϸ����NP-1��NP-2�ľ������ƵĽṹ���������������װ���л�������C1�CC6��C2�CC4��C3�CC5λ���γ������������C1�������еĵ�һ�����װ���л���C2:�ڶ�������ͼ3���������-�����أ�HBD1-4������36��50�������ᣬ���а����������װ���л�������λ��C1�CC5��C2�CC4��C3�CC5�γ������������ͼ3������HBD-1��λ�����γɵĶ������HNPs��ͬ����Щ�Ĵ�����ɣ�����Ƶ�ƽ����ˮ��ָ��Ҳ����������NP-1���⡣��ˮ��ָ�������ĵ������ˮ�Ի���ˮ�ԡ���ˮ��ָ��Խ����Խ�����ĵ���ˮ�Ծ�Խǿ��Kyte��Doolittle����
����Щ�������������ϸ���ĵĿ������Ե��о����������ǶԷ�֦�˾����ľ�����л��ԣ���С�־�Ũ�ȣ�MIC��ֵ��2.5��50��/����֮�䡣��������ͬ�·���NP-1����Ҫ�Ļ����ģ���50��/������Ũ���¿�����98.9%��������˷�֦�˾�H37Ra���ꡣNP-1�Ļ�������ΪHNP-1��PG-1��Np-2��HNP-2��ͬ�����Ķ�������ͬ�±�����HNP-1���ж����Ľ�˷�֦�˾�H37Rv����İ����������Ũ��(IC50)����С�־�Ũ�ȣ�MIC��ֵ�ֱ�Ϊ0.8��/������2.5��/���������ǻ�֤������48Сʱ�ڣ���40��/������HNP-1������Ⱦ�˽�˷�֦�˾�H37Rv��С��J744A����ϸ��ʱ��������98%��H37Rv��90HNP-1��J744A����ϸ��ϵ��ϸ������Ҳ�ϵ͡�ʹ�ø����ٴ���֦�˾������꣨������ҩ���꣩���о�������HNP-1��NP-1��PG-1��HBD-2��HBD-3��DZ�ڵĿ���֦�˾��ġ�Ȼ����HBDs��Ч������HNPs��PG-1��
���˽�˷�֦�˾��⣬��Щ����������ϸ���Ķ����֦�˾��Ͱ��ڷ�֦�˾�Ҳ���ֳ������Ŀ������ԡ���Ũ��Ϊ5.0��g/mLʱ�����������ȣ�HNP1-3�ܹ���������ϸ����������������⣬���о�����HNP1-3�Ŀ������Բ�������ϸ��������̬��ơ�þ���Ȼ��ƵĴ��ڡ�ͨ����HNP�Ŀ�����������ӵ���ˮ��֬�Գ�����ء�HNP-1��HNP-2��HNP-3����ˮ�����ֳ����ߵĿ���˻��ԡ����仰˵����HNP-1��ȥ��һ�������ᣬ���߽������ᵥ���滻Ϊ�춬��������3�����ఱ����仯�Դ���ͻ����ʾ�������ή���ĵĿ���˻��ԡ�
������HNP��ȣ�HNP-4�Լ��ָ��������Ծ��Ŀ������Խϵ͡�Ȼ����HNP-4�Է�֦�˾��Ļ�����δ�õ��о�������-�����Ǽ���ͬ�µ��о����������HNP-4ɱ�����ԽϵͿ�����������йأ��������Ӱ��ᡣ���⣬�б����ƣ���NP-1��NP-2�е�һ���������滻Ϊ������ή���俹��֦�˾����ԣ����������Ϊ����ɼ�����1����λ���������Ӱ��Ậ���뿹��֦�˾�����֮��ʸ���ص�ԭ���Բ���ȷ��
������HNP��ȣ�HNP-1�Է�֦�˾������ֱ��ֳ����ߵ�ɱ�����ԣ����������Щ�ĵ����÷�ʽ�йء�������ϸ��Ĥ��������Ҫ���ðе㣩����⣬HNP-1�����Ծ��緽ʽ��ϸ���Ķ�������DNA��ϣ��������Ҫ���ðе㡣Ȼ������HNP-1�ṹ���Ƶ�Դ�����ӵ�NP-1������1��Ϊ�ξ��и�ǿ��ɱ�����ԣ�ԭ���в������
����HNP�ṹ���Թ�ϵ���о���������Щ���еĶ�������俹������������Ҫ���á�κ����ͬ�·��֣�ʧȥ��������ƻ���-�����ص������ṹ����ʹ��Զ��ֲ�ԭ��Ļ���ɥʧ�����ܴ�����ս����ͨ���ֹ�����������Ĺ����ĺϳɷ������ѳɹ��ϳ��˺��������HNP�����ġ���������ɼ����ܵ��о�������HNP-1�Ŀ������Բ����������ض��Ķ����ģʽ���ܹ��������������Ϊ����һ������������������ﱻ���־�����ԭʼHNP-1���ƵĿ������ԡ�Ȼ����HNP-1�����������������ԡ��������ϼ���ͬ�·��֣�������-���нṹ������HNP-1�������Ծ��п������ԡ������γ����������Զ��������������ս�����ڹ�ȥ�����У���һ����ȡ����������չ��
2.2 | �������������Ȼ��
�������ϣ���E50-52�⣬�Ƕ�����ĵİ��װ���л����������ߡ�����E50-52�����������װ���л���������֮���δ�γɶ�����������еĴ�����Ķ�����������ɣ���HCL-2�����ԣ��Ϳ�������A����״�������ԣ����������������ԣ���ʸ���ɡ�ͨ������������ڿ���������������Ҫ���ã���Ϊ��Щ����ͨ�����Ŵ�����ɵ�ϸ��ϸ��Ĥ���������á�Ȼ�����¶����Ŀ���֦�˾����Կ�����ͨ������RNA�������ʻ�ϸ���ڵ�����ϳ���ʵ�ֵġ����Ƶأ��¶�����Ĥ�ܽ����Ҳ�������俹�������з�����Ҫ���á��¶����������ɵ�ϸ����֬����ã�ͨ��Zn(2+)�\dependent;���γɹѾ۸�����Ӷ���������ͨ���γɣ����Ĥȥ������ϸ��ϸ�����������⣬�¶����ڽ��ɫ���������û����ҩ�Է�չ�Ļ��ơ�����������ڸ��ĵ����������ʣ�ʹ���ܹ��ܿ�����ĵ����������ʵ���ҩ���ơ�������HCL-2�Ŀ������Ա���Ϊ����������ڵ�������ý鵼�ģ�����������A�����û����в������
�������������Ȼ�ĵĿ���˻��Լ���4���������IJ��ֽ��������ǵĿ���֦�˾����ԡ��ӱ�4���Կ�����ͨ������£�����������3147��lassomycin��lariatinA������ù�ء���ù�ء�ecumicin��wollamides��rufomycinI��������A��nisinA��I��ϸ���ؼ��壩����Խ�˷�֦�˾���ţ��֦�˾��ͳܹ���֦�˾��ľ�������У��俹��֦�˾��������������ģ���4�������ܱ�4�е����ݱ�������һ�㣬����Ҫע����ǣ����Dz�δֱ�ӽ���Щ�����������Ի���������бȽϣ���֮��Ȼ����Ȼ������ù�غ���ù������Ϊ���߿����ҩ�������������ҩ������ʹ�á�Ȼ������Щҩ���Ѳ�����Ϊ���߿����ҩ��ʹ�á�����Щ�ĶԽ�˷�֦�˾����Ե��ڶ��о����бȽϱ�����lariatinA��nisinA��mCRAMP��LL-37�����ԡ�ͬ�����������3147��nisinA�Խ�˷�֦�˾�H37Ra�Ļ��Ը���MIAP��
Ȼ��������nisinA�ľ���������ϸ�����ԣ�Ҫά����������ѪҺ�����Ʒ�֦�˾������Ũ���ľ���ս�ԡ����⣬����ù�غ�lassomycin�����֦�˾��Ļ��Ը���Ci-MAM-A24��PR-39��LL-37����wollamideA��B����ֳ����ѵĻ��ԡ���Ci-MAM-A24��LL-37��ȣ�����ţ��֦�˾������磨һ����������ļ���ţ��֦�˾����꣩���������ø�ǿ���෴��II��ϸ����E50-52�ѱ�֤���Խ�˷�֦�˾�H37Rv�Ļ��Դ���ecumicin��lassomycin��֬��II��Ͽ�����teixobactin����4������������һ����۲��������ڴ���Ҫָ�����ǣ��ڱȽϲ�ͬʵ���ұ�����������ظ�������������£�Ӧ�����Դ�����Ƚϡ�
2.3 | �ϳ���
��������֪�������б����ľ��п���֦�˾����Եĺϳ��ľ�Ϊ�����ģ�����2018�걨��������������������NZX���������ױ������ϳ��ĵĿ���֦�˾�DZ������ӡ����̣�������������õĻ��ԣ������ģ����ȶ��ԡ�ͨ�����������û��Եĺϳ��Ĵ�����ɣ����������ȶ������ã��䲻�ȶ���ָ��ֵ�ϵͣ�С��40��������Ȼ�IJ�ͬ����ȷ���ϳ��Ŀ���֦�˾����Ե��о������Ϊ��˷�֦�˾����꣬����ţ��֦�˾���ܹ���֦�˾���������ꡣ
�ںϳ����У�WKWLKKWIK��CP26��E2��E6�Խ�˷�֦�˾������൱�ߵĻ��ԣ�����С�־�Ũ�ȣ�MIC���ֱ�Ϊ1.45��2.1��2.6��3.2��g/mL����һ�����һ�����ܽ�������Щ�ĵİ�������ɣ�����Ramon-Garcia����ͬ��������ģ�������Ϊ���������������ᣨLys����ɫ���ᣨTrp�����Ӱ��ᣨVal���л�������֮����ڹ�����WKWLKKWIK���������ᣨ44.4%����ɫ���ᣨ33.3%���������Ӱ��ᣬ��CP26���������ᣨ26.9%������3.8%��ɫ�����7.7%���Ӱ�����ɡ�E2��E6����������л����������Ӱ��ᣬ�ֱ�Ϊ12.5%��25%��
���IDR-HH2��IDR-1018��D-5��pK-34�Խ�˷�֦�˾�H37Rv�Ļ��Խ������о�������IDR-1018����С�־�Ũ�ȣ�MIC��Ϊ16��g/mL����IDR-HH2��D-5��pK-34��MICֵ��30��50��g/mL֮�䣬Ӧ��Ϊ�еȻ��ԡ���D-LAK�ĵ��о������������ܹ������Ͷ�ҩ��MDR���㷺��ҩ��TDR���Ľ�˷�֦�˾����ꣻȻ�������ǵĻ�����������D-5����D-5����Ҳֻ���еȻ��ԣ�MICΪ30-50��g/mL��������б���һ�ָ������װ���ĺϳ���NZX�Խ�˷�֦�˾�H37Rv���ꡢǿ��������ٴ��Ͷ�ҩ�������MICֵΪ27.6��g/mL��NZX����Ȼ��plectasin��һ�����������NZX��438.4��g/mLŨ���¶�����ϸ���������Ҿ������õ������ȶ��ԣ���ʹ���Ϊ�Կ���˲�������������ǰ��������ҩ���ѡ�
2.4 | �����ĵķ���
�Ļ����Ӱ�������֬�ġ����ء����ġ����ĺ����ģ�ͼ4������Щ���ӵ�������������������Ҿ��ж��صĻ�ѧ�ṹ�����ױ�����ø���⣬����������пڷ��������öȡ�������ù��A��B��BB-3497�Լ��������peptoid-1����������1-C134mer��1-Pro9��1-11mer���ѱ�֤ʵ���²��Ժͷ��²��Է�֦�˾����п���֦�˾����ԡ�������������ϸ��ϸ��Ĥ������ù�غ�BB-3497����Է�֦�˾�������ϳ�;���������á���ù��ͨ������ATP��ø���������Ʒ�֦�˾�����������BB-3497��ͨ�����Ƶ����ʺϳɷ������á�
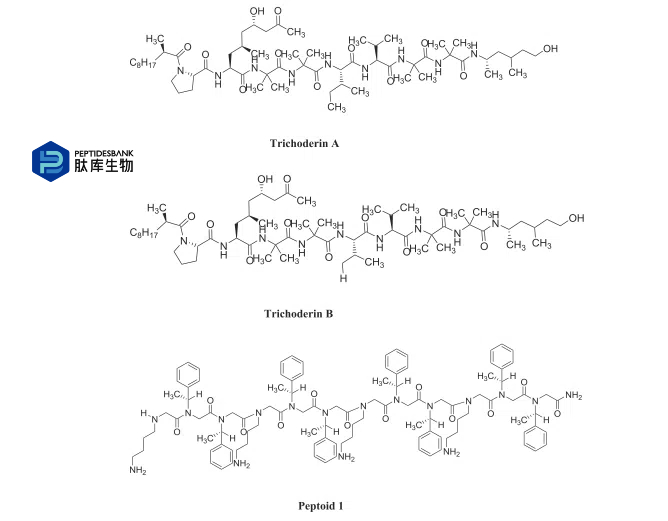
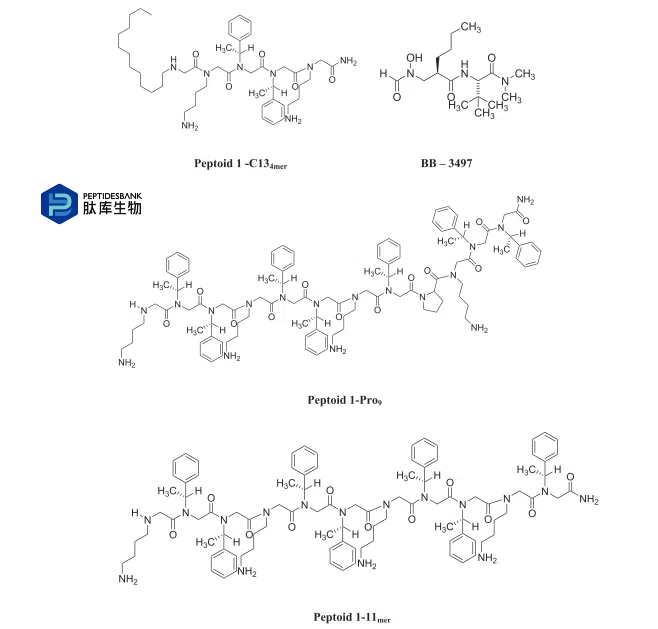
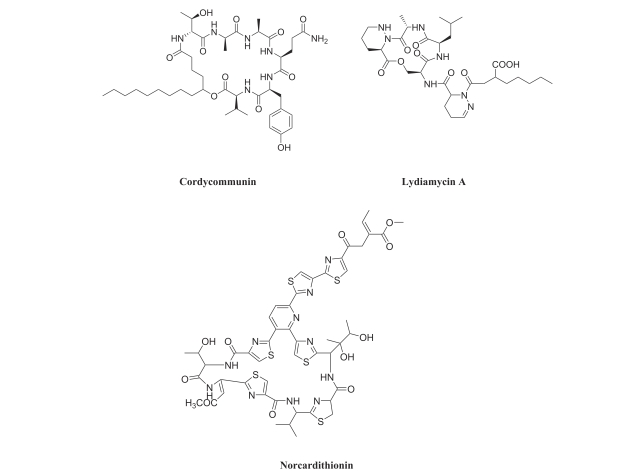
ͼ4 �����ĵķ��ӵĻ�ѧ�ṹ
ȥ������һ����Ȥ���������ʣ�������Ҫ������ѧ���ԣ��翹�����������Ϳ����ԡ���״ȥ���������ʡ����Ծ��غ�����ù��A�Խ�˷�֦�˾����ֳ����ԣ�����С�־�Ũ�ȣ�MIC��ֵ�ֱ�Ϊ12.9��12.5��g/mL�����²���ŵ���Ͼ��ٰ������ֲ��������ġ���ŵ�����ģ��ѱ������Է�֦�˾����к�ǿ�Ļ��ԣ��Խ�˷�֦�˾�H37Rv���������ƽ��ҩ�����MICֵΪ0.78��g/mL��Ȼ������Щȥ���ĺ����ĵĺϳɷ����������û�����δ��������
3 | ����
��ͼ5��ʾ�Ŀ�ͨͼ��ʾ�������������ͨ����ϸ��ϸ��Ĥ����û�����ϸ��������ϳɣ����֦���ᡢ�ľ��ǻ������Ǿ��ǵ�����ϳɣ������Ʒ�֦�˾���Ȼ������Щ����������DNA��RNAΪ�е㣬����DNA���ʵĺϳɡ�
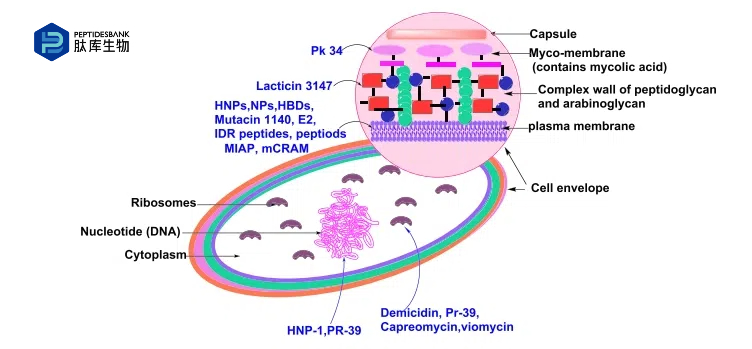
ͼ5 ��֦�˾���ϸ���ṹ����������÷�ʽ
һЩ��������չ�ֳ������п����ҩ���൱�Ŀ����Ч�����������ҩ�������¡�����ƽ���Ұ���������ù�طֱ�����0.025��0.4��0.5��1��/������Ũ�������ƽ�˷�֦�˾�ʵ���Ҿ��꣨H37Rv�����ֱ���0.2��0.8��8.0��5��g/mL��Ũ�ȶ�H37Rv���������ھ���ϸ���ڣ����д�������Щҩ��Ҳ������ϸ���ڵĽ�˷�֦�˾����ѷ�����������HNP-1��NP-1��nisinA��E50-52��rufomycin��ecumicin��lassomycin��teixobactin��trichoderinA��trichoderinB��BB-3497����DZ�ڵĿ����ҩ�����ã���Ϊ���Ƕ�ʵ���Ҿ������С�־�Ũ�ȣ�MIC�����ơ�
���˾��п���֦�˾������⣬�˷����أ�HNPs������ʾ������������ȱ�ݲ�����HIV����DZ�ڿ��������ԡ���ά�ļ���ͬ�¿�չ���о�֤����HNP1-3�ܹ�ͨ��������CD4Tϸ��ʹHIV��������ʧ�
��HNP-1���������Ե��о�������HNP-1��Ũ��Ϊ5��g/mLʱ��HIV-1��������л��ԡ���һ���о����֣�HNP-1������CD4+Tϸ���е���øC�Ļ��ԣ�������Ѫ��������1��g/mL��Ũ�Ⱦ�������ʾ���ԡ���Щ���ֱ�����HNP-1���ܶ�����HIV�ͽ�˲��ϲ���Ⱦ�Ļ������á�
����-�����Ǽ���ͬ�¶Ժϳ��Ŀ���˻��Ե��о�ּ��̽���ĵİ�������������Խ�˷�֦�˾��Ŀ�������֮��Ĺ�ϵ�����о����������ɫ����������Ậ�������ӻ���ǿ�������ԣ��������ᡢ�������ᡢ��������Ӱ��Ậ��������������ƻ��ԡ���ǰ��������һЩ�����й����ĵĿ���֦�˾��������䰱�������й�ϵ�Ĺ۲���������-�����ǵ��о����һ�¡���Ҳ��ì��֮�������ĸ�������л���HNP-1��ʾ���Ƚ�������������л���HNP-2��ǿ�Ļ��ԡ���Ҫ����ȱ��ϵͳ���о����������ݲ��㣬����ȷʶ���ĵİ������������俹��˻���֮���ϵ�����ٵ���ս��
�����г��ַ���Ȼ������ͻ��Ŀ���߿����������ڵ��ȶ��ԺͿڷ��������öȡ����б������������������������õ�Ѫ���ȶ��ԡ�ͬ���������������A�������������3147��³��ù�ء�����ù�ء�����������ù���ء������BB-3497����������Ҳ���ܾ������õ�Ѫ���ȶ��ԣ�ֵ�ý�һ���о������⣬ͨ���ھ���DZ�ڿ���˻��Ե������������ʵ������������������Ȼ������ͻ��ģ���Ѫ���ȶ���Ҳ�п��ܵõ���ߡ�
4 | ����
��֮������������Ȼ�ͺϳ����Լ������ĵ�С���ӱ���������DZ�ڵĿ���˻��ԡ�����һЩ������Ϊ�����Ͷ�ҩ�㷺��ҩ��˲��Լ��ϲ���Ⱦ HIV ���ߵ�����ҩ���Ҫ��һ����չϵͳ�о�����ȷ����Щ�ĵİ����������������֮��Ĺ�ϵ��ͨ����������Ľṹ���Σ����õ�������Щ�ĵĹ�Ч��ϵ���������ڿ���������Ч���Ͷ�ҩ���㷺��ҩ��˲��Լ��ϲ���Ⱦ HIV ���ߵ�����ҩ�














