
ФПЕФ
ЬНЬжЙІФмадФЩУзздзщзАЖрыФKLPPФ§НКЖдЙиНкШэЙЧШБЫ№ЕФаоИДзїгУЁЃ
ЗНЗЈ
ХрбјШЫЙЧЫшМфГфжЪИЩЯИАћЃЈBMSCsЃЉЃЌНЋBMSCsЗжЮЊBMSCs-KLD-12зщЃЈBMSCsгыKLD-12Ф§НКЙВХрбјЃЉКЭBMSCs-KLPPзщЃЈBMSCsгыKLPPФ§НКЙВХрбјЃЉЃЌЗжБ№ааШэЙЧгеЕМЗжЛЏХрбјЃЌMTTЗЈМьВтЯИАћЕФдіжГЛюадЁЃНЋШЫШэЙЧзщжЏЗжЮЊШэЙЧ-KLPPзщЃЈжЦзїШэЙЧШБЫ№ЧјВЂЬюГфKLPPФ§НКНјааХрбјЃЉЁЂШэЙЧ-KLD-12зщЃЈжЦзїШэЙЧШБЫ№ЧјВЂЬюГфKLD-12Ф§НКНјааХрбјЃЉЁЂШэЙЧзщЃЈНіжЦзїШэЙЧШБЫ№ЧјЃЉЁЃCalcein-AM/PIЫЋШОЗЈМьВтBMSCs-KLD-12зщМАBMSCs-KLPPзщЕФЯИАћЖОадЁЃХрбј49 dКѓЃЌЪеМЏШэЙЧзщЁЂШэЙЧ-KLD-12зщЁЂШэЙЧ-KLPPзщЕФШэЙЧзщжЏНјааЧаЦЌЃЌВЂааАЂЖћаТРЖШОЩЋЁЃWestern blotЗЈМьВтИїзщжаЂёаЭНКдЃЈCol-ЂёЃЉЁЂЂђаЭНКдЃЈCol-ЂђЃЉЁЂЂњаЭНКдЃЈCol-ЂњЃЉЕФБэДяЁЃ
НсЙћ
гыBMSCs-KLD-12зщБШНЯЃЌBMSCs-KLPPзщХрбј1 dЁЂ3 dЁЂ7 dЕФЯИАћдіжГТЪОљУїЯддіМгЃЈP<0.05ЃЉЃЌЧвCol-ЂёЁЂCol-ЂђЁЂCol-ЂњЕФЯрЖдБэДяЫЎЦНУїЯддіМгЃЈP<0.05ЃЉЁЃCalcein-AM/PIЫЋШОЩЋМьВтБэУїBMSCs-KLPPзщКЭBMSCs-KLD-12зщЯИАћЛюадЛљБОвЛжТЃЌKLPPФ§НКЮоЯИАћЖОадЁЃгыШэЙЧ-KLD-12зщБШНЯЃЌШэЙЧ-KLPPзщШэЙЧаоИДзїгУИќУїЯдЃЈP<0.05ЃЉЃЌЧвCol-ЂёЁЂCol-ЂђЁЂCol-ЂњЕФЯрЖдБэДяЫЎЦНИќИпЃЈP<0.05ЃЉЁЃ
НсТл
ЙІФмадФЩУзздзщзАЖрыФKLPPФ§НКЖдЙиНкШэЙЧШБЫ№ОпгаСМКУЕФаоИДзїгУЁЃ
ЙиНкШэЙЧШБЫ№ЪЧвЛжжГЃМћЕФЙиНкМВВЁЃЌЦфЬиЕуЪЧШэЙЧзщжЏВПЗжЛђЭъШЋЫ№ЛЕЃЌбЯжигАЯьЛМепЕФЩњЛюжЪСПЃЌФбвдздгњ[1-2]ЁЃЫфШЛФПЧАвбОгавЛаЉжЮСЦШэЙЧШБЫ№ЕФЗНЗЈЃЌШчздЬхШэЙЧвЦжВКЭЙЧЫшДЬМЄМСЕШЃЌЕЋЭљЭљЖМДцдкжюШчЙЉЬхВЛзуЁЂЪжЪѕДДЩЫДѓвдМАШэЙЧНсЙЙКЭЙІФмФбвдЛжИДе§ГЃЕШвЛЯЕСаЮЪЬтЁЃгЩгкЙиНкШэЙЧШБЫ№ЕФЗЂВЁдвђШдШЛВЛУїШЗЃЌвЉЮяжЮСЦаЇЙћВЂВЛУїЯдЃЌЖјШЫЙЄЙиНкжУЛЛжЮСЦЕФЗбгУвВЯрЕБИпАКЃЌвђДЫбаЗЂОпгааоИДЙиНкШэЙЧзїгУЕФгеЕМСЦЗЈОпгаживЊвтвх[3]ЁЃ
ЙІФмадФЩУзздзщзАЖрыФKLPPФ§НКвђЦфОпгаПЩЖЈжЦадКЭЙуЗКЪЪгУадЃЌвбГЩЮЊвНбЇКЭЩњЮяММЪѕСьгђЕФвЛИібаОПШШЕу[4]ЁЃKLPPФ§НКЪЧЭЈЙ§АќКЌВПЗжЙІФмЛЏЕФВрСДКЭыФЛљжЎМфЕФЙВМлКЭЧтМќЯрЛЅзїгУЕФзщКЯЖјаЮГЩЕФЃЌЦфОпгадкЗжзгЫЎЦНЩЯНјааЖЈжЦЕФФмСІЃЌдквЉЮяЪфЫЭЁЂзщжЏЙЄГЬКЭдйЩњвНбЇЗНУцЗЂЛгживЊзїгУ[5]ЁЃНќФъРДЃЌПЩПиОлКЯЙ§ГЬдЪаэдіМгЖдЖрыФЫЎФ§НКЕФСїБфадКЭЩњЮябЇЬиадЕФПижЦЃЌвдТњзуИїжжЩњЮявНбЇгІгУжаЕФЬиЖЈвЊЧѓ[6]ЁЃДЫЭтЃЌЙІФмЛЏыФађСадкГЩНКЙ§ГЬжаПЩвдЭЈЙ§ЙВМлМќгыЦфЫћЗжзгЃЈШчЕААзжЪЁЂЗЧБрТыRNAЁЂDNAЃЉЗЂЩњЯрЛЅзїгУЃЌДгЖјВњЩњОпгаРэЯыЬиадЕФЖрЙІФмЫЎФ§НКЃЌШчПЩвдЛКЪЭПЙОњвЉЮяКЭЩњЮяЛюадЗжзгЕФЙІФмадЫЎФ§НК[7]ЁЃШЛЖјЃЌФПЧАЛЙВЛЧхГўKLPPФ§НКЖдШэЙЧЫ№ЩЫаоИДЕФзїгУЁЃБОбаОПжМдкЬНЬжKLPPФ§НКЖдШэЙЧШБЫ№ЕФаоИДзїгУЁЃ
1 ВФСЯгыЗНЗЈ
1.1 ШэЙЧзщжЏ
бЁШЁгкЮвдКЙиНкЭтПЦНјааШЋЯЅЙиНкжУЛЛЪѕЕФРЯФъЫЋЯЅЙиНкЙЧЙиНкбзЛМеп10Р§ЃЌФъСф58ЁЋ81ЫъЃЌЦНОљЃЈ67.2ЁР5.9ЃЉЫъЃЛВЁГЬ3ЁЋ18ФъЃЌЦНОљЃЈ12.1ЁР1.8ЃЉФъЁЃЛМепОљЮЊЫЋЯЅЙиНкЙЧЙиНкбзЃЌГіЯжВЛЭЌГЬЖШЛћаЮЁЂОЗТЮЁЂЙІФмеЯАЛђзюДѓЧќЧњЪмЯоЃЌОXЩфЯпМьВщЗЂЯжВЛЭЌГЬЖШЙІФмадЭЫЛЏЃЌМфЯЖвьГЃБфаЁЃЌПЩМћУїЯдвьГЃВЁРэадИФБфЃЌНсКЯСйДВжЂзДеяЖЯЮЊЭэЦкЯЅЙиНкЙЧадЙиНкбзЃЌОљВЩШЁШЋЯЅЙиНкжУЛЛЪѕжЮСЦЁЃЪеМЏШЋЯЅЙиНкжУЛЛЪѕжаНиГ§ЖЊЦњЕФзщжЏВЂЛёШЁШэЙЧзщжЏЁЃБОбаОПОЛМепжЊЧщЭЌвтЃЌВЂЛёЕУЮвдКвНбЇТзРэЮЏдБЛсХњзМ[2022ЃЈПЦбаLЃЉЕкЃЈ51ЃЉКХ]ЁЃ
дкЮоОњЛЗОГЯТЃЌЫцЛњбЁШЁ3Р§ШэЙЧзщжЏЃЌгУ5 mmЕФЛЗаЮзщжЏВљШЁГіжБОЖ5 mmЕФдВаЮШэЙЧЦЌЃЌЪЙгУ2 mmЕФЛЗаЮзщжЏВљдкИїШэЙЧЦЌжабыжЦзївЛИіжБОЖ2 mmЕФШэЙЧШБЫ№ЧјгђЁЃЪЙгУKLPPФ§НКЬюГфШэЙЧШБЫ№ЧјгђЃЌдк37 ЁцЯТгкХрбјЯфФкЗѕг§ХрбјЃЌУП2 dИќЛЛвЛДЮХрбјвКЃЌЩшЮЊШэЙЧ-KLPPзщЁЃЫцЛњбЁШЁ3Р§ШэЙЧзщжЏгУKLD-12Ф§НКЬюГфЃЌЩшЮЊШэЙЧ-KLD-12зщЃЌЦфгрВйзїгыШэЙЧ-KLPPзщвЛжТЁЃдкЮоОњЛЗОГЯТЃЌЫцЛњбЁШЁ3Р§ШэЙЧзщжЏжЦзївЛИіжБОЖ2 mmЕФШэЙЧШБЫ№ЧјгђЃЌдк37 ЁцЯТгкХрбјЯфФкЗѕг§ХрбјЃЌУП2 dИќЛЛвЛДЮХрбјвКЃЌЩшЮЊШэЙЧзщЁЃДІРэ49 dЃЌЪеМЏИїзщШэЙЧзщжЏгУгкКѓајЪЕбщМьВтЁЃ
1.2 ЪдМСгыВФСЯ
ШЫЙЧЫшМфГфжЪИЩЯИАћЃЈbone marrow mesenchyml stem cells,BMSCsЃЉЙКгкЩЯКЃИЅдЊЩњЮяПЦММгаЯоЙЋЫОЁЃKLD-12гыKLPPФ§НКОљгЩЪЕбщЪвзджїКЯГЩЁЃфхЛЏввЖЇШОЩЋЪдМСКЭШэЙЧЗжЛЏгеЕММСKartogeninЃЈKGNЃЉЙКгкББОЉАйАТРГВЉЙЋЫОЁЃЖўрпјМзЫсЃЈbicinchoninic acid, BCAЃЉЪдМСКаЁЂMTTЪдМСКаЁЂАЂЖћаТРЖШОЩЋЪдМСКаЁЂмчЫиКьШОЩЋЪдМСКаОљЙКгкЩЯКЃБЬдЦЬьЩњЮяПЦММгаЯоЙЋЫОЁЃИЦЛЦТЬЫи-ввѕЃєЧМзЛљѕЅШОЩЋЪдМСКаЙКгкЮїАВЦыдРЩњЮяПЦММгаЯоЙЋЫОЁЃЂёаЭНКдЃЈcollagen-ЂёЃЌCol-ЂёЃЉЁЂЂђаЭНКдЃЈcollagen-ЂђЃЌCol-ЂђЃЉЁЂXаЭНКдЃЈcollagen-ЂњЃЌCol-ЂњЃЉЁЂGAPDHЕФвЛПЙОљЙКгкУРЙњAbcamЙЋЫОЁЃ
1.3 BMSCsХрбј
BMSCsжУгкDMEM/F12ЃЈ1ЁУ1ЃЌУРЙњHycloneЙЋЫОЃЉХрбјвКжаЃЌХрбјвКжаЬэМг10% FBSЃЈУРЙњHycloneЙЋЫОЃЉЁЂ100 U/mLЧрУЙЫиЁЂ100 U/mLСДУЙЫиЃЌдк37 ЁуCЁЂКЌ5% CO2ЕФХрбјЯфжаХрбјЃЌУПИє24 hЛЛвКвЛДЮЃЌ48 hДЋДњвЛДЮЃЌНЋЖдЪ§ЩњГЄЦкЕФBMSCsгУгкКѓајЪЕбщЁЃ
1.4 ЯИАћЗжзщДІРэ
НЋBMSCsЗжЮЊBMSCs-KLD-12зщКЭBMSCs-KLPPзщЁЃЦфжаНЋBMSCs-KLD-12зщBMSCsНгжжЕНKLD-12Ф§НКжаХрбј24 hЃЌЪеМЏЯИАћЃЛНЋBMSCs-KLPPзщBMSCsНгжжЕНKLPPФ§НКжаХрбј24 hЃЌЪеМЏЯИАћЁЃгУгкШэЙЧЗжЛЏгеЕМЁЃ
1.5 ШэЙЧЗжЛЏгеЕМ
НЋBMSCs-KLD-12зщКЭBMSCs-KLPPзщЯИАћдХрбјвКИќЛЛЮЊКЌ50 nmol/L KGNЕФDMEM/F12ХрбјЛљЃЈКЌ10% FBSЁЂ100 U/mLЧрУЙЫиЁЂ100 U/mLСДУЙЫиЃЉЃЌгк37 ЁцЁЂКЌ5% CO2ЕФХрбјЯфжаНјааШэЙЧЗжЛЏгеЕМЃЌЗжБ№Хрбј1 dЁЂ3 dЁЂ7 dНјааЯИАћдіжГКЭШэЙЧЗжЛЏФмСІЕФМьВтЁЃ
1.6 MTTЪЕбщ
BMSCs-KLD-12зщКЭBMSCs-KLPPзщгеЕМШэЙЧЗжЛЏКѓ1 dЁЂ3 dЁЂ7 dЗжБ№МгШыMTTШмвКЃЌЗѕг§4~6 hКѓЃЌНЋХрбјУѓжаЕФMTTОЇЬхШмНтгкШѕЫсадФђЫиШмвКжаЃЌШЛКѓЭЈЙ§УИБъвЧМьВтИїзщЕФODжЕЁЃ
1.7 Calcein-AM/PIЫЋШОЗЈМьВтЯИАћЖОад
ЪеМЏBMSCs-KLD-12зщКЭBMSCs-KLPPзщЕФШэЙЧЯИАћЃЌЖрОлМзШЉЙЬЖЈ15 minЃЌPBSЧхЯД3ДЮЃЌУПДЮ5 minЁЃМгШыПЙУИвК2 mLЗѕг§30 minЃЌвжжЦЗЧЬивьадУИЃЛВЂНЋCalcein-AMЬэМгЕНБъБОжаШОЩЋ15 minЃКгУPBSЯДЕгБъБО3ДЮЃЌУПДЮ5 minЃЌPIШОЩЋ5 minЃЌШЅГ§ЖргрЕФШОЩЋвКЃЛНЋШОЩЋКѓЕФБъБОЗХдкгЋЙтЯдЮЂОЕЯТХФееЙлВьЁЃ
1.8 АЂЖћаТРЖШОЩЋ
ШэЙЧ-KLPPзщЁЂШэЙЧ-KLD-12зщКЭШэЙЧзщЕФШэЙЧБъБОХрбј49 dКѓЃЌгУPBSЯДЕг3ДЮЃЌУПДЮ5 minЁЃгУ0.1 mol/LЕФбЮЫсШмвКДІРэШэЙЧЧаЦЌ10 minЃЌдк1%АЂЖћаТРЖШОЩЋШмвКжаЗѕг§10 hЁЃЫцКѓХФееЙлВьЁЃ
1.9 Western blotМьВтШэЙЧЗжЛЏБъжОЮя
МьВтBMSCs-KLD-12зщЁЂBMSCs-KLPPзщЁЂШэЙЧзщЁЂШэЙЧ-KLPPзщЁЂШэЙЧ-KLD-12зщжаШэЙЧЗжЛЏЯрЙиЕААзЃЌАќРЈCol-ЂёЁЂCol-ЂђЁЂCol-ЂњЁЃгУRIPAЛКГхвКСбНтЯИАћЛђзщжЏЬсШЁзмЕААзЁЃЕААзХЈЖШгУBCAЪдМСКаВтЖЈЁЃДЫЭтЃЌЪЙгУ12% SDS-PAGEФ§НКЗжРыЕААзЃЌВЂНЋЦфзЊвЦЕНPVDFФЄЩЯЁЃНЋФЄгУ5%ЭбжЌХЃФЬЗтБе2 hЃЌШЛКѓдк4 ЁцЯТгывЛПЙЗѕг§10 hЁЃУтвпИДКЯЮягУРБИљЙ§бѕЛЏЮяУИХМСЊЕФПЙЭУIgGПЙЬхЃЈ1ЁУ5 000ЃЉЗѕг§ЁЃзюКѓЪЙгУWestern blotЛЏбЇЗЂЙтМьВтЕААзаХКХБэДяЁЃЫљгаЪЕбщОљжиИД3ДЮЁЃПЙЬхЮЊCol-ЂёЃЈ1ЁУ1 000ЃЉЁЂCol-ЂђЃЈ1ЁУ1 000ЃЉЁЂCol-ЂњЃЈ1ЁУ1 000ЃЉЁЃ
1.10 ЭГМЦбЇЗжЮі
Ъ§ОнЪЙгУGraphPad PRISM 5.01НјааЭГМЦбЇЗжЮіЃЌе§ЬЌЗжВМЕФЪ§ОнвдОљЪ§ЁРБъзМВюЃЈx-ЁРsЃЉБэЪОЁЃСНзщМфЕФЪ§ОнВювьВЩгУtМьбщЁЃЕЅвђЫиЗНВюЗжЮіЦРЙРОљЪ§жЎМфЕФВювьЃЌВЂНјааLSD-tЕФЖржиБШНЯЃЌвдЦРЙРСНзщжЎМфЕФЭГМЦВювьЁЃМьбщЫЎзМЮЊІС=0.05ЃЌP<0.05ЮЊВювьгаЭГМЦбЇвтвхЁЃ
2 НсЙћ
2.1 KLPPФ§НК
ЭЈЙ§жЪЦзКЭИпаЇвКЯрЩЋЦзбщжЄЃЌБОбаОПжЦБИЕФKLPPФ§НКБЛжЄУїКЯГЩГЩЙІЁЃKLPPФ§НКЕФЯрЖдЗжзгжЪСПЮЊ1 498.26ЃЌДПЖШЩЬЮЊ94.12%ЁЃKLPPФ§НКаЮГЩСЫФЩУзЯЫЮЌЃЌЯЫЮЌжБОЖЦНОљЮЊЃЈ13.5ЁР5.3ЃЉnmЃЌГЄЖШПЩДя650 nmЁЃетаЉФЩУзЯЫЮЌНЛжЏдквЛЦ№ЃЌаЮГЩСЫЭјзДЕФЖрПзНсЙЙЁЃСэЭтЃЌ0.5%ЕФKLPPФ§НКФмЙЛПьЫйздзщзАЩњГЩЫЎФ§НКЃЌНсЙЙЭъећОљдШЃЌгазуЙЛЕФФкОлСІБЃГжЙЬЖЈаЮзДЃЌМћЭМ1ЁЃ

2.2 KLPPФ§НКЖдBMSCsдіжГЕФгАЯь
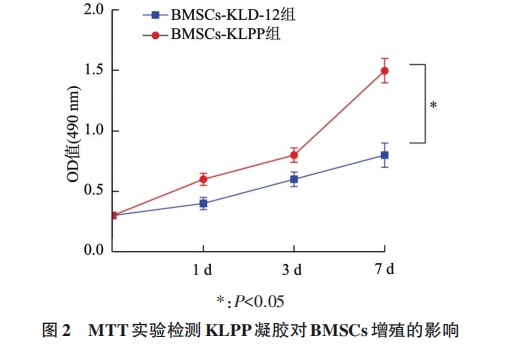
гыBMSCs-KLD-12зщБШНЯЃЌBMSCs-KLPPзщХрбј1 dЁЂ3 dКЭ7 dЕФЯИАћдіжГЛюадЃЈ490 nmДІODжЕЃЉОљдіМгЃЈP<0.05ЃЉЃЌЧвОљЫцзХЪБМфЕФбгГЄЖјУїЯддіМгЃЈP<0.05ЃЉЃЌМћЭМ2ЁЃ
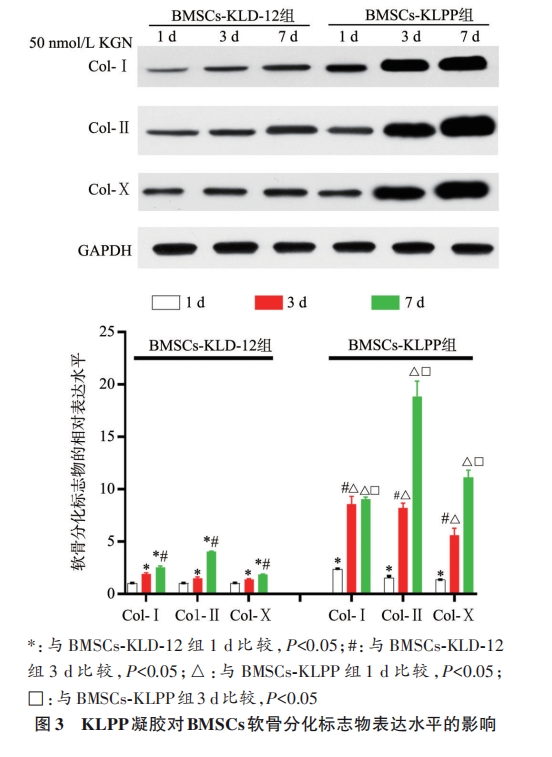
2.3 KLPPФ§НКДйНјBMSCsЕФШэЙЧЗжЛЏ
гыBMSCs-KLD-12зщБШНЯЃЌBMSCs-KLPPзщCol-ЂёЁЂCol-ЂђЁЂCol-ЂњЕФЯрЖдБэДяЫЎЦНУїЯддіМгЃЈP<0.05ЃЉЃЌМћЭМ3ЁЃ
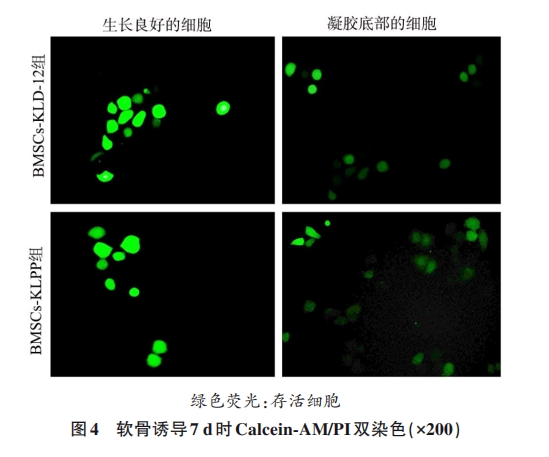
2.4 KLPPФ§НКЮЌГжШэЙЧЯИАћЕФДцЛю
Calcein-AM/PIЫЋШОЩЋМьВтБэУїЃЌBMSCs-KLPPзщКЭBMSCs-KLD-12зщЯИАћЛюадЛљБОвЛжТЁЃШэЙЧгеЕМ7 dЪБЃЌKLPPФ§НККЭKLD-12Ф§НКжаЖМЗЂЯжДѓСПЛюЕФШэЙЧЯИАћЃЌМЋЩйЫРЭіЯИАћЁЃKLPPФ§НКжаЕФЯИАћБЃГждВаЮЃЌKLPPФ§НКПзЕзВПЯИАћГЪЗФДИзДЛђЫѓаЮЃЌМћЭМ4ЁЃБэУїKLPPФ§НКПЩвдСМКУЕижЇГжБЃЛЄШэЙЧЯИАћЕФЩњГЄЁЃ
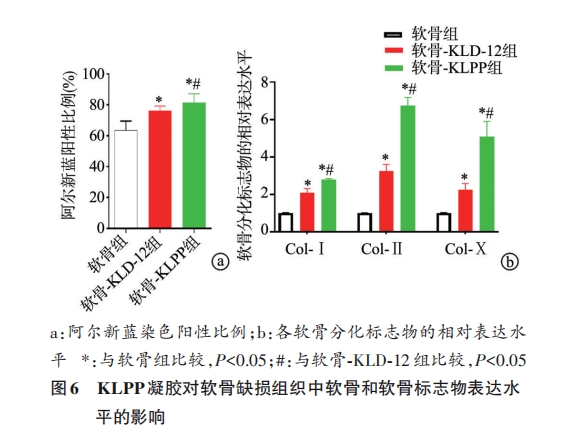
2.5 KLPPФ§НКДйНјШэЙЧШБЫ№ЕФаоИД
АЂЖћаТРЖШОЩЋЯдЪОЃКгыШэЙЧзщБШНЯЃЌШэЙЧ-KLD-12зщКЭШэЙЧ-KLPPзщШэЙЧдіЩњЛюдОЃЌШОЩЋбєадБШР§УїЯдЩ§ИпЃЌ2зщШэЙЧШБЫ№аоИДзїгУОљНЯУїЯдЃЌЧвШэЙЧ-KLPPзщНЯШэЙЧ-KLD-12зщИќМгУїЯдЃЈP<0.05ЃЉЁЃгыШэЙЧзщБШНЯЃЌШэЙЧ-KLD-12зщКЭШэЙЧ-KLPPзщCol-ЂёЁЂCol-ЂђЁЂCol-ЂњЕФЯрЖдБэДяЫЎЦНОљУїЯддіМгЃЈP<0.05ЃЉЃЌЧвШэЙЧ-KLPPзщНЯШэЙЧ-KLD-12зщдіМгИќЯджјЃЈP<0.05ЃЉЃЌМћЭМ5ЁЂ6ЁЃ

3 ЬжТл
ЙиНкШэЙЧЫ№ЛЕКѓЕФздЮваоИДФмСІЗЧГЃгаЯоЃЌШєВЛМАЪБжЮСЦЃЌМДЪЙЪЧНЯаЁЕФЫ№ЩЫвВЛсЫцзХЪБМфЕФЭЦвЦЗЂеЙГЩИќбЯжиЕФВЁБфЃЌзюжеЕМжТећИіЙиНкЕФЭЫБфКЭЙЧЙиНкбз[8]ЁЃФПЧАЃЌШэЙЧШБЫ№ЬсГЋНзЬнжЮСЦЃЌМДИљОнМВВЁЕФВЛЭЌЗЂеЙНзЖЮбЁдёВЛЭЌЕФжЮСЦЗНЪНЃЌАќРЈНЕЕЭЬхжЪСПЁЂВЙГфгЊбјЁЂЖЭСЖЁЂЪЙгУвЉЮяКЭЭтПЦЪжЪѕжЮСЦЕШ[2]ЁЃгЩгкФПЧАБЃЪижЮСЦЕФаЇЙћгаЯоЃЌЙиНкФкзЂЩфвЉЮяЕФСЦаЇВЛШЗЧа[9-10]ЃЌШЫЙЄЙиНкжУЛЛЪѕШдЪЧжЮСЦбЯжиЙиНкШэЙЧШБЫ№ЕФН№БъзМЁЃЕЋШЫЙЄЙиНкМйЬхМлИёИпАКЃЌдіМгСЫвНСЦИКЕЃЃЌвђДЫЃЌбаОПаТЕФШэЙЧаоИДЪжЖЮЪЎЗжБивЊЁЃKLPPФ§НКгыДЋЭГKLD-12Ф§НКОпгаЯрЫЦЕФФЩУзНсЙЙКЭСїБфадФмЁЃБОбаОПЭЈЙ§зджїКЯГЩKLPPФ§НКЃЌВЂЙлВьKLPPФ§НКЖдШэЙЧШБЫ№ЕФаоИДзїгУЃЌвдЦкЮЊЙиНкШэЙЧШБЫ№ЬсЙЉаТЕФжЮСЦВпТдЁЃ
ФкдДадИЩЯИАћЕФдЮЛШэЙЧдйЩњММЪѕдкШэЙЧШБЫ№ЕФжЮСЦжаЪмЕНСЫЙуЗКЙизЂЃЌИУММЪѕРћгУШЫЬхздЩэЕФдйЩњФмСІРДаоИДШэЙЧзщжЏЃЌБмУтСЫЭтдДадЯИАћДјРДЕФВЛРћгАЯь[11]ЁЃЮЂЙЧелЪЧЙиНкШэЙЧаоИДЕФГЃгУВпТдЃЌРћгУBMSCsЗжЛЏЕФдРэРДЪЙШэЙЧзщжЏдйЩњЁЃШЛЖјЃЌаТзщжЏДѓЖрЪЧЯрЖдНЯШѕЕФЯЫЮЌШэЙЧЃЌЖјВЛЪЧЭИУїШэЙЧЁЃдвђПЩФмЪЧеаФМЕФИЩЯИАћЪ§СПВЛзу[12]ЁЃвђДЫЃЌФмЙЛИФЩЦКЭдіЧПФкдДадИЩЯИАћОлМЏЕФЛЏбЇгеЕММСЛђЩњЮягеЕМжЇМмГЩЮЊСЫбаОПНЙЕу[13]ЁЃ
KLD-12Ф§НКЪЧФПЧАбаОПжаБШНЯГЩЪьЕФздзщзАФЩУзЖрыФВФСЯЃЌНќМИФъвбБЛЙњЭтгУгкФкдДадШэЙЧЯИАћЕФФММЏ[14]ЁЃШЛЖјГЃЙцЕФKLD-12Ф§НКВЛФмТњзуШэЙЧШБЫ№аоИДЖдBMSCsОлМЏЕФИпашЧѓ[15]ЁЃБОбаОПЭЈЙ§ЪЙгУСНИіИЪАБЫс(G)ВаЛљзїЮЊМфИєСДЃЌНЋОпгаШэЙЧгеЕМзїгУЕФЙІФмЛљађDHLSDHLSDNYTLDIDRAIHЬэМгЕНKLD-12ЕФC-ФЉЖЫЃЌДгЖјжЦдьСЫАБЛљЫсађСаЮЊKLDLKLDLKLDLGGDHLS DHLSDNYTLDEDRAIHЕФЙІФмадФЩУзздзщзАЖрыФKLPPФ§НКЁЃетжжВФСЯМШБЃСєСЫФЩУзздзщзАЖрыФKLD-12ПЩвдздзщзАГЩНКЕФЬиадЃЌгжОпБИСЫПЩвдгеЕМШэЙЧЯИАћдіжГЕФЙІФмЃЌЦфПЩвдЭЈЙ§ЮЂДДЕФЗНЪНзЂШыЙиНкФкЃЌВЂдкЙиНкФкЬсЙЉШѓЛЌМАЫмаЭЬюВЙШэЙЧШБЫ№УцЕФзїгУЃЌдкШэЙЧШБЫ№жЮСЦжаПЩФмОпгаНЯДѓгХЪЦЁЃ
ЮЊСЫУїШЗKLPPФ§НКдкШэЙЧШБЫ№аоИДЗНУцЕФзїгУЃЌБОбаОПЖдБШЙлВьСЫKLPPФ§НКгыKLD-12Ф§НКЖдBMSCsШэЙЧЗжЛЏгеЕМКѓЯИАћдіжГЛюСІЕФгАЯьвдМАЖдШэЙЧШБЫ№аоИДЕФзїгУЃЌНсЙћЯдЪОЃЌKLPPФ§НКПЩЯджјЬсИпШэЙЧЗжЛЏКѓBMSCsЕФдіжГЛюСІЃЌВЂДйНјBMSCsжаШэЙЧЯИАћдйЩњБъжОЮяCol-ЂёЁЂCol-ЂђЁЂCol-ЂњЕФЕААзБэДяЃЌЖјЧвKLPPФ§НКЖдШэЙЧЯИАћдйЩњБъжОЮяЕФДйНјзїгУУїЯдДѓгкKLD-12Ф§НКЁЃLuЕШ[16]БЈЕРСЫШэЙЧЯИАћдкгеЕМЯТПЩвдЯђжмЮЇзщжЏВФСЯФкЧЈвЦЃЌДгЖјгаРћгкзщжЏЙЄГЬШэЙЧЕФећКЯЁЃLevinsonЕШ[17]НЋШэЙЧПХСЃЧЖШыЯЫЮЌЕААзКЭНКдЕААзФ§НКжаЃЌВЂдкХрбј28 dКѓЙлВьЕНУїЯдЕФШэЙЧЯИАћЩњГЄЁЃNgЕШ[9]БЈЕРЃЌдкЬхЭтШэЙЧШБЫ№ФЃаЭжаЃЌДѓПзОлввЯЉДМ(PVA)жЇМмДйНјСЫШэЙЧЯИАћДгЫожїШэЙЧЧЈвЦЕНжЇМмЃЌВЂИФЩЦСЫНчУцећКЯЁЃетаЉбаОПЖМжЄУїСЫШэЙЧЯИАћПЩвдЧЈвЦНјШызщжЏЙЄГЬВФСЯВЂдкВФСЯЕФжЇГжЯТИќКУЕиДйНјШэЙЧШБЫ№ЧјгђЕФаоИДЁЃБОбаОПжаKLPPФ§НКвВЭЌбљЬсЙЉСЫДйНјШэЙЧЩњГЄЕФЙІФмађСаКЭжЇМмНсЙЙЃЌНсЙћЯдЪОЃЌдкKLPPФ§НКФкШэЙЧЯИАћЩњГЄУїЯдгХгкЖдеезщЁЃвђДЫЃЌЮвУЧШЯЮЊKLPPФ§НКОпгаНЯКУЕФДйНјШэЙЧЗжЛЏКЭШэЙЧЯИАћЩњГЄЕФзїгУЁЃСэЭтЃЌБОбаОПжЄЪЕСЫKLPPФ§НКгыKLD-12Ф§НКОпгаЯрЫЦЕФЯИАћЖОадЃЌОљПЩвдСМКУЕижЇГжБЃЛЄШэЙЧЯИАћЕФЩњГЄЁЃЮЊНјвЛВНбщжЄKLPPФ§НКЕФШэЙЧШБЫ№аоИДзїгУЃЌБОбаОПРћгУСйДВШэЙЧзщжЏБъБОЃЌНЈСЂШэЙЧШБЫ№ШэЙЧЦЌЃЌОЙ§ГЄЦкЕФKLPPФ§НКжЮСЦЗЂЯжЃЌKLPPФ§НКОпгаНЯКУЕФШэЙЧаоИДЁЂНчУцећКЯКЭШэЙЧдйЩњзїгУЃЌЧваЇЙћЧПгкKLD-12Ф§НКЁЃЮвУЧЭЦВтетгыKLPPФ§НКОпБИСЫНЯКУЕФШэЙЧЯИАћдіжГгеЕМЙІФмвдМАНЯКУЕФШэЙЧЯИАћКЭBMSCsЕФФММЏЙІФмУмЧаЯрЙиЁЃНјвЛВНМьВтШэЙЧЯИАћБъжОЮяCol-ЂёЁЂCol-ЂђЁЂCol-ЂњЕФЕААзБэДяЗЂЯжЃЌдкШэЙЧШБЫ№жЮСЦжаKLPPФ§НКЖдШэЙЧЯИАћБъжОЮяCol-ЂёЁЂCol-ЂђЁЂCol-ЂњБэДяЕФДйНјзїгУДѓгкKLD-12Ф§НКЃЛЖјЮДОжЮСЦЕФШэЙЧШБЫ№ВЂЮДгњКЯЃЌЧвЦфжажївЊвдЯЫЮЌзщжЏЛђЯЫЮЌШэЙЧЮЊжїЁЃвђДЫЃЌKLPPФ§НКЪЧвЛжжМЋОпЧБСІЕФШэЙЧШБЫ№аоИДКђбЁепЁЃ
злЩЯЫљЪіЃЌЙІФмадФЩУзздзщзАЖрыФKLPPФ§НКПЩДйНјBMSCsЯИАћШэЙЧЗжЛЏКѓЕФЯИАћЛюСІЃЌаоИДЪмЫ№ЕФЭИУїШэЙЧВЂДйНјЦфдйЩњЃЌИФЩЦШэЙЧШБЫ№ЧјгђЕФНчУцећКЯЁЃвђДЫЃЌKLPPФ§НКНЋЪЧвЛжжКмгаЧАЭОЕФШэЙЧдйЩњЕФКђбЁепЃЌВЛашвЊШЮКЮЭтРДЯИАћЛђЛЏбЇв§геМСЁЃ
Утд№ЩљУїЃКБОЮФЮЊаавЕНЛСїбЇЯАЃЌАцШЈЙщдзїепМАддгжОЫљгаЃЌШчгаЧжШЈЃЌПЩСЊЯЕЩОГ§ЁЃЮФеТБъзЂгазїепМАЮФеТГіДІЃЌШчашдФЖСдЮФМАВЮПМЮФЯзЃЌПЩдФЖСддгжОЁЃ








