’Σ“ΣΘΚΕύκΡΉ‘ΉιΉΑ–Έ≥…ΒΡΕύΩΉΫαΙΙ «–¬“Μ¥ζΕύΩΉ≤ΡΝœ, ‘Ύ¥ΏΜ·ΓΔ¥ΪΗ–ΓΔΖ÷άκΚΆ“©ΈοΒίΥΆΒ»Νλ”ρΨΏ”–ΚήΚΟΒΡ”Π”Ο«ΑΨΑ. κΡΜυΕύΩΉ≤ΡΝœΒΡΩΉΡΎ≥δ¬ζΑ±ΜυΥα≤ύΝ¥, “ρ¥ΥΩ…“‘Ά®ΙΐΚœάμ…ηΦΤΜρ–όΗΡκΡ–ρΝ–ά¥ΒςΫΎΤδΩΉΨΕ¥σ–ΓΚΆ–‘Ρή. ΙΠΡήΜυΆ≈ΚΆΫπ τάκΉ”ΒΡ“ΐ»κΫχ“Μ≤Ϋά©’ΙΝΥΕύκΡΜυΕύΩΉ≤ΡΝœΒΡΫαΙΙ”κ–‘Ρή. ‘Ύ’βΤΣΉέ ω÷–, Έ“Ο«Χ÷¬έΝΥκΡΜυΕύΩΉ≤ΡΝœΒΡ…ηΦΤΓΔΚœ≥…ΓΔΉιΉΑΦΑΤδ–‘Ρή, ≤ΔΉέ ωΝΥΫϋΡξά¥Τδ‘Ύ≤ΜΆ§Νλ”ρΒΡ”Π”Ο.
κΡ“ΜΑψ”…2~50ΗωΑ±ΜυΥαΆ®ΙΐΑ±ΜυΚΆτ»ΜυΆ―Υ°ΥθΚœ–Έ≥…ΒΡκΡΦϋΝ§Ϋ”Εχ≥…ΓΘκΡΙψΖΚ¥φ‘Ύ”Ύ…ζΈοΧε÷–Θ§ «…ζΈοΧε≤ΜΩ…»±…ΌΒΡΙΠΡή≥…Ζ÷Θ§ «¥σΉ‘»Μ¥Ά”η»ΥάύΒΡάώΈοΓΘ”κΒΑΑΉ÷ œύ±»Θ§κΡΒΡΖ÷Ή”Ήι≥…ΚΆΫαΙΙΗϋΈΣΦρΒΞΘ§‘Ύ…ηΦΤΫΉΕΈΚή»ί“Ή‘Λ≤βΤδΫαΙΙΚΆΙΠΡήΓΘκΡΜυΡ…ΟΉ≤ΡΝœ“―ΙψΖΚ”Π”Ο”Ύ…ζΈοΓΔΜ·―ßΓΔ≤ΡΝœΩΤ―ßΒ»Νλ”ρ[1®C4]ΓΘ
Ζ÷Ή”Ή‘ΉιΉΑΉςΈΣΉ‘»ΜΫγ÷–Τ’±ι¥φ‘ΎΒΡΜυ±Ψœ÷œσ÷°“ΜΘ§ «–μΕύ÷Ί“Σ…ζΟϋΜνΕ·ΒΡΜυ¥Γ[5Θ§6]DNAΒΡΥΪ¬ί–ΐΫαΙΙΓΔΒΑΑΉ÷ ΒΡΗΏΦΕΫαΙΙΕΦ «Ζ÷Ή”Ή‘ΉιΉΑΒΡΒδ–ΆάΐΉ”Θ§”κΒΑΑΉ÷ ΒΡΉ‘ΉιΉΑ––ΈΣάύΥΤΘ§κΡΖ÷Ή”Ά®ΙΐΖ«Ι≤ΦέœύΜΞΉς”ΟΉ‘ΉιΉΑ–Έ≥…Ης÷÷”––ρΫαΙΙΘ§»γΡ…ΟΉœΥΈ§[7Θ§8]ΓΔΡ…ΟΉΝΘΉ”[9]ΓΔΡ…ΟΉΙή[10]ΓΔΡ“≈ί[11], nanoribbons [12]ΚΆΥ°ΡΐΫΚ[13Θ§14]”ΑœλκΡΉιΉΑΒΡΖ«Ι≤ΦέœύΜΞΉς”Ο÷ς“ΣΑϋά®«βΦϋΓΔΠ–-Π–Ε―Μΐ[15]ΓΔΨ≤ΒγœύΜΞΉς”ΟΚΆ ηΥ°œύΜΞΉς”Ο[16]pHΓΔΈ¬Ε»Β»ΆβΫγ¥ΧΦΛΕΦΜα”Αœλ…œ ωΖ«Ι≤ΦέœύΜΞΉς”ΟΘ§“ρ¥Υ’β–©“ρΥΊ“≤≥…ΈΣ―–ΨΩ»Υ‘±―–ΨΩΚΆΩΊ÷ΤΉ‘ΉιΉΑΙΐ≥ΧΒΡΙΛΨΏ[17Θ§18]Ά®Ιΐ…ηΦΤœλ”ΠΗς÷÷¥ΧΦΛΒΡ–¬ΫαΙΙΘ§Ή‘ΉιΉΑκΡΝλ”ρ»ΓΒΟΝΥ÷Ί¥σΫχ’Ι[19]¥ΥΆβΘ§“Μ–©ΨΏ”–ΧΊΕ®ΙΠΡήΒΡΉιΖ÷“≤Ά®ΙΐΙ≤ΉιΉΑΜρΙ≤Φέ≈ΦΝΣΒΡΖΫ Ϋ”κκΡΫαΚœΘ§Η≥”ηκΡΫαΚœΈο–¬ΒΡ–‘÷ [20®C23]ΓΘ
Ε‘ΕύΩΉ≤ΡΝœΒΡΧΫΥς¥”Έ¥ΆΘ÷ΙΘ§Ζ– ·ΒΡ―–ΨΩ[24]ΓΔΫπ τ”–ΜζΙ«ΦήΘ®MOFΘ©[25]“‘ΦΑ”–Μζ≥§Ζ÷Ή”ΕύΩΉ≤ΡΝœ[26Θ§27]»ΓΒΟΝΥΩ…œ≤ΒΡΫχ’ΙΘ§ΕύκΡ”…”ΎΨΏ”–ΝΦΚΟΒΡ…ζΈοœύ»ί–‘ΚΆ ÷–‘Θ§‘Ύ…ζΈο¥ΏΜ·ΓΔ ÷–‘Φλ≤β”κΖ÷±φΓΔΤχΧεΈϋΗΫΓΔ“©Έο δΥΆΒ»ΖΫΟφ”–Ή≈«±‘ΎΒΡ”Π”Ο[28].Ε‘κΡΉ‘ΉιΉΑΒΡΖαΗΜΝΥΫβ ΙΒΟΤδ–‘ΡήΚΆΫαΙΙ‘Ύ…ηΦΤΫΉΕΈΨΆΡήΒΟΒΫΚήΚΟΒΡ‘Λ≤βΓΘ“ρ¥ΥΘ§κΡΜυΕύΩΉ≤ΡΝœ¥”ΤδΥϊΕύΩΉ≤ΡΝœ÷–Ά―”±Εχ≥ωΘ§≥…ΈΣΫϋ °Ρξά¥―–ΨΩ»Υ‘±ΒΡ―–ΨΩ»»ΒψΓΘ‘Ύ’βΤΣΉέ ω÷–Θ§Έ“Ο«ΉήΫαΝΥκΡΜυΕύΩΉ≤ΡΝœΒΡΉν–¬Ϋχ’ΙΘ§≤ΔΧ÷¬έΝΥΥϋΟ«ΒΡ…ηΦΤ≤Ώ¬‘ΦΑΤδΉςΈΣΕύΩΉ…ζΈο≤ΡΝœΒΡ«±‘Ύ”Π”ΟΓΘ»ΜΚσΘ§Έ“Ο«Ε‘Ή‘ΉιΉΑκΡΜυΕύΩΉ≤ΡΝœ‘ΎΈ¥ά¥Μ·―ßΓΔ…ζΈοΚΆ≤ΡΝœΩΤ―ß÷–ΒΡ«±ΝΠΫχ––ΝΥ…ν»κΒΡΖ÷ΈωΓΘ
κΡΜυΕύΩΉ≤ΡΝœΒΡ…ηΦΤ”κΧΊ–‘
Ά®ΙΐΚœάμ…ηΦΤκΡ–ρΝ–Θ§≈δ“‘Κœ ΒΡ»ήΦΝΚΆΆβΫγΧθΦΰΘ§Ω…“‘Κή»ί“ΉΒΊΩΊ÷ΤκΡΉ‘ΉιΉΑ≥…ΕύΩΉΫαΙΙΓΘΆ®ΙΐΗΡ±δΗςΈΜΒψΒΡΑ±ΜυΥα≤–ΜυΘ§Ω…“‘Κœάμ…ηΦΤκΡ–ρΝ–Θ§ ΙΤδ’έΒΰ≥…ΕΰΦΕΫαΙΙΘ§Αϋά®Π¬Ν¥ΓΔΠΝ¬ί–ΐΓΔΗΈΥΊΝ¥ΚΆΨμ«ζ¬ί–ΐΘ®ΖΫΑΗ 1Θ©’β ΙΈ“Ο«ΡήΙΜάϊ”ΟΧλ»ΜΩΉœΕΒΡΡ≥–©ΧΊ–‘ΚΆΙΠΡήΘ§Εχ’β–©ΧΊ–‘ΚΆΙΠΡή « Ι”Ο¥ΪΆ≥ΕύΩΉ≤ΡΝœΈόΖ® Βœ÷ΒΡ[49]ΓΘ
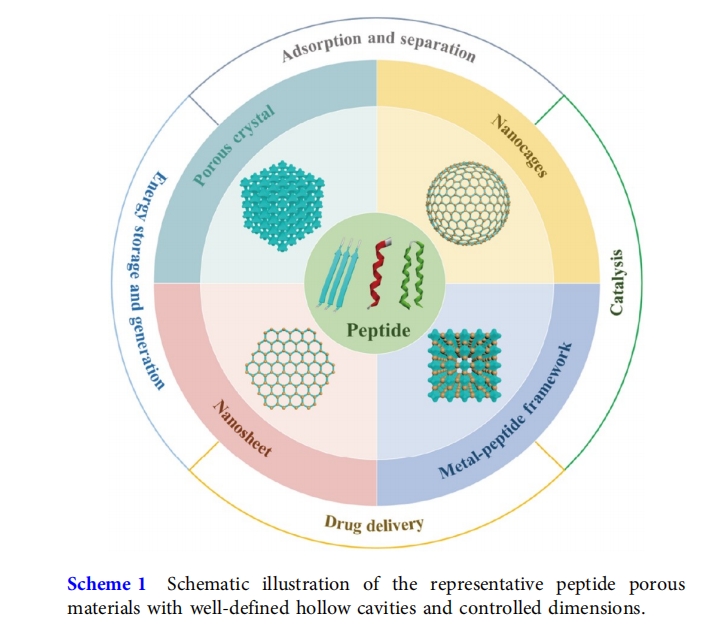
ΡΩ«ΑΈΣ÷ΙΘ§ΡήΙΜΉ‘ΉιΉΑ≥…ΗΏΕ»”––ρΕύΩΉ≤ΡΝœΒΡκΡΑϋά®ΕΰκΡΓΔ»ΐκΡΓΔΕύκΡΘ®±μ 1’β–©κΡΩ…“‘Ή‘ΉιΉΑ≥…ΨΏ”–ΨΪ»ΖΕ®÷ΤΩΉΫαΙΙΒΡΕύΈ§ΕύΩΉ≤ΡΝœΘ§Αϋά®ΕΰΈ§Θ®2DΘ©ΕύΩΉΡΛΘ§3DΕύΩΉΨßΧεΚΆΕύΩΉΡ…ΟΉΝΐΘ®ΖΫΑΗ 1¥ΥΆβΘ§MOFΆυΆυΨΏ”–ΫœΗΏΒΡΩΉœΕ¬ ΚΆ±»±μΟφΜΐΘ§“‘κΡΖ÷Ή”ΈΣ≈δΧεΒΡΫπ τκΡΙ«ΦήΫϋΡξά¥“≤»ΓΒΟΝΥΆΜΤΤ–‘ΒΡ≥…Ιϊ[50Θ§51]ΓΘ


”κ¥ΪΆ≥ΕύΩΉ≤ΡΝœœύ±»Θ§κΡΜυΕύΩΉ≤ΡΝœΨΏ”–“‘œ¬ΧΊΒψΘ®ΖΫΑΗ 2Θ© Ήœ»Θ§κΡΩ…“‘ΉςΈΣ ÷–‘≈δΧεΘ§”Ο”Ύ÷Τ±ΗΕ‘ΩΆΧεΖ÷Ή”ΨΏ”–ΗΏΕ‘”≥―Γ‘ώ–‘ΒΡΕύΩΉ≤ΡΝœ[28]Θ§Ω…”Ο”Ύ ÷–‘Ζ÷άκΚΆ¥ΏΜ·[52]Τδ¥ΈΘ§κΡ÷ςΝ¥ΈΣΑκΗ’–‘Θ§Ά§ ±ΨΏ”–“ΜΕ®ΒΡ»α–‘Θ§“ρ¥Υ“‘κΡ≈δΧεΈΣΙ«ΦήΒΡκΡΜυΕύΩΉ≤ΡΝœΩ… ”ΈΣΓΑΨßΧεΚΘΟύΓ±Θ§Τδ–ΈΉ¥ΚΆΩΉΨΕΩ…ΥφΆβΫγ¥ΧΦΛΕχΕ·Χ§±δΜ·Θ§¥”Εχ”–ΆϊΚœ≥…ΨΏ”–ΕάΧΊΙΠΡήΒΡ÷«Ρή≤ΡΝœ[34Θ§46]ΒΎ»ΐΘ§Ά®ΙΐΩΊ÷ΤΝ¥≥ΛΚΆ≤ύΝ¥œύΜΞΉς”ΟΘ§Ω…“‘Κœάμ…ηΦΤκΡΜυΕύΩΉ≤ΡΝœΘ§ΜώΒΟ»Έ“βΒΡΩΉΨΕΚΆ–‘÷ [35Θ§39]Θ§Ηϋ÷Ί“ΣΒΡ «ΥϋΟ«ΨΏ”–…ζΈοœύ»ί–‘«“ΕΨ–‘ΒΆΘ§¥”Εχ‘ΎΈϋΗΫΖ÷άκΓΔ¥ΏΜ·ΓΔ“©Έο δΥΆΓΔΡήΝΩ¥φ¥Δ”κΖΔΒγΒ»ΗςΗωΝλ”ρ’Ιœ÷≥ωΨό¥σΒΡ”Π”Ο«ΑΨΑΓΘ
”…ΕΰκΡΚΆ»ΐκΡΉ‘ΉιΉΑΒΡΕύΩΉ≤ΡΝœ
ΨΏ”–Ζ÷Ή”¥σ–ΓΩΉΨΕΒΡΕΰκΡΜυ≤ΡΝœ‘ΎΖ÷Ή”Ζ÷άκ÷–ΨΏ”–÷Ί“Σ“β“ε[53®C55]Θ§Εΰ―θΜ·ΧΦΒΡ≤ΕΜώ[56]ΓΔ¥ΔΤχΩβ[57®C59]ΚΆΙΠΡή…η±Η[60]ΕΰκΡ «“Μ÷÷“Ή”ΎΜώΒΟΒΡΙΙΫ®ΩιΘ§Ω…Ά®Ιΐ≥§Ζ÷Ή”Ή‘ΉιΉΑΙΙΫ®Έ»Ε®ΒΡΕύΩΉ≤ΡΝœΓΘΆ®ΒάΡΎΒΡΙ≤ΫαΨß»ήΦΝΆ®≥ΘΩ…“‘Άξ»Ϊ»Ξ≥ΐΘ§Εχ≤ΜΜαΤΤΜΒΕύΩΉΕΰκΡΨßΧεΒΡΩ’ΦδΫαΙΙΓΘΕύΩΉΕΰκΡΒΡΩΉΨΕœύΕ‘Ϋœ–ΓΘ§ΩΉΟήΕ»ΗΏΘ§¥”ΕχΨΏ”–ΫœΗΏΒΡ±μΟφΜΐΚΆΩΉœΕ¬ [49]ΓΘ
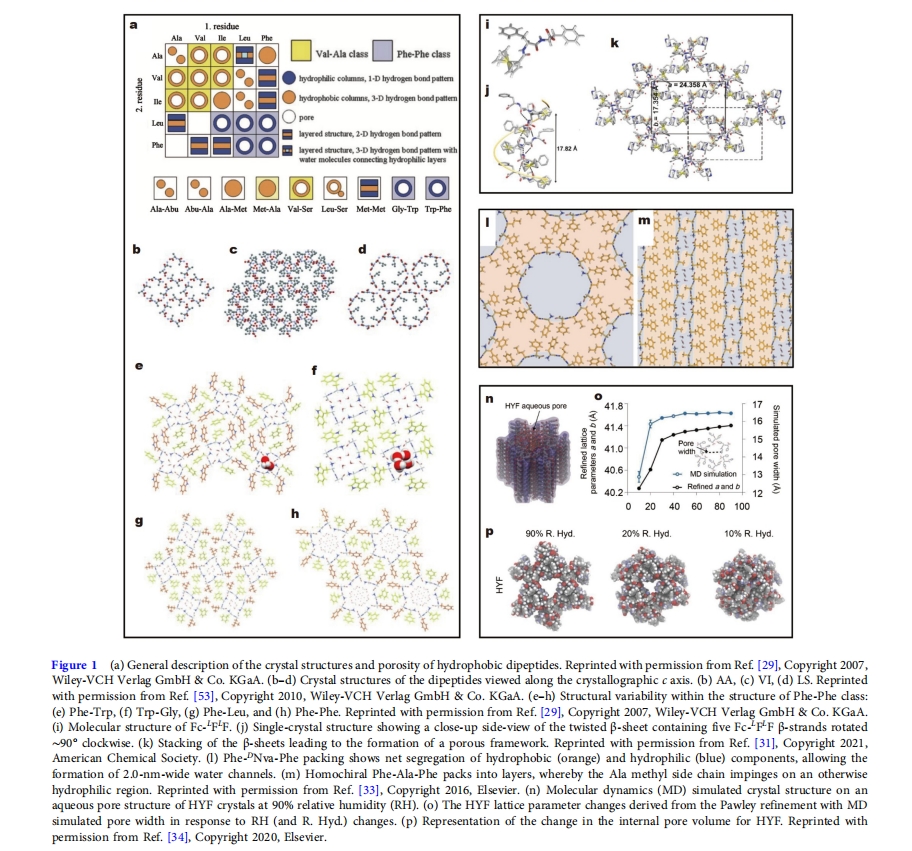
1996 ΡξΘ§Görbitz ΚΆ Gundersen[61]ΖΔœ÷Κ§”–ΝΫΗω ηΥ°≤–ΜυΒΡΕΰκΡVal-AlaΘ®VAΘ©ΨΏ”–ΓΑΩ’÷––ΡΆ®ΒάΓ±ΒΡΨßΧεΫαΙΙΘ§≤ΔΆΤ≤βΤδΥϊ ηΥ°ΕΰκΡ“≤Μα”–άύΥΤΒΡΫαΙΙΓΘ’β «ΙΊ”ΎΕύΩΉΕΰκΡΨßΧεΒΡ Ή¥Έ±®ΒάΘ§ΈΣΕΰκΡΕύΩΉ≤ΡΝœΒΡ―–ΨΩΒλΕ®ΝΥΜυ¥ΓΓΘ’ΐ»γΆΤ≤βΒΡΡ«―υΘ§GörbitzΖΔœ÷ΤδΥϊΝυ÷÷ ηΥ°ΕΰκΡ“≤ΨΏ”– ηΥ°ΩΉΚΆœύΆ§ΒΡ3D«βΦϋΆχ¬γΓΘ ηΥ°≤ύΝ¥‘Ύ’β–©ΫαΙΙ÷––Έ≥…”κΝυ±Ώ–Έ÷αΤΫ––ΒΡΆ®ΒάΡΎ±μΟφ[62]ΓΘ“ρ¥Υ’β–©ΕΰκΡ±ΜΆ≥≥ΤΈΣ VA άύΕύΩΉΕΰκΡΘ®ΆΦ 1aΘ©VA άύ «Εά“ΜΈόΕΰΒΡΘ§“ρΈΣΩ…“‘‘Ύ≤ΜΤΤΜΒκΡΥό÷ς÷ßΦήΒΡ«ιΩωœ¬»Ξ≥ΐΆ®ΒάΡΎΒΡΙ≤ΫαΨß»ήΦΝΖ÷Ή”ΓΘ
ΒΎΕΰ÷÷ΕΰκΡΕύΩΉ≤ΡΝœ≥ΤΈΣ Phe-Phe (FF) άύΓΘΥϋΟ«ΨΏ”–“ΜΈ§«βΦϋΚΆ«ΉΥ°Ά®ΒάΘ§≤Δ«“Μυ”ΎΨΏ”–Ϋœ¥σ≤ύΜυΒΡ≤–ΜυΘ§άΐ»γ LeuΓΔPhe ΚΆ Trp (ΆΦ 1aΓΔe-h)ΓΘΕύΩΉFFΡ…ΟΉΙήΨΏ”–Ζ«Ζ≤ΒΡΜζ–Β«ΩΕ»Θ§“‘ΦΑΗΏΜ·―ßΚΆ»»Έ»Ε®–‘ΓΘΥϋΟ«“―±Μ”ΟΉς÷ΐ‘λ“χΡ…ΟΉœΏΒΡΡΘΑε[63]ΉςΈΣ“©Έο δΥΆΒΡΡ…ΟΉ‘ΊΧε[64]Μρ…ζ≥Λ‘ΎΒγΦΪ…œ”Ο”Ύ¥ΔΡή[65]ΚΆ“Μ¥ζ[66]ΓΘ
FF Ω…“‘Ά®ΙΐΤδΥϊΙΠΡήΉιΫχ“Μ≤Ϋ–ό ΈΓΘΆθΒ»»ΥΓΘ[»ΐ °Θ§31]±®ΒάΝΥ‘ΎκΡΒΡCΡ©ΕΥ“ΐ»κΕΰΟ·ΧζΘ®FcΘ©ΜυΆ≈ΓΘΕΰΟ·Χζ-Εΰ±Ϋ±ϊΑ±ΥαΘ®Fc-FFΘ©κΡΩ…“‘”κΕΰΦέΦΉΜυΏΏύΚΖ¥άκΉ”Ή‘ΉιΉΑ≥…ΕύΩΉΨßΧεΓΘΨßΧεΒΡΜυ±ΨΫαΙΙ «¬ί–ΐΉ¥ΒΡFc-FFΕΰΨέΧεΘ§”…κΡCΡ©ΕΥΒΡ ÷–‘ΕΰΑΖΚΆΥ°Ζ÷Ή”Έ»Ε®Ά®Ιΐ«Ω«βΦϋΚΆΨ≤ΒγœύΜΞΉς”ΟΘ®ΆΦ 1i®CkΘ©ΓΘ ÷–‘‘ΎΫαΨßΙΐ≥Χ÷–ΤπΉ≈÷ΝΙΊ÷Ί“ΣΒΡΉς”ΟΓΘFc-¥σΚ≈F¥σΚ≈FΚΆΡξ¥ζ-(+)-2-ΦΉΜυΏΏ‘ζ“ρ (S-MP) Μρ Fc-Β¬FΒ¬FΚΆR-(−)-2-ΦΉΜυΏΏ‘ζ“ρ (R-MP)Θ§ΕχΕ‘”Ύ Fc-¥σΚ≈F¥σΚ≈F ΚΆ R-MP ΜρFc-Β¬FΒ¬FΚΆ S-MPΘ§ΟΜ”––Έ≥…ΨßΧεΓΘFc-¥σΚ≈F¥σΚ≈F ΚΆ S-MP ≥ œ÷“ΜΈ§ΫΜ≤φ Π¬ ΦΙ÷υΘ§ « Fc-¥σΚ≈F¥σΚ≈F ΨΏ”–Ήσ ÷–‘ΓΘΕχ Fc-Β¬FΒ¬F ΚΆ R-MP ≥ œ÷ Fc-Β¬FΒ¬F ΒΪ”Ο”“ ÷[31]ΓΘ
Ήι≥…κΡΒΡΑ±ΜυΥαΒΡ ÷–‘“≤Μα”ΑœλΕύΩΉΫαΙΙΒΡ–Έ≥…[32Θ§33Θ§67]. Marchesan ΒΡΆ≈Ε”[33]…ηΦΤΝΥ“ΜœΒΝ– ηΥ°¥σΚ≈ΓΣ±Ϋ±ϊΑ±ΥαΓΣΒ¬- «ΒΡ-¥σΚ≈-Phe »ΐκΡΘ§Τδ÷– d-Xaa «Β¬-÷§ΖΨΉεΑ±ΜυΥαΓΘΒΞΨßX…δœΏ―ή…δΘ®XRDΘ© ΐΨίœ‘ Ψ“λ ÷–‘»ΐκΡΚΆΆ§ ÷–‘»ΐκΡΒΡΑϋΉΑ¥φ‘Ύœ‘÷χ≤ν“λΓΘΕ‘”Ύ±Ϋ±ϊΑ±Υα-Β¬-Nva-Phe «“Μ÷÷ΨΏ”–ΕύΩΉΥ°Ά®ΒάΒΡΝΫ«ΉΙΙœσΘ§»γΆΦΥυ ΨΆΦ 1lœύΖ¥Θ§Ά§ ÷–‘»ΐκΡ Phe-Ala-Phe –Έ≥…÷¬ΟήΒΡ≤ψΉ¥ΫαΙΙΘ®ΆΦ1mΘ©ΓΘ
”κΕΰκΡœύ±»Θ§»ΐκΡΒΡ÷ςΝ¥”…”Ύ–ρΝ–Ϋœ≥ΛΕχΗϋΦ”»α»ΆΘ§“ρ¥Υ»ΐκΡΉιΉΑ–Έ≥…ΒΡΙ«ΦήΫαΙΙΗϋΦ”»α»ΆΘ§Ω…“‘ΨΏ”–ΧΊΕ®ΒΡΝΠ―ßΚΆΩΉœΕ–‘÷ ΓΘάΐ»γΘ§Ulijn Ά≈Ε”[34]±®ΒάΝΥΥΡ÷÷»ΐκΡ–ρΝ–HYF (His-Tyr-Phe)ΓΔYFH (Tyr-Phe-His)ΓΔΒμΖέΜ·DYF (Asp-Tyr-Phe-NH 2 )ΚΆYFD (Tyr-Phe-Asp-NH 2 )ΒΡΉ‘ΉιΉΑΓΘΖ÷±πΒΟΒΫΝΥHYFΓΔDYFΚΆYFDΒΡ’κΉ¥ΨßΧε“‘ΦΑYFHΒΡΈόΕ®–ΈΨέΦ·ΧεΓΘ―–ΨΩΝΥ≤ΡΝœΕ‘≤ΜΆ§œύΕ‘ ΣΕ»±δΜ·ΒΡΫαΙΙœλ”ΠΓΘ―–ΨΩΖΔœ÷Θ§‘ΎΡ…ΟΉΕύΩΉ»ΐκΡΨßΧεΒΡ’τΖΔ”’ΒΦ«ΐΕ·Ιΐ≥Χ÷–Θ§Υ°-«βΦϋΒΡΦ”«Ω¥ΌΫχΝΥΡήΝΩΉΣ“Τ≤Δ«ΐΕ·ΩΉΨΕ ’ΥθΓΘΕ‘»ΐ÷÷ΨßΧε»ΐκΡΒΡ±»ΫœΖΔœ÷Θ§HYF–Έ≥…ΒΡΥ°ΩΉΫαΙΙΨΏ”–Ηϋ«ΩΒΡ«βΦϋΆχ¬γΘ§“ρ¥ΥΘ§HYF‘Ύ”ΟΉςΥ°œλ”Π(WR)≤ΡΝœ ±“≤ΨΏ”–ΗϋΗΏΒΡΡήΝΩΟήΕ»Θ®ΆΦ 1nΘ§oΘ©ΓΘ
ΕύκΡΉ‘ΉιΉΑΕύΩΉ≤ΡΝœ
”κΕΰκΡΚΆΙ―κΡœύ±»Θ§ΕύκΡ”…”ΎΉι≥…Α±ΜυΥα ΐΝΩΫœΕύΘ§ΨΏ”–Ηϋ¥σΒΡΩ……ηΦΤ–‘ΚΆΝιΜν–‘ΓΘΉ‘ΉιΉΑ–ΈΧ§≤ΜΫω»ΓΨω”ΎΑ±ΜυΥα–ρΝ–Θ§ΜΙ»ΓΨω”ΎΤδΕΰΦΕΫαΙΙΚΆΜ·―ß–ό Έ[68]ΓΘ
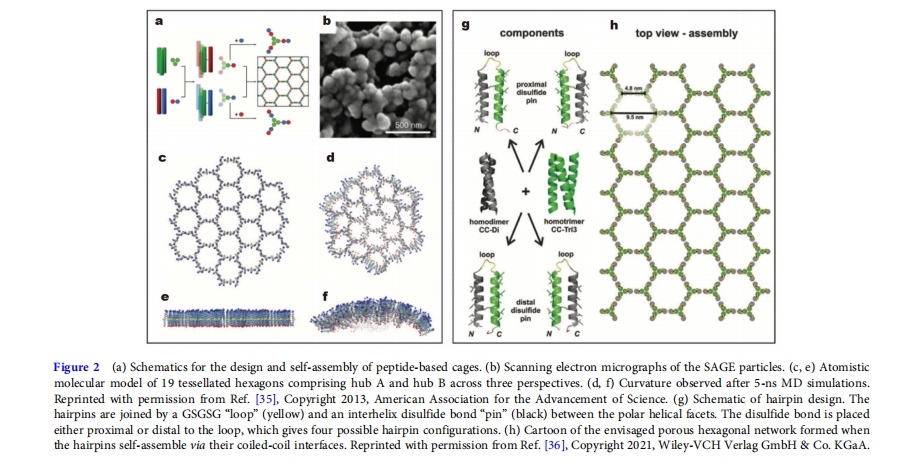
2013 ΡξΘ§Woolfson Ά≈Ε”[35]Χα≥ωΝΥΉ‘ΉιΉΑΝΐΉ¥Ω≈ΝΘ SAGE ΒΡ…ηΦΤΘ§ΗΟΩ≈ΝΘ”…ΝΫΗωΨμ«ζ¬ί–ΐκΡΜυ–ρΓΔ“ΜΗω“λΕΰΨέΧεΚΆ“ΜΗωΆ§»ΐΨέΧε…ηΦΤΕχ≥…ΓΘΝΫ÷÷κΡΕΦΚ§”–Ω…“‘Ά®ΙΐΕΰΝρΦϋΝ§Ϋ”ΒΡΑκκΉΑ±Υα≤–ΜυΘ§“ρ¥Υ»ΐΨέΧε–Έ≥…Νυ±Ώ–ΈΆχ¬γΒΡΕΞΒψΘ§ΕΰΨέΧεΉςΈΣΤδ±Ώ‘ΒΘ®ΆΦ 2aΘ©ΓΘ’β–©≥…Ζ÷Ζ«≥ΘΝιΜνΘ§Ω…“‘–Έ≥…÷±ΨΕΈΣ100Ρ…ΟΉΘ®ΆΦ2b-fΘ©ΉνΫϋΘ§Woolfson ΒΡ―–ΨΩ–ΓΉι[36]Χα≥ωΝΥ“Μ÷÷–¬–ΆκΡœΒΆ≥Θ§Ά®Ιΐ‘ΎΝΫΗωΕΰΦΕΫαΙΙ‘ΣΥΊ÷°ΦδΖ≈÷ΟΓΑΕΰΝρΦϋœζΓ±Θ§Ω…“‘–Έ≥…Ρ…ΟΉΩ≈ΝΘΜρΕύΩΉΤ§ΓΘΥϊΟ« Ι”Ο GSGSG –ρΝ–Ν§Ϋ”ΝΫΗωΉ‘ΉιΉΑΨμ«ζ¬ί–ΐ 3 ΤΏκΡΙΙΫ®ΩιΘΚΆ§–ΆΕΰΨέΧε (CC-Di) ΚΆΆ§–Ά»ΐΨέΧε (CC-Tri3)Θ®ΆΦ 2gΓΔhΘ©ΓΘœζΕΛΒΡΈΜ÷ΟΕ‘ΥυΒΟ≥§Ζ÷Ή”ΉιΉΑΧεΒΡΆΊΤΥΫαΙΙ”–÷Ί¥σ”ΑœλΓΘΫϋΕΥΝ§Ϋ”ΒΡΕΰΝρΦϋ≤ζ…ζΖβ±’ΒΡ«ρ–ΈΈοΧεΘ§Τδ÷±ΨΕΈΣ~100Ρ…ΟΉΘ§Εχ‘ΕΕΥΝ§Ϋ”ΒΡΕΰΝρΦϋ‘ρ–Έ≥…Τ§Ή¥ΉιΉΑΓΘ
≤Χ œ―–ΨΩΉι[37Θ§38]±®ΒάΝΥ 1:1 ΠΝ/¥σΚ≈-Μ«θΘΜυ-ΠΟ-AA ‘”Μ·κΡΘ§œ‘ Ψ≥ωΟς»ΖΒΡ«βΦϋ”“–ΐ¬ί–ΐΓΘ¥ΥΆβΘ§ΨßΧεΕ―Μΐ±μΟς«βΦϋ 1D ΫαΨßκΡΙ«Φή (HPF) ”…ΆΖΈ≤Ζ÷Ή”ΦδΚΆΖ÷Ή”ΡΎ«βΦϋ±Θ≥÷ΓΘΆ®Ιΐ“ΐ»κΦρΒΞΒΡΙ≤ΦέΫ”ΆΖΩ…“‘–Έ≥…ΕΰΨέΧε’έΒΰΓΘΆ®ΙΐΙΧΕ®Ι≤ΦέθΘΑΖΦϋΘ§ΕΰΨέΧε±μœ÷≥ωά≠Ν¥Ή¥»ΐΦΕΫαΙΙ (ΆΦ 3aΆ®ΙΐΙψΖΚΒΡΖ÷Ή”Φδ«βΦϋΘ§Ω…“‘–Έ≥…ΕΰΈ§≥§Ζ÷Ή”Άχ¬γΘ§»γΆΦΥυ ΨΆΦ 3bΘ§»ΜΚσΫΪΤδΉιΉΑ≥…ΗϋΗΏ”––ρΒΡ»ΐΈ§ΕύΩΉΩρΦήΓΘ
ΉνΫϋΘ§Nguyen ΒΡΆ≈Ε”[39]άϊ”Ο ηΥ°–‘Π–Ε―Μΐ≤–Μυ–ό ΈΒΡΈ»Ε®ΠΝ-¬ί–ΐΫαΙΙΘ§ΙΙΫ®ΝΥ“ΜΗωΙΠΡή–‘ΕύΩΉκΡΩρΦήUIC-1Θ®ΆΦ 3cΘ©ΓΘΠΝ-¬ί–ΐΕΰΦΕΫαΙΙΧαΙ©ΝΥ–μΕύΕάΧΊΒΡΈΜ÷ΟΘ§Ω…Ά®Ιΐ≤ύΝ¥ΒΡΙφ‘ρΤΏκΡ≈≈Ν–Ϋχ––Βς’ϊΘ®ΆΦ 3d‘≤Εΰ…ΪΤΉΆΦœ‘ ΨUIC-1’έΒΰ≥…ΠΝ¬ί–ΐΫαΙΙΘ®ΆΦ 3e,fUIC-1ΒΡΨßΧεΫαΙΙœ‘ ΨΝΥΤδ¥σ–ΆΨΊ–ΈΈόœόΆ®ΒάΒΡΨßΗώΘ®ΆΦ3gΘ©ΓΘ”…”ΎΥϋΜυ”ΎΫœ≥ΛΒΡκΡΘ®Ψ≈ΗωΑ±ΜυΥαΘ©Θ§“ρ¥ΥΜΙΩ…“‘ΗϋΚœάμΒΊΗΡ±δΥϋ“‘“ΐ»κ–¬ΒΡΙΠΡήΜυΆ≈Θ§Ά§ ±±ΘΝτ“ΜΑψΒΡΩρΦήΫαΙΙΓΘΉν÷Ί“ΣΒΡ «Θ§UIC-1 ”––μΕύΈΜΒψά¥”≈Μ·ΩΉΙΠΡήΘ§≤ΔΡήΆ§ ±»ί»ΧΕύ÷÷ΙΠΡή±δΜ·ΓΘ¥ΥΆβΘ§UIC-1ΓΔUIC-1-B5MΘ®ΒΎΈεΗω≤–ΜυΆΜ±δΈΣΒΑΑ±ΥαΘ©ΓΔUIC-1-B7MΘ®ΒΎΤΏΗω≤–ΜυΆΜ±δΈΣΒΑΑ±ΥαΘ©ΚΆ UIC-1-B5DΘ®ΒΎΈεΗω≤–ΜυΆΜ±δΈΣΧλΕ§Α±ΥαΘ©ΨßΧεΕ‘ MeCN ÷–ΒΡΡα¬όΚλ±μœ÷≥ω≤ΜΆ§ΒΡΈϋΗΫΡήΝΠΘ§±μΟς UIC-1 ΨßΧεΒΡΫαΙΙΩ…“‘Ά®ΙΐΒςΫΎά¥ΜώΒΟΕ‘ΩΆΧεΖ÷Ή”ΒΡ”≈“λΒΡΈϋΗΫ–‘ΡήΓΘ
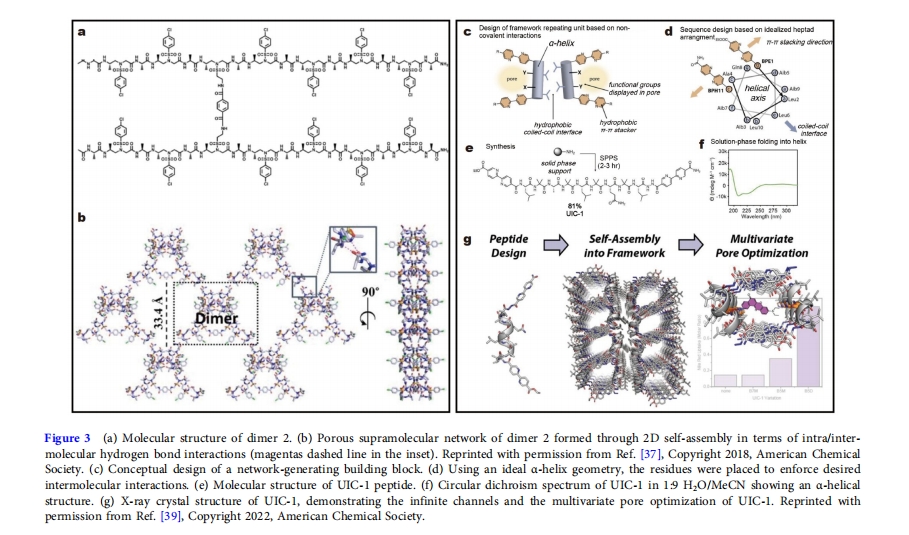
Ϋπ τκΡΙ«Φή (MPF)
MOF «“Μ÷÷ΕύΩΉ”–Μζ-ΈόΜζ‘”Μ·ΨßΧε≤ΡΝœΘ§ΨΏ”–ΫœΗΏΒΡ±»±μΟφΜΐΚΆΩΉœΕ¬ [69Θ§70],‘ΎΙβ―ßΓΔΤχΧε¥Δ¥φ”κΖ÷άκΓΔΕ‘”≥ΧεΖ÷άκΓΔ¥ΏΜ·ΓΔΜ·―ߥΪΗ–ΓΔ“©Έο δΥΆΒ»Νλ”ρ’Ιœ÷≥ωΨό¥σΒΡ«±ΝΠΓΘMPFs «–¬“Μ¥ζΒΡMOFsΘ§ΕύκΡΒΡ…ζΈοœύ»ί–‘ ΙΒΟMPFsΡήΙΜΦθ…ΌΕ‘…ζΧ§ΜΖΨ≥ΒΡ≤Μάϊ”ΑœλΓΘ”κΤδΥϊMOFsœύ±»Θ§MPFsΨΏ”–«ΑΥυΈ¥”–ΒΡΫαΙΙ»α»Ά–‘Θ§ΡήΕ‘ΜΖΨ≥ΒΡ±δΜ·±μœ÷≥ω≤ΜΆ§ΒΡœλ”ΠΓΘΒ±»ήΦΝΩΆΧε≥ΐ»ΞΚσΘ§Η’–‘MPFsΟΜ”–Β·–‘±δ–ΈΘ§Εχ»α–‘MPFs‘ρ±μœ÷≥ωΉ‘ ”ΠΒΡΩΉœΕ¬ ΓΘΕύκΡ≈δΧεΒΡ ÷–‘“‘ΦΑΤδΥυΚ§ΒΡΕύ÷÷ΙΠΡήΜυΆ≈ ΙΒΟMPFsΨΏ”–ΙψάΪΒΡ”Π”Ο«ΑΨΑ[71]ΓΘ
ΕύκΡ”κΫπ τάκΉ””–Εύ÷÷≈δΈΜΖΫ ΫΘΚΑ±Μυ-N‘≠Ή”Ω…“‘Ά®Ιΐ”κτ»Μυ-O‘≠Ή”ρϋΚœ”κΫπ τάκΉ”≈δΈΜ[40Θ§51Θ§72®C76]ΜρΒΞ≥ί–Έ Ϋ[46Θ§75Θ§77Θ§78]≥ΐΝΥN,O-ρϋΚœΖΫ ΫΆβΘ§τ»Μυ-O‘≠Ή”ΜΙΩ…“‘Ά®ΙΐΒΞ≥ίΖΫ Ϋ”κΫπ τάκΉ”≈δΈΜ[40Θ§46Θ§73®C75Θ§77®C79]Μρ syn-syn «≈Ϋ”[40Θ§80]¥ΥΆβΘ§Α±ΜυΥα÷–ΒΡΧΊΕ®ΙΠΡήΜυΆ≈“≤Ω…“‘≤Έ”κ”κΫπ τάκΉ”ΒΡ≈δΈΜΘ§»γHisΖ÷Ή”÷–ΒΡΏδΏρΜυ-N‘≠Ή”“≤Ω…“‘”κΫπ τάκΉ”“‘ΒΞ≥ί≈δΈΜ[76Θ§77]Μρ”κΑ±Μυ-N‘≠Ή”ΚΆ―«Α±Μυ-N‘≠Ή”ρϋΚœ[45Θ§46Θ§76]Κœάμ…ηΦΤΕύκΡΒΡΑ±ΜυΥα–ρΝ–Ω…“‘ΧΊ“βΈΣΫπ τάκΉ”ΧαΙ©ΫαΚœΈΜΒψΘ§»γAspΓΔGluΩ…“‘ΧαΙ©ΫœΕύΒΡO‘≠Ή”ΫαΚœΈΜΒψΘ§HisΩ…“‘ΧαΙ©ΫœΕύΒΡN‘≠Ή”ΫαΚœΈΜΒψΘ§‘ΎΑ±ΜυΥα÷–“ΐ»κΏΝύΛΜυ“≤Ω…“‘ΫΪΫπ τάκΉ”≈δΈΜΒΫΏΝύΛΜυ-N‘≠Ή”…œ[47]Θ§’β «Ϋπ τάκΉ”ΒΡ≥ΘΦϊ≈δΈΜΒψ[47Θ§50]ΓΘ
≤ΜΆ§ΒΡΫπ τάκΉ””κΆ§“Μ÷÷ΕύκΡΫαΚœΘ§Μα–Έ≥…≤ΜΆ§ΒΡΫαΙΙΚΆ–‘÷ ΓΘGly-Asp”κZn 2+≈δΈΜ–Έ≥…ΕΰΈ§MPFΘ§Τδ÷–Zn 2+ΈΣΈε≈δΈΜ[40]ΗΟΕΰκΡΫΪΥΡΗωZn 2+Ά®ΙΐNΓΔOρϋΚœ”κGlyΜυΆ≈Ν§Ϋ”Θ§≤Δ”κAspΜυΆ≈…œΒΡτ»Μυ-O‘≠Ή”ΒΞ≥ίΫαΚœΓΘ”κZn 2+œύ±»Θ§Co2+ΕύΝΥ“ΜΗωΫπ τΫαΚœΈΜΒψΓΘ‘ΎCo(Gly-Asp)÷–Θ§Co 2+ΈΣΝυ≈δΈΜΓΘ÷ΒΒΟΉΔ“βΒΡ «Θ§Co2+≥ΐΝΥ”κNΓΔOρϋΚœΘ§”κτ»Μυ-O‘≠Ή”ΒΞ≥ίΫαΚœΆβΘ§ΜΙ”κAspΜυΆ≈…œΒΡΝΫΗωτ Μυ-O‘≠Ή”ρϋΚœΘ§–Έ≥…ΕάΧΊΒΡΤΏ‘ΣΜΖΓΘ
MOF ΩΉœΕΕ»ΒΡ ”Π–‘Ω…“‘Ά®ΙΐΫπ τ≈δΈΜΦΗΚΈ–ΈΉ¥ΚΆΝ§Ϋ”ΧεΒΡΉ‘”…Ε»ά¥ΨωΕ®[81]MPFΩ…“‘ΗυΨίκΡ≤ύΝ¥ΒΡ–‘÷ ά¥œ‘ ΨΫαΙΙΒΡΦαΙΧ–‘ΜρΝιΜν–‘[71]. Zn(Gly-Thr) 2”…≈δΈΜ–Έ≥…–Ω2+ΕχGly-ThrΨΏ”–Βδ–ΆΒΡΗ’–‘ΕύΩΉΫαΙΙΘ®ΆΦ 4a, bΘ©[41]ΟΩΗωZn 2+Ά®ΙΐNΓΔOρϋΚœΘ§”κΝμΆβΝΫΗωΕΰκΡΒΡτ»Μυ-O‘≠Ή”ΒΞ≥ίΫαΚœΘ§”κΝΫΗωΕΰκΡ≈δΈΜΘ§–Έ≥…≈Λ«ζΒΡΑΥΟφΧεΙΙ–ΆΓΘThr≤ύΝ¥…œΒΡτ«ΜυΩ…“‘Φ”«Ω”κΑ±ΜυΒΡ«βΦϋœύΜΞΉς”ΟΘ§‘Ύ≤ψΡΎΚΆ≤ψΦδ–Έ≥…«βΦϋΆχ¬γΘ§”––ßΧαΗΏ»ΐΈ§ΫαΙΙΒΡ–≠Ά§Ής”ΟΚΆΈ»Ε®–‘ΓΘ≥ιΩ’»ήΦΝΚσΘ§Zn(Gly-Thr) 2»‘±Θ≥÷ΤδΫαΨß–‘ΚΆΩΉœΕ¬ Θ§≤ΔΕ‘CO 2 /CH 4±μœ÷≥ωΈϋΗΫ―Γ‘ώ–‘ΓΘ¥ΥΆβΘ§Ής’ΏΚœ≥…ΝΥΚώΕ»ΈΣ0.67 Ρ…ΟΉΆ®Ιΐ…υΜζ–ΒΑΰάκΩιΉ¥ΚξΙέΨßΧεΘ®ΆΦ 4cΘ©ΓΘ
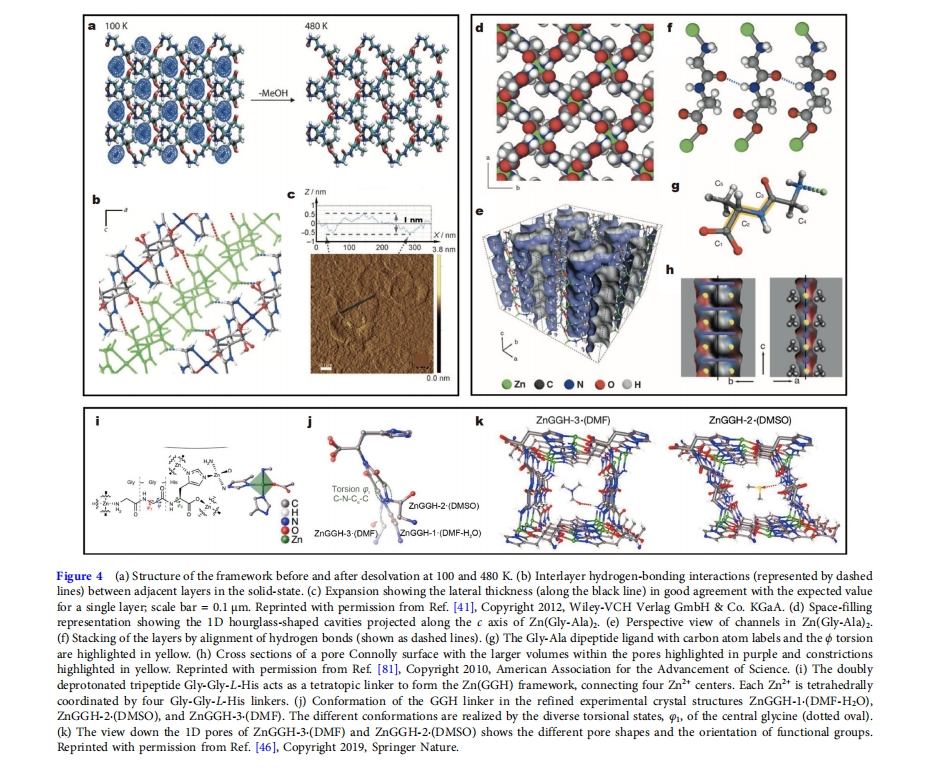
œύΖ¥Θ§Zn(Gly-Ala) 2ΟΜ”–τ«ΜυΘ§“ρ¥ΥΟΜ”–ΕνΆβΒΡ«βΦϋ[81]ΟΩΗωZn 2+ΒΞ≥ίΜ·ΚœΈο”κΝΫΗωΕΰκΡΒΡΑ±Μυ-N‘≠Ή”ΚΆΝμΆβΝΫΗωΕΰκΡΒΡτ»Μυ-O‘≠Ή”–Έ≥…ΥΡΟφΧεΙΙ–ΆΘ®ΆΦ4d-hΘ©ΓΘ≥ιΩ’»ήΦΝΚσΘ§Zn(Gly-Ala) 2ΒΡΩΉΫαΙΙΥζœί±’ΚœΘ§ΫαΨßΕ»ΚΆΩΉœΕ¬ ¥σΖυΫΒΒΆΓΘΒΪΒ±”κ CO 2Μρ CH 3 OH Β»ΦΪ–‘Ζ÷Ή”Ϋ”¥Ξ ±Θ§Zn(Gly-Ala) 2Μα÷πΫΞΜ÷Η¥‘≠”–ΒΡΕύΩΉΫαΙΙΓΘΕΰκΡΒΡΒΆΡή≈ΛΉΣΩΊ÷ΤΦΉΜυΒΡΈΜ÷ΟΘ§¥”Εχ≤ζ…ζΉ‘ ”ΠΒΡΩΉœΕ¬ ΓΘ‘ΎΜυ”Ύ»ΐκΡΒΡ MPF ÷–“≤Ιέ≤λΒΫΝΥ”κ MPF άύΥΤΒΡΓΑΚΘΟύΉ¥––ΈΣΓ±[45Θ§46]Ε‘”Ύ Zn(Gly-Gly-His) (ΆΦ4i-kΘ©[46]Θ§ΟΩΗω Zn 2+ΕΦ «ΒΞ≥ίΜ·ΚœΈοΘ§”κΥΡΗω»ΐκΡΝ§Ϋ”Ά®Ιΐ“ΜΗωΑ±Μυ-N‘≠Ή”ΓΔ“ΜΗωτ»Μυ-N‘≠Ή”ΚΆΝΫΗωΏΝύΛΜυ-N‘≠Ή”–Έ≥…ΥΡΟφΧε≈δΈΜΓΘ‘Ύ“ΜΕ®ΒΡ»ήΦΝΧθΦΰœ¬Θ§Zn(Gly-Gly-His)ΡήΜ·―ß“ΐΖΔΕύκΡΙΙœσ±δΜ·Θ§–Έ≥…9÷÷≤ΜΆ§ΒΡΨßΧεΫαΙΙΘ§Αϋά®8÷÷»ήΦΝΜ·ΨßΧεΚΆ1÷÷ΥζœίΨßΧεΓΘZn(Gly-Gly-His)Ω…Ά®ΙΐΒΑΑΉ÷ ΒΡΒΞΦϋ–ΐΉΣ÷Ί–¬Βς’ϊΩΉ–ΈΚΆΖ«Ι≤ΦέΦϋΡΘ ΫΘ§ Βœ÷Ε‘–ΓΖ÷Ή”ΩΆΧεΈϋΗΫΒΡΒςΩΊΓΘ
κΡΜυΕύΩΉ≤ΡΝœΒΡ”Π”Ο
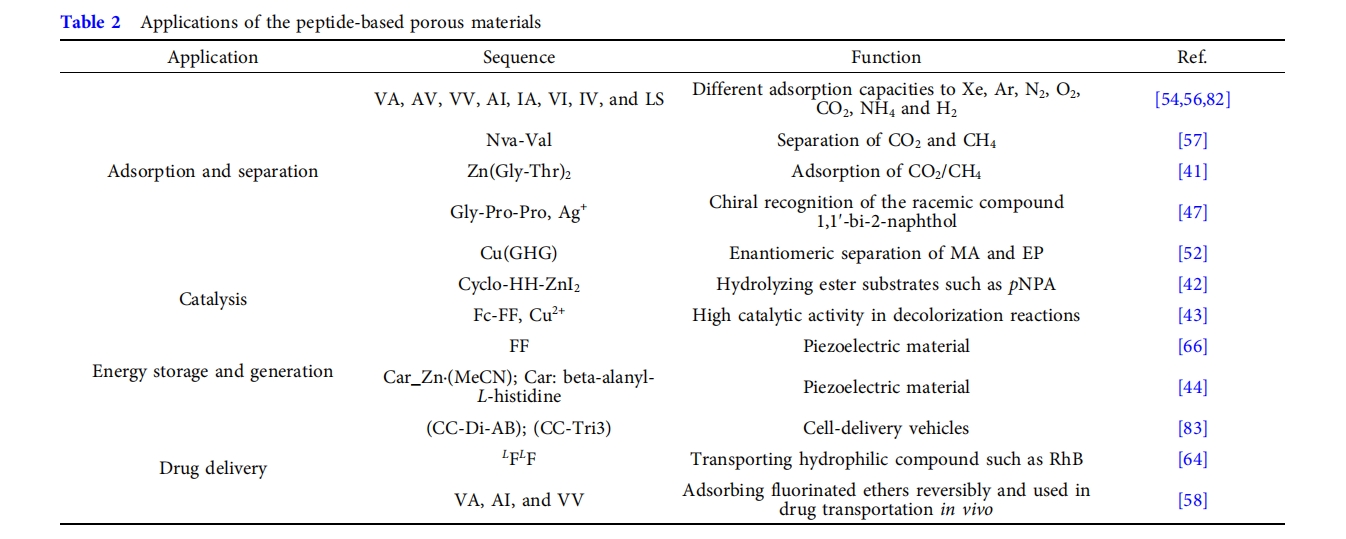
ΦΗΚθΈόœόΒΡ–ρΝ–Ω…Ρή–‘ ΙΒΟκΡΨΏ”–ΙψάΪΒΡΖΔ’Ι«ΑΨΑΓΘ’βάοΘ§Έ“Ο«ΫΪΉήΫα”Ο”ΎΈϋΗΫΓΔΖ÷άκΓΔ¥ΏΜ·ΓΔ¥ΔΡήΚΆ“©ΈοΒίΥΆΒΡκΡΜυΕύΩΉ≤ΡΝœΒΡΉν–¬Ϋχ’ΙΘ§Τδ÷–“Μ–©κΡΩ…“‘‘Ύ±μ 2ΓΘ
ΈϋΗΫΖ÷άκ
―–ΨΩΖΔœ÷Θ§κΡΜυΕύΩΉ≤ΡΝœΕ‘≤ΜΆ§Έο÷ ΒΡΈϋΗΫΡήΝΠ≤ΜΆ§Θ§ΫχΕχΨΏ”–Ά®ΙΐΈϋΗΫΖ÷άκ≤ΜΆ§Έο÷ ΒΡ«±ΝΠΓΘ―–ΨΩ»Υ‘±“―Ψ≠Ε‘ΤχΧεΈϋΗΫΚΆΖ÷άκΫχ––ΝΥ―–ΨΩ[29Θ§41Θ§53Θ§54Θ§59Θ§77Θ§82]“‘ΦΑ ÷–‘Ε‘”≥ΧεΒΡΖ÷άκ[47Θ§52Θ§72]ΓΘ
‘ΎΤχΧεΖ÷άκΖΫΟφΘ§«ΑΤΎ―–ΨΩ“―Ψ≠÷ΛΟςΝΥΕΰκΡΨßΧεΕ‘XeΓΔArΓΔN 2ΓΔO 2ΓΔCO 2ΓΔNH 4ΚΆH 2Β»ΤχΧεΒΡΈϋΗΫ–‘Ρή [29Θ§53Θ§54Θ§59Θ§82].IVΚΆVI±Μ»œΈΣ «ΈϋΗΫH2ΒΡάμœκ≤ΡΝœ [82]ΕΰκΡ VAΓΔAVΓΔVVΓΔAIΓΔIAΓΔVIΓΔIV ΚΆ LS ΨυΨΏ”–ΫΪ CO2¥”N2 ÷–Ζ÷άκΒΡΡήΝΠ [56]¥ΥΆβΘ§AVΓΔVAΚΆIV“≤±μœ÷≥ωΕ‘CO2ΒΡ”≈œ»ΈϋΗΫΘ§ΕχΕ‘NH4ΒΡ”≈œ»ΈϋΗΫ [56]. ΑΔΖΫΥςΒ»»ΥΓΘ[54]”–±®Βά≥ΤΘ§ΥΡ÷÷ ηΥ°ΕΰκΡVIΘ§IAΘ§IVΘ§VVΨßΧεΖέΡ©Ω…“‘Α¥’’ArΘ§O 2Θ§N 2ΒΡΥ≥–ρΫχ––ΈϋΗΫΘ§¥”Εχ±μœ÷≥ωAr/O 2―Γ‘ώ–‘ΓΘ
‘Ύ51ΓψCΚΆΫ”Ϋϋ’φΩ’ΒΡΧθΦΰœ¬Θ§VIΒΡAr/O 2―Γ‘ώ–‘¥οΒΫ1:30Θ§’β «Έό“χΈϋΗΫΦΝ÷–≤βΒΟΒΡΉνΗΏ÷ΒΓΘ¥ΥΆβΘ§”…”Ύ≥Ώ¥γ≈≈≥β–ß”ΠΘ§AAΨßΧεΨΏ”–ΗϋΗΏΒΡO 2 /N 2―Γ‘ώ–‘Θ®“ΜΗω(O 2 /N 2 ) > 124) ±»ΤδΥϊ≤ΡΝœ[53]“ρ¥ΥAAΒΞΨßΡΛ”–ΆϊΉςΈΣ―Γ‘ώ–‘…χΆΗ≤ΡΝœΒΡΙΛ≥Χ”Π”ΟΓΘ
”…”ΎΨΏ”–ΝΫΗω ηΥ°≤ύΝ¥ΒΡΕΰκΡΫαΙΙΫωœό”ΎΫαΚœΒΑΑΉ÷ ≤–ΜυΘ§“ρ¥ΥΤδΉςΈΣΈϋΗΫΦΝΒΡ»Ϊ≤Ω«±ΝΠ»‘Έ¥ΒΟΒΫ≥δΖ÷ΩΣΖΔΓΘGörbitz ΚΆΥϊΒΡΆ§ ¬[57]≥Δ ‘ΧμΦ”Ζ«ΒΑΑΉ÷ Α±ΜυΥα¥σΚ≈-Α±ΜυΕΓΥαΘ®ABUΘ§““Μυ≤ύΝ¥Θ©ΚΆ¥σΚ≈-2-Α±ΜυΈλΥαΘ®¥σΚ≈-’ΐγ”Α±ΥαΓΔNvaΓΔn-±ϊΜυ≤ύΝ¥Θ©ά¥ΧΫΥςΗΟ ηΥ°ΕΰκΡΦ“ΉεΒΡά©’ΙΓΘΉς’ΏΫι…ήΝΥ °÷÷–¬ΒΡΕΰκΡΫαΙΙΒΡΚœ≥…ΚΆ±μ’ςΓΘCO 2ΚΆ CH 4‘Ύ195«ßΚΆ1 ΑΆ Θ®1 ΧθΘ©=10 5 ≈ΝΘ©÷ΛΟςΝΥ–¬ΕΰκΡΒΡ”άΨΟΩΉœΕ–‘ΓΘ÷ΒΒΟ“ΜΧαΒΡ «Θ§Nva-Val‘Ύ 50 ±Ε‘ CO 2 /CH 4ΒΡ―Γ‘ώ–‘ΈΣ1 ΑΆΓΘ’βœν―–ΨΩΈΣ―Α’“”…ΗϋΕύ≤Μ―Α≥ΘΒΡΖ«ΒΑΑΉ÷ Α±ΜυΥαΉι≥…ΒΡΤδΥϊΕύΩΉΕΰκΡ≤ΡΝœΧαΙ©ΝΥΥΦ¬ΖΓΘ
”…”ΎΙΧ”–ΒΡΗΏΩΉœΕ¬ Θ§MOF ‘ΎΤχΧε¥φ¥ΔΚΆΖ÷άκΖΫΟφœ‘ Ψ≥ω”Π”Ο«ΑΨΑΓΘΤυΫώΈΣ÷ΙΘ§Ης÷÷κΡΝ§Ϋ”ΒΡ MOF ΕΦ±μœ÷≥ωΝΥΤχΧε¥φ¥Δ–‘Ρή[41Θ§77]÷ςΩΆΧεœύΜΞΉς”ΟΒΡ≤ΜΆ§ΒΦ÷¬MPFΕ‘ΤχΧεΈϋΗΫΨΏ”–―Γ‘ώ–‘Θ§œύ±»»α–‘MPFΘ§Η’–‘MPFΤΨΫηΤδΫαΙΙΦαΙΧΓΔ ”Π–‘«ΩΒ»ΧΊΒψ”–Άϊ≥…ΈΣ–¬“Μ¥ζΖ¬…ζΕύΩΉ≤ΡΝœ[41]Zn(Gly-Thr) 2 «“Μ÷÷Βδ–ΆΒΡΗ’–‘MPFΘ§ΨΏ”–ΝΦΚΟΒΡΤχΧεΈϋΗΫΡήΝΠΚΆΈϋΗΫ―Γ‘ώ–‘Θ§ΗΟ≤ΡΝœΩ…“‘ΈϋΗΫCO2 /CH4 Θ§ΕχΕ‘N2ΈόΩΉΓΘ[41]. ΈϋΗΫΒ»Έ¬œΏ273«ßΫαΙϊ±μΟς Zn(Gly-Thr) 2 MPF Ε‘ CO2 ΒΡΈϋΗΫ”≈œ»”Ύ CH4 , ΉνΗΏ CO2 /CH4Ζ÷άκ±»ΈΣ 14:1 (wt%:wt%)1 ΑΆΓΘMPF Ηϋ«ψœρ”ΎΈϋΗΫ CO2Θ§“ρΈΣκΡΝ§Ϋ”Χε÷–ΒΡΦΪ–‘ΜυΆ≈Θ®»γΑ±ΜυΚΆτ«ΜυΘ©Μα”κ CO2 ΖΔ…ζΥΡΦΪ-≈ΦΦΪœύΜΞΉς”ΟΓΘ’β÷÷œύΜΞΉς”Ο Ι CO2ΡήΙΜΩλΥΌά©…ΔΒΫ MPF ΡΎ≤ΩΒΡΩ’«Μ÷–ΓΘ
ΗΏΩΉœΕ¬ ΓΔΕύΜν–‘ΈΜΒψΚΆ ÷–‘ ΙΒΟMPF‘ΎΧΊΕ®Ζ÷Ή”ΒΡ Ε±πΚΆΡ≥–©Ε‘”≥ΧεΒΡ―Γ‘ώ–‘Ζ÷άκΖΫΟφΨΏ”–Ψό¥σ”≈ Τ[47Θ§52Θ§72]. ¦gΧοΒ»»ΥΓΘ[47]‘Ύ»ΐκΡGly-Pro-ProΝΫΕΥ“ΐ»κ¥χθΘΑΖΦϋΒΡ3-ΏΝύΛΜυΘ§ΗΡ±δΫπ τ≈δΈΜΈΜΒψΘ§ΟΩΗωAg +”κΝΫΗωκΡΒΡΏΝύΛΜυ-N≈δΈΜΘ§”κΫπ τάκΉ”≈δΈΜΚσΘ§κΡΝ¥ΨΪ»ΖΙΧΕ®‘ΎPΔρ¬ί–ΐΙΙœσ…œΘ§–Έ≥…œΏ–‘¬ί–ΐΝ¥Θ®ΆΦ 5aκΡΒΡ¬ί–ΐΙΙœσΚΆΏΝύΛΜυΆ≈ΒΡΠ–Ε―ΜΐΙ≤Ά§Ής”ΟΘ§–Έ≥…ΝΥ“ΜΗωΨΏ”–ΝΫΗω≤ΜΆ§≥Ώ¥γΒΡ“ΜΈ§ ÷–‘Ά®ΒάΒΡ»ΐΈ§“λΩΉΆ®ΒάΆχ¬γΘ®ΆΦ 5bΘ©ΓΘΫœ¥σΒΡ“ΜΗωΆ®ΒάΨΏ”–Ήσ ÷ΥΪ¬ί–ΐΙ«ΦήΘ§ΏΝύΛΜυΆ≈ΒΡΠ–Ε―Μΐ‘ω«ΩΝΥΫαΙΙΒΡΈ»Ε®–‘ΓΘΝμ“ΜΗωΫœ–ΓΒΡΆ®Βά±Μ»ήΦΝΚΆ“θάκΉ”ΫτΟήΧν≥δΓΘΫœ¥σΒΡΆ®Βά÷±ΨΕΈΣ2.2Ρ…ΟΉΘ§’β ΙΒΟΆβœϊ–ΐΜ·ΚœΈο 1,1'-ΥΪ-2-ίΝΖ”ΡήΙΜ Βœ÷ ÷–‘ Ε±πΓΘ”…”ΎΆβœϊ–ΐΜ·ΚœΈο±»Ρ…ΟΉΆ®Βά–ΓΒΟΕύΘ§κΡΆ®ΒάΡΎ±μΟφΒΡ–‘÷ Ω…Ρή « ÷–‘Ζ÷±φΒΡ‘≠“ρΓΘ¥ΥΆβΘ§MPF ΜΙ±Μ÷ΛΟς ”Ο”Ύ…ζΈοΒΆΨέΈοΒΡΖ÷Ή” Ε±πΘ®ΆΦ 5cΘ©ΓΘ
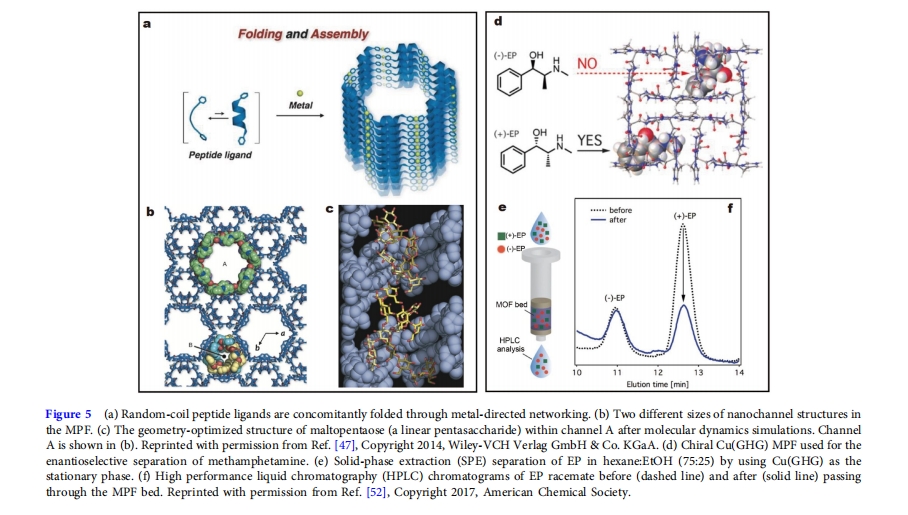
ΦΉΜυ±Ϋ±ϊΑΖ (MA) ΚΆ¬ιΜΤΦν (EP) «ΝΫ÷÷ΙψΖΚ”Ο”Ύ”ιά÷ΚΆ÷ΈΝΤ“©ΈοΒΡ ÷–‘ΦΪ–‘“©ΈοΓΘCu(GHG) MPF “―”Ο”Ύ’βΝΫ÷÷“©ΈοΒΡΕ‘”≥ΧεΖ÷άκΘ®ΆΦ5d-fΘ©[52]. »ΐκΡ Gly-¥σΚ≈-His-Gly (GHG)Ά®ΙΐΗ Α±ΥαΒΡΠΧ2-τ»Υα«≈”κCu 2+œύΜΞΝ§Ϋ”–Έ≥…ΥΡ¬ί–ΐΝ¥Θ§ΫχΕχΙΙ≥…“ΜΈ§Ά®ΒάΓΘΦρΒΞΒΊΫΪCu(GHG)”κΝΫ÷÷“©ΈοΒΡΆβœϊ–ΐΜλΚœΈοΜλΚœΦ¥Ω…±μœ÷≥ωΟςœ‘ΒΡΖ÷±φ–ßΙϊΓΘ(+)-MAΚΆ(+)-EP‘Ύ4ΚΆ6Γφ ±Ζ÷±πœ‘ Ψ≥ω30%Γά3%ΚΆ37%Γά3%ΒΡΈϋΗΫ2 –Γ ±ΓΘΕχœύ”ΠΒΡ“λΙΙΧεΦΗΚθ‘ΎΆ§“Μ ±ΦδΡΎ≤Μ±ΜΈϋΗΫΘ§«βΦϋΡήΒΡ≤ν“λΒΦ÷¬Ε‘”≥Χε―Γ‘ώ–‘ΈϋΗΫΘ§(+)-Ε‘”≥ΧεΜα”κMPF–Έ≥…ΗϋΕΧΒΡ«βΦϋΘ§¥”ΕχΨΏ”–ΗϋΗΏΒΡΦϋΡήΓΘΜυ”Ύ¥ΥΘ§Ής’ΏΫχ“Μ≤Ϋ“‘MPFΈΣΙΧœύίΆ»Γ÷υΙΧΕ®œύΘ§Ε‘(Γά)-EPΆβœϊ–ΐΜλΚœΈοΫχ––ίΆ»ΓΖ÷άκΘ®ΆΦ 5eΘ©ΗΟœΒΆ≥Ω…“‘¥”Β»ΡΠΕϊΕ‘”≥ΧεΜλΚœΈο÷–Χα»Γ≥ω 54% Γά 2% (+)-EPΘ§4 Ζ÷÷”Θ®ΆΦ 5fΘ©ΓΘ
¥ΏΜ·
Χλ»ΜΟΗΙψΖΚ¥φ‘Ύ”Ύ…ζΈοΧεΡΎΘ§ΨΏ”–ΦΪΗΏΒΡ–ß¬ ΚΆ―Γ‘ώ–‘Θ§ΥφΉ≈Ε‘Χλ»ΜΟΗ―–ΨΩΒΡ…ν»κΘ§»ΥΙΛ…ηΦΤΒΡκΡΜυ¥ΏΜ·ΦΝ“≤ΟφΝΌΜζ”ωΚΆΧτ’ΫΓΘΆ®Ιΐ…ηΦΤΦρΒΞΒΡκΡ≤ΔΒςΩΊΤδΉ‘ΉιΉΑΘ§Έ“Ο«Ω…“‘ΜώΒΟ“ΜœΒΝ–ΨΏ”–”––ρΕύΩΉΫαΙΙΒΡΡ…ΟΉΨßΧεΘ§’β–©Ρ…ΟΉΨßΧεΩ…“‘ΈΣ¥ΏΜ·ΧαΙ©–μΕύΜν–‘ΈΜΒψΘ§ «“Μ÷÷ΜΖΨ≥”―ΚΟΒΡΗΏ–ß…ζΈο¥ΏΜ·ΦΝ[42]ΓΘ
≥¬Β»»ΥΓΘ[42] ήΒΫΧΦΥατϊΟΗΜν–‘ΈΜΒψΫαΙΙΒΡΤτΖΔΘ§“‘ΜΖΉ¥ΕΰΉιΑ±ΥαΘ®cyclo-HHΘ©ΈΣΙΙΫ®ΩιΘ§”κΒβΜ·–Ω“ΜΤπΘ§÷Τ±Η≥ωΨΏ”–Υ°ΫβΜν–‘ΒΡΜΖ-HH-ZnI 2Ρ…ΟΉœΏΓΘΡ…ΟΉœΏΒΡ≥§ΫαΙΙ”…–μΕύΡ…ΟΉΩ≈ΝΘΉι≥…Θ§Κ§”–ΖαΗΜΒΡ¥ΏΜ·Μν–‘ΈΜΒψΘ®ΆΦ 6aΘ©Ε‘θΞάύΒΉΈοΒΡΥ°ΫβΨΏ”–ΫœΗΏΒΡΜν–‘Θ§άΐ»γ“≥-œθΜυ±Ϋ““ΥαθΞΘ®“≥NPA)Θ§Τδ”––ßΥ°ΫβΜν–‘ΈΣ93.21(mol L -1 ) -1 s -1ΓΘΥϋΟςœ‘ΗΏ”ΎœΗΑϊ÷ήΤΎΒΑΑΉ-HHΚΆΒΞΨßΜΖ-HH-ZnI 2ΓΘΆ§ ±Θ§ΜΖ-HH-ZnI 2Ρ…ΟΉœΏΝν»ΥΨΣ―»ΒΊΈ»Ε®Θ§≤Δ«“Ω…÷ΊΗ¥ Ι”Ο–‘ΦΪΦ―Θ§“ρ¥Υ’β÷÷ΦρΒΞΒΡ≥§Ζ÷Ή”≤Ώ¬‘ΈΣΉνœ»ΫχΒΡ…ζΈο¥ΏΜ·ΦΝΧαΙ©ΝΥ“Μ÷÷”–Έϋ“ΐΝΠΒΡ–¬Χφ¥ζΖΫΑΗΓΘ
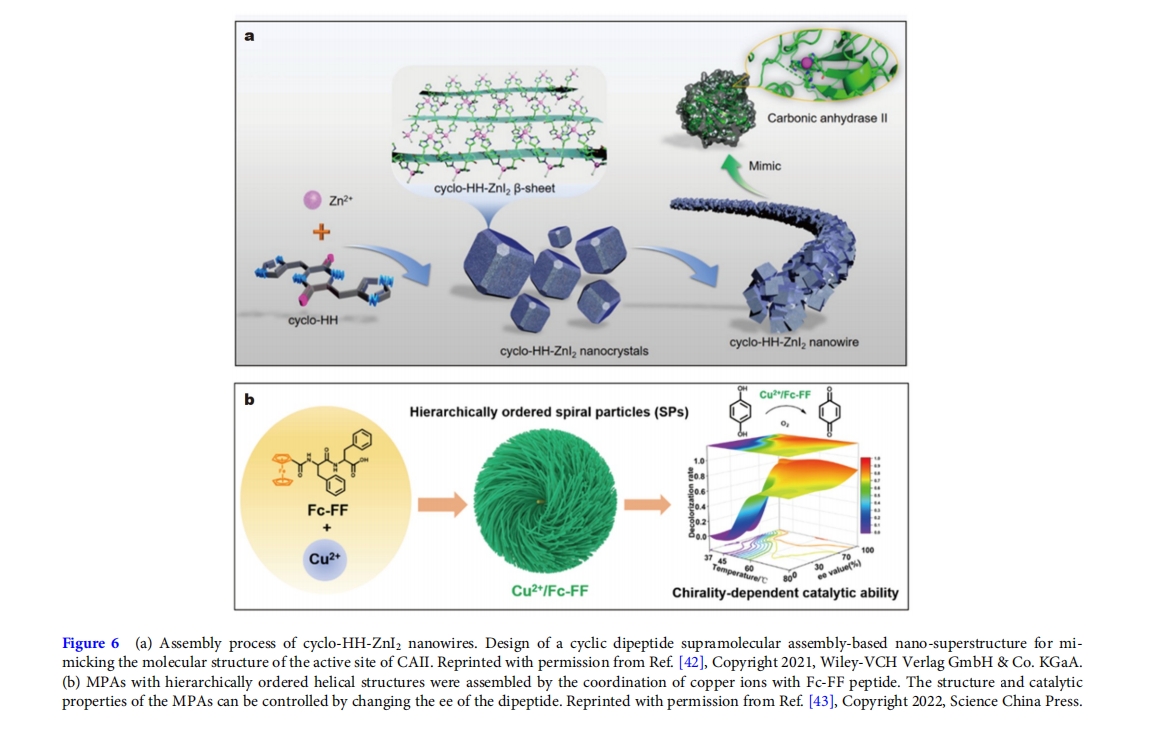
ΝθΒ»»ΥΓΘ[43]±®ΒάΝΥ“Μ÷÷ΨΏ”–Ζ÷ΦΕ¬ί–ΐΫαΙΙΒΡΫπ τκΡΉιΉΑΧε (MPA)Θ§Ά®Ιΐ Fc-FF ”κΕΰΦέΆ≠άκΉ” (Cu 2+ ) ΒΡ≈δΈΜΕχ–Έ≥…ΓΘMPA Ω≈ΝΘ”…¬ί–ΐΉι÷·ΒΡΡ…ΟΉœΥΈ§Ήι≥…Θ§’β–©Ρ…ΟΉœΥΈ§Ω…“‘”κΕ‘ ΐ¬ί–ΐœύΙΊΝΣΓΘ’β–© MPA «Ζ÷≤ψ«“ΕύΩΉΒΡΘ§ΗΜΚ§ Fc ΚΆ Cu 2+ΗΟΗ¥ΚœΈοΨΏ”–ΦΪΚΟΒΡ«ΉΚΆ–‘Θ§ΡήΙΜ‘ΎΆ―…ΪΖ¥”Π÷–±μœ÷≥ω‘ΕΗΏ”ΎΧλ»ΜΤαΟΗΒΡ¥ΏΜ·Μν–‘ΓΘ¥ΥΆβΘ§Ά®ΙΐΩΊ÷ΤΈ¬Ε»ΚΆΕ‘”≥ΧεΙΐΝΩΘ®eeΘ©Ω…“‘Κœ≥…“ΜœΒΝ–ΨΏ”–≤ψΉ¥ΫαΙΙΒΡMPAΓΘΨΏ”–ΫœΗΏee÷ΒΒΡκΡΕ‘”≥ΧεΜαΉ‘ΉιΉΑ≥…ΗΏΕ»Η¥‘””––ρΒΡΫαΙΙΘ§”κΨΏ”–ΫœΒΆee÷ΒΒΡκΡΉιΉΑΒΡΫαΙΙœύ±»Θ§’β–©ΫαΙΙΨΏ”–ΗϋΗΏΒΡ±μΟφΜΐΚΆΩΉœΕ¬ Θ§¥”Εχ‘ω«Ω¥ΏΜ·Μν–‘ΓΘ’β–©ΫαΙϊΈΣ ÷–‘‘Ύ“ΐΒΦ…ζΈοΖ÷Ή”Ή‘ΉιΉΑ≥…ΗΏΕ»”––ρΓΔΕύΩΉΒΡΙΠΡή≤ΡΝœΖΫΟφΒΡ÷Ί“ΣΉς”ΟΧαΙ©ΝΥ–¬ΒΡΦϊΫβΘ®ΆΦ 6bΘ©ΓΘ
Ρή‘¥¥Δ¥φΚΆΖΔΒγ
≥§ΦΕΒγ»ίΤς“ρΤδΗΏΙΠ¬ ΟήΕ»ΚΆœύΕ‘Ϋœ¥σΒΡΡήΝΩΟήΕ»Εχ≥…ΈΣ”–«ΑΆΨΒΡ¥ΔΡή…η±ΗΓΘκΡΜυΕύΩΉ≤ΡΝœ“―±Μ÷ΛΟςΨΏ”–ΝΦΚΟΒΡ≥§ΦΕΒγ»ίΤς–‘Ρή[84]ΓΘ±≠Ή”Β»»Υ[84]ΖΔœ÷κΡΡ…ΟΉΙή’σΝ–œ‘÷χΧαΗΏΝΥ≥§ΦΕΒγ»ίΤςΒγΦΪΒΡΒγ»ίΓΘκΡΡ…ΟΉΙή–ό ΈΒγΦΪΒγ»ίΒΡ‘ωΦ”Ιι“ρ”Ύ–ό ΈΧΦΒγΦΪ…œΩ…”ΟΒΡΒγΦΪ±μΟφΜΐΒΡ‘ωΦ”ΓΘΫαΙϊΧα Ψ”Αœλ≥§ΦΕΒγ»ίΤςΒγ»ίΒΡΙΊΦϋ“ρΥΊ «κΡΡ…ΟΉΙήΡ…ΟΉΆ®ΒάΒΡ Σ±μΟφΜΐΓΘ
κΡΡ…ΟΉΙήΜρΕύΩΉΨßΧε“≤ΨΏ”–ΝΦΚΟΒΡ―ΙΒγ–‘[66Θ§85®C87]ΚΆΧζΒγ–‘[88Θ§89]ΓΘ2016ΡξΘ§»ν¬»»ΥΓΘ[66]‘ΎκΡΉ‘ΉιΉΑΙΐ≥Χ÷–Ά®Ιΐ ©Φ”Βγ≥Γ (EF) Βœ÷ΦΪΜ·ΩΊ÷ΤΘ®ΆΦ 7a, b),¥”Εχ–Έ≥…¥Ι÷±≈≈Ν–ΒΡΈΔΑτ’σΝ–Θ®ΆΦ7c®CfΘ©‘ΎΝΫΗωœύΖ¥ΖΫœρ…œΜώΒΟΝΥΨυ‘»ΒΡΦΪΜ·Θ§≤Δ«“”––ß―ΙΒγ≥Θ ΐdFF’σΝ–≤ΡΝœ÷–ΒΡ33÷÷¥οΒΫ17.9pmV −1Θ§’βΫχ“Μ≤Ϋ÷ΛΟςΝΥΩΣ¬ΖΒγ―Ι1.4 ΖϋΙΠ¬ ΟήΕ»3.3Ρ…ΆΏΓΛάεΟΉ−2Ω…“‘ Ι”ΟΜυ”Ύ FF κΡΒΡ…ζ≥…Τς…ζ≥…Θ®ΆΦ 7gΓΔh”…ΨΏ”–Ω…ΩΊ―ΙΒγΧΊ–‘ΒΡκΡ«ΐΕ·ΒΡ…η±ΗΈΣ…ζΈο“Ϋ―ß”Π”ΟΧαΙ©ΝΥΩ…‘Ό…ζΚΆ…ζΈοœύ»ί–‘ΒΡΡή‘¥Θ§≤ΔΈΣ”κ»ΥΧεΉι÷·Φφ»ίΒΡœ¬“Μ¥ζΕύΙΠΡήΒγΉ”≤ζΤΖ¥ρΩΣΝΥ¥σΟ≈ΓΘ
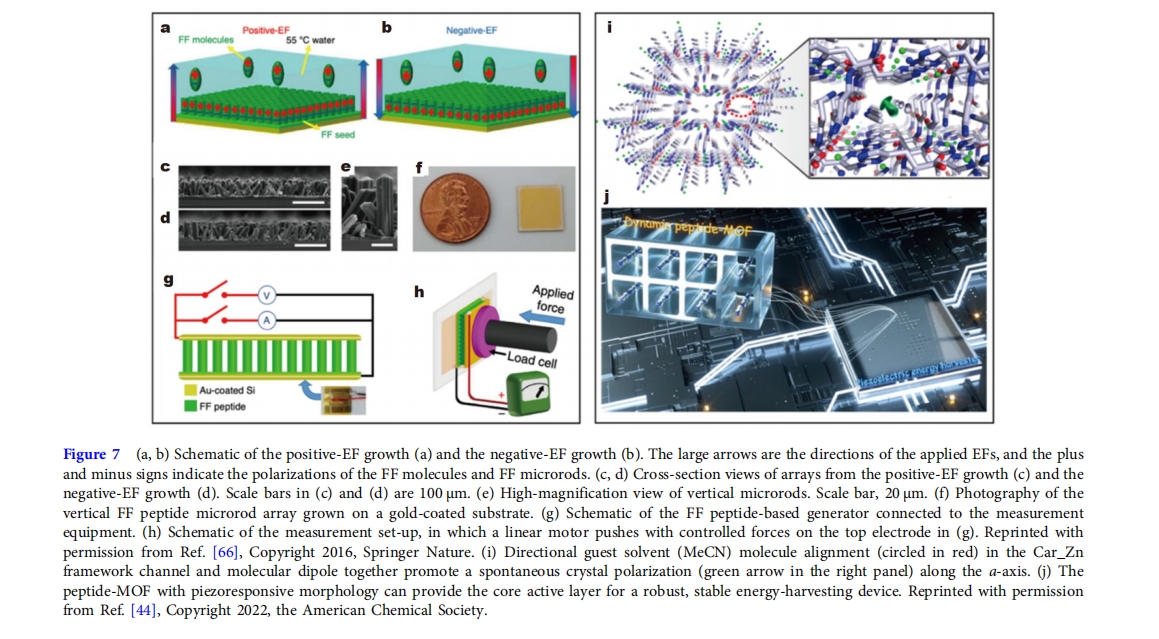
Ϋϋ»’Θ§≥¬Β»»ΥΓΘ[44]±®ΒάΝΥ Car_Zn κΡ-MOF ΒΡ¥σ–ΆΩΆΧεΧΊ“λ–‘ΜζΒγœλ”ΠΘ§ΗΟœλ”Π”…Έε÷÷≤ΜΆ§ΒΡΩΆΧεΖ÷Ή”ΉιΉΑΕχ≥…Θ§Φ¥“λ±ϊ¥Φ (IPA)ΓΔΕΰΦΉΜυΦΉθΘΑΖ (DMF)ΓΔ±ϊΆΣΓΔ““κφ (MeCN) ΚΆ““¥Φ (EtOH)ΓΘCar_ZnΓΛ(MeCN) MOF ΫαΨßΈΣΉνΒΆΕ‘≥ΤœΒΆ≥Θ®Ω’Φδ»ΚΝΉ1) ΨΏ”–≤Μ ή‘Φ χΒΡΦΪΜ·Θ§¥”Εχ≤ζ…ζ÷Ί“ΣΒΡ―ΙΒγœλ”ΠΓΘ―–ΨΩΖΔœ÷Θ§Ά®ΙΐΩΊ÷ΤΆ®Βά÷–ΩΆΧεΖ÷Ή”ΒΡΖΫœρΩ…“‘ Βœ÷œ‘Ή≈ΒΡ―ΙΒγœλ”ΠΘ®ΆΦ 7i,j). Ι”ΟCar_ZnΓΛ(MeCN)ΨßΧεΉςΈΣ”–‘¥‘ΣΦΰΘ§ΗΟΖΔ…ζΤςΩ…“‘≤ζ…ζΈ»Ε®ΓΔ«ΩΨΔΒΡΩΣ¬ΖΒγ―Ι1.4 Ζϋ‘ΎΆβΝΠΉς”Οœ¬Εΰ °Έε ΖώΤΒ¬ ΈΣ0.1Κ’Ή»ΓΘ
“©Έο δΥΆ
κΡΉ‘ΉιΉΑ–Έ≥…ΒΡΕύΩΉΫαΨß≤ΡΝœΩ…ΉςΈΣ“©ΈοΒίΥΆΒΡ‘ΊΧεΘ§ΨΏ”–ΝΦΚΟΒΡ…ζΈοœύ»ί–‘ΚΆΫœΗΏΒΡΜ·―ßΕύ―υ–‘Θ§Ω…“‘…ηΦΤΚœ ΒΡΜθΈο«ΉΚΆΝΠΚΆΑ–œρΡήΝΠΘ§ Βœ÷ΗΏ–ßΒΡ“©ΈοΒίΥΆΓΘWoolfsonΩΈΧβΉι[83]±®ΒάΝΥ“Μ÷÷”…κΡΉ‘ΉιΉΑΒΡΡ…ΟΉΝΐΘ®ΆΦ 8a)ΓΘΡ…ΟΉΝΐ–Έ≥…Ιΐ≥Χ÷–Θ§“λ÷ ¬ί–ΐΘ®CC-Di-ABΘ©ΒΡΝΫΗω≤ύΝ¥Ά®ΙΐΕΰΝρΦϋ‘Ύ»ήΦΝ±©¬ΕΟφ…œ”κΠΝ¬ί–ΐΕύκΡΘ®CC-Tri3Θ©ΒΡ»ΐΨέΧεΝ§Ϋ”Θ§–Έ≥…–ΓΖ÷Ή”≈δΧεΘ§≈δΧεΝ§Ϋ”–Έ≥…Νυ±Ώ–ΈΨßΗώΘ§ΨßΗώ―”…λ–Έ≥…«ρ–ΈΡ…ΟΉΝΐΓΘ’β–©Ή‘ΉιΉΑΒΡκΡΖ÷Ή”Ρ…ΟΉΝΐΩ…“‘±ΜœΗΑϊ…ψ»ΓΘ§Ά§ ±Ρ…ΟΉΝΐΒΡ÷––ΡΜΙΩ…“‘»ίΡ…ΤδΥϊ”–ΜζΖ÷Ή”Θ§Αϋά®“©ΈοΖ÷Ή”ΓΘ“ρ¥ΥΘ§¥ΥάύΡ…ΟΉΝΐΩ…“‘ΉςΈΣ“©Έο‘ΊΧεΘ§ΫΪ“©ΈοΖ÷Ή”ΒίΥΆΒΫœΗΑϊ÷–ΓΘΆ®Ιΐ–ό ΈκΡΖ÷Ή”…œ¥χΒγ≤–ΜυΘ§»γ¥χ’ΐΒγΒΡάΒΑ±ΥαΘ®LysΘ©≤–ΜυΜρ¥χΗΚΒγΒΡΙ»Α±ΥαΘ®GluΘ©≤–ΜυΘ§Ω…“‘ΗΡ±δΡ…ΟΉΝΐ±μΟφΒΡΒγΚ…Ζ÷≤ΦΘ§’βΫΪ”ΑœλΡ…ΟΉΝΐΚΆœΗΑϊ÷°ΦδΒΡœύΜΞΉς”ΟΓΘ
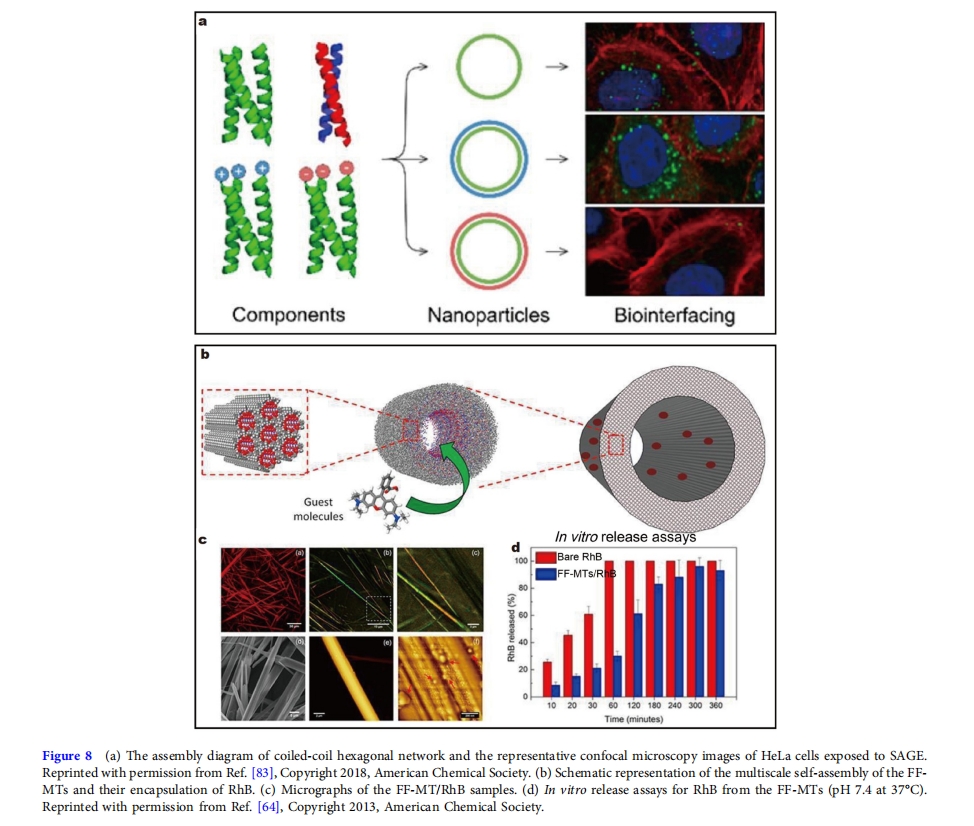
’β¥σΚ≈-Εΰ±Ϋ±ϊΑ±ΥαΩ…“‘Ή‘ΉιΉΑ≥…ΈΔΙήΘ®FF-MTΘ©Θ§Ω…ΉςΈΣ“©Έο δΥΆΒΡ«±‘Ύ‘ΊΧε[64]. ΉιΉΑΙΐ≥Χ»γΆΦΥυ ΨΆΦ 8bΤδ÷–ΝυΗω FF ΒΞ‘Σ–Έ≥…“ΜΗωΜΖΉ¥ΝυΨέΧεΘ§ΥφΚσΝυΨέΧεΕ―Βΰ–Έ≥…’≠Ά®ΒάΘ§ΤδΖΕΒ¬ΜΣ÷±ΨΕ‘ΦΈΣ10ΑΘΓΘœΝ’≠ΒΡΆ®Βά“‘Νυ±Ώ–ΈΕ―Μΐ–Έ ΫΉ‘ΫαΚœΘ§–Έ≥…±ΓΤ§ΓΘ±ΓΤ§ΒΡ≤χ»Τ–Έ≥…Ρ…ΟΉΦΕΙήΘ§’β–©ΙήΉν÷’Ω…“‘‘ΎΗϋ¥σΒΡ≥ΏΕ»…œΉ‘ΉιΉΑΘ§–Έ≥…ΈΔ≥ΏΕ»ΙήΉ¥≈≈Ν– χΓΘAlvesΒ»»ΥΓΘ[64] Ι”ΟκΡΈΔΙή‘Υ δΡΘ–Ά«ΉΥ°Μ·ΚœΈο¬όΒΛΟς B (RhB)ΓΘœ‘ΈΔΆΦœώœ‘ ΨΜθΈοΨυ‘»Ζ÷≤Φ‘Ύ FF-MT ÷–Θ®ΆΦ 8cΘ©Θ§ ΚΆΧεΆβ Β―ι±μΟςΘ§FF-MT ÷– RhB ΒΡ ΆΖ≈Ήώ―≠“ΜΦΕΕ·ΝΠ―ßΘ§’βΩ…“‘ΒςΫΎΗΚ‘ΊΒΡ ΆΖ≈Θ®ΆΦ 8d),«“ΕΨ–‘ΫœΒΆΓΘ
≤Φά≠ΩΤΒ»»ΥΓΘ[58]ΉνΫϋΘ§―–ΨΩ»Υ‘±ΧΫΥςΝΥΕύΩΉΕΰκΡΨßΧεΉςΈΣΜ”ΖΔ–‘“©Έο»ίΤςΒΡ”Π”ΟΓΘΥϊΟ«―–ΨΩΝΥΕΰκΡ VAΓΔAIΓΔVVΓΔIV ΚΆ IA ¥”Τχœύ÷–Ω…ΡφΒΊΈϋΗΫ“ΜœΒΝ–”ΟΉς¬ιΉμΦΝΒΡΜ”ΖΔ–‘ΖζΜ·Ο―ΓΘ’β–©ΕΰκΡΨßΧεΒΡ≥Ώ¥γΖ÷≤Φ‘ΦΈΣ30Ρ…ΟΉΘ§ Κœ―Σ“Κ‘Υ δΚΆœΗΑϊΡΎΜ·ΓΘ“ρ¥ΥΘ§ΕΰκΡΨßΧε”–Ω…Ρή”Ο”Ύ“©Έο‘Υ δΜνΈϋΗΫΒ»Έ¬œΏ±μΟςΘ§VAΓΔAIΓΔVVΘ®ΩΉΨΕ¥σ”Ύ4ΑΘΘ©ΡήΙΜ”––ßΈϋΗΫΩΆΧεΘ§ΕχIAΚΆIVΘ®ΩΉΨΕ‘ΦΈΣ3.5ΑΘ)≈≈≥ΐ¬ιΉμ“©ΓΘ273«ßΚΆ 80®C100 Ά– Θ®1 Ά–=133.3≈ΝΥΙΩ®Θ©Ήν¥σΈϋΗΫ÷Β¥οΒΫ170®C200 ΚΝΡΠΕϊ-1Θ§œύΒ±”Ύ≥§Ιΐ 20% ΒΡ÷ΊΝΩΓΘΈϋΗΫ»»‘Ύ 35®C50«ßΫΙΕζmol −1Θ§’β”κ“―±®ΒάΒΡΕύΩΉ≤ΡΝœ÷–ΈϋΗΫ¬ιΉμΦΝΒΡΉνΗΏ÷ΒœύΒ±[90]ΓΘ
ΉήΫα”κ’ΙΆϊ
κΡΜυΕύΩΉ≤ΡΝœ «“Μ÷÷ΦΪΨΏ«ΑΨΑΒΡ–¬–ΆΕύΩΉ≤ΡΝœΘ§ΨΏ”–ΗΏΕ‘”≥―Γ‘ώ–‘ΓΔΚΘΟύ––ΈΣΓΔΩ…Ε®÷Τ–‘ΚΆ…ζΈοœύ»ί–‘Β»ΧΊΒψΓΘΕΰκΡΓΔΙ―κΡΚΆΕύκΡ“‘ΦΑMPFΚή»ί“ΉΉιΉΑ≥…ΕύΩΉΫαΙΙΓΘΜυ”ΎΖ÷Ή”Ή‘ΉιΉΑΒΡ―–ΨΩ ΙΒΟ‘Ύ…ηΦΤΫΉΕΈ‘Λ≤βκΡΒΡΫαΙΙΚΆΙΠΡή±δΒΟ»ί“ΉΓΘ“―Ψ≠ΩΣΖΔ≥ωΗς÷÷ΡΘΡβΗ®÷ζΙΛΨΏά¥…ηΦΤκΡ–ρΝ–ΓΘpHΓΔΈ¬Ε»ΚΆΤδΥϊΆβ≤ΩΜΖΨ≥ΒΡΒςΫΎ“≤Ω…“‘ΩΊ÷ΤκΡΜυΕύΩΉ≤ΡΝœΒΡΫαΙΙΚΆΙΠΡήΓΘΩΉœΕΡΎ≤ΩΩ…“‘…ηΦΤΙΠΡήΜ·ΒΡ≤ύΝ¥Θ§ΈΣκΡΜυΕύΩΉ≤ΡΝœΒΡΕύΙΠΡή”Π”ΟΒλΕ®ΝΥΜυ¥ΓΓΘ
”…”Ύ≥ΛκΡΒΡΗ¥‘”–‘“‘ΦΑ»±ΖΠ”––ßΒΡΚœ≥…ΖΫΖ®Θ§ΡΩ«Α±®ΒάΒΡκΡΜυΕύΩΉ≤ΡΝœ¥σΕύ «”…ΦρΒΞΒΡΕΧκΡΉιΉΑΕχ≥…Θ§…ηΦΤ≥ωΨΏ”–”κ…ζΈο¥σΖ÷Ή”άύΥΤΒΡΫαΙΙΕύΙΠΡή–‘ΒΡΗΏΙΠΡήκΡΜυΕύΩΉ≤ΡΝœ»‘ «ΩΤ―–»Υ‘±ΒΡΡ―ΧβΓΘΫϋΤΎΘ§NguyenΒ»»ΥΓΘ[39]ΩΣΖΔΝΥ“Μ÷÷Ζ«Ι≤Φέ≤Ώ¬‘ΫΪΫœ≥ΛΒΡκΡΉιΉΑΒΫΨßΧεΩρΦή÷–Θ§ΈΣάϊ”ΟΫœ≥ΛΒΡκΡΚœ≥…κΡΜυΕύΩΉ≤ΡΝœΧαΙ©ΝΥ“Μ÷÷Ω…––ΒΡ≤Ώ¬‘ΓΘ»ΜΕχΘ§ΜΙ–η“ΣΗϋΕύΒΡΚœ≥…≤Ώ¬‘Θ§’βΩ…“‘ΤτΖΔ―–ΨΩ»Υ‘±Κœ≥…Η¥‘”«“ΙΠΡή–‘ΒΡΕύΩΉ≤ΡΝœΓΘ
¥ΥΆβΘ§ΫϋΡξά¥ΙΊ”ΎκΡΜυΕύΩΉ≤ΡΝœΗΏΕ»”––ρΜ·ΒΡ―–ΨΩ“≤‘Ϋά¥‘ΫΕύΘ§ΒΪ’β–©―–ΨΩ¥σΕύ «Μυ”Ύ≈Φ»ΜΒΡΖΔœ÷Θ§…ηΦΤ≥ωΨΏ”–‘ΛΤΎΩΉΫαΙΙΚΆΙΠΡήΒΡκΡΕύΩΉ≤ΡΝœ»‘»Μ °Ζ÷άßΡ―ΓΘΫϋά¥Θ§ΥφΉ≈»ΥΙΛ÷«ΡήΒΡΖΔ’ΙΘ§κΡΕύΩΉ≤ΡΝœΒΡΦΤΥψ…ηΦΤΫΪ≥…ΈΣΩ…ΡήΘ§ ΙΒΟκΡΜυΕύΩΉ≤ΡΝœΒΡ…ηΦΤΚΆΚœ≥…¥οΒΫ«ΑΥυΈ¥”–ΒΡΨΪΕ»ΚΆΗ¥‘”Ε»Θ§Η≥”η≤ΡΝœΕάΧΊΒΡΙΠΡήΓΘ
¥ΥΆβΘ§κΡΜυΕύΩΉ≤ΡΝœ‘Ύ…ζΈο¥ΏΜ·ΓΔΤχΧεΈϋΗΫΖ÷άκΓΔΕ‘”≥Χε―Γ‘ώ–‘Ζ÷άκΓΔ“©ΈοΒίΥΆΒ»Νλ”ρœ‘ Ψ≥ωΝΥΨό¥σΒΡ”Π”Ο«±ΝΠΘ§ΒΪ“Σ’φ’ΐ Βœ÷ ΒΦ ”Π”ΟΜΙ–η“ΣΗΕ≥ωΗϋΕύΒΡ≈§ΝΠΓΘ Ήœ»Θ§”…”ΎκΡΜυΕύΩΉ≤ΡΝœ±Ψ…μΒΡ ÷–‘ΚΆΩ…Ε®÷Τ–‘Θ§Υϋ”–ΆϊΉςΈΣΙΧœύ Βœ÷¥ΪΆ≥ΖΫΖ®ΈόΖ® Βœ÷ΒΡΗΏ–ßΕ‘”≥Χε…ΪΤΉΖ÷άκΓΘΤδ¥ΈΘ§ΡΩ«Α¥σΕύ ΐΙΊ”ΎκΡΜυΕύΩΉ≤ΡΝœ”Ο”Ύ¥ΏΜ·ΒΡ±®Βά»‘»Μ±μœ÷≥ωœύΕ‘ΫœΒΆΒΡ―Γ‘ώ–‘ΓΘ“ρ¥ΥΘ§Ά®ΙΐΚœάμ…ηΦΤκΡΜυΕύΩΉ≤ΡΝœ÷–ΒΡκΡ–ρΝ–ΜρΫχ––Μ·―ß–ό ΈΘ§”–ΆϊΜώΒΟΗΏ–ßΓΔΗΏ―Γ‘ώ–‘ΒΡ…ζΈο¥ΏΜ·ΦΝΓΘΒΎ»ΐΘ§ΒΫΡΩ«ΑΈΣ÷ΙΘ§ΡΩ«ΑΙΊ”ΎκΡΜυΕύΩΉ≤ΡΝœ‘Ύ…ζΈο“Ϋ―ß÷–ΒΡ”Π”Ο±®ΒάΫœ…ΌΘ§Έ¥ά¥”Π÷¬ΝΠ”Ύ…ηΦΤΨΏ”–ΚΘΟύ––ΈΣΓΔ¥ΧΦΛœλ”Π–‘ΚΆΒΆΕΨ–‘ΒΡ…ζΈοœύ»ί–‘≤ΡΝœΘ§’β–©≤ΡΝœ”–Άϊ”Ο”Ύ“©Έο δΥΆΚΆΑ©÷Δ÷ΈΝΤΓΘ
Οβ‘π…υΟςΘΚ±ΨΈΡΈΣ––“ΒΫΜΝς―ßœΑΘ§Αφ»®Ιι‘≠Ής’ΏΦΑ‘≠‘”÷ΨΥυ”–Θ§»γ”–«÷»®Θ§Ω…ΝΣœΒ…Ψ≥ΐΓΘΈΡ’¬±ξΉΔ”–Ής’ΏΦΑΈΡ’¬≥ω¥ΠΘ§»γ–η‘ΡΕΝ‘≠ΈΡΦΑ≤ΈΩΦΈΡœΉΘ§Ω…‘ΡΕΝ‘≠‘”÷ΨΓΘ