
’Σ“ΣΘΚΕύκΡ–ό ΈΒΡpHΟτΗ–÷§÷ ΧεΉςΈΣ“©ΈοΜρΚΥΥαΒΡ‘ΊΧεΩ…“‘÷ςΕ·Α–œρ÷ΉΝω≤ΩΈΜΘ§ ΙΩΙ÷ΉΝω“©ΈοΜρΚΥΥα‘ΎΧΊΕ®«χ”ρ ΆΖ≈Θ§ΫΒΒΆ“©ΈοΕ‘’ΐ≥ΘΉι÷·ΜρœΗΑϊΒΡΕΨΗ±Ής”ΟΓΔΧαΗΏ“©ΈοΘ·ΚΥΥαΒΡ÷ΈΝΤ–ßΙϊΓΘ± ’Ώ÷ς“Σ¥”ΕύκΡ–ό ΈΒΡpHΟτΗ–÷§÷ ΧεΒΡ Ά“©Μζ÷ΤΓΔ–ό ΈΖΫ ΫΚΆ”Π”ΟΒ»ΖΫΟφΫχ––Ήέ ωΘ§ΈΣΕύκΡ–ό ΈΒΡpHΟτΗ–÷§÷ ΧεΒΡ÷Τ±ΗΦΑΩΙ÷ΉΝω“©Έο‘ΊΧε…ηΦΤΖΫΟφΒΡ―–ΨΩΧαΙ©œύ”Π≤ΈΩΦΓΘ
÷§÷ ΧεΉν≥θ”…BanghamΒ»[1] Ιέ≤λΝΉ÷§‘ΎΥ°÷–ΒΡΖ÷…Δ–‘Ή¥ ±ΖΔœ÷Θ§”…”ΎΤδ ηΥ°«ΉΥ°Ής”ΟΘ§ΝΉ÷§ ηΥ°ΕΥœρΡΎ≤ΩΨέΦ·Θ§Εχ«ΉΥ°ΕΥΒΡ«βΦϋΚΆΥ°œύΦϋΚœ±©¬Ε‘ΎΆβΘ§–Έ≥…ΨΏ”–ΥΪΖ÷Ή”≤ψΫαΙΙΒΡ±’ΚœΡ“≈ίΓΘ÷§÷ ΧεΨΏ”–ΫœΚΟΒΡ…ζΈοœύ»ί–‘Θ§ΈόΕΨΓΔΈό»ή―Σ–‘ΓΔΈόΟβ“Ώ‘≠–‘Θ§Ω……ζΈοΫΒΫβΘ§“ρ¥Υ≥…ΈΣΡΩ«ΑΉν≥Θ”ΟΒΡ‘ΊΧε≤Δ‘Ύ“©Έο¥Ϊ δΖΫΟφΖΔΜ”ΝΥ÷Ί“ΣΒΡΉς”Ο[2]ΓΘ÷§÷ Χε±μΟφ“Ή±Μ–ό ΈΘ§Ω…“‘Αϋ‘ΊΗςάύ“©ΈοΖ÷Ή”ΜρΚΥΥαΖ÷Ή”[3-4]ΓΘ¥ΪΆ≥÷§÷ ΧεΒΡΝΉ÷§≥…Ζ÷”κœΗΑϊΡΛ≥…Ζ÷ΗΏΕ»œύΥΤΘ§ΨΏ”–±ΜΕ·Α–œρ–‘Θ§“ΉΦ·÷–”ΎΜζΧεΒΡΆχΉ¥ΡΎΤΛœΒΆ≥Θ§»±ΖΠΧΊΕ®ΒΡΉι÷·Α–œρ–‘Θ§ΒΦ÷¬œύ”ΠΒΡ÷ΈΝΤ–‘ΚΥΥαΚΆ ηΥ°–‘“©ΈοΒΡάϊ”Ο¬ ΫœΒΆΓΘΫϋΦΗΡξΘ§ΙζΡΎΆβ―–ΨΩ’Ώ¬Ϋ–χ÷Τ±Η≥ωpHΟτΗ–÷§÷ Χε[5]ΓΔ»»ΟτΗ–÷§÷ Χε[6]ΓΔ≥§…υ≤®ΟτΗ–÷§÷ Χε[7]ΚΆΙβΟτΗ–÷§÷ Χε[8]Β»Ης÷÷ΙΠΡή–‘÷§÷ Χε”Ο”Ύ“©ΈοΘ·ΚΥΥαΒΡΗΏ–ߥΪΒίΓΘ
÷ΉΝωœΗΑϊΨΏ”–Άζ ΔΒΡΧ«ΫΆΫβΡήΝΠΘ§»±―θΦΑ”–―θΧθΦΰœ¬ΕΦΡή≤ζ…ζ¥σΝΩΒΡ¥ζ–Μ≤ζΈο»ιΥαΘ§Φ”…œ÷ Ή”±Ο(H+-ATPase)ΦΑά¥Ή‘ΝΉΥαΈλΧ«ΆΨΨΕΒΡCO2Ής”ΟΘ§ΒΦ÷¬÷ΉΝωΉι÷·Ψ÷≤ΩΈΔΜΖΨ≥pH÷Β(5.8~7.0)ΒΆ”Ύ’ΐ≥ΘΉι÷·(7.4)[9]ΓΘάϊ”Ο÷ΉΝωΉι÷·Ψ÷≤ΩΈΔΜΖΨ≥ΒΡ’β÷÷ΧΊ–‘Θ§pHΟτΗ–÷§÷ Χε‘ΎΈΔΥαΜΖΨ≥œ¬≤ζ…ζ“ΜΕ®ΒΡΫαΙΙ ±δΜ·Θ§¥”ΕχΉς”Ο”Ύ÷ΉΝωΉι÷·≤Δ ΆΖ≈“©ΈοΓΘΤδ÷–Θ§ΕύκΡ–ό ΈΒΡ pHΟτΗ–÷§÷ ΧεΘ§Ω…άϊ”ΟΗς÷÷ΙΠΡή–‘ΕύκΡΒΡΥαΟτΗ–ΓΔΑ–œρΦΑ¥© ΡΛΉς”Ο[10-11] ,‘ω«Ω÷§÷ ΧεΒΡpHΟτΗ––‘ΓΔΧαΗΏpHΟτΗ–÷§÷ Χε Ε‘÷ΉΝωΉι÷·ΒΡΑ–œρΫαΚœΡήΝΠΘ§–Έ≥…Εύœλ”Π–‘ΜρΕύΙΠΡή–‘÷§÷ ΧεΘ§ΫιΒΦ÷§÷ Χε‘Ύ÷ΉΝωΜΖΨ≥œ¬ ΆΖ≈“©ΈοΘ§œ‘÷χΧαΗΏ“©ΈοΒΡ…ζΈο άϊ”Ο¬ ≤ΔΫΒΒΆΤδΕΨΗ±Ής”ΟΓΘ“ρ¥ΥΘ§ΫϋΡξά¥ΕύκΡ–ό ΈΒΡpHΟτΗ– ÷§÷ Χε≥…ΈΣ“©Έο¥ΪΒίœΒΆ≥ΒΡ―–ΨΩ»»ΒψΓΘ± ’Ώ÷ς“Σ¥”ΕύκΡ–ό Έ ΒΡpHΟτΗ–÷§÷ ΧεΒΡ Ά“©Μζ÷ΤΓΔ–ό ΈΖΫ ΫΚΆ”Π”ΟΒ»ΖΫΟφΫχ––Ήέ ωΘ§“‘ΤΎΕ‘pHΟτΗ–÷§÷ Χε“©ΈοΘ·ΚΥΥα¥ΪΒίœΒΆ≥ΒΡ―–ΨΩΧαΙ©≤ΈΩΦΓΘ
1 ΕύκΡ–ό ΈΒΡpHΟτΗ–÷§÷ ΧεΒΡΉι≥…ΦΑ Ά“©Μζ÷Τ
± ’ΏΉέ ωΒΡ÷§÷ ΧεpHΟτΗ––‘÷ς“Σ”–3÷÷–Έ ΫΧεœ÷ΘΚΔΌ÷Τ±ΗΜυ¥Γ÷§÷ ΧεΒΡ≤ΡΝœΘ§άΐ»γΨΏ”–pHΟτΗ––‘ΒΡΝΉ÷§ΜρΒ®ΙΧ¥ΦΘΜΔΎpHΟτΗ––‘ΕύκΡΘΜΔέΤδΥϊΨΏ”–pHΟτΗ––‘ΒΡΦϋΜρ≤ΡΝœΓΘ
‘γΤΎ÷Τ±ΗpHΟτΗ–÷§÷ ΧεΒΡ≤ΡΝœ÷ς“Σ”…ΝΫ«Ή–‘ΒΡΕΰ”ΆθΘΝΉ÷§θΘ““¥ΦΑΖ(dioleoylphosphatidylethanolamine, DOPE)ΚΆ“θάκΉ”÷§άύΘ§»γΒ®ΙΧ¥ΦγζγξΥαΒΞθΞ(cholesterylhemisuccinate,CHEMS)ΦΑ”ΆΥαΒ»≤ΡΝœΆ®ΙΐΒςΫΎΤδ±»άΐΚœ≥…[12]ΓΘ‘Ύ…ζάμpH÷Β(7.4)ΧθΦΰœ¬Θ§DOPEΚΆCHEMSΩ…“‘–Έ≥…Έ»Ε®ΒΡ÷§÷ ΧεΥΪΖ÷Ή”≤ψΓΘ‘Ύ÷ΉΝωΉι÷·ΈΔΜΖΨ≥pH÷Β(5.8~7.0)Μρ’Ώ»ήΟΗΧεpH÷Β(4.5~5.0)ΒΡΧθΦΰœ¬Θ§÷ Ή”Μ·ΒΡDOPEΚΆCHEMSΒΦ÷¬÷§÷ ΥΪΖ÷Ή”≤ψΒΡΫαΙΙ”…ΫτΟήΉΣ±δ≥… ηΥ…Θ§ΡΎ≤ΩΒΡ“©ΈοΜρΚΥΥαΒΟΒΫ ΆΖ≈[13]ΓΘάύΥΤΒΡΘ§“Μ–©Κ§”–÷§-ΨέΚœΈοΒΡΗ¥ΚœΫαΙΙΘ§Ά§―υΩ…“‘÷Τ±Η≥ωpHΟτΗ––‘÷§÷ Χε[14]ΓΘ‘γΤΎΒΡ’β–©÷§÷ ΧεΑ–œρ–‘Ϋœ≤νΘ§÷§÷ ΧεΫχ»κΜζΧεΚσΘ§»ί“Ή±ΜΖ«ΧΊΕ®œΗΑϊΡΎΆΧΘ§‘Ύ»ήΟΗΧεΒΡΥα–‘ΜΖΨ≥œ¬ ΆΖ≈ΩΙΑ©“©ΈοΘ§ΥπΚΠ’ΐ≥ΘœΗΑϊΜρΉι÷·ΓΘ
ΫϋΡξά¥Θ§”…”ΎΕύκΡΖ÷Ή”ΒΡ…ζΈοΕύ―υ–‘Θ§‘Ϋά¥‘ΫΕύΨΏ±ΗΧΊ Ε®ΙΠΡήΒΡΕύκΡ±Μ≤ΜΕœΖΔœ÷ΚΆ―–ΨΩΘ§άΐ»γΫαΙΙΫœΈΣΦρΒΞΒΡΕύΨέ ΉιΑ±Υα(poly-histidine)[15] ΚΆΕύΨέάΒΑ±Υα(poly-lysine)[16] ,“‘ ΦΑ‘¥Ή‘ΝςΗ–≤ΓΕΨΒΡINF7κΡ(GLFEAIEGFIENGWEGMIDGW- YGC)[17]ΕΦΨΏ”–Ϋœ«ΩΒΡpHΟτΗ––‘ΓΘΤδΥϊ―–ΨΩΫœΕύΒΡΙΠΡή–‘ ΕύκΡΑϋά®Έ¬Ε»ΟτΗ––‘ΕύκΡ[18]ΓΔΕύΨέ―τάκΉ”Θ·œΗΑϊ¥©ΡΛκΡ[19]ΓΔ÷ΉΝωΑ–œρκΡ[20-21]Β»ΓΘΕύκΡΨΏ”–“ΜΗωœ‘÷χΒΡΫαΙΙ–‘”≈ ΤΘ§Φ¥Ω… “‘‘Ύ≤Μ”Αœλ‘≠”–ΙΠΡή–‘ΕύκΡΤ§ΕΈΒΡΜυ¥Γ…œΘ§Ά®ΙΐΙΧœύΚœ≥…Μρ …ζΈοΚœ≥…Θ§‘ΎΕύκΡΒΡ“ΜΕΥΜρΝΫΕΥ“ΐ»κ–¬ΒΡΙΠΡή–‘ΕύκΡ–ρΝ–Θ§ΜώΒΟΕύΙΠΡή–‘»ΎΚœκΡ[22]ΓΘΫαΚœ’β–©≤ΜΆ§ΙΠΡή–‘ΒΡΕύκΡΘ§Εύ κΡ–ό ΈΒΡ÷§÷ Χε≤ΜΫωΨΏ”–pHΟτΗ––‘Θ§ΜΙΩ…“‘ΨΏ±ΗΕύΙΠΡή–‘Θ§άΐ»γάϊ”Ο ήΧεΘ·≈δΧεΫαΚœΖΫ Ϋά¥Α–œρ÷ΉΝωœΗΑϊΓΘ’β÷÷ΨΏ”– ή ΧεΘ·≈δΧεΫαΚœΡήΝΠΒΡpHΟτΗ–÷§÷ ΧεΫχ»κœΗΑϊΒΡΜζ÷ΤΘ§ΆυΆυ≤Μ Ά§”ΎΤ’Ά®÷§÷ ΧεΒΡ»ΎΚœΖΫ ΫΓΘ»γάύΥΤRGD/ΠΝVΠ¬3[23] Μρ’Ώ Transferrin/TfR[24] ΒΡΫαΚœΖΫ ΫΘ§Μα”’ΒΦ÷ΉΝωΉι÷·œΗΑϊ÷ςΕ·ΡΎ ΆΧ÷§÷ ΧεΦΧΕχ ΆΖ≈“©ΈοΘ·ΚΥΥαΘ§¥ΥάύΕύκΡ–ό ΈΒΡpHΟτΗ–÷§÷ Χε“©ΈοΘ·ΚΥΥα ΆΖ≈Ιΐ≥ΧΘ§ΦϊΆΦ1ΓΘ
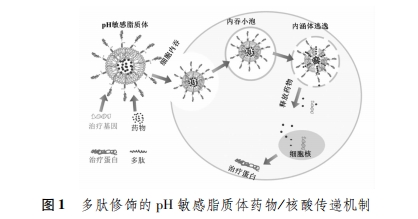
2 ΕύκΡ–ό ΈpHΟτΗ–÷§÷ ΧεΒΡ–ό ΈΖΫ Ϋ
ΝΉ÷§ΚΆΒ®ΙΧ¥Φ «Κœ≥…÷§÷ ΧεΒΡ÷ς“Σ≤ΡΝœΘ§―–ΨΩ’ΏΆ®ΙΐΕύ κΡΕ‘ΝΉ÷§ΚΆΒ®ΙΧ¥ΦΒΡ–ό Έ÷Τ±Η≥ωΕύ÷÷ΕύκΡ–ό ΈΒΡ pH ΟτΗ–÷§ ÷ ΧεΓΘ¥ΥΆβΘ§÷±Ϋ”ΫΪ–ΓΖ÷Ή”ΕύκΡΤ§ΕΈ«Ε»κΒΫ÷§÷ ΧεΡΎΘ§÷Τ±Η ΕύκΡ«Ε»κ–Ά pH ΟτΗ–÷§÷ ΧεΒΡ―–ΨΩ“≤”–±®ΒάΓΘ
2. 1 ΕύκΡ–ό ΈΝΉ÷§άύ
ΕύκΡ÷ς“ΣΆ®ΙΐΕύ÷÷Μ·―ßΦϋΚœΒΡΖΫ Ϋ–ό ΈΝΉ÷§[25]ΓΘάΐ»γZhaoΒ»[26]ΫΪpHΟτΗ–κΡ[H7K(R2 )2]Ά®ΙΐθΘΑΖΦϋΚΆΕΰ”≤÷§θΘΝΉ÷§θΘ““¥ΦΑΖ(1,2-distearoyl-sn-glycero-3-phosphoethano-lamine,DSPE)Ν§Ϋ”Θ§≤…”Ο±ΓΡΛΖ÷…ΔΖ®÷Τ±Η≥ωΑϋ‘ΊΕύ»α±»–«ΒΡpHΟτΗ–÷§÷ ΧεΓΘΆ§ΡξΘ§XiaΒ»[27] ≤…”ΟΦ”≥…Ζ¥”ΠΫΪDSPE-PEG2000-MalΚΆΨΏ”–pHœλ”Π–‘ΒΡœΗΑϊ¥©ΡΛκΡTHκΡ[AGYLL-GHINLHHLAHL(Aib)HHIL-Cys]Ν§Ϋ”Θ§Κœ≥…ΝΥDSPE-PEG2000-TH,»ΜΚσΫΪ¥σΕΙΝΉ÷§ΓΔΒ®ΙΧ¥ΦΓΔDSPE-PEG2000-OMeΚΆDSPE-PEG2000-THΑ¥’’ΡΠΕϊ±»59ΓΟ33ΓΟ2ΓΟ6÷Τ±Η≥ωΕύκΡ–ό ΈΒΡpHΟτΗ–÷§÷ ΧεΓΘΕύκΡ–ό ΈΝΉ÷§ΒΡ÷ς“ΣΦϋΚœΖΫ ΫΦϊΆΦ2ΓΘ

2. 2 ΕύκΡ–ό ΈΒ®ΙΧ¥Φάύ
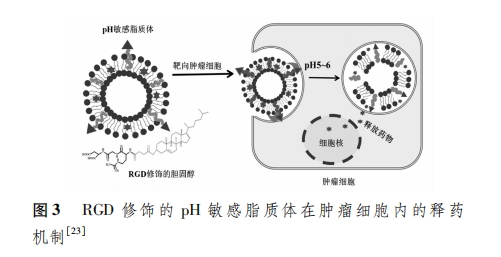
Β®ΙΧ¥ΦΨΏ”–ΒςΫΎΝΉ÷§ΥΪΖ÷Ή”≤ψΝςΕ·–‘ΒΡΉς”ΟΓΘΨΏ”–pHΟτΗ––‘ΒΡCHEMS «“Μ÷÷Ω…±Μ÷ Ή”Μ·ΒΡΒ®ΙΧ¥ΦΘ§‘ΎΥα–‘ΧθΦΰœ¬Θ§÷ Ή”Μ·ΒΡCHEMS”…”ΎΨ≤Βγ≥βΝΠΉς”ΟΘ§‘λ≥…÷§÷ ΥΪΖ÷Ή”≤ψΫαΙΙΒΡΤΤΜΒ[28]ΓΘ―–ΨΩ’ΏΫΪΙΠΡή–‘ΕύκΡΤ§ΕΈΚΆCHEMSΆ®ΙΐθΘΑΖΦϋΝ§Ϋ”Θ§÷Τ±Η≥ωΗς÷÷ΕύκΡ–ό ΈΒΡpHΟτΗ–÷§÷ ΧεΓΘ»γChangΒ»[23] ΫΪΑ–œρ’ϊΚœΥΊΠΝvΠ¬3ΒΡ–ΓΖ÷Ή”κΡRGDΚΆCHEMSΆ®ΙΐθΘΑΖΦϋœύΝ§Θ§RGD–ό ΈΒΡpHΟτΗ–÷§÷ ΧεΡή”––ßΑ–œρΠΝvΠ¬3Ιΐ±μ¥οΒΡΑ©œΗΑϊΘ§‘ω«ΩΕύΈςΥϊ»ϋΒΡ“©”Ο–ßΙϊΓΘΤδRGD–ό ΈCHEMSΒΡΖΫ ΫΦΑpHΟτΗ–÷§÷ ΧεΒΡ Ά“©Ιΐ≥ΧΦϊΆΦ3ΓΘ
GALA(WEAALAEALAEALAEHLAEALAEALEALAA) «“Μ÷÷pHΟτΗ–ΒΡΡΛ»ΎΚœκΡΘ§ΤδκΡΝ¥‘Ύ…ζάμpHΧθΦΰœ¬“‘ΈόΙφΨμ«ζΈΣ÷ςΘ§Εχ‘ΎΥα–‘ΧθΦΰœ¬Θ§ΗΜΚ§Ι»Α±ΥαΒΡκΡΝ¥÷ Ή”Μ·Θ§GALAΒΡΫαΙΙ‘ρ“‘ΠΝ¬ί–ΐΈΣ÷ς[29]ΓΘKakudoΒ»[30]ΫΪGALAΚΆ¬»ΦΉΥαΒ®ΙΧ¥ΦθΞΆ®ΙΐθΞΦϋΝ§Ϋ”Θ§÷Τ±Η≥ωGALAκΡ–ό ΈΒ®ΙΧ¥ΦΒΡpHΟτΗ–÷§÷ ΧεΓΘ
2. 3 ΕύκΡ«Ε»κ–Ά
άύΥΤ”Ύ GALA , –μΕύ pH ΟτΗ–ΕύκΡ‘ΎΥα–‘ΧθΦΰœ¬Θ§ΜαΒΦ÷¬ κΡΝ¥ΕΰΦΕΫαΙΙΒΡ±δΜ·Θ§»γΙϊΫΪ¥ΥάύΕύκΡ«Ε»κΒΫΝΉ÷§ΥΪΖ÷Ή” ≤ψΘ§÷Τ±ΗΒΟΒΫΒΡ pH ΟτΗ–÷§÷ ΧεΜαΥφΉ≈ pH ÷ΒΜΖΨ≥ΒΡ±δΜ·ΗΡ ±δΤδΥΪΖ÷Ή”≤ψΒΡΈ»Ε®–‘Θ§¥”Εχ ΆΖ≈ΩΙ÷ΉΝω“©ΈοΜρΚΥΥαΓΘ
άΐ»γΘ§Sosunov Β»[31] ΦΑ Yao Β»[32] ―–ΨΩ’Ώ≤…”Ο pH ΟτΗ–Εύ κΡ pHLIP ( ACEQNPIYWARYADWLFTTPLLLLDLALLVDADE GT)«Ε»κΒΡΖΫ Ϋ÷Τ±ΗΝΥ pH ΟτΗ–÷§÷ ΧεΓΘReja Β»[33] …ηΦΤΝΥ “ΜœΒΝ–ΕύκΡΘ§ΥϋΟ«ΒΡ ηΥ°Α±ΜυΥαΚΆΦΪ–‘Α±ΜυΥαΦδΗτ≈≈Ν–Θ§‘Ύ ΕΰΦΕΫαΙΙ…œΡή–Έ≥… pH ΟτΗ–ΒΡ“λ‘¥ΕΰΨέΧεΘ§…ζάμΧθΦΰœ¬≥ œ÷ ¬ί–ΐΫαΙΙΘ§÷§÷ ΧεΒΡΝΉ÷§ΥΪΖ÷Ή”≤ψΈ»Ε®Θ§ΒΪ «‘Ύ pH 5. 5 ΒΡΜΖ Ψ≥÷–Θ§ΕύκΡ÷ Ή”Μ·Θ§ΤδΫαΙΙ”…¬ί–ΐΫαΙΙΉΣ±δ≥…Υ……ΔΒΡΈόΙφΨμ «ζΘ§“λ‘¥ΕΰΨέΧεΫβΨέΘ§¥”Εχ Ι pH ΟτΗ–÷§÷ ΧεΡΎΒΡ“©ΈοΒΟ“‘ Ά Ζ≈ΓΘΤδ÷–Θ§P3 ( LKKIKDKLEKIKSKLYKIKNELAKIKKL) ”κ P5 (LKKIKDKLEKZKSKLYKIKNELAKIKKL) –Έ≥…ΒΡ“λ‘¥ΕΰΨέΧε pH ΟτΗ––‘ΉνΈΣΆΜ≥ωΓΘ
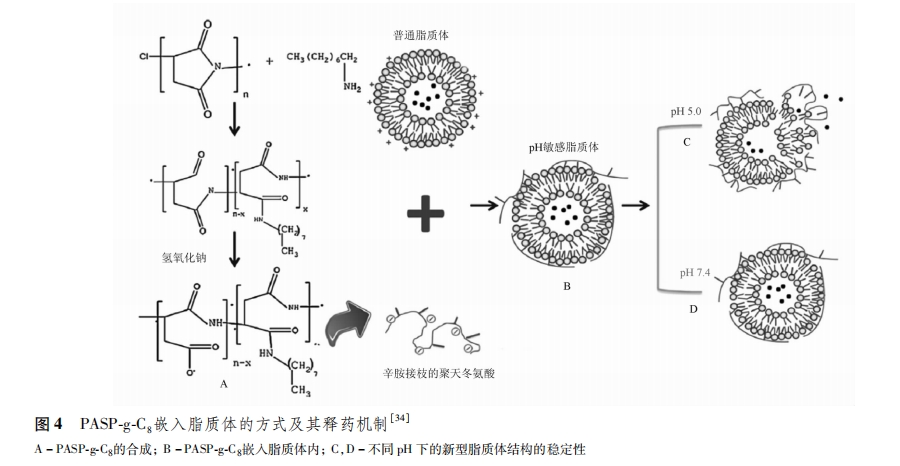
”…”Ύ’βάύΕύκΡ–η“Σ’ϊΧε«Ε»κΒΫ÷§÷ ΧεΒΡ ηΥ°≤ψΘ§“ρ¥ΥΕύκΡ–ρΝ–÷–“ΜΑψΚ§”–ΫœΕύΒΡ ηΥ°–‘Α±ΜυΥαΘ§άΐ»γΝΝΑ±Υα(L)ΓΔ“λΝΝΑ±Υα(I)ΓΔ…ΪΑ±Υα(W)ΓΔγ”Α±Υα(V)ΓΔ±ϊΑ±Υα(A)Β»ΓΘΙΐΕύΒΡ ηΥ°–‘Α±ΜυΥαΗχ÷§÷ ΧεΒΡ÷Τ±Η¥χά¥“ΜΕ®ΒΡάßΡ―Θ§“ρ¥Υ‘ΎΕύκΡ«Ε»κ–ΆpHΟτΗ–÷§÷ Χε÷–Θ§ Ι”ΟΝΫ«Ή–‘‘”ΚœκΡΒΡΖΫ ΫΉνΈΣ≥ΘΦϊΓΘάΐ»γΘ§WangΒ»[34]Ά®Ιΐ«Ε»κΒΡΖΫ ΫΫΪ–ΝΑΖΫ”÷ΠΒΡΨέΧλΕ§Α±Υα(PASP-g-C8)≤ε»κΒΫ÷§÷ Χε÷–Θ§ΦϊΆΦ4ΓΘ ηΥ°–‘C8Ω…“‘ΫΪΨέΚœΈοΓΑΟΣΕ®Γ±‘Ύ÷§÷ Χε ηΥ°«χΘ§ΨέΧλΕ§Α±ΥαΒΡ”Έάκτ»ΥαΜυΆ≈‘ρΩ…“‘‘ΎΥα–‘ΧθΦΰœ¬ΖΔ…ζ÷ Ή”Μ·ΕχΫιΒΦΙΙœσΒΡ±δΜ·Θ§¥”Εχ Ι“©ΈοΒΟΒΫΩλΥΌ ΆΖ≈ΓΘHamaΒ»[35] ΫΪΫ”÷Π °ΑΥΆιΥαΒΡpHΟτΗ–ΕύκΡSAPSP(stearyl-GGGGHGAHEHAGHEHAAGEHHA-HE-NH2)«Ε»κΒΫ÷§÷ ΧεΡΎΘ§ΧαΗΏΝΥ÷§÷ ΧεΕ‘÷ΉΝωΈΔΜΖΨ≥ΒΡΑ–œρ–‘ΓΘJiangΒ»[36] ÷Τ±ΗΒΡ÷§÷ Χε«Ε»κΝΥ °ΑΥΆιΥαΫ”÷ΠΒΡR6H4(stearyl-R6H4),R6H4ΦφΨΏpHΟτΗ––‘(H4)ΦΑœΗΑϊ¥©ΡΛ(R6)ΒΡΙΠΡήΘ§–Έ≥…ΝΥ“Μ÷÷ΕύΙΠΡή–‘pHΟτΗ–÷§÷ ΧεΓΘ
”–“βΥΦΒΡ «Θ§SuΒ»[37]…ηΦΤΝΥ2ΧθΨΏ”–pHΟτΗ––‘Θ§Ά§ ±”÷ΗΜΚ§’ΐΒγΚ…ΒΡΕύκΡ–ρΝ–(AWWKKKGGNNNΓΔAWWRRRG-GNNN),”…”ΎΨΏ”– ηΥ°–‘AWW,ΕύκΡΩ…“‘ΓΑΟΣΕ®Γ±ΒΫ÷§÷ ΧεΒΡ ηΥ°«χΘ§Ά§ ±ΗΜΚ§’ΐΒγΚ…ΒΡάΒΑ±ΥαΘ·ΨΪΑ±ΥαΤ§ΕΈ”÷Ω…“‘”κ±μΟφ¥χΗΚΒγΚ…ΒΡ÷§÷ ΧεΆ®ΙΐΨ≤ΒγΉς”ΟΕχ–Έ≥…÷§÷ ΧεΒΡΓΑΆβ“¬Γ±Θ§’βΦ» «“Μ÷÷ΕύκΡ«Ε»κ–ΆΘ§Ά§ ±“≤ «“Μ÷÷ΕύκΡ–ό ΈΝΉ÷§–ΆΒΡpHΟτΗ–÷§÷ ΧεΓΘ
3 ΕύκΡ–ό ΈΒΡpH ΟτΗ–÷§÷ ΧεΉςΈΣ‘ΊΧεΒΡ÷ς“Σ”Π”Ο
3. 1 ΕύκΡ–ό Έ pH ΟτΗ–÷§÷ ΧεΉςΈΣ ηΥ°–‘“©ΈοΒΡ‘ΊΧε
ΈΣΝΥΫβΨω ηΥ°–‘ΩΙ÷ΉΝω“©ΒΡ…ζΈοάϊ”ΟΕ»ΒΆΚΆΑ–œρ–‘≤ν Β»Έ ΧβΘ§Ά®≥Θ Ι”ΟΈοάμΑϋ¬ώΒΡΖΫΖ®ΫΪ“©ΈοΑϋΉΑΒΫ÷§÷ ΧεΡΎΓΘ÷§÷ ΧεΒΡΝΉ÷§ΥΪΖ÷Ή”≤ψΨΏ”–ΑϋΉΑ ηΥ°–‘“©ΈοΒΡΧλ»Μ”≈ ΤΓΘ÷ΉΝωΉι÷·ΈΔΜΖΨ≥ «»θΥα–‘ΜΖΨ≥Θ§pH‘ΦΈΣ5.8~7.0[9]ΓΘ“ρ¥ΥΘ§pHΟτΗ–÷§÷ Χε≥…ΈΣ“Μ÷÷÷Ί“ΣΒΡΩΙ÷ΉΝω“©Έο‘ΊΧεΘ§ ήΒΫ‘Ϋά¥ ‘ΫΕύ―ß’ΏΒΡΙΊΉΔΓΘ
DingΒ»[38] άϊ”ΟΥαΟτΗ–κξΦϋ…ηΦΤΝΥ“Μ÷÷¥©ΡΛκΡ(GGRRRRRRRRR)–ό ΈΒΡpHΟτΗ–÷§÷ ΧεΓΘΫαΙϊΖΔœ÷Θ§pHΟτΗ–÷§÷ Χε–·‘ΊΒΡDiR”ΪΙβΧΫ’κ‘Ύ–Γ σΒΡ÷ΉΝω≤ΩΈΜΥυΖΔ≥ωΒΡ”ΪΙβ–≈Κ≈Οςœ‘ΗΏ”ΎΤδΥϊ‘ΊΧεΒΡ–≈Κ≈Θ§ΧεΡΎ“©ΈοΖ÷≤Φ Β―ιΫχ“Μ≤Ϋ÷Λ ΒΘ§¥©ΡΛκΡ–ό ΈΒΡpHΟτΗ–÷§÷ ΧεΫΒΒΆΝΥ“©Έο‘ΎΤδΥϊΉι÷·ΤςΙΌΒΡΖ÷≤ΦΓΘZhaoΒ»[26] άϊ”ΟΨΏ”–Εύ±έΫαΙΙΒΡpHΟτΗ–κΡ[H7K(R2)2]–ό ΈΝΉ÷§–Έ≥…pHΟτΗ–÷§÷ ΧεΑϋ‘ΊΕύ»α±»–«ΓΘΧεΆβ Β―ιΫαΙϊ÷Λ ΒΘ§‘ΎpH5.5 ±÷§÷ ΧεΒΡ Ά“©ΝΩ¥οΒΫ85%,‘Ε‘Ε¥σ”ΎpH7.4 ±20%ΒΡ Ά“©ΝΩΘ§œ‘ Ψ≥ωΫœ«ΩΒΡpHΟτΗ––‘ΓΘΧεΡΎ“©ΈοΖ÷≤Φ Β―ι“≤÷Λ ΒΘ§’β÷÷pHΟτΗ–÷§÷ Χε‘ωΦ”ΝΥ“©Έο‘Ύ÷ΉΝω≤ΩΈΜΒΡ ΆΖ≈Θ§Ε‘–Γ σΫΚ÷ ΝωΉι÷·ΨΏ”–Ηϋ«ΩΒΡ“÷÷ΤΉς”ΟΓΘ
ShiΒ»[39]άϊ”ΟΜΖ–ΈΒΡ÷ΉΝωΑ–œρ–ΓΖ÷Ή”κΡ[c(RGDfK)] ΚΆ¥©ΡΛTHκΡ≈ΦΝΣΘ§÷Τ±ΗpHΟτΗ–÷§÷ Χε≤ΔΑϋ‘ΊΉœ…Φ¥ΦΓΘΜν Χε”Αœώ―ßœ‘ ΨΘ§pHΟτΗ–÷§÷ ΧεΉι÷ΈΝΤΒΡΚ…Νω–Γ σΧεΡΎ÷ΉΝω “÷÷Τ¬ ΈΣ85.04%,‘Ε‘ΕΗΏ”ΎΤδΥϊΕ‘’’ΉιΓΘΕχKorenΒ»[40] ≤…”ΟΨ≠ΒδΒΡ¥©ΡΛκΡTATΓΔΩΙΑ©ΩΙΧε2C5Ά§ ±–ό ΈΝΉ÷§Θ§÷Τ±Η ΝΥ“Μ÷÷ΫαΙΙΗϋΈΣΗ¥‘”ΒΡpHΟτΗ–Οβ“Ώ÷§÷ ΧεΘ§≤ΔΑϋ‘ΊΕύ»α±» –«ΓΘ≥ΐΝΥpHœλ”Π–‘Θ§’β÷÷ΕύΙΠΡή÷§÷ ΧεΆ§ ±ΜΙΨΏ”–ΝΦΚΟΒΡ ¥©ΡΛΡήΝΠΦΑΧΊ“λΒΡΑ–œρ–‘ΓΘΫαΙϊœ‘ ΨΘ§‘ΎpH5.0ΧθΦΰœ¬Θ§MCF-7œΗΑϊΚΆHeLaœΗΑϊ…ψ»κΒΡ÷§÷ ΧεΟςœ‘ΗΏ”ΎΤδ‘ΎpH 7.4 ±ΒΡ…ψ»κΘ§Ά§ ± Βœ÷ΝΥΕύ»α±»–«‘Ύ÷ΉΝωœΗΑϊΒΡ”––ß ΗΜΦ·ΓΘ
¥ΥΆβΘ§≥ΐΝΥΕ‘÷§÷ ΧεΒΡΆβ‘ΎΫαΙΙΦ”“‘ΗΡΫχΘ§ΈΣΝΥ”ΠΕ‘÷ΉΝωΒΡΕύ÷ΊΡΆ“©–‘Έ ΧβΘ§÷§÷ ΧεΩ…Αϋ‘ΊΕύ÷÷“©ΈοΓΘLiuΒ»[41] άϊ”ΟHer-2ΩΙΧε–ό ΈpHΟτΗ–÷§÷ ΧεΘ§Ά§ ±Αϋ‘ΊΈ§ά≠≈ΝΟΉΘ®“λ≤ΪΕ®Θ©ΚΆΕύ»α±»–«Θ§”––ß“÷÷ΤΝΥHer-2Ιΐ±μ¥οΒΡ»ιœΌΑ©Ήι÷·Θ§“÷÷Τ¬ Χα…ΐ÷Ν83.9%ΓΘ
3. 2 ΕύκΡ–ό ΈΒΡ pH ΟτΗ–÷§÷ ΧεΉςΈΣΚΥΥα¥ΪΒίΒΡ‘ΊΧε
ΥφΉ≈ΚΥΥα―–ΨΩΒΡΖΔ’ΙΘ§άΐ»γ÷ΈΝΤ–Ά÷ ΝΘDNAΓΔsiRNAΓΔmiRNAΚΆsnoRNAΒ»Εύ÷÷ΙΠΡή–‘ΚΥΥα±ΜΖΔœ÷ΨΏ”–÷Ί“ΣΒΡ“Ϋ ”ΟΦέ÷ΒΓΘΒΪ’β–©ΚΥΥαΖ÷Ή”Θ§ΧΊ±π «RNA»ί“Ή±ΜΧεΡΎRNase ΫΒΫβΓΘάϊ”ΟΕύκΡ–ό ΈΒΡpHΟτΗ–÷§÷ ΧεΕ‘ΚΥΥαΫχ––Αϋ‘ΊΘ§Ω… “‘ΧαΗΏΜυ“ρ÷ΈΝΤΒΡ–ßΙϊΓΘ
HatakeyamaΒ»[42]ΫΪGALAΝ§ΒΫΒ®ΙΧ¥Φ…œ÷Τ±Η≥ωpHΟτΗ–÷§÷ ΧεΘ§≤Δ―–ΨΩΤδ¥ΪΒίsiRNAΚσΒΡΜυ“ρ≥ΝΡ§–ßΙϊΓΘΫαΙϊ÷Λ ΒΘ§‘Ί»κsiRNAΒΡpHΟτΗ–÷§÷ ΧεΒΡΧεΆβΜυ“ρ≥ΝΡ§–߬ ”κsiRNA±Ψ…μ≤ΔΟΜ”–≤ν±πΘ§ΒΪ‘Ύ–Γ σ÷ΉΝωΉι÷·÷––߬ ΧαΗΏΝΥ40%,ΥΒΟς”ΟGALAκΡ–ό ΈΒΡpHΟτΗ–÷§÷ ΧεΩ…“‘”––ß±ΘΜΛΚΥΥα≤ΔΫΪΤδΑ–œρ¥ΪΒίΒΫ÷ΉΝω≤ΩΈΜΓΘΫϋΡξά¥Θ§–ό Έ÷§÷ ΧεΒΡΕύκΡ–ρΝ–…ηΦΤΒΟΗϋΈΣΨΪΟνΘ§ΙΠΡή“≤”ζΖΔΆΜ≥ωΓΘάΐ»γΘ§XiangΒ»[43]…ηΦΤΝΥ“Μ÷÷–¬–ΆΒΡpHΟτΗ––ΆœΗΑϊ¥©ΡΛκΡ(activatablecell-penetratingpeptide,ACPP)ΓΘ–ό Έ÷§÷ ΧεΒΡACPP”…÷–ΦδΒΡΒΑΑΉΟΗ«–ΈΜΒψΝ§Ϋ”ΝΫΕΥΒΡΕύΨέ―τάκΉ”Θ·¥©ΡΛκΡR8ΚΆΕύΨέ“θάκΉ”κΡ(GHE)4,–Έ≥…÷§÷ Χε-R8-ΟΗ«–ΈΜΒψ-(GHE)4 ΒΡΫαΙΙΓΘ‘Ύ÷ΉΝωΉι÷·ΈΔΜΖΨ≥ΒΡΒΆpH÷Βœ¬Θ§R8ΚΆ(GHE)4÷°Φδ”…Ψ≤ΒγΈϋ“ΐΉΣΈΣ≈≈≥βΓΘΆ§ ±Θ§ΟΗ«–ΈΜΒψ±Μ÷ΉΝωΉι÷·Ιΐ±μ¥οΒΡMMP2/9«–ΕœΘ§R8–ρΝ–ΦΧ–χ±ΘΝτ‘Ύ÷§÷ Χε…œΘ§–– Ι¥©ΡΛκΡΒΡΙΠΡήΓΘ’β“ΜΙΐ≥ΧΉν÷’¥ΌΫχΝΥACPP–ό ΈΒΡpHΟτΗ–÷§÷ Χε‘ΎΧΊΕ®ΒΡ÷ΉΝωΉι÷·≤ΩΈΜ±ΜœΗΑϊΡΎΆΧΘ§‘ω«ΩΝΥΑϋΉΑΒΡsiRNAΕ‘ΙΊΦϋ‘≠Α©Μυ“ρPlk1ΒΡ≥ΝΡ§–ßΙϊΓΘ
ΡΩ«ΑΘ§ΙΙΫ®άύΥΤΦΠΈ≤ΨΤΝΤΖ®ΒΡpHΟτΗ–÷§÷ ΧεΙ≤¥ΪΒί“©ΈοΚΆΚΥΥαΒΡ―–ΨΩ“≤‘ΎΩΣ’ΙΓΘάΐ»γΘ§LiΒ»[44]…ηΦΤΒΡpHΟτΗ–÷§÷ ΧεΡήΙΜΆ§ ±Αϋ‘Ίœ≤ ςΦνΚΆsiRNAΓΘYaoΒ»[45]÷Τ±ΗΝΥΡήΆ§ ±Αϋ‘ΊΥςά≠Ζ«ΡαΓΔsiRNAΒΡpHΟτΗ–÷§÷ ΧεΓΘάϊ”ΟpHΟτΗ–ΕύκΡH6L9–ό ΈΒΡ÷§÷ Χε‘ΎΓΑ»ήΟΗΧεΧ”“ίΓ±ΚσΘ§ ΆΖ≈ΒΡmiRNAΚΆœ≤ ςΦνΙ≤Ά§Ής”Ο”ΎΑ©œΗΑϊΘ§Ά®Ιΐœ¬ΒςHoxd10ΒΡ±μ¥οΚΆΕ‘œΗΑϊΒΡ÷±Ϋ”…±…ΥΉς”ΟΘ§”’ΒΦœΗΑϊΒΡΒρΆωΚΆΜΒΥά[46]ΓΘ
4 Ϋα”ο”κ’ΙΆϊ
ΕύκΡ–ό ΈΒΡpHΟτΗ–÷§÷ ΧεΉςΈΣ“©ΈοΘ·ΚΥΥα‘ΊΧεΘ§ΨΏ”–pHΟτΗ––‘ΦΑΕ‘÷ΉΝωΉι÷·ΒΡΑ–œρ–‘Β»ΧΊ’ςΘ§Ω… Βœ÷“©ΈοΘ·ΚΥΥα‘Ύ÷ΉΝω≤ΩΈΜΒΡΨέΦ·ΦΑΩλΥΌ ΆΖ≈Θ§Φθ…ΌΝΥΩΙ÷ΉΝω“©ΈοΒΡΕΨΗ±Ής”ΟΘ§ΧαΗΏ“©ΈοΒΡάϊ”Ο¬ Θ§ΨΏ”–ΝΦΚΟΒΡ”Π”Ο«ΑΨΑΓΘΕύκΡ–ό ΈΒΡpHΟτΗ–÷§÷ ΧεΒΡΖΔ’ΙΡΩ«ΑΜΙ¥φ‘Ύ÷νΕύ’œΑ≠Θ§ΤδΈ»Ε®–‘ΦΑΧΊ“λ–‘ΜΙ”–¥ΐΫχ“Μ≤ΫΧαΗΏΓΘœύ–≈ΥφΉ≈―–ΨΩΒΡ…ν»κΚΆ÷Τ±ΗΦΦ θΒΡ≥… λΘ§―–ΨΩ’ΏΡήΙΜ―–÷Τ≥ωΗϋΗΏ–ßΈ»Ε®ΒΡpHΟτΗ–÷§÷ Χε”Π”Ο”Ύ÷ΉΝωΒΡΝΌ¥≤÷ΈΝΤΓΘ
Οβ‘π…υΟςΘΚ±ΨΈΡΈΣ––“ΒΫΜΝς―ßœΑΘ§Αφ»®Ιι‘≠Ής’ΏΦΑ‘≠‘”÷ΨΥυ”–Θ§»γ”–«÷»®Θ§Ω…ΝΣœΒ…Ψ≥ΐΓΘΈΡ’¬±ξΉΔ”–Ής’ΏΦΑΈΡ’¬≥ω¥ΠΘ§»γ–η‘ΡΕΝ‘≠ΈΡΦΑ≤ΈΩΦΈΡœΉΘ§Ω…‘ΡΕΝ÷–Ιζ“©―ß‘”÷Ψ2018Ρξ6‘¬ΒΎ53ΨμΒΎ11ΤΎ






