
еЊвЊ:ВЁОњИаШОбЯжиЭўаВзХШЋШЫРрЕФЩњУќНЁПЕ,гЩгкПЙЩњЫиЕФРФгУЕМжТФЭвЉОњВЛЖЯзЬЩњ,ДЋЭГПЙЩњЫивЉЮяПЊЗЂГйжЭ,ЦШЧаашвЊПЊЗЂаТаЭПЙОњЗжзгЁЃРћгУЛЏбЇЗНЗЈЙЙНЈПЙОњИпЗжзгВФСЯЛђПЙОњвЉЮяЕФЕнЫЭЬхЯЕ,ЪЧЖдПЙФЭвЉОњЕФгаСІЮфЦїЁЃБОЮФжиЕуНщЩмСЫНќФъРДИїРрПЙОњИпЗжзгВФСЯдкЩшМЦЁЂКЯГЩЗНУцЕФбаОПНјеЙ,вдМАдкЖдПЙВЁОњФЭвЉадЮЃЛњжаЕФгІгУЗНЯђКЭЧАОАЁЃ
ЯИОњБщВМгкЮвУЧЕФЩњДцЛЗОГжа,ЦфжаДѓВПЗжПЩвдгыШЫРрКЭЦНЯрДІ,ЕЋШдгажкЖржТВЁОњЛсв§Ц№ИїРрМВВЁ,дкТўГЄЕФШЫРрРњЪЗжа,етаЉвўВидкШЫРрЩэБпЕФЩБЪжЭЈЙ§вЛЕРаЁаЁЕФЩЫПкБуФмЕМжТжТУќИаШОЁЃжБЕН1928Фъ,AlexanderFlemingЗЂЯжЧрУЙЫи,ВЂгк20ЪРМЭ40ФъДњЭЖШыСйДВЪЙгУ,ЮвУЧНјШыЁАПЙЩњЫиЪБДњЁБ,ИїРрПЙЩњЫивЉЮяЯрМЬЮЪЪР,ЪЙШЫРргЕгаСЫЕжПЙВЁОњИаШОЕФгаСІЮфЦї[1] ЁЃШЛЖјКУОАВЛГЄ,ШЫРрЖдПЙЩњЫиГЄЦкЙ§СПКЭВЛЧЁЕБЕФЪЙгУ,МБОчМгЫйСЫВЁОњФЭвЉадЭЛБфЕФЗЂЩњ,ИїРрФЭвЉОњВЛЖЯГіЯж,зюже,ОпгаЖржиФЭвЉадЕФЁАГЌМЖЯИОњЁБЮЪЪР,ЪЙЯИОњИаШОЕФжЮСЦФбЖШдіДѓ[2] ЁЃОнЪРНчЮРЩњзщжЏ(WHO)2019ФъЗЂВМЕФБЈИц,ШЋЧђФПЧАУПФъжСЩйга70ЭђШЫЫРгкФЭвЉадВЁОњИаШО,ШєвдФПЧАЕФЧїЪЦМЬајЗЂеЙ,ЕН2050ФъШЋЧђУПФъЫРгкФЭвЉОњИаШОЕФШЫЪ§ПЩФмЛсдіМгЕН1000ЭђШЫ/Фъ[3] ЁЃОнЪРНчвјааМЦЫу,вдЯждкЧїЪЦЕН2050Фъ,ПЙЩњЫиФЭвЉадЮЪЬтдьГЩЕФШЋЧђОМУЫ№ЪЇУПФъНЋГЌЙ§2ЭђвкУРдЊ[4] ,ЖдСИЪГКЭЫЧСЯЕФЩњВњЁЂУГвзЕШЗНУцЕФгАЯьИќЪЧВЛПЩЙРСПЁЃ
ШЛЖјИљОнУРЙњЪГЦЗвЉЦЗМрЖНЙмРэОж(FDA)ЕФЪ§ОнЯдЪО,зд1980ФъжЎКѓЯЪгааТПЙЩњЫивЉЮяНјШыЪа ГЁ[5] ,вЛЗНУцЪЧбИЫйЗЂеЙЕФВЁОњФЭвЉадЪЙЕУвбгаПЙЩњЫиЪЇаЇ,СэвЛЗНУцЪЧаТвЉбаЗЂЕФМшФбКЭГйЛКЁЃ2014Фъ,WHOаћВМШЫРрвбНјШыЁАКѓПЙЩњЫиЪБДњЁБ[5] ЁЃГ§СЫМгЧПеўИЎМрЙмгыаћДЋ,в§ЕМЮРЩњЯЕЭГЁЂХЉФСвЕКЭЙЋжк е§ШЗПДД§ВЂПЦбЇЪЙгУПЙЩњЫижЎЭт,ЦШЧавЊЧѓбаОПепУЧЛ§МЋЬНЫїаТЕФПЙОњВФСЯКЭЗНЗЈРДгІЖдетвЛЮЃЛњЁЃНќ ФъРД,ЛљгкИпЗжзгВФСЯЕФаТаЭПЙОњВФСЯКЭвЉЮяЕнЫЭЬхЯЕж№НЅГЩЮЊбаОПШШЕу,ЭЈЙ§ЬьШЛИпЗжзгаоЪЮЁЂКЯГЩПЙ ОњЖрыФМАЦфИпЗжзгРрЫЦЮяЁЂПЙОњвЉЮяЕнЫЭдиЬхЁЂЙтЖЏСІПЙОњСЦЗЈЕШПЩвдгааЇЩБУ№ВЁОњ,зшжЙ/МѕЛКФЭвЉад ЕФЗЂЩњЁЃБОЮФНЋЖдЩЯЪіЛљгкИпЗжзгЕФПЙОњВФСЯКЭЗНЗЈНјаазмНсКЭИХРЈ,вдЦкЮЊбАевЦЦНтВЁОњФЭвЉадЮЃЛњ ПЩааЗНАИЬсЙЉЦєЪОЁЃ
1 ЬьШЛПЙОњыФМАЦфзїгУЛњжЦ
1974Фъ,Ш№ЕфПЦбЇМвG.BomanЕШДгУМЮЦЬьВЯЖъгМ(samiacynthia)ЬсШЁГівЛжжОпгаПЙОњЛюадЕФЖр ыФ:ЬьВЯЫи(Cecropins)ЁЊЁЊЁЊетЪЧЪРНчЩЯзюдчЗЂЯжЕФЬьШЛПЙОњыФ(Antimicrobialpeptides,AMP)жЎвЛ[6, 7] ЁЃжЎКѓДѓСПбаОПЗЂЯж,ЖржжЖрбљЕФПЙОњыФЙуЗКДцдкгкЖЏЮяЁЂжВЮяКЭЮЂЩњЮяЕФУтвп/ЗРгљЯЕЭГжа,вђДЫвВБЛГЦЮЊЫожїЗРгљыФ(Host-defensepeptides,HDP),НижЙЕНФПЧА,вбОга3000гржжПЙОњыФБЛБЈЕР[8] ЁЃетРрПЙОњыФБЛГЦЮЊЁАаТвЛДњЕФПЙЩњЫиЁБЁЃВЛЭЌгкДЋЭГПЙЩњЫиЕФЪЧ,ПЙОњыФдкГЄЦк(МИЧЇЩѕжСЪ§ЭђФъ)ЗЂЛгзїгУЕФЭЌЪБ,ВЂУЛгав§Ц№ВЁОњЕФФЭвЉад,гаПЦбЇМвШЯЮЊетгыПЙОњыФгыЯИОњЯИАћФЄзїгУЕФЖРЬиПЙОњЛњжЦгаУмЧаЕФЙиСЊЁЃ
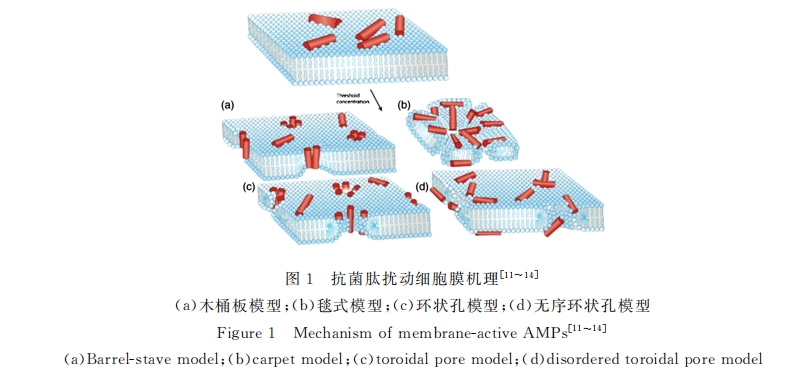
ЭЈЙ§ЖдПЙОњыФЕФНсЙЙбаОПЗЂЯж,ЫфШЛЫќУЧгаЖржжВЛЭЌЕФЖўМЖНсЙЙ(a-Тна§ЁЂІТ-елЕўЁЂЛЗыФЕШ),ЕЋПЙОњыФвЛАуЖМОпгагЩЪшЫЎАБЛљЫсВаЛљКЭе§ЕчКЩАБЛљЫсВаЛљЙЙГЩЕФСНЧзадНсЙЙ[9, 10] ЁЃЮЂЩњЮяЕФЯИАћФЄжаКЌгаНЯЖрЕФДјИКЕчадЕФСзжЌЗжзг,баОПепвЛАуШЯЮЊ,ПЙОњыФЕФе§ЕчадСНЧзадНсЙЙПЩвдгыДјИКЕчЕФЮЂЩњЮяЯИАћФЄЯрЛЅзїгУ,ШХЖЏВЂЦЦЛЕЦфСзжЌЫЋЗжзгВу,ДгЖјДяЕНЩБОњЕФаЇЙћЁЃеыЖдетвЛзїгУЛњжЦ,баОПепУЧЬсГіСЫЖржжФЃаЭ[11~13] ,НЯЮЊОЕфЕФга(a)ФОЭААхФЃаЭЁЂ(b)ЬКЪНФЃаЭЁЂ(c)ЛЗзДПзФЃаЭКЭ(d)ЮоађЛЗзДПзФЃаЭЕШ(ШчЭМ1ЫљЪО)ЁЃвЛАуШЯЮЊ,ПЙОњыФЭЈЙ§е§ЕчКЩЦЌЖЮгыДјИКЕчЕФЯИОњЯИАћФЄЯрЮќв§ЁЂЧзКЭ,ШЛКѓЦфЪшЫЎЦЌЖЮгыЯИАћФЄЯрЛЅзїгУ,ШХЖЏВЂЦЦЛЕСзжЌЫЋЗжзгВуНсЙЙ,ЕМжТЯИОњЕФЕђЭі[14] ЁЃ
ЫфШЛФПЧАвбЗЂЯжСЫ3000гржжПЙОњыФ,ЕЋЪЧеце§гІгУгкСйДВЕФШДКмЩйЁЃетЪЧгЩгквЛВПЗжПЙОњыФдкзїгУМССПЯТЖддКЫЩњЮяКЭецКЫЩњЮяЖМЛсЬхЯжЖОад,ЖдВИШщЖЏЮяЛсВњЩњШмбЊЕШЖОКІзїгУЁЃСэЭт,ПЙОњыФдкЖЏЮяЬхФкШнвзБЛЕААзУИЫЎНт,дкИпбЮЛЗОГЁЂЖўМлбєРызгЕШгАЯьЯТЛсаЮГЩОлМЏЬх;ВЂЧвПЙОњыФЕФЬсШЁКЭДПЛЏНЯЮЊРЇФбЧвАКЙѓЁЃЮЊПЫЗўПЙОњыФЕФетаЉШБЕу,баОПепУЧжТСІгкЭЈЙ§ЛЏбЇЗНЗЈФЃФтПЙОњыФЕФНсЙЙКЭЙІФм,РДШЫЙЄКЯГЩПЙОњОлыФЁЂРрыФКЭЫќУЧЕФИпЗжзгФЃФтЮя;ДѓСПбаОПвВвбОБэУї,ЛЏбЇЗНЗЈПЩвдвдЕЭГЩБОКЯГЩГіОпгаЙуЦзПЙОњадКЭИпбЁдёадЕФПЙОњыФМАЦфРрЫЦЮя[15] ЁЃ
2 ПЙОњИпЗжзгВФСЯ
НќФъРД,ЫцзХЖдПЙОњВФСЯЕФбаОПВЛЖЯЩюШы,ИпЗжзгВФСЯж№НЅЭЛЯдГіЦфгХЪЦЁЃЮвУЧНЋДгПЙОњОлЖрыФ/ОлАБЛљЫсЁЂПЙОњЬьШЛИпЗжзгМАЦфбмЩњЮяЁЂПЙОњыФЕФИпЗжзгФЃФтЮяЁЂЛљгкИпЗжзгЕФПЙОњвЉЮяЕнЫЭЬхЯЕвдМАЙтЖЏСІПЙОњИпЗжзгВФСЯетМИИіЗНУц,злЪіНќФъРДПЙОњИпЗжзгВФСЯЕФбаОПНјеЙЁЃ
2.1 ПЙОњОлЖрыФ/ОлАБЛљЫс
ПЙОњыФдкЫожїЬхФкКЌСПКмЕЭ,Г§СЫРћгУЛљвђЙЄГЬРДЭЈЙ§ЮЂЩњЮяЗЂНЭЩњВњПЙОњыФЭт,ЖржжЛЏбЇЗНЗЈПЩвдгУРДКЯГЩПЙОњыФМАЦфФЃФтЮяЁЃ1963Фъ,MerrifieldДДСЂЕФЙЬЯрКЯГЩЗЈЪЧФПЧАгУРДКЯГЩПЙОњыФЕФГЃгУЗНЗЈ,НЋАБЛљЫсЕФCФЉЖЫЙЬЖЈдкВЛШмЪїжЌЩЯ,ШЛКѓдкДЫЪїжЌЩЯвРДЮЫѕКЯАБЛљЫсЁЂбгГЄыФСД,ШЛКѓНЋыФСДДгЪїжЌЩЯЗжРыЁЂЬсДПЁЃДЫЗНЗЈКЯГЩОлЖрыФЕФВйзїМђЕЅ,ЕЋЪЧДцдкађСаЖЬЁЂЫљашЪБМфГЄЁЂКЯГЩЕФаЇТЪКЭДПЖШЕЭЁЂГЩБОИпЕШЮЪЬт,етаЉЮЪЬтЯожЦСЫОлЖрыФЙЬЯрКЯГЩЗЈЕФгІгУЗЖЮЇЁЃ
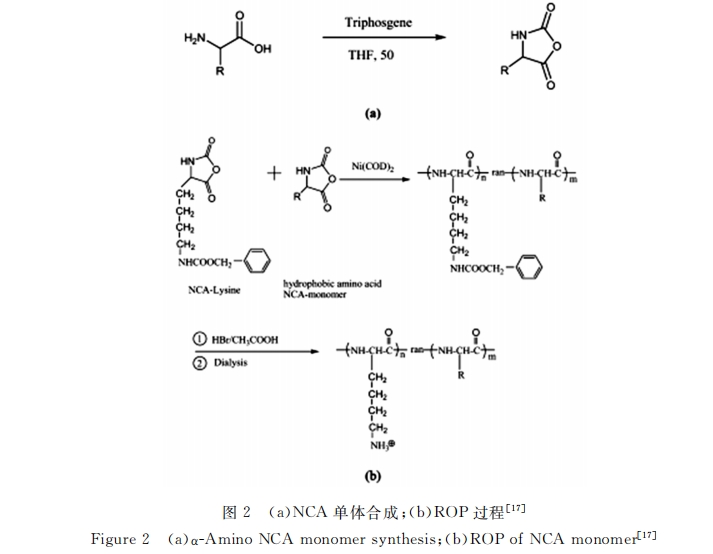
ЪєгквѕРызгПЊЛЗОлКЯ(ROP)ЕФІС-АБЛљЫсєШФкЫсєћ(NCA)ЗЈКЯГЩІС-ОлЖрыФ/ОлАБЛљЫсвђЦфММЪѕЭЈгУЁЂКЯГЩжмЦкЖЬЁЂГЩБОЕЭЁЂВйзїМђЕЅЁЂВњТЪИпЕШгХЕуБЛЙуЗКЪЙгУ[16] ЁЃНќФъРД,баОПепУЧВЩгУNCAЕФЗНЗЈКЯГЩ СЫЖржжІС-ОлЖрыФ/ОлАБЛљЫсВЂгІгУгкПЙОњСьгђ,ЛёЕУСЫЯджјаЇЙћЁЃChan-ParkЕШзюдчБЈЕРСЫРћгУNCAЗЈ КЯГЩОпгаПЙОњЙІФмЕФОлЖрыФЁЃШчЭМ2ЫљЪО,баОПШЫдБРћгУNi(COD)2 в§ЗЂШ§ЙтЦјЗЈКЯГЩЕФL-БНБћАБЫс NCAЁЂNІХ-мабѕєЪЛљ-L-РЕАБЫсNCAгыL-ССАБЫсNCA,дкDMFШмМСжаЪЕЯжROPЗДгІ,ЕУЕНСЫЮоЙцЙВОл ЖрыФ,ВЂЩИбЁГіСЫПЙОњаЇЙћзюМбЕФзщКЯ,ЖдE.coli,P.aeruginosa,S.aureus ЕФзюаЁвжОњХЈЖШ(MIC)Дя ЕН31ІЬg/mL[17] ЁЃ
HammondдђВЩгУШВ-ЕўЕЊЕуЛїЛЏбЇЕФЗНЗЈ,дкдЄЯШаоЪЮгаШВЛљЕФЁЂгЩNCAЗЈКЯГЩЕФОлЙШАБЫсжїСДЩЯ,НгжІЩЯВЎАЗЁЂжйАЗЁЂЪхАЗКЭМОяЇЛЏЕФВрСД,ЬНОПВрСДЖдПЙОњадФмЕФгАЯь,НсЙћЯдЪО,етаЉКЯГЩЕФбєРызгОлЖрыФЖдS.aureusКЭE.coliОпгаЙуЦзЕФПЙОњадФм,ВЂЧвОпгаЗЧГЃЕЭЕФШмбЊадФм[18, 19] ЁЃChengПЮЬтзщБЈЕРСЫЖржжNCAЗЈКЯГЩЕФПЙОњЖрыФ,ЖдИяРМЪЯвѕЁЂбєадЯИОњОпгаЙуЦзЕФЩБУ№аЇЙћ,ВЂЧвЩшМЦКЯГЩСЫОпгаPHЯьгІадЕФПЙОњЖрыФ,РћгУЯИОњИаШОДІPHЕФЮЂаЁВюБ№,ЪЕЯжІСТна§КЭздгЩОэЧњжЎМфЕФзЊБф,ОЁСПМѕЩйЖдВИШщЖЏЮяЯИАћЕФЖОад,ЭЌЪБЛЙФмБЃГжИпПЙОњЛюад[16, 20, 21] ЁЃDuПЮЬтзщНЋNCAКЯГЩЕФПЙОњЖрыФНјвЛВНГЌжЇЛЏ,ЪЙДјгаНЯЕЭе§ЕчКЩЕФПЙОњЖрыФОпгаИпаЇЕФЩБОњзїгУ[22] ЁЃГ§ДЫжЎЭт,вВВЩгУАБЛљаоЪЮЕФОлІХ-МКФкѕЅ(PCL-NH2)в§ЗЂL-БНБћАБЫсNCAгыNІХ-мабѕєЪЛљ-L-РЕАБЫсNCAОлКЯ,ЕУЕНСЫЧЖЖЮаЭЕФПЙОњЖрыФ[23] ЁЃLiuЕШбаОПЗЂЯж,бЁдёСљМзЛљЖўЙшЕЊЛЏяЎзїЮЊв§ЗЂМС,ПЩвдв§ЗЂРЕАБЫсЁЂ+-маЛљ-L-ЙШАБЫсЕШАБЛљЫсЕФNCAИпаЇЁЂПьЫйЕиОлКЯ,ПЙОњЪЕбщНсЙћЯдЪО,ДЫЗНЗЈКЯГЩЕФОлАБЛљЫсЖд S. aureus mu50, S. aureus USA300LAC, E. coli JM109 ЕФ MICДяЕН 12ІЬg/mL[24] ЁЃ
Г§ЩЯЪіВЩгУNCAЗЈКЯГЩПЙОњыФжЎЭт,ПЦбаЙЄзїепЛЙВЛЖЯПЊЗЂГіаТЕФПЙОњыФКЯГЩЗНЗЈЁЃжаПЦдКгІЛЏЫљЬегбЛЊЕШПЊЗЂГівЛжжФкѕЃАЗКЯГЩЖрыФЕФЗНЗЈ,ВЂГЩЙІКЯГЩСЫДЋЭГNCAЗЈЮоЗЈКЯГЩЕФІХ-ОлРЕАБЫс(ІХ-PL)ПЙОњыФ,НтОіСЫЮоЗЈЪЙгУЛЏбЇЗНЗЈКЯГЩжБСДІХ-PLетИіЙЋШЯадФбЬт[25] ЁЃ
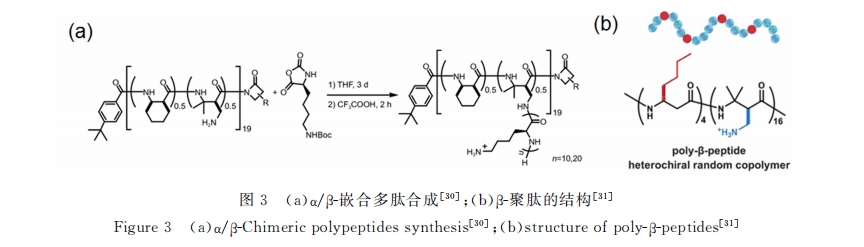
GellmanКЭLiuЕШГЄЦкжТСІгкФЃФтHDpЕФФсСњ-3РрПЙОњІТ-ОлыФбаОП[26~29] ЁЃзюНќ,LiuБЈЕРСЫвдІТ- ОлыФЮЊжїСДНгжІІС-ОлАБЛљЫсЕФІС/ІТ-ЧЖКЯЖрыФ[30] (ШчЭМ3aЫљЪО),ЖдUSA300ЁЂUSA300LacЕФMICДяЕН 0.38ІЬmol/LЁЃЪшЫЎЦЌЖЮ/бєРызгЕФБШР§УмЧаЙиЯЕЕНПЙОњыФЕФПЙОњаЇЙћ,ЛљгкетжжЙЙ-аЇЙиЯЕ,гжЩшМЦКЯГЩ СЫВЛЭЌЪшЫЎЦЌЖЮ/бєРызгБШР§ЕФІТ-ОлыФ(ШчЭМ3bЫљЪО),ОпгагХвьЕФПЙОњаЇЙћ,ЖдS. aureus(ATCC 6538)ЁЂS.aureus(USA300)ЁЂS.aureus(USA300LAC)ЕФMICДяЕН6.25ІЬg/mL,ВЂЧвгыЯИОњГЄЪБМфзї гУ,ЮогеЗЂЯИОњФЭвЉадМЃЯѓ[31] ЁЃ
2.2 ПЙОњЬьШЛИпЗжзгМАЦфбмЩњЮя
здШЛНчжаДцдкДѓСПЕФЬьШЛИпЗжзгЛЏКЯЮя,ЦфжавЛаЉОпгавЛЖЈЕФПЙОњадФмЁЃзюГЃМћЕФЬьШЛПЙОњИпЗжзг ШчПЧОлЬЧ,ЪЧвЛжжДје§ЕчКЩЕФжБСДаЭЖрЬЧ,гЩМзПЧЫиОХЈМюДІРэЭбШЅввѕЃЛљКѓЕУЕНЕФ,жївЊРДдДгкаЗПЧЁЂЯКПЧЁЂБДПЧЕШМзПЧРрПЧЬхЁЃПЧОлЬЧЕФАБЛљПЩвддкЕЭpHЯТБЛжЪзгЛЏЖјДје§Ечад,ОпгавЛЖЈЕФПЙОњаЇЙћЁЃЕЋЪЧдкжаадЩњРэЬѕМўЯТ,ПЧОлЬЧШмНтадКмВю,КмФбЗЂЛгЦфПЙОњаЇЙћ,ЫљвдашвЊЖдЦфНјааЛЏбЇаоЪЮ,ДгЖјЕУ ЕНПЙОњЛюадИпЁЂШмНтадКУЕФПЧОлЬЧбмЩњЮяЁЃ
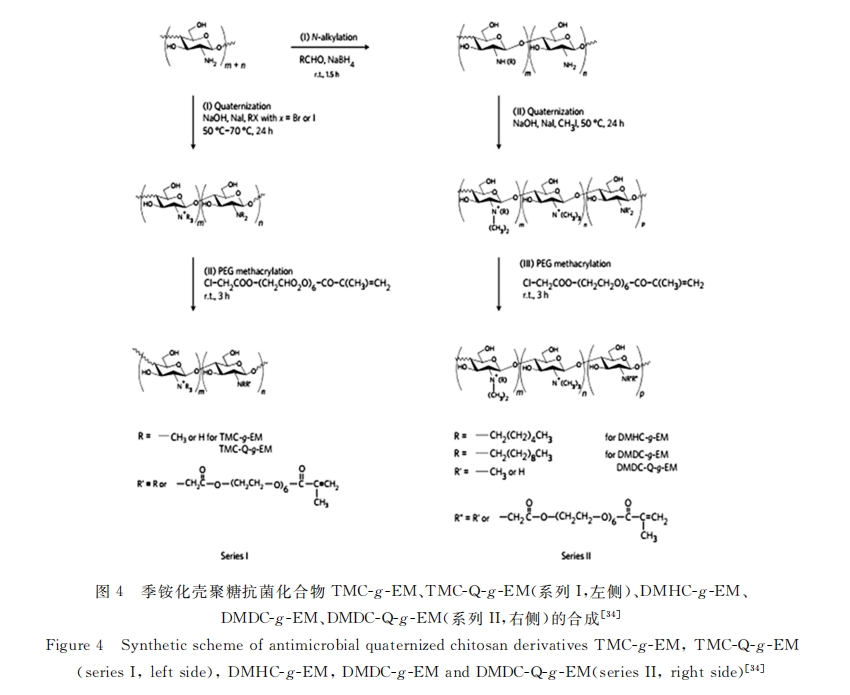
ПЧОлЬЧЗжзгНсЙЙжаКЌгаЛюЦУЕФєЧЛљКЭАБЛљ,ОпгаКмИпЕФЗДгІЛюад,ЭЈЙ§МОяЇбЮЛЏЁЂМОчlбЮЛЏЁЂывЛљЛЏЕШЗНЪНгыЦфЫќЛЏКЯЮяЕФИФадаоЪЮ,жЦБИЕУЕНВЛЭЌЕФПЧОлЬЧПЙОњбмЩњЮя[32~34] ЁЃLiЕШБЈЕРСЫвдЙяЛљЖўМзЛљАЗПЧОлЬЧ(ИпЖШМОяЇЛЏ)НгжІОлМзЛљБћЯЉЫсввЖўДМѕЅ(DMDC-Q-g-EM)КЭОлЖўБћЯЉЫсввЖўДМѕЅЮЊЛљДЁЕФПЙОњЫЎФ§НК(ШчЭМ4ЫљЪО)ЁЃИУФ§НКЖдЭТЬМйЕЅАћОњЁЂДѓГІИЫОњЁЂН№ЛЦЩЋЦЯЬбЧђОњЁЂИЏЦЄСцпУЙОњЕШЖМОпгаСМКУЕФПЙОњаЇЙћ,ВЂЬсГіСЫвЛжжЮяРэПЙОњЛњжЦ,вѕРызгЯИОњФЄВПЗжЯёИКРызгКЃУрвЛбљБЛЮќНјЫЎФ§НКЕФФкВПФЩУзПзжа,ЕМжТЮЂЩњЮяФЄЦЦЛЕ,НјЖјЕМжТЮЂЩњЮяЫРЭіЁЃДЫЭт,ЖЏЮяЪЕбщБэУї,DMDC-Q-g-EMЫЎФ§НКЭПВугыМвЭУНсФЄОпгаСМКУЕФЩњЮяЯрШнад,ЖдЩЯЦЄЯИАћКЭЕзВуЛљжЪЮоЖОад[34] ЁЃ
El-NewehyвдТШввѕЃЛЏКЭфхввѕЃЛЏПЧОлЬЧЮЊдСЯКЯГЩСЫвЛЯЕСаМОяЇбЮКЭМОчlбЮ,ВЂбаОПСЫЫќУЧЖдИяРМЪЯвѕадОњЁЂИяРМЪЯбєадОњКЭецОњЕФПЙОњЛюад,дкЯрЭЌЕФЗДИКРызгЬѕМўЯТ,МОчlбЮИФадПЧОлЬЧЖдЫљВтЮЂЩњЮяЕФПЙОњЛюадИпгкМОяЇбЮИФадПЧОлЬЧ[33] ЁЃNiuдђРћгУєШМзбѕЛљОлввЖўДМ(mpEG-COOH)дкПЧОлЬЧНсЙЙжав§ШыЧзЫЎЦЌЖЮ,ЭЈЙ§АБЛљбЧАЗМзЭщЛЧЫс(AIMSOA)ЖдПЧОлЬЧНјааывЛљЛЏ,жЦБИСЫЫЋЙІФмПЧОлЬЧбмЩњЮяCS-G/mpEG,ЫќПЩвддкВЛв§Ц№ШмбЊЛђЯИАћЖОадЕФЧщПіЯТ,ЭЈЙ§ИпаЇбЁдёадЕиЦЦЛЕЯИОњФЄЩБЫРИяРМЪЯбєадОњ,дкНЯПэЕФХЈЖШЗЖЮЇФкгааЇвжжЦН№ЛЦЩЋЦЯЬбЧђОњЕФЩњГЄ,ВЂЧвЦфШмНтадвВЕУЕНСЫЬсИп[32] ЁЃ
МзПЧЫивВЪЧДје§ЕчКЩЕФЬьШЛКЌЕЊЖрЬЧИпЗжзг,гыПЧОлЬЧвЛбљ,ЗжзгНсЙЙжавВКЌгаЛюЦУЕФєЧЛљКЭАБЛљ,ПЩЭЈЙ§ЛЏбЇИФадЕУЕНМзПЧЫиПЙОњбмЩњЮяЁЃCaiПЮЬтзщВЩгУМђЕЅЕФЗНЗЈдкKOH/ФђЫиЫЎШмвКжаМђЕЅЕижЦБИСЫвЛЯЕСаМОяЇЛЏЕФІТ-МзПЧЫибмЩњЮяЁЃЫќУЧЖдДѓГІИЫОњЁЂН№ЛЦЩЋЦЯЬбЧђОњЁЂАзЩЋФюжщОњКЭУзИљУЙОљБэЯжГіСМКУЕФПЙОњЛюад,MICЗжБ№ЮЊ8ЁЂ12ЁЂ60КЭ40ІЬg/mL,ВЂЧвОпгаСМКУЕФЩњЮяЯрШнад[35, 36] ЁЃ
ЯЫЮЌЫиКЭЕэЗлвВЪЧКЌСПЗЧГЃЗсИЛЕФЬьШЛИпЗжзг,ЕЋЪЧЫќУЧздЩэВЛОпгаПЙОњЛюад,вЛАуЭЈЙ§в§ШыЦфЫќПЙОњЮяжЪРДНјааИФад,ДгЖјЛёЕУПЙОњадФмЁЃР§Шч,CaiПЮЬтзщгжжЦБИСЫОпгаПЙОњЛюадЕФИпЧПЖШЯЫЮЌЫи/УЩЭбЭС/фхЛЏЪЎСљЭщЛљпСрЄИДКЯФЄ,ЖдН№ЛЦЩЋЦЯЬбЧђОњКЭДѓГІИЫОњОљОпгаСМКУЕФПЙОњЛюад,ЭЌЪБОпгаСМКУЕФЛњаЕадФмЁЃHongЕШВЩгУдЮЛЩњЮяКЯГЩЗЈжЦБИСЫПЧОлЬЧ/ЯИОњЯЫЮЌЫиИДКЯПЙОњЗѓСЯ,ЖдДѓГІИЫОњКЭН№ЛЦЩЋЦЯЬбЧђОњОљОпгавжОњадФм,ЧвПЙОњаЇЙћЫцзХПЧОлЬЧКЌСПЕФдіМгЖјдіЧП[37] ЁЃGuoЭЈЙ§ЕуЛїЛЏбЇжЦБИСЫвЛЯЕСаЕэЗлбмЩњЮя[38] ,ФмЙЛвжжЦДѓГІИЫОњКЭН№ЛЦЩЋЦЯЬбЧђОњЕФЩњГЄ,гыЕэЗлЯрБШ,ЦфбмЩњЮяЛёЕУСЫИќЧПЕФПЙОњЛюад[39] ЁЃ
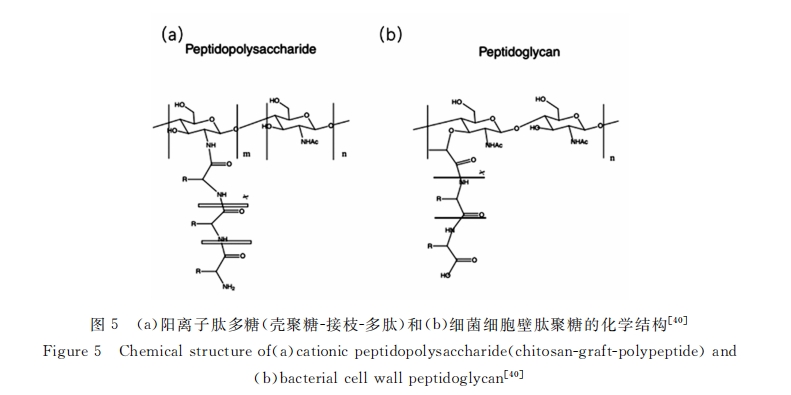
Г§СЫЩЯЪіГЃМћЕФЛЏбЇаоЪЮжЎЭт , НќФъРДНЋПЙОњыФгыЖрЬЧНсКЯв§Ц№СЫШЫУЧЕФЙуЗКЙизЂ ЁЃзїепПЮЬтзщЛљ гкЯИОњыФОлЬЧНсЙЙ , ЙЙНЈСЫвЛЯЕСагаРрЫЦНсЙЙЕФбєРызгыФЖрЬЧ(ШчЭМ5 ЫљЪО),ЫќУЧОпгаСМКУЕФПЙОњКЭПЙецОњЛюад , вдМАЯрБШгкВИШщЖЏЮяЯИАћ , ЖдЯИОњОпгаИпбЁдёад(бЁдёадвЛАуСПЛЏЮЊАыШмбЊХЈЖШЖдзюаЁвжОњХЈЖШЕФБШжЕ) [40~42] ЁЃCS-g-K16ЙВОлЮяФмЙЛгааЇвжжЦСйДВЩЯЕФИяРМЪЯвѕадЯИОњ(ДѓГІИЫОњ , ЭТЬМйЕЅАћОњ)ЁЂ ИяРМЪЯбєадЯИОњ(Н№ЛЦЩЋЦЯЬбЧђОњ)вдМАецОњ(АзЩЋФюжщОњ , ИЏЦЄСцпУЙОњ),ОпгаЕЭЕФ MIC(5~20ІЬg/ mLЛђ 0.2~0.9ІЬmol/L),ЖдВЁдОњКЭШЫКьЯИАћгаИпбЁдёад(>5000~10000) [40] ЁЃCS-g-EPLЙВОлЮядкДѓ Ъѓ MRSAИаШОФЃаЭжаЯдЪОСЫНЯЧПЕФПЙОњаЇЙћ , logжЕНЕЕЭСЫ 4.66[41] ЁЃDex-g -KnFm ЙВОлЮядк 17 ДњЪБОљ ЮДгеЕМ MRSAФЭвЉ,ыФЖрЬЧ DexL-g -K12.5-F12.5-50%ЕФбЁдёадЪЧЖрыФЗжзгзюДѓжЕЕФ 200БЖвдЩЯ[42] ЁЃ
гыДЫРрЫЦ,SahariahЭЈЙ§ЕуЛїЛЏбЇНЋЖЬПЙОњыФanoplinНгжІдкПЧОлЬЧЩЯКЯГЩСЫПЙОњыФanoplinКЭПЧОлЬЧЕФХМСЊЮяЁЃгыanoplinКЭПЧОлЬЧБШ,етаЉХМСЊЮяЖдН№ЛЦЩЋЦЯЬбЧђОњЁЂЗрГІЧђОњЁЂДѓГІИЫОњКЭЭТЬМйЕЅАћОњЕФПЙОњЛюадЖМЬсИпСЫ,ЬиБ№ЪЧДѓГІИЫОњ(MICЕЭжС4ІЬg/mL)ЁЃЖјLiuЭЈЙ§ЯЏЗђМюЗДгІНЋШщЫсСДЧђОњыФnisinНгжІЕН2,3-ЖўШЉЯЫЮЌЫиЩЯ,ЫљЕУЕФN-3ыФЖрЬЧБЁФЄЖдИяРМЪЯбєадОњКЭИяРМЪЯвѕадОњОљгаНЯКУЕФПЙОњЛюад[43] ,ЖјЧвЦфвжОњФмСІБШДПЯЫЮЌЫиФЄИп4ИіЪ§СПМЖ[44] ЁЃ
ЬьШЛПЙОњЛЏКЯЮяРрБ№ЗБЖр,ВЂУЛгаЭъШЋПЊЗЂРћгУ,ВЂЧвЖдгкЦфПЙОњЛњРэЩаЮДЭъШЋЧхГў,гаД§НјвЛВНбаОПЁЃР§Шч,ПЧОлЬЧЕФПЙОњЛюадЪмЕНжюЖрвђЫиЕФгАЯь,ЖдЦфПЙОњЛњжЦЕФНтЪЭвВВЛОЁЯрЭЌ,ЦфжаФЄЦЦЛЕЪНЕФЮяРэЩБОњФЃЪН,ЪЧЭЈЙ§ЦЦЛЕЯИОњЯИАћФЄЖјЕМжТЯИОњЫРЭіЕФ,ВЛвзв§Ц№ФЭвЉадЁЃвђДЫ,НсКЯЬьШЛПЙОњЛЏКЯЮяЕФгХЪЦ,ВЂЖдЦфНјаааоЪЮИФад,ИГгшЦфгХвьЕФЮяРэПЙОњадФм,гаЭћЪЙЦфГЩЮЊгІЖдФЭвЉадЮЃЛњЕФБИбЁВФСЯЁЃ
2.3 ПЙОњыФИпЗжзгФЃФтЮяЕФКЯГЩ
ЬьШЛИпЗжзгЕФаоЪЮгаЦфОжЯоад , ЖјРћгУИпЗжзгКЯГЩЗНЗЈ , ЭЈЙ§ЖдЕЅЬхЕФаоЪЮКЭЕїХф , РДРэадФЃФтПЙОњ ыФЕФСНЧзадНсЙЙдђОпгаИќЧПЕФВйзїадКЭПЩПиад ЁЃ
ЮЊСЫИќНгНќЕиФЃФтПЙОњыФ,DegradoКЭTewЕШЩшМЦКЯГЩСЫвЛжжаТаЭПЙОњЕЭОлЮяЁЊЁЊЁЊЁАелЕўЬхЁБ,ЦфЮЊвЛжжЛљгкЗМАЗКЭІТ-АБЛљЫсЙЧМмЕФЖЬађСаЬивьадЙбОлЮя,дкОпгаСНЧзадзщЗжЕФЭЌЪБ,ЛЙФмелЕўГЩРрЫЦПЙОњыФЕФЖўМЖНсЙЙ,ПЩЭЈЙ§ЕїећЗжзгНсЙЙгХЛЏРДЕїНкПЙОњЛюадКЭЖОадЁЃжЎКѓНЋетаЉПЙОњелЕўЬхзїЮЊОВТізЂЩфПЙЩњЫи,НсЙћБэУї,ЯИОњВЛвзЖдетРрЛЏКЯЮяВњЩњФЭвЉадЁЃШЛЖј,дкЖдетаЉПЙОњелЕўЬхЕФадФмЩИбЁжаЗЂЯж,гавЛаЉЖўМЖНсЙЙгыЦфПЙОњыФФИАхВЛЬЋЯрЫЦЕФЗжзгвВОпгаСМКУЕФЩњЮябЇадФм[45] ЁЃЛљгкетаЉГЩЙћ,баОПШЫдБПЊЭиСЫПЙОњыФИпЗжзгФЃФтЮяЕФЩшМЦгыКЯГЩЁЃ
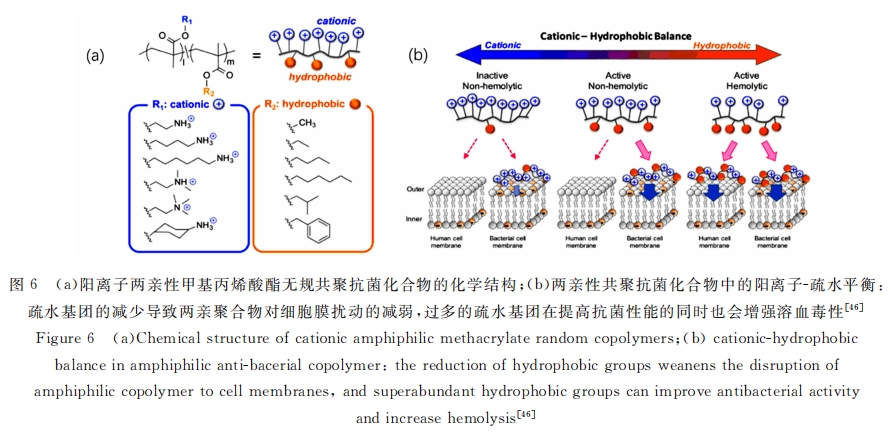
ПЙОњыФИпЗжзгКЯГЩФЃФтЮяПЩвдгЩКЌгаЫцЛњађСаЕФбєРызгЛђЪшЫЎВрСДЕФЕЅЬхОлКЯЖјГЩЁЃkurodaБЈЕРСЫвдлЯЛљЮЊзЊвЦМСжЦБИСЫМзЛљБћЯЉЫсѕЅРрЙВОлЮя,ШчЭМ6aЫљЪОЁЃЭЈЙ§здгЩЛљОлКЯЗНЗЈ,АбКЌгаяЇИљбєРызгЕФЧзЫЎЕЅЬхЧАЬхЁЊЁЊМзЛљБћЯЉЫсЪхЖЁбѕєЪЛљАБЛљввѕЅКЭОпгаВЛЭЌЪшЫЎГЬЖШЕФЪшЫЎЕЅЬхШчМзЛљБћЯЉЫсМзѕЅЁЂМзЛљБћЯЉЫсЖЁѕЅКЭМзЛљБћЯЉЫсМКѕЅЕШНјааЙВОл,зюКѓгУШ§ЗњввЫсЭбБЃЛЄ,ЕУЕНСНЧзадЙВОлИпЗжзг,етаЉИпЗжзгФЃФтЮяЖдДѓГІИЫОњОпгаЯджјЕФПЙОњзїгУЁЃСэЭт,ЭЈЙ§баОПЕЅЬхзщГЩКЭЪшЫЎЛљЭХЕФЛЏбЇНсЙЙЖдПЙОњЛюадКЭШЫРрЯИАћЕФЖОадЗЂЯж,ЙВОлЮяЕФПЙОњЛюадКЭШмбЊЛюадОљЫцЪшЫЎВрСДКЌСПЕФдіМгЖјдіЧП,вђДЫОлКЯЮяЕФбєРызг-ЪшЫЎаджЎМфЕФЦНКтгІИУгХЛЏ,дкЬсИп/БЃГжЦфПЙОњЛюадЕФЭЌЪБНЕЕЭ/ПижЦШмбЊЛюад,вдДяЕНзюгХЕФбЁдёадЁЃШчЭМ6bЫљЪО,ЮЂЩњЮяКЭВИШщЖЏЮядкЯИАћФЄЙЙГЩЩЯДцдкЧјБ№:ЮЂЩњЮяЯИАћФЄЕФЫЋЗжзгВуСНВрОљЗжВМзХДѓСПЕФДјИКЕчЕФСзжЌ,ЪЙЦфГЪЯжЧПИКЕчад;ЖјВИШщЖЏЮяЯИАћФЄдђЮЊЗЧЖдГЦНсЙЙ,ДјИКЕчЕФСзжЌжЛЗжВМгкФквЖ,ЭтвЖгЩЕчжаадЕФСзжЌЙЙГЩ,ЪЙЦфГЪЯжНЯШѕЕФИКЕчадЁЃШБЗІЪшЫЎВрСДЕФбєРызгОљОлЮяПЩвдЭЈЙ§ОВЕчЯрЛЅзїгУНЯЧПЕиНсКЯдкЯИОњЯИАћФЄЩЯ,ЖјгыШЫРрЯИАћФЄзїгУНЯШѕЁЃЫцзХСНЧзадПЙОњЛЏКЯЮяжаЪшЫЎЛљЭХБШР§ЕФдіМг,ЦфЖдСзжЌЫЋЗжзгВуЪшЫЎФкКЫЕФШХЖЏвВдкдіЧП,вђДЫдкИќЧПЕиШХЖЏЦЦЛЕЯИОњЯИАћФЄЕФЭЌЪБ,вВПЩвдЦЦЛЕШЫРрЯИАћФЄ,ЕМжТШмбЊаддіЧПЁЃвђДЫ,ашвЊЕїПиЗжзгФкбєРызг-ЪшЫЎаджЎМфЕФЦНКт,РДгХЛЏСНЧзЙВОлЮяЕФПЙОњКЭШмбЊадФм[46] ЁЃ
LienkampЕШНЋвЛЯЕСаВЛЖдГЦЖўШЁДњЕФЖўвТПЕЫсЕЅЬхгыN, N-ЖўМзЛљБћЯЉѕЃАЗ(DMAA)ЭЈЙ§здгЩЛљЙВОлКЯ,ЕУЕНПЙОњыФФЃФтЙВОлЮя(SMAMPs)ЁЃНсЙћБэУї,ЭЈЙ§ИФБфЭщЛљСДГЄЖШгыDMAAКЌСППЩвдИФБфОлКЯЮяЕФЪшЫЎад,ЕБЭщЛљВрСДзюГЄЁЂDMAAКЌСПзюЕЭЪБ,ПЙОњЛюадзюЧПЁЃгЩгкетаЉОлКЯЮяЩњЮяЛюадЕФЗжзгСПвРРЕад,ашвЊНјвЛВНгХЛЏЕФЪЧЖрЗжЩЂад,ПЩвдЭЈЙ§ПЩПиздгЩЛљОлКЯЕФЗНЗЈРДЪЕЯжo TewВЩгУПЊЛЗзЊЮЛОлКЯ(ROMP)жЦБИСЫвЛЯЕСаОпгаВЛЭЌНсЙЙБфЛЏЕФОлКЯЮя,ЭЈЙ§ЖдНсЙЙгыЛюадЙиЯЕЕФбаОП,ЗжЮіЗжзгСПЁЂЕчКЩЁЂЪшЫЎадЁЂЗДРызгКЭОлКЯЮяНсЙЙЖдПЙОњаЇЙћЕФгАЯь[47] oЁЃПЙОњбаОПБэУї,ЫцзХОлКЯЮяЪшЫЎадЕФдіМг,ЦфMICжЕПЊЪМГЪЩЯЩ§ЧїЪЦ,ЕБОлКЯЮяСДжаМфВПЗжЪшЫЎЪБ,ЦфПЙОњЛюадзюИп;гыЕЅЕчКЩФЃФтЮяЯрБШ,ЕЅЬхКЌгаИќЖрбєРызгЕчКЩЕФОлКЯЮяОпгаИќИпЕФПЙОњад;ЗжзгСПЖдПЙОњадФмЕФгАЯьПЩФмгыОлКЯЮяНсЙЙгаЙи[48]ЁЃ
yang КЭ HedrickКЯГЩЕФПЙОњОлЬМЫсѕЅФмЙЛбЁдёадЕигыЯИОњЯИАћФЄЯрЛЅзїгУ , ЪзЯШЭЈЙ§ОВЕчФЄЕоКЯ зїгУгеЕМФЄећКЯ , НјЖјЪЙФЄВЛЮШЖЈ , зюжеЕМжТЯИОњЯИАћСбНтКЭЫРЭіo ПЙОњОлЬМЫсѕЅЖдИяРМЪЯбєадОњ ЁЂИяРМ ЪЯвѕадОњКЭецОњЖМгабЁдёвжжЦЕФФмСІ[49] ЁЃ
ШчНёвбОПЊЗЂГіаэЖрОпгабЁдёадЕФПЙОњыФОлКЯЮя , гЩгкОлКЯЮяжабєРызгЕчКЩКЭЪшЫЎаджЎМфЕФЦНКт , ЪЙЕУЫќУЧФмбЁдёадЕигыЯИОњЕФвѕРызгжЌжЪФЄ , ЖјВЛЪЧгыСНадРызгВИШщЖЏЮя(ШЫЕФКьЯИАћ)ФЄзїгУo ЮЊСЫЬН ОПСНЧзадПЙОњОлКЯЮяжаЕФЧтМќЪЧЗёгажњгкетжжЬивьадФЄЕФНсКЯ , Divakara ЕШЭЈЙ§ѕЅЕФвьЙЙШЁДњ , ЪЙЦфѕЃ АЗВПЗждк N-ЭщЛљТэРДѕЃбЧАЗЛљСНЧзОлКЯЮяЕФВрСДжаЕФЧтМќаЇСІВЛЭЌo баОПБэУї , гыѕЅЖдгІЮя(EC3P)Яр БШ , ѕЃАЗОлКЯЮя(AC3P)ЪЧвЛжжгааЇЕФПЙОњМС , ОпгаИпЕФЦЦФЄадФм , жЄЪЕСЫЧтМќдкЯИОњФЄЯрЛЅзїгУжаЕФжи вЊзїгУ , етНЋжњгкНёКѓЩшМЦЬивьадФЄЛюадЗжзгЕФЯИОњФЄ[50] ЁЃ
ТБАЗПЙОњЛЏКЯЮяНќФъРДвВБЛЙуЗКЙизЂ,ЫќЪЧвЛжжЗжзгНсЙЙжаКЌгаЕЊТБЙйФмЭХЕФгаЛњЛЏКЯЮя,ЭЈГЃгЩNЁЊHМќОДЮТБЫсбЮзїгУзЊБфГЩNЁЊXМќРДжЦБИЁЃЦфПЙОњдРэЪЧгЩгкТБдзгДјгае§ЕчКЩЧвОпгабѕЛЏад,ЭЈЙ§ЪЭЗХЧПбѕЛЏадЕФТБЫибєРызгЦЦЛЕЯИАћФЄ,ЛђНјШыЕНЮЂЩњЮяЬхФк,ИЩШХЯИАћУИЕФЛюадКЭДњаЛЙ§ГЬ,ДгЖјЕМжТЯИОњЫРЭіЁЃRenПЮЬтзщдкN-ТБАЗПЙОњЙВОлЮяМАПЙОњМСЕФжЦБИЗНУцГжајЬНЫї,РћгУПЧОлЬЧКЭєЧМзЛљКЃвђзїЮЊдСЯЗДгІЩњГЩСЫТБАЗЧАЧ§ЬхНгжІПЧОлЬЧ[51] ,гжЭЈЙ§РызгФ§НКЗЈжЦБИСЫИФадПЧОлЬЧФЩУзЮЂЧђ,КѓгжНЋИФадПЧОлЬЧФЩУзЮЂЧђТШЛЏ,НсЙћЯдЪО,ИФадКѓЕФФЩУзЮЂЧђОпгаИќМггХвьЕФПЙОњадФмЁЃГ§ДЫжЎЭт,ИФадКѓЕФПЧОлЬЧвдХМЕЊЖўвьЖЁыцЮЊв§ЗЂМС,КЯГЩСЫТБАЗПЙОњМС 3-(3,-БћЯЉЫсБћѕЅ)-5,5-ЖўМзЛљКЃвђ(APDMH)[52] ,ВЂгыввЫсввЯЉѕЅ(Vac)ЙВОл,КЯГЩСЫПЙОњЙВОлЮя[P(APDMH-c.-VAc)],ЭЈЙ§НўзеЙЄве,ећРэЕНБћТкЮоЗФВМЩЯЁЃDongПЮЬтзщжТСІгкПЊЗЂПЙОњN-ТБАЗВФСЯ,ВЩгУздгЩЛљЙВОл,КЯГЩИКдиN-ТБАЗЕФОлМзЛљБћЯЉЫсМзѕЅ(PMMA)ФЩУзСЃзгзїЮЊаТаЭПЙОњМС,етжжПЙОњМСОпгаГЄЦкЮШЖЈЕФПЙОњадФм[53]ЁЃ
2.4 ЛљгкИпЗжзгЕФПЙОњвЉЮяЕнЫЭЬхЯЕ
Г§СЫБОЩэОпгаПЙОњЙІФмЕФИпЗжзг , РћгУИпЗжзгРДзіЮЊПЙОњвЉЮя(ШчПЙЩњЫи ЁЂПЙОњыФЕШ)ЕФжЧФм/АаЯђЕн ЫЭЬхЯЕ , ЪЕЯжПЙОњвЉЮяЕФАДашЪЭЗХ , ПЩвдДѓЗљНЕЕЭвЉЮяЕФгУСП , БмУтвЉЮяЕФГжајЙ§СПЪЙгУ , ЖдгкНЕЕЭВЁОњ ФЭвЉадЕФЗЂЩњ , вВОпгаМЋЦфживЊЕФвтвх ЁЃ
saadБЈЕРСЫвЛжжНЋЫЎФ§НКзїЮЊПЙОњЛЗБћЩГаЧвЉЮя(CFX)диЬхЕФжЦБИЗНЗЈ,КЯГЩСЫN-Ш§МзЛљПЧОлЬЧ(TMC)/єШМзЛљЛЦдЫсФЦНК(CMXG)ЫЎФ§НК,ВЂвдЛЗБћЩГаЧзїЮЊФЃаЭвЉЮяЁЃНсЙћБэУї,ЛЗБћЩГаЧГЩЙІЕиДгжЦБИЕФЫЎФ§НКжаВєШыКЭЪЭЗХЁЃЮЊСЫЗРжЙЬхФкжВШыЦїаЕИаШОЕШвЛЯЕСаЮЪЬт[54] ,AshbaugПЊЗЂСЫвЛжжгЩЧЖШыдкОлМКФкѕЅ(PCL)БЁФЄжаЕФОлШщЫс-єЧЛљввЫсЙВОлЮя(PLGA)ФЩУзЯЫЮЌзщГЩЕФИДКЯЭПВу,гУгкаЭЌДЋЕнПЙЩњЫиЁЃЭЈЙ§ИФБфPLGA:PCLОлКЯЮяЕФБШР§,ПЩвдЕнЫЭВЛЭЌжжРрЕФПЙЩњЫи[55] ЁЃЭЌбљЕФ,жЌжЪЬхвВЪЧвЛжжживЊЕФвЉЮяЕнЫЭдиЬх,ChhibbeВЩгУжЌжЪЬхзїЮЊЪЩОњЬхЕФдиЬхдкаЁЪѓЬхФкХрбјЪЩОњЬхПЙЬх,ВЂЖдЛьКЯбЊЧхжаКЭгЮРыЪЩОњЬхКЭжЌжЪЬхМаГжЪЩОњЬхЕФФмСІНјааЦРЙРЁЃЪЕбщНсЙћЯдЪО,АќЗтЕФЪЩОњЬхЕФжаКЭПЙЬхОпга100%ЕФБЃЛЄзїгУЁЃгЮРыЕФЪЩОњЬхдкгыПЙЬхЯрЛЅзїгУКѓ3hФкБЛжаКЭ,ВЂЧв,жЌжЪЬхФмЙЛНЋАќзЁЕФЪЩОњЬхдЫЫЭЕНОоЪЩЯИАћФк,ЕМжТЯИАћФк94.6%ЗЮбзСДЧђОњЫРЭіЁЃФЩУзПХСЃдкЕнЫЭПЙЩњЫиКЭЦфЫќвЉЮяЗНУцБэЯжГіКмЖргХвьЕФадФм,ЕЋЦфАаЯђаЇТЪЕШгаД§НјвЛВНЬсИп[56] ЁЃ
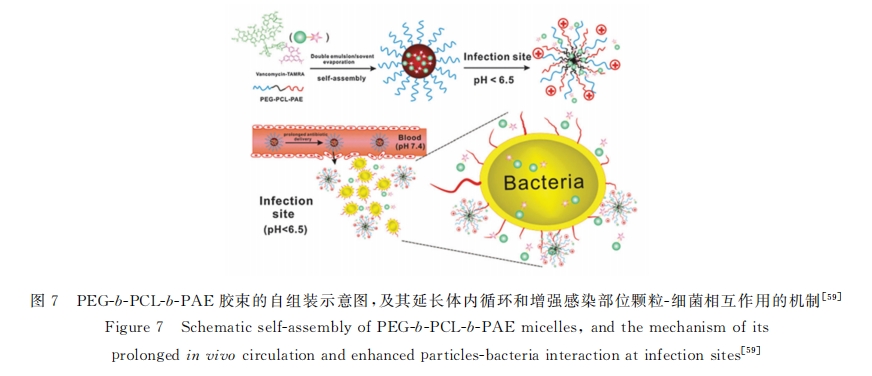
ДЫЭт,ВЁОњвзаЮГЩЩњЮяБЛФЄ(Biofilm),ЩњЮяБЛФЄЕФФ§НКзДЛљжЪОпгаЦСеЯаЇгІ,ВЩгУДЋЭГЕФИјвЉЗНЪН, ПЙЩњЫиФбвдЩјЭИ,ЮоЗЈНЋвЉЮяЫЭДяЩњЮяБЛФЄФкВП,ЕМжТжЮСЦаЇЙћВЛРэЯыЁЃЭЌЪБ,гЩгкЩњЮяБЛФЄдкжЮСЦЙ§ГЬ жаОпгаГжОУад,ЪЙЦфЖдПЙЩњЫиЕФФЭвЉаддіЧП,вђДЫМБашПЊЗЂвЛжжФмЙЛПЫЗўЩњЮяБЛФЄИаШОЕФаТВпТдЁЃЮЊДЫ, shiПЮЬтзщЩшМЦСЫвЛЯЕСаздЪЪгІФЩУзЕнЫЭЯЕЭГЁЃЦфжа,ЩшМЦСЫИКдигаЙтУєМСЕФЛьКЯПЧВуНКЪј,РћгУЦфИЛ МЏЁЂДЉЭИВЂЭЃСєдкЩњЮяБЛФЄФкВПЕФЬиад,ФмЙЛЖдОпгаЖржиФЭвЉадЕФЩњЮяБЛФЄНјааЙтееЩБУ№[57] ЁЃРрЫЦЕФ, ЫћУЧгжжЦБИСЫвЛжжБэУцздЪЪгІЁЂШ§ТШЗгИКдиЕФНКЪјФЩУздиЬх,гЩгкНКЪјФЩУздиЬхдкЩњРэPHЬѕМўЯТЕФвў ЩэаджЪ,ФмЙЛДЉЭИН№ЛЦЩЋЦЯЬбЧђОњЩњЮяБЛФЄ;ЖјдкЯИОњБэУцИННќЕФЕЭВЁРэPHЬѕМўЯТ,е§ЕчКЩдкЩњЮяБЛФЄ жаЛ§РлВЂНЋЦфздЩэАаЯђЕНИКЕчКЩЯИОњЯИАћБэУц,ФЩУздиЬхБЛЯИОњжЌЗОУИЫЎНт,ЪЭЗХвЉЮя[58] ЁЃЭЌЪБ,ЮЊСЫ бгГЄКЭМгЧПЬхФкПЙЩњЫиЕФДЋЕн,гжвдPEGЁЂPCLКЭОл(ІТ-АБЛљѕЅ)(PAE)ЮЊЛљДЁжЦБИЕУЕНШ§ЧЖЖЮОлКЯЮя PEG-b-PCL-b-PAE,ШчЭМ7ЫљЪО,гУгкЭђЙХУЙЫи(van)ЕФАаЯђКЭДЋЕнЁЃгЩгкPAEОпгавРРЕгкPHЕФЕчКЩ зЊЛЛЬиад,ЧвPEG-b-PCL-b-PAE/vanЪЧдкЩњРэЛЗОГжаОпгаИКЕчКЩКЭжТУмЕФФЩУзПХСЃ,гаРћгкбгГЄбЛЗЁЃЕБЫќЕНДяЫсадИаШОЮЛЕуЪБ,ИКЕчКЩзЊЛЏЮЊе§ЕчКЩ,НјЖјМгЧПЫќгыЯИОњЕФНсКЯ,діЧПСЫvanЕФЛ§Рл[59] ЁЃ
2.5 ЙтЖЏСІПЙОњИпЗжзгВФСЯ
ЙтФмОпгаЛЗБЃад ЁЂПЩдйЩњад ЁЂдЖГЬВйПиКЭПЩЕїНкВЈГЄЕШгХЕу , вђДЫЙтЯьгІадИпЗжзгВФСЯГЩЮЊбаОПШШЕу жЎвЛ ЁЃЙтЖЏСІПЙОњЛЏбЇСЦЗЈ(Photodynamic antibacterial theraPy, PDAT)ЪЧРћгУЙтУєМСКЭПЩМћЙтЛђзЯЭт Йт , ЭЈЙ§бѕЛЏЫ№ЩЫЖдЮЂЩњЮяВњЩњЙтЖОадЗДгІ[60] ЁЃPDATШчЙћФмЙЛЬцДњПЙЩњЫигУгкОжВПИаШОЕФжЮСЦ , НЋга аЇЛКНтФЭвЉадЮЃЛњ ЁЃФПЧА , пВпјРрМАЦфбмЩњЮяЪЧвЛРрЗЧГЃживЊЕФЙтУєМС ЁЃШЛЖј , пВпјКмШнвздкЪшЫЎЕФ Іа-Іа ЯрЛЅзїгУЕФЛљДЁЩЯаЮГЩОлМЏЬх , МѕЩйЕЅЯпЬЌбѕЕФЩњГЩ ЁЃ ЮЊДЫ , zhang ПЮЬтзщвдКЌгаКљТЋ[7](CB[7])МО яЇбЮЛљЕФпВпјбмЩњЮя(Por)ЮЊдСЯжЦБИСЫвЛЯЕСаГЌЗжзгЙтУєМС ЁЃ ЕБЦфгы CB[7]НсКЯКѓ , ЙтУєМСЕФПЙОњЛю аддкКкАЕжаДІгкЙиБезДЬЌ , ЖјдкАзЙтееЩфЯТПЙОњЛюадДІгкПЊЦєзДЬЌ ЁЃ ЪЕбщНсЙћБэУї , етаЉаЁЗжзгЖдВИШщ ЖЏЮяЯИАћМИКѕУЛгаЯИАћЖОад , етвЛбаОПЗНЯђНЋЮЊМОяЇбЮРрЩБОњМСГЄЦкЖдПЙЯИОњЛ§РлЬсЙЉвЛжжаТВпТд[61] ЁЃ
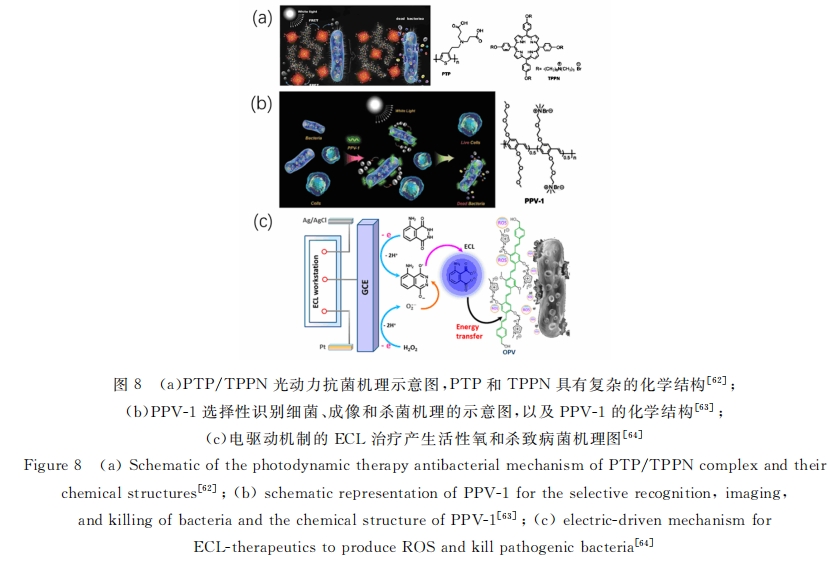
гЩгкОпгаСМКУЕФЙтЮяРэаджЪ,бєРызгЙВщюОлКЯЮяБЛЙуЗКгІгУгкЩњЮяДЋИаЦїЁЂГЩЯёКЭЩњЮявНбЇЕШСьгђЁЃwangПЮЬтзщКЯГЩСЫвЛжжаТаЭвѕРызгЫЎШмадОлрчЗд(PTP)КЭвЛжжбєРызгпВпј(TPPN),СНепЭЈЙ§ОВЕчЯр ЛЅзїгУаЮГЩИДКЯЮя,ШчЭМ8aЫљЪО,дкАзЙтееЩфЯТ,PTPЯђTPPNНјаагааЇЕФФмСПзЊвЦ,ЬсИпСЫTPPNВњ ЩњЕЅЯпЬЌбѕЕФаЇТЪ,ФмЙЛгааЇЕиНјааЩБОњ[62] ЁЃЮЊСЫИќКУЕибЁдёадЪЖБ№ЁЂГЩЯёКЭЩБУ№ЯИОњ,ЫћУЧгжКЯГЩСЫ вЛжжОпгаОлввЖўДМВрСД(PPV-1)ЕФЖрЙІФмбєРызгбмЩњЮя,ШчЭМ8bЫљЪО,бєРызгPPV-1ЭЈЙ§ОВЕчЯрЛЅзїгУ бЁдёадЪЖБ№НсКЯЯИОњ,дкАзЙтееЩфЯТВњЩњШ§ЯпЬЌбѕ,НјЖјбѕЛЏЫ№ЩЫгааЇЩБЫРЯИОњ[63] ЁЃAPDTДцдкЕФжївЊ ЮЪЬтЪЧЙтдкЩњЮязщжЏжаЕФДЉЭИЩюЖШгаЯо,ЮЊДЫЙЙНЈСЫвЛжжЛљгкЕчЛЏбЇЗЂЙт(ECL)ЕФЕчжТЗЂЙтЩБОњЯЕЭГ, ШчЭМ8cЫљЪОЁЃECLПЩгУгкМЄЗЂЙтУєМС,OPVзїЮЊвЛжжИпаЇЕФЙтУєМС,ЮќЪеECLЕФЗЂЩф,ВЛдйвРРЕгкЮя РэЙтдДВњЩњЛюадбѕ(ROS)ЁЃетжжаТВпТдБмУтСЫЭтВПЙтдДЕФЪЙгУ,дкЩюВПзщжЏЫ№ЩЫжЮСЦжаОпгаКмДѓ ЧБСІ[64] ЁЃ
Г§пВпјРрМАЦфбмЩњЮяЁЂбєРызгЙВщюОлКЯЮяЭт,ГЃМћЕФЙтУєМСЛЙгаЗдрчрКРрЁЂЬЊнМРрМАЦфбмЩњЮяЕШЁЃДЋЭГЕФЗдрчрКРрЙтУєМСАќРЈбЧМзЛљРЖЁЂМзБНАЗРЖЕШЁЃSyedРћгУ670nmМЄЙтЙтдД,баОПСЫбЧМзЛљРЖЙВщюЬМФЩУзЙм(MBCNTs)ЖдДѓГІИЫОњКЭН№ЛЦЩЋЦЯЬбЧђОњЩњЮяБЛФЄЕФПЙОњЛюадЁЃдкЪдбщХрбјЛљжа,ЙтЖЏСІЪЇЛюЯдЪОДѓГІИЫОњКЭН№ЛЦЩЋЦЯЬбЧђОњЕФlogжЕЗжБ№МѕЩй4.86КЭ5.55[65] ЁЃСэЭт,TeradaЕШЬНОПСЫдкАзТБЙтЕФМЄЗЂЯТ,ЙтУєМСГроККьЫи/бЧМзЛљРЖСЊКЯгІгУЖдБфаЮСДЧђОњЩњЮяБЛФЄЕФПЙОњзїгУ,баОПНсЙћЯдЪО,ЕБГроККьЫиКЭбЧМзЛљРЖЕФХЈЖШЮЊ100ІЬMКЭ250ІЬMЪБ,PDATСЊКЯГроККьЫи/бЧМзЛљРЖОљгХгкЙтУєМСЕЅЖРЪЙгУЕФаЇЙћ[66] ЁЃЬЊнМРрЛЏКЯЮягыпВпјНсЙЙЯрРрЫЦ,вбБЛгУзїЙтУєМСЁЃЮЊДЫ,LeeжЦБИСЫПЧОлЬЧ/Ш§ОлСзЫсбЮФЩУзСЃзгАќЗтЬЊнМ,ЖдАзЩЋФюжщОњНјааЩБУ№ЁЃАќЗтЕФЬЊнМДЉЭИЯИАћЕФФмСІдіЧП,ЪЕбщНсЙћЯдЪОАзЩЋФюжщОњЕФДцЛюТЪНіЮЊ20%[67] ЁЃ
2.6 ПЙОњИпЗжзгЕФгІгУ
ЩЯЪіИїРрПЙОњИпЗжзг,дкНјвЛВНзїЮЊвЉЮяДњЬцПЙЩњЫигІгУгкСйДВЗНУцЛЙУцСйКмДѓЕФЬєеНЁЃЕЋФПЧА,ИїЩЋИїбљЕФПЙОњИпЗжзгВФСЯПЩвдЭЈЙ§ПЙОњЭПВуЕШЗНЗЈгІгУгквНСЦЦїаЕЁЂЮРЩњЯћЖОЁЂЫЎДІРэЕШСьгђ,ДгЖјМѕЩйПЙЩњЫиЕФгУСП,бгЛКЦфФЭвЉадЕФВњЩњЁЃР§Шч,гІгУгкСйДВЪжЪѕ,ЭЈЙ§ЖдЪжЪѕЪвФкгУЦЗЁЂЦїОпНјааПЙОњЭПВуаоЪЮ,ПЩвдДяЕННЯИпЕФНрОЛЕШМЖ,МѕЩйИаШОЕФЗЂЩњ,МѕЩй/БмУтПЙЩњЫиЕФЪЙгУ,ДгЖјМѕЛКФЭвЉадЕФзЬЩњЁЃ
РћгУбєРызгПЙОњОлКЯЮядкВФСЯБэУцЙЙНЈОлКЯЮяЫЂЁЂЫЎФ§НКЭПВуЕШПЩвдЩњГЩОпБИПЙОњЙІФмЕФБэУцЁЃklibanovЕШЭЈЙ§зЯЭтЙтв§ЗЂНЋСНадЕФN-ЭщЛљОлввЯЉбЧАЗОлбєРызгбЮЙВМлНгжІдкУожЏЮяБэУц,ЙЙНЈвЛВу гРОУВЛЪЭЗХЕФПЙОњЭПВу,ФмГЄЦкгааЇЕжПЙН№ЛЦЩЋЦЯЬбЧђОњКЭДѓГІИЫОњЕФШыЧж[68] ЁЃHancockЪзЯШЭЈЙ§Бэ УцдзгзЊвЦздгЩЛљОлКЯ(SI-ATRp)дкюбБэУцаЮГЩвЛВуКЌТэРДѕЃбЧАЗЛљЕФОлКЯЮяЫЂ,дйРћгУТэРДѕЃбЧАЗЛљ КЭСђДМЕФМгГЩЗДгІНсКЯTet213ПЙОњыФ(ШчЭМ9ЫљЪО)[69] ЁЃyangРћгУОлввЖўДМШ§ЧЖЖЮОлКЯЮягыКЌЮЌЩњЫи EЕЅдЊЕФДје§ЕчЕФОлЬМЫсѕЅ,ЭЈЙ§ЮяРэНЛСЊ,жЦБИПЩНЕНтЕФПЙОњЫЎФ§НК,ПЩгааЇЧхГ§ЩњЮяБЛФЄ[70] ЁЃ
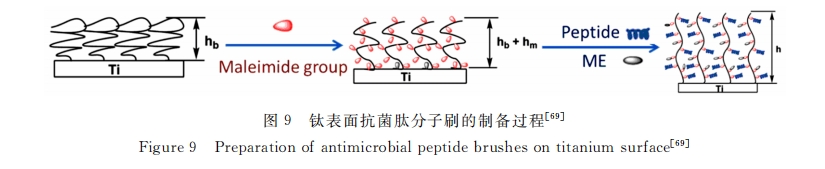
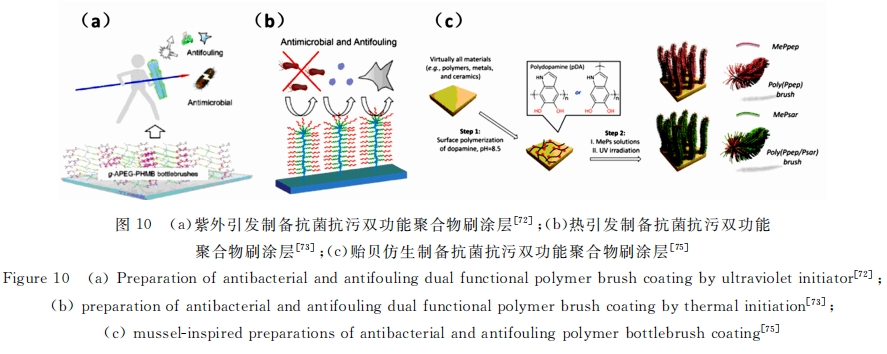
бєРызгПЙОњИпЗжзгдкВФСЯБэУцПЩвддкЖЬЦкФкгааЇЩБУ№гыЦфНгДЅЕФЯИОњ , ЕЋНЯЧПЕФЯрЛЅзїгУЛсЕМжТЭП ВуЕФЩњЮяЮлЫ№(Biofouling)КЭЪЇаЇ ЁЃе§Шч Lienkamp ЮФжаЬсМАЕФ,ЁАашвЊЦяЪПКЭГЧЧНВХФмгааЇКДЮРГЧБЄЁБ, ЭПВужЛгаМцОпПЙОњКЭПЙЮлЙІФм,ВХФмГЄЦкгааЇЕжгљЯИОњЕФШыЧж ЁЃзїепПЮЬтзщдкжЦБИПЙОњПЙЮлЫЋЙІФмЭПВу ЗНУцЕФбаОПНЯЮЊГЩЪьОпЬх[71] ЁЃШчЭМ 10aЫљЪО , ЭЈЙ§зЯЭтв§ЗЂдкЛљЕзБэУцНгЩЯОпгаПЙЮлЙІФмЕФОлввЖўДМ КЭПЙОњаЇЙћЕФОлСљбЧМзЛљЫЋыв , ИУЭПВувЛЗНУцФмгааЇЕжПЙЕААз ЁЂбЊаЁАх ЁЂЯИОњдкЦфЩЯЕФеГИН , СэвЛЗНУцЖд гкЩйЪ§еГИНдкБэУцЕФЯИОњвВФмгааЇЩБЫР[72] ЁЃЮЊСЫПЫЗўЙтв§ЗЂЮоЗЈгУгкОпгаИДдгаЮзДЧЛЬхЕФвНСЦЦїаЕЕФ ШБЯн,БЪепПЮЬтзщКѓајПЊЗЂСЫЛљгкШШв§ЗЂЕФЭПВу[73] , дк 121ЁцИпбЙУ№ОњЕФЭЌЪБ , ПЩвддкЛљВФЩЯЙЙНЈгааЇЕФ ПЙОњПЙЮлЭПВу(ЭМ 10b ЫљЪО)ЁЃънБДЗТЩњЗЈаЮГЩЕФОлЖрАЭАЗВуПЩвдеГИНгкШЮвтВФСЯБэУц , ВЂЧвдкЙтееЯТПЩ вдЩњГЩздгЩЛљ[74] ЁЃгжРћгУОлЖрАЭАЗзіЮЊБэУцв§ЗЂМС , НгжІСЫ NCA ЗЈКЯГЩЕФПЙОњЖрыФ(Meppep)КЭПЙЮл ОлМЁАБЫсРрыФ(Mepsar),ИУЭПВуВЛНіФмгааЇЩБЫРИяРМЪЯвѕ ЁЂбєадОњ , ИќПЩвжжЦЩњЮяБЛФЄаЮГЩГЌЙ§ 7d[75] ЁЃ
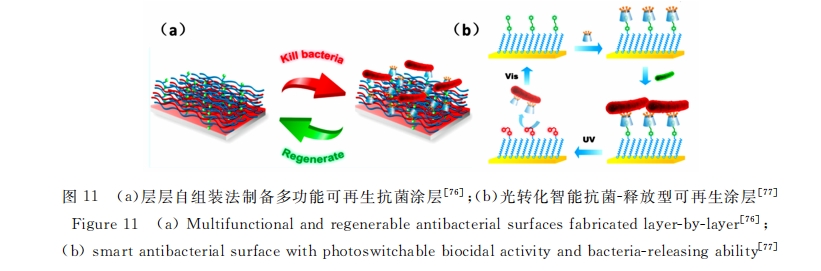
ЫцзХЖдПЙОњЭПВубаОПЕФЩюШы , ЙЙНЈЯьгІад ЁЂжЧФмадЕФПЙОњЭПВудНРДдНЮќв§баОПепЕФаЫШЄ ЁЃChenПЮЬтзщНќФъРДЙЙНЈСЫвЛЯЕСаОпгаЯьгІадЕФЩБОњЧвздЪЭЗХЕФЭПВу ЁЃШчЭМ 11aЫљЪО , ЭЈЙ§жїПЭЬхзїгУЙЙНЈЕФПЙОњ ЭПВудкгааЇЩБОњКѓ , ОМђЕЅНўХнМДПЩНтГ§жїПЭЬхзїгУЪЭЗХЫРОњ , зіЕНБэУцздЧхНр[76] ЁЃНјвЛВНЕиРћгУЙтПи жїПЭЬхзїгУ , МђЛЏЭПВуздЪЭЗХЙ§ГЬ[77] , ШчЭМ 11b ЫљЪО , ЭЈЙ§ПЩМћЙт/зЯЭтЕФзЊЛЛ , ХМЕЊБНгЩЗДЪНЯђЫГЪННс ЙЙзЊБф , БэУцМДПЩЪЕЯжПЙОњКѓЕФздЧхНр ЁЃСэЭт , XuПЮЬтзщРћгУЯЏЗђМюЗДгІдкєЧЛљСзЛвЪЏЩЯЙЙНЈЫсЯьгІЭП Ву , дкЯИОњИаШОВњЩњЕФЮЂЫсЛЗОГЯТЛсв§Ц№ЯЏЗђМюМќЖЯСб , ЪЭЗХЧьДѓУЙЫи , ЪЕЯжвЉЮяЕФЯьгІадЪЭЗХ[78] ЁЃ
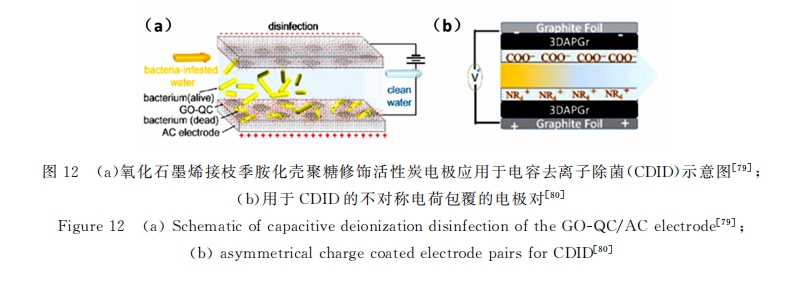
ДЫЭт,гЩгкФЭвЉОњдкЫЎЬхЛЗОГжазЬЩњТћбг,ПЙОњВФСЯгІгУгкЫЎДІРэСьгђвВОпгаЩюдЖЕФвтвхЁЃШчЭМ12aЫљЪО,Chan-parkПЮЬтзщРћгУбѕЛЏЪЏФЋЯЉНгжІМОяЇЛЏЕФПЧОлЬЧаоЪЮЛюадЬПЕчМЋ(GO-QC/AC),ЭЈЙ§ЕчШнШЅРызг(Capacitive deionization, CDI)ММЪѕИпаЇЮќИНЫЎжаЕФОњ,ДгЖјЪЕЯжвЛВНЗЈОЛЫЎГ§Оњ(Capacitive deionization disinfection,CDID)[79] ЁЃШчЭМ12bЫљЪО,РћгУЗЧЖдГЦЙІФмЛЏЮЂПзЛюЛЏ3DЪЏФЋЯЉЕчМЋ,ПЩвдЭЌЪБгааЇШЅГ§ЫЎжаЕФбЮКЭОњ[80] ЁЃQiuЭЈЙ§дкЛюадЬПЕчМЋБэУцЭПИВвЛВуМОяЇЛЏЕФОлввЯЉпСрЄ,зіЕНЕЭЕчбЙИпСїЫйЕиИпаЇГ§Оњ[81] ЁЃ
3 змНсгыеЙЭћ
ФПЧА,ПЙОњИпЗжзгВФСЯЕФбаОПжївЊМЏжадкЫќУЧЕФЛЏбЇКЭНсЙЙЗНУцЁЃЫцзХбаОПЕФЩюШы,адФмгХвьЕФПЙОњИпЗжзгВФСЯе§дкБЛВЛЖЯПЊЗЂГіРДЁЃ
ИпЗжзгВФСЯПЩвдзїЮЊжЧФм/АаЯђвЉЮяЕнЫЭЬхЯЕ,НЋвЉЮяОЋзМЕнЫЭЕНИаШОВПЮЛ,ИпаЇЗЂЛгвЉЮязїгУ,БмУтвЉЮяЕФЙ§СПЪЙгУ,ДгЖјНЕЕЭВЁОњФЭвЉадЕФЗЂЩњЁЃЭЌЪБ,гЩгкЙтЖЏСІПЙОњСЦЗЈОпгаИБзїгУаЁЁЂбЁдёадКУЕШгХЕу,НќФъРДЪмЕНМЋДѓЙизЂЁЃЙтУєМСдквЛЖЈВЈГЄЕФЙтЕФМЄЗЂЯТ,ВњЩњROS,НјЖјЩБОњЁЃ
ПЙОњИпЗжзгВФСЯЕФбаОПЕУЕНСЫГЄзуЕФЗЂеЙ,ЕЋШдДцдквЛаЉЮЪЬт,ШчПЙОњОлКЯЮяЕФПЙОњЛњРэЩаЮДЭъШЋЧхГў,ашвЊНјвЛВНбаОП;вЉЮяЕнЫЭЬхЯЕЕФАаЯђадвВгаД§ЬсИпЁЃПЙОњИпЗжзгВФСЯдкЩњЮявНвЉКЭЩњВњЩњЛюжаЕФгІгУ,вВгаД§НјвЛВНЬНЫїКЭЭЦНјЁЃЭЈЙ§баОПепЕФВЛЖЯЩюШыбаОПКЭЬНЫї,ШчЙћПЙОњИпЗжзгВФСЯПЩвдгУзївЉЮяРДДњЬцПЙЩњЫиЕФЪЙгУ,НЋКмДѓГЬЖШЩЯНЕЕЭ/МѕЛКФЭвЉадЕФЗЂЩњ,ЦЦНтВЁОњФЭвЉадЮЃЛњЁЃ
Утд№ЩљУїЃКБОЮФЮЊаавЕНЛСїбЇЯАЃЌАцШЈЙщдзїепМАддгжОЫљгаЃЌШчгаЧжШЈЃЌПЩСЊЯЕЩОГ§ЁЃЮФеТБъзЂгазїепМАЮФеТГіДІЃЌШчашдФЖСдЮФМАВЮПМЮФЯзЃЌПЩдФЖСддгжОЁЃ














