
’Σ“Σ …ηΦΤΚœ≥…ΝΥΨΏ”– 2 ΗωΜν–‘–ρΝ–ΒΡœΏ–‘ΚΆΜΖΉ¥ΕύκΡΦΑΨΏ”–ΒΞΗωΜν–‘–ρΝ–ΒΡΕΧΝ¥ΕύκΡ, ―–ΨΩΝΥΥϋΟ«ΒΡ…±ΨζΜν–‘ΓΔ œΗΑϊΕΨ–‘ΦΑ»ή―Σ–‘. ΫαΙϊ±μΟς, œΏ–‘κΡΚΆΜΖΉ¥κΡΒΡ…±ΨζΜν–‘ΗΏ”ΎΕΧΝ¥κΡ. άϊ”ΟΦΤΥψΡΘΡβΒΡΖΫΖ®ΦΤΥψΝΥΕύκΡ”κœΗΨζœΗΑϊΡΛ÷–“Μ÷÷÷Ί“ΣΒΡ≥…Ζ÷ΝΉ÷§θΘΗ ”Ά(DMPG)ΒΡΫαΚœΡή. ΫαΙϊ±μΟς, ΕύκΡ-DMPG ΒΡΫαΚœΡή”κΕύκΡΒΡ…±ΨζΜν–‘ΨΏ”–ΫœΗΏΒΡœύΙΊ–‘, œΏ–‘ΚΆΜΖΉ¥ΕύκΡ”κ DMPG ΒΡΫαΚœΡή¥σ”ΎΕΧΝ¥κΡ. œΏ–‘ΚΆΜΖΉ¥ΕύκΡΨυΚ§”– 2 ΗωΜν–‘–ρΝ–, Ω…ΧαΙ©ΕύΗωΚ…’ΐΒγΑ±ΜυΥα”κΚ…ΗΚΒγΒΡΝΉ÷§ΫαΚœ, ΫαΚœΡήΫœ¥σ, …±ΨζΜν–‘Ϋœ«Ω. ≤…”ΟΡΘΡβ…ζΈοΡΛΕ‘Τδ÷–ΦΗΧθΕύκΡΒΡΉς”ΟΜζάμΫχ––ΝΥ≥θ≤Ϋ―–ΨΩ. ΫαΙϊ±μΟς, ΗΟάύΕύκΡ”–Ω…Ρή Ι’ΐ≥Θ≤Η»ιΕ·ΈοœΗΑϊΒΡœΗΑϊΡΛ≤ζ…ζΩΉΕ¥; ΕχΕ‘”ΎœΗΨζœΗΑϊΡΛ, ΕύκΡ≤ΔΈ¥‘ΎΡΛ…œ≤ζ…ζΟςœ‘ΩΉΕ¥, Εχ «“ΐΤπΝΥœΗΨζœΗΑϊΡΛΒΡΨέΦ·.
ΥφΉ≈¥ΪΆ≥ΩΙ…ζΥΊ‘Ύ“Ϋ“©ΓΔ ≥ΤΖΓΔ –σΡΝ“ΒΚΆΥ°≤ζ“ΒΒ»Νλ”ρΒΡάΡ”Ο“‘ΦΑœΗΨζΆΜ±δΥΌΕ»ΒΡΦ”Ωλ, ΚήΕύœΗΨζΕ‘¥ΪΆ≥ΩΙ…ζΥΊΒΡΩΙ“©–‘Έ Χβ»’ΫΞΆΜ≥ω, »ΜΕχ‘ΎΙΐ»ΞΒΡ 30 Ρξ÷–»¥ΟΜ”–“Μ÷÷’φ’ΐ“β“ε…œΒΡ–¬÷÷άύΒΡΩΙΨζ“©Έο≥ωœ÷‘Ύ –≥Γ…œ[1]. “ρ¥Υ, ―Α’“ΩΙ…ζΥΊΒΡΧφ¥ζΤΖΤ»‘ΎΟΦΫό. ΩΙΨζκΡ(AMPs)ΒΡ≥ωœ÷”–Ω…Ρή Ι’βΨ÷ΟφΒΟΒΫΗΡΙέ[2], Υϋ «Υό÷ςΖά”υΧεœΒ÷–Χλ»ΜΟβ“ΏΒΡ“ΜΗω÷Ί“ΣΉι≥…≤ΩΖ÷. Χλ»ΜΟβ“Ώ‘ΎΈΔ…ζΈο«÷œ°Υό÷ςœΗΑϊΚσΦΗΖ÷÷”ΡΎΤτΕ·, “÷÷Τ≤Γ‘≠Χεά©…Δ, ΈΣΥό÷ςœΗΑϊΧαΙ©ΒΎ“Μ ±ΦδΒΡ±ΘΜΛ. ΩΙΨζκΡΙψΖΚΖ÷≤Φ”ΎΉ‘»ΜΫγ÷–,ΨΏ”–ΙψΤΉΩΙΨζ–‘, Ρ≥–©ΩΙΨζκΡΜΙΨΏ”–ΩΙΑ©–‘ΦΑΩΙ≤ΓΕΨ–‘[3,4]. ―–ΨΩ±μΟς, œΗΨζΒΡœΗΑϊΡΛ «ΩΙΨζκΡΒΡ÷ς“ΣΉς”ΟΑ–ΈΜ, ΩΙΨζκΡΆ®ΙΐΤΤΜΒœΗΑϊΡΛΒΡΆξ’ϊ–‘, ΙΤδ≤ζ…ζΩΉΕ¥Μρ’ΏΆΏΫβΕχ ΙΡΎ≤ΩΈο÷ ΆβΝς, Μρ’Ώ¥©ΆΗœΗΑϊΡΛΫχ»κœΗΑϊΡΎ≤Ω, Η…‘Λ“Μ–©÷Ί“ΣΒΡœΗΑϊΙΐ≥Χ, ¥”Εχ¥οΒΫ…±ΨζΉς”Ο[5]. ΕχΕ‘”ΎΈΔ…ζΈοά¥ΥΒ, ΗΡ±δΤδœΗΑϊΡΛΒΡΉι≥…ΚΆ≥…Ζ÷¥ζΦέΨό¥σ, “ρ¥ΥΩΙΨζκΡΤ’±ιΨΏ”–±»ΫœΒΆΒΡΩΙ“©–‘, ΨΏ”–«±‘ΎΒΡ”Π”ΟΦέ÷Β[6].
ΗυΨίΧλ»ΜΩΙΨζκΡΒΡΧΊ–‘Ϋχ––…ηΦΤ «ΖΔœ÷–¬ΩΙΨζκΡΒΡ÷Ί“ΣΆΨΨΕ[7]. ―–ΨΩ±μΟς, ΚήΕύΚ§”–ΕύΗωΜν–‘Τ§ΕΈΒΡΕύκΡΨΏ”–ΫœΗΏΒΡ…ζΈοΜν–‘, »γ WLBU2[8], V4[9], Tritrpticin ΒΡΕ‘≥ΤΡΘΡβκΡ[10]ΚΆ Gramicidin S[11]Β».¥ΥΆβ, ΚήΕύΩΙΨζκΡ‘Ύ»ή“Κ÷– «ΒΞΧε, ”κ…ζΈοΡΛœύΫαΚœ ±–Έ≥…ΝΫ«ΉΒΡΕΰΨέΧε, »γ Pexiganan(MSI-78)[12],PG-1[12]ΚΆ Sushi 3[13]Β». Ε‘”Ύ’β–©ΩΙΨζκΡΕχ―‘, ΕΰΨέΧε «ΤδΜν–‘ΙΙœσ, ΕχΕΰΨέΧε“≤Ω… ”ΈΣΖ÷Ή”÷–Κ§”–2 ΗωΜν–‘–ρΝ–. ¥σ≤ΩΖ÷ΩΙΨζκΡΨΏ”–ΝΫ«Ή–‘ΫαΙΙ, ΥΪΜν–‘–ρΝ– ΙΤδΝΫ«Ή–‘Φ”«Ω, ”–÷ζ”Ύ…ζΈοΜν–‘ΒΡ±μœ÷.“ρ¥Υ, ΨΏ”–ΥΪΜν–‘–ρΝ–ΒΡΕύκΡΩ…ΡήΨΏ”–Ηϋ«ΩΒΡ…ζΈοΜν–‘. ±ΨΈΡ…ηΦΤΝΥΚ§”–ΥΪΜν–‘–ρΝ–ΒΡΩΙΨζκΡ, ―–ΨΩΥΪΜν–‘–ρΝ– «Ζώ”–÷ζ”ΎΧαΗΏΩΙΨζκΡΒΡΜν–‘. Φχ”ΎΕύκΡΒΡΜ·―ßΚœ≥…≥…±Ψ, ΨΏ±ΗΩΙΨζΜν–‘ΒΡΕΧκΡΨΏ”–¥σ≈ζΝΩ…ζ≤ζΒΡ«±ΝΠ, “ρ¥Υ±ΨΈΡ―Γ»ΓΩΙΨζκΡ ΐΨίΩβ(http: / / aps. unmc. edu / AP / main. php)÷–ΨΏ”–ΫœΕΧ–ρΝ–ΒΡΕύκΡ Ac-RRWWRF-NH2(Combi-1) ΚΆ Ac-FRWWHR-NH2(Combi-2)ΉςΈΣΜν–‘–ρΝ–. ’β 2 ΧθΕύκΡΨυΈΣ≤ΜΕ‘≥Τ–ρΝ–, ΈΣΦ”«ΩΕύκΡΒΡΝΫ«Ή–‘, –ηΫΪ Combi-1 ΚΆ Combi-2 ΒΡ–ρΝ–ΒΏΒΙ, Ρφ–ρΒΡΩΙΨζκΡ «Ζώ»‘”–Μν–‘…–≤Μ«ε≥ΰ, “ρ¥Υ±ΨΈΡΩΦ≤λΝΥΡφ–ρΒΡ Combi-1 ΚΆ Combi-2 ΒΡΜν–‘. ΫΪ Combi-1 ΚΆ Combi-2 ΦΑΡφ–ρΒΡ Combi-1 ΚΆCombi-2 ΉςΈΣΜν–‘–ρΝ–, ≤Έ’’ V4 ΒΡΫαΙΙ[9] …ηΦΤ≥ωΨΏ”–ΥΪΜν–‘–ρΝ–ΒΡΕύκΡ, ≤β ‘ΝΥΤδ…±ΨζΜν–‘ΓΔ ΕΨ–‘ΓΔ»ή―Σ–‘ΦΑ”κΡΘΡβ…ζΈοΡΛΒΡœύΜΞΉς”Ο, ≤Δ‘Υ”ΟΦΤΥψΡΘΡβΒΡΖΫΖ®ΦΤΥψΝΥΥυ…ηΦΤΒΡΕύκΡ”κœΗΨζΒΡœΗΑϊΡΛ÷–“Μ÷÷÷Ί“ΣΒΡΝΉ÷§ΓΣΓΣΓΣΝΉ÷§θΘΗ ”ΆΒΡΫαΚœΡή. ΕΰΝρΦϋΜΖΜ·”–÷ζ”ΎΈ»Ε®ΕύκΡΒΡΫαΙΙ, “ρ¥Υ±ΨΈΡΜΙ…ηΦΤΝΥΨΏ”–ΒΞΗωΕΰΝρΦϋΒΡΜΖΉ¥ΕύκΡ≤ΔΩΦ≤λΤδ…±ΨζΜν–‘, ΈΣΩΙΨζκΡΒΡ…ηΦΤΧαΙ©ΝΥ“άΨί.
1 Β―ι≤ΩΖ÷
1. 1 ‘ΦΝ”κ“«Τς
ΗοάΦ œ“θ–‘ΨζΑϋά®¥σ≥ΠΗΥΨζ(Escherichia coli)ΓΔ Ά≠¬ΧΦΌΒΞφΏΨζ(Pseudomonas aeruginosa)ΓΔ ±Ϊ¬ϋ≤ΜΕ·ΗΥΨζ(Acinetobacter baumannii)ΚΆ »¬σ―ΩΙ――χΒΞΑϊΨζ( Stenotrophomonas maltophilia); ΗοάΦ œ―τ–‘ΨζΑϋά®ΫπΜΤ…ΪΤœΧ―«ρΨζ(Staphyloccocus aureus)ΓΔ ΧΌΜΤΈΔ«ρΨζ(Micrococcus luteus)ΚΆΩί≤ί―ΩφΏΗΥΨζ(Bacillus subti-lis). Τδ÷–, ¥σ≥ΠΗΥΨζΓΔ ΫπΜΤ…ΪΤœΧ―«ρΨζΓΔ ΧΌΜΤΈΔ«ρΨζΦΑΩί≤ί―ΩφΏΗΥΨζ”…Κ”Ρœ Γ ≥ΤΖ“©ΤΖΦλ―ιΥυΧαΙ©,Τδ”ύΨζ÷ξ”…ΝΌ¥≤Ζ÷άκΒΟΒΫ. »Υ÷ßΤχΙή…œΤΛœΗΑϊ÷ξ(BEAS-2B œΗΑϊ)”…÷Θ÷ί¥σ―ßΈβΈάΕΪΫΧ ΎάΓ‘υ; ΫΓΩΒ≥…ΡξΆΟΉ” 1 ÷Μ, ”…Κ”Ρœ Γ÷Θ÷ί¥σ―ßΕ·Έο Β―ι÷––ΡΧαΙ©; Εύ’≥ΨζΥΊ B(Polymyxin B, PB)ΙΚΉ‘”Ύ Sigma ΙΪΥΨ;Triton X-100 ΙΚΉ‘”Ύ±±Ψ©Υςά¥±Π…ζΈο”–œόΙΪΥΨ; ΝΉ÷§θΘΒ®Φν(DMPC) ”κΝΉ÷§θΘΗ ”Ά(DMPG) ΨυΙΚ”ΎAvanti Polar Lipids Inc(ΟάΙζ); ΤδΥϋΜ·―ß ‘ΦΝΨυΈΣΙζ≤ζΖ÷Έω¥Ω; Υυ”ΟΥ°ΗυΨί Β―ι“Σ«σ≤…”Ο≥§¥ΩΥ°ΜρΕΰ¥Έ’τΝσΥ°.Spectra MR ΟΗ±ξ“«(ΟάΙζ DYNEX ΙΪΥΨ); RST3000 ΒγΜ·―ßΙΛΉς’Ψ(Υ’÷ί»πΥΦΧΊ“«Τς”–œόΙΪΥΨ).
1. 2 Β―ιΖΫΖ®
1. 2. 1 …±Ψζ Β―ι Χτ»Γ ΝΩΨζ÷÷‘ΎΙΧΧε Luria-Bertani(LB) ≈ύ―χΜυ÷–Μ°œΏ, ‘Ύ≈ύ―χœδ÷–”Ύ 37 “φΙΐ“Ι≈ύ―χ. Χτ»Γ ΝΩ¥Π”ΎΕ‘ ΐ…ζ≥ΛΤΎΒΡœΗΨζ”Ύ…ζάμ―ΈΥ°÷–, ≈δ÷ΤΉ«Ε»ΈΣ 0έ± 5 ~ 1 ¬σ œΉ«Ε»ΒΡΨζ–ϋ“Κ, ¥Υ ±œΗΨζΨζ¬δ ΐ‘ΦΈΣ 1X10^8 CFU/ mL, Ι”Ο ±œΓ Ά÷Ν 1X10^6 CFU/ mL. ≈δ÷Τ≈®Ε»ΈΣ 2 mg / mL ΒΡΕύκΡ»ή“Κ. ≤…”ΟΈΔΝΩ»βΧάΕΰ±ΕœΓ ΆΖ®≤βΕ®Κœ≥…ΕύκΡΕ‘ΗςœΗΨζΒΡΉν–Γ“÷Ψζ≈®Ε»(MIC). Ά§ ±Ϋχ––»ήΦΝΓΔ ÷ΜΦ”Ψζ“Κ≤ΜΦ”ΕύκΡΒΡ“θ–‘Ε‘’’ΚΆΦ”»κΕύ’≥ΨζΥΊ B ΒΡ―τ–‘Ε‘’’, ΟΩΗωΕύκΡΤΫ––Ϋχ–– 3 ¥Έ. ÷Ο”Ύ 37 “φΚψΈ¬œδ÷–≈ύ―χ 12 h, Ιέ≤λΩΉΡΎ»ή“ΚΒΡΜλΉ««ιΩω, 96 ΩΉΑεΆ§≈≈÷–»β―έΥυΦϊ≥Έ«εΩΉΥυΕ‘”ΠΒΡΉν–Γ≈®Ε»Φ¥ΈΣΗΟΕύκΡΒΡ MIC ÷Β.
1. 2. 2 ΕΨ–‘ Β―ι ”ΟΚ§ 10% (ΧεΜΐΖ÷ ΐ)ΧΞ≈Θ―Σ«εΒΡ RPMI 1640(Κ§ 100 U/ mL «ύΟΙΥΊΚΆ 100 U/ mL Ν¥ΟΙΥΊ)≈ύ―χΜυ≥ΘΙφ≈ύ―χ BEAS-2B œΗΑϊ. ≤…”ΟΕ‘ ΐ…ζ≥ΛΤΎΒΡ BEAS-2B œΗΑϊ, ”ΟΚ§ 10% ΧΞ≈Θ―Σ«εΒΡ RPMI1640 ≈ύ―χ“ΚΒςΫΎœΗΑϊ≈®Ε»ΈΣ 5X10^4 Cells/ mL, Ϋ”÷÷ΒΫ 96 ΩΉΑε. ≈ύ―χ 12 h Κσ, Φ”»κ≤ΜΆ§≈®Ε»ΒΡΕύκΡ(÷’≈®Ε»Ζ÷±πΈΣ 2.5, 5, 10, 20, 40, 80, 160 ΚΆ 320 ug / mL), ΟΩ÷÷ΕύκΡ≈®Ε»…η 4 ΗωΗ¥ΩΉ, ≤Δ…η≤ΜΦ”œΗΑϊ“ΚΒΡΒςΝψΩΉΚΆ÷ΜΦ”œΗΑϊ“ΚΓΔ ≤ΜΦ”κΡ“ΚΒΡΩ’ΑΉΕ‘’’ΩΉ. ≤…”Ο MTT Ζ®≤βΕ®œΗΑϊΕΨ–‘, ”Ύ 490 nm ≤®≥Λœ¬≤βΕ®ΙβΟήΕ»÷Β.
1. 2. 3 »ή―Σ–‘ Β―ι Ζ÷±π≥Τ»ΓΗςΕύκΡ, ”Ο0.9% (÷ ΝΩΖ÷ ΐ)…ζάμ―ΈΥ°»ήΫβ, ≈®Ε»ΈΣ1000 ug / mL, “ά¥ΈΕΰ±ΕœΓ ΆΦ”»κΒΫ 96 ΩΉΑε÷–, ΟΩΩΉ 50 uL, ΟΩΗω―υΤΖΤΫ–– 3 ¥Έ(÷’≈®Ε»Ζ÷±π 500, 250, 125, 64, 32, 16 ΚΆ8 ug / mL). ≥ι»ΓΫΓΩΒΆΟΉ”ΒΡ–¬œ ―Σ“Κ, Φ”»κΒΫΚ§”– 1 g / L ΗΈΥΊΡΤΒΡάκ–ΡΙή÷–, “‘ 1000 r/ min ΉΣΥΌάκ–Ρ5 min, Τζ»Ξ…œ«ε“Κ, Ζ÷άκΒΟΚλœΗΑϊ. ‘Ό”Ο 0.9% …ζάμ―ΈΥ°œ¥Β” 2 ¥Έ, ÷ΊΗ¥άκ–Ρ≤ΌΉς, Τζ»Ξ…œ«ε“Κ, ΒΟΒΫ―ΙΜΐΚλœΗΑϊ. »Γ 2 ΒΈ―ΙΜΐΚλœΗΑϊΦ”»κ 4 mL …ζάμ―ΈΥ°Φ¥ΒΟ 2% (ΧεΜΐΖ÷ ΐ)ΚλœΗΑϊ–ϋ“Κ. »Γ 2% ΚλœΗΑϊ–ϋ“Κ 50 uL, “ά¥ΈΦ”»κΒΫ…œ ω 96 ΩΉΑεΗςΩΉ÷–. ”ΟΚ§ 1% ΚλœΗΑϊΒΡ…ζάμ―ΈΥ°ΚΆ’τΝσΥ°Ζ÷±πΉςΈΣΩ’ΑΉ“θ–‘Ε‘’’ΚΆ 100% »ή―Σ―τ–‘Ε‘’’. ”Ύ 37 Ε»œ¬“Γ¥≤’ώΒ¥ΖθΜ· 4 h. ¥ΐΚλœΗΑϊ≥ΝΒμ, Έϋ»Γ 40 uL …œ«ε“ΚΦ”»κΒΫΝμ“ΜΗωΗ…ΨΜΒΡ 96 ΩΉΑε÷–, ≤…”ΟΟΗ±ξ“«‘Ύ 540 nm ≤®≥Λœ¬≤βΕ®ΈϋΙβΕ».
1. 2. 4 ΕύκΡΚΆΝΉ÷§ΒΡœύΜΞΉς”Ο ≤…”Ο»ΐΒγΦΪΧεœΒ―–ΨΩΕύκΡ”κΝΉ÷§ΒΡœύΜΞΉς”Ο: ΡΛ–ό Έ≤ΘΧΦΒγΦΪΈΣΙΛΉςΒγΦΪ, ±ΞΚΆΗ Ι·ΒγΦΪΈΣ≤Έ±»ΒγΦΪ, ≤§ΒγΦΪΈΣΕ‘ΒγΦΪ. ΒγΫβ“ΚΈΣ 1 mmol / L ΒΡ K3Fe(CN)6/ K4Fe(CN)6»ή“Κ(ΑϋΚ§ 0.1 mol / L KCl). ΫΪ≤ΘΧΦΒγΦΪ‘Ύ»ΐ―θΜ·Εΰ¬ΝΖέΡ©÷–≈ΉΙβΚσ, “ά¥Έ‘ΎœθΥα(ΧεΜΐ±» 1 :1)ΓΔΈόΥ°““¥ΦΚΆΕΰ¥ΈΥ°÷–≥§…υ«εœ¥ 1 min, ”ΟΒΣΤχ¥ΒΗ…. ≈δ÷Τ 4 mg / mL DMPC ≥…ΡΛ“Κ(¬»Ζ¬»ή“Κ) ΦΑ 4 mg / mLDMPG ≥…ΡΛ“Κ[V(ΦΉ¥Φ) : V(¬»Ζ¬)= 1:3]. ΫΪ 5 uL DMPC Μρ DMPG ≥…ΡΛ“ΚΒΈΆΩ‘Ύ≤ΘΧΦΒγΦΪ±μΟφ, ΝάΗ…Κσ‘Ύ 0.1 mol / L KCl »ή“Κ÷–Υ°Μ· 30 min, ÷ΤΒΟΝΉ÷§ΥΪ≤ψΡΛ–ό ΈΒγΦΪ. ΫΪΗΟ–ό ΈΒγΦΪ‘ΎΒγΫβ“Κ÷–Ϋχ––―≠ΜΖΖϋΑ≤≤βΕ®, …®ΥΌΈΣ 50 mv / s. »ΜΚσΫΪΒγΦΪΫΰ≈ί‘Ύ“ΜœΒΝ–≈®Ε»ΒΡΕύκΡ»ή“Κ÷– 30 min, ‘Ό‘ΎΒγΫβ“Κ÷–Ϋχ––―≠ΜΖΖϋΑ≤≤βΕ®. Ά®Ιΐ 2 ¥Έ≤βΕ®ΒΡ―θΜ·ΖεΒγΝς≤νά¥ΚβΝΩΕύκΡ”κΝΉ÷§ΥΪ≤ψΡΛΒΡœύΜΞΉς”Ο.
≤Έ’’ΈΡœΉ[14]ΖΫΖ®÷Τ±Η÷§÷ Χε. ΫΪ 100 uL 1 mg / mL ΒΡΕύκΡ»ή“ΚΦ”»κ 96 ΩΉΑε÷–, “ά¥ΈΕΰ±ΕœΓ Ά,ΟΩΩΉ»ή“ΚΧεΜΐ 50 uL. ΟΩΩΉΦ”»κ 30 uL 2 mg / mL ΒΡ÷§÷ Χε, ΙΕύκΡΉν÷’≈®Ε»“ά¥ΈΈΣ 625, 313, 156, 78ΚΆ 39 ug / mL. “Έ¬œ¬Ζθ”ΐ 20 min, ”ΟΟΗ±ξ“«”Ύ 600 nm ≤®≥Λœ¬≤βΕ®ΙβΟήΕ»÷Β(OD600 ). “‘Φ”»κ 50 uL ΒΡPBS ΜΚ≥ε“ΚΈΣ“θ–‘Ε‘’’, Φ”»κ 50 uL 10% ΒΡ Trion X-100 ΈΣ―τ–‘Ε‘’’. ΟΩΗωΕύκΡΤΫ––Ϋχ–– 3 ¥Έ.
1. 2. 5 ΦΤΥψΡΘΡβ ≤…”ΟΝΉ÷§θΘΗ ”Ά(DMPG)ΡΘΡβœΗΨζœΗΑϊΡΛ, Ε‘ΕύκΡ”κ DMPG ΒΡΫαΚœΡήΫχ––ΦΤΥψ. ΕύκΡ”κ DMPG Ζ÷Ή”ΒΡ≥θ ΦΙΙ–Ά”… Gaussian view ΚΆ Amber »μΦΰ÷–ΒΡ leap ΡΘΩιΙ≤Ά§ΙΙΫ®. ΦΤΥψ Ι”Ο Gaussian09 »μΦΰ[15], ≤…”Ο PM3 ΑκΨ≠―ιΥψΖ®≤Έ’’ΈΡœΉ[16,17]Ε‘ DMPG ΦΑΗςΗωΕύκΡΖ÷Ή”Ϋχ––ΙΙ–Ά”≈Μ·. »ΜΚσΕ‘ΕύκΡ”κ DMPG Ζ÷Ή”ΒΡΗ¥ΚœΈοΫχ––”≈Μ·ά¥ΡΘΡβΕύκΡ”κ DMPG Ζ÷Ή”ΒΡœύΜΞΉς”Ο, ”…”ΎΗ¥ΚœΈοΖ÷Ή”ΝΩΫœ¥σ,ΡΘΡβ ±»‘»Μ≤…”Ο PM3 ΑκΨ≠―ιΥψΖ®. ΕύκΡ”κ DMPG ÷ς“ΣΆ®ΙΐΨ≤ΒγΉς”ΟΫαΚœ, Ά§ ±–Έ≥…«βΦϋ, ΦΤΥψ ±–η“ΣΆ§ ±ΩΦ¬«ΝΫ÷÷Ής”Ο. ≤…”Ο“‘œ¬ΙΪ ΫΦΤΥψΕύκΡ”κ DMPG Ζ÷Ή”ΒΡΫαΚœΡή, ”Ο“‘ΚβΝΩΕΰ’Ώ÷°ΦδΒΡœύΜΞΉς”Ο≥ΧΕ».

Ϋ÷–, E ΈΣ”≈Μ·ΚσΗςΉιΖ÷ΒΡΒΞΒψΡή. ΦΤΥψ ±ΨΓΝΩΩΦ¬«≤ΜΆ§ΒΡΫαΚœΡΘ Ϋ, ¥”Εχ ΙΕύκΡ”κ DMPG ¥οΒΫΉν”≈ΫαΚœ.
2 ΫαΙϊ”κΧ÷¬έ
2. 1 ΕύκΡΒΡ…ηΦΤ
ΡΩ«Α, –¬ΩΙΨζκΡΒΡΖΔœ÷÷ς“Σ“άάΒ”ΎΕ‘Χλ»ΜΩΙΨζκΡΦΑΚœ≥…≤ζΈοΒΡ¥σΙφΡΘ…Η―Γ, ΉιΚœΜ·―ßΕ‘”Ύœ»ΒΦΜ·ΚœΈοΒΡΖΔœ÷ΨΏ”–÷Ί“ΣΉς”Ο. Combi-1 ΚΆ Combi-2 «≤…”ΟΉιΚœΜ·―ßΖΫΖ®Ψ≠Ιΐ¥σΙφΡΘ…Η―ΓΒΟΒΫΒΡΩΙΨζκΡ, Ε‘Εύ÷÷œΗΨζΦΑΫΆΡΗΨζΨΏ”–ΙψΤΉ…±ΨζΜν–‘, ΕχΕ‘≤Η»ιΕ·ΈοœΗΑϊΦΑΚλœΗΑϊΈόΕΨΜρΨΏ”–Ϋœ–ΓΕΨ–‘. Combi-1 Ε‘Εύ÷÷œΗΨζΒΡ…±ΨζΜν–‘œύΒ±Μρ”≈”ΎΧλ»ΜΩΙΨζκΡ(IC50 = 5 ~ 39 ug / mL)[18]. Combi-1 ΚΆ Combi-2 ΨυΚ§”– 6 ΗωΑ±ΜυΥα≤–Μυ, κΡΝ¥≥ΛΕ»ΫœΕΧ, ΒΪ»¥±μœ÷≥ωΫœΚΟΒΡ…±ΨζΜν–‘ΦΑΫœΒΆΒΡΕΨ–‘, “ρ¥ΥΨΏ”–―–ΨΩ“β“ε. ±ΨΈΡ―ûà Combi-1 ΚΆ Combi-2 ΉςΈΣ“ΜΗωΜν–‘–ρΝ–, ≤Έ’’ V4 ΩΙΨζκΡΒΡ…ηΦΤ, ≤…”Ο GSG ΫΪ2 ΗωΜν–‘–ρΝ–Ν§Ϋ”–Έ≥…Κ§”–ΥΪΜν–‘–ρΝ–ΒΡœΏ–‘ΕύκΡ. Combi-1 ΚΆ Combi-2 ΨυΈΣ≤ΜΕ‘≥Τ–ρΝ–, ΈΣ ΙœΏ–‘ΕύκΡ¥”ΫαΙΙ…œΝΫ«Ή–‘ΗϋΦ”œ‘÷χ, ≤…”ΟΡφ–ρΒΡΕύκΡ Ac-FRWWRR-NH2(r-Combi-1) ΚΆ Ac-RHWWRF-NH2(r-Combi-2)ΚΆœύ”ΠΒΡ’ΐ–ρΕύκΡœύΫαΚœ…ηΦΤ–Έ≥…œΏ–‘ΕύκΡ Ac-RRWWRFGSGFRWWRR-NH2(l-Combi-1) ΚΆ Ac-FRWWHRGSGRHW-WRF-NH2(l-Combi-2). ΈΣΫχ“Μ≤ΫΙΧΕ®ΕύκΡΒΡΙΙœσ, Ι ηΥ°ΟφΗϋ ηΥ°, «ΉΥ°ΟφΗϋ«ΉΥ°, ≤…”ΟΖ÷Ή”ΡΎΕΰΝρΦϋΜΖΜ·œΏ–‘ΕύκΡ, –Έ≥…ΜΖΉ¥ΒΡΚ§”–ΥΪΜν–‘–ρΝ–ΒΡΕύκΡ Ac-CRRWWRFGSGFRWWRRC-NH2(c-Combi-1)ΚΆ Ac-CFRWWHRGSGRHWWRFC-NH2(c-Combi-2).
2. 2 ΕύκΡ MIC ÷ΒΒΡ»ΖΕ®
≤…”ΟΡΩ ”Ζ®, Ιέ≤λ»β―έΥυΦϊΒΡ≥Έ«εΩΉΥυΕ‘”ΠΒΡΉν–Γ≈®Ε», ΩΦ≤λΝΥΕύκΡΕ‘Εύ÷÷ΗοάΦ œ“θ–‘ΨζΚΆ―τ–‘ΨζΒΡ…±ΨζΜν–‘, ΫαΙϊΦϊ±μ 1. ΨΏ”–ΒΞΗωΜν–‘–ρΝ–ΒΡΕύκΡ Combi-1 κΡΝ¥Υδ»ΜΫœΕΧ, ΒΪ»‘ΨΏ”–ΫœΚΟΒΡ…±ΨζΜν–‘, Ε‘Εύ÷÷ΗοάΦ œ“θ–‘ΨζΚΆ―τ–‘ΨζΒΡ MIC ÷ΒΈΣ 32 ~ 64 mg / mL(≥ΐΩί≤ί―ΩφΏΗΥΨζ). ”κ Combi-1 –ρΝ–Άξ»ΪœύΖ¥ΒΡ r-Combi-1 Ε‘¥σΕύ ΐΨζ÷÷…±ΨζΜν–‘¥σ¥σΫΒΒΆ. ΫΪ Combi-1 ΚΆ r-Combi-1 ”Ο GSG Ν§Ϋ”Υυ–Έ≥…ΒΡl-Combi-1 ±μœ÷≥ωΗϋΚΟΒΡ…±ΨζΜν–‘, Ε‘Υυ―–ΨΩΒΡΨζ÷÷ΒΡ MIC ÷ΒΈΣ 8 ~ 32 mg / mL. Ε‘Εύ÷÷Ψζ÷÷Εχ―‘,l-Combi-1 ΒΡ…±ΨζΜν–‘±» Combi-1 ΧαΗΏ‘Φ 1 ±Ε. Ζ÷Ή”ΡΎΕΰΝρΦϋΜΖΜ·ΒΡ c-Combi-1 ΒΡ…±ΨζΜν–‘”κœΏ–‘ΒΡl-Combi-1 Μυ±ΨœύΒ±(≥ΐΗω±πΨζ÷÷Άβ). ”…ΉιΚœΜ·―ßΥυΜώΒΟΒΡ Combi-2 Μν–‘≤ΜΦΑ Combi-1, Ε‘Εύ ΐΨζ÷÷…±ΨζΜν–‘≤ΜΦ―. Ρφ–ρΒΡ r-Combi-2 Ε‘¥σΕύ ΐΨζ÷÷ΦΗΚθΈό…±ΨζΜν–‘. ΒΪΫΪΕΰ’Ώ”Ο GSG Ν§Ϋ”ΥυΒΟ l-Combi-2 ΒΡ…±ΨζΜν–‘¥σ¥σΧαΗΏ, Ε‘¥σΕύ ΐΨζ÷÷ΒΡ MIC ÷ΒΫœΒΆ. ΜΖΜ·ΒΡ c-Combi-2 ±» l-Combi-2 …±ΨζΡήΝΠ…‘”–ΫΒΒΆ,ΒΪ»‘±μœ÷≥ω“ΜΕ®ΒΡ…±ΨζΜν–‘. “‘…œΫαΙϊ±μΟς, Ρφ–ρΒΡΕύκΡΚΆ’ΐ–ρΒΡΕύκΡΥδ»Μ÷Μ «Α±ΜυΥα–ρΝ–œύΖ¥, ΒΪΜν–‘œύ≤νΫœ¥σ, ’βΩ…Ρή”κΕύκΡΙΙ–Ά≤ΜΆ§”–ΙΊ. ΨΏ”–ΥΪΜν–‘–ρΝ–ΒΡœΏ–‘ΕύκΡΨΏ”–ΫœΗΏΒΡ…±ΨζΡήΝΠ, ±»ΨΏ”–ΒΞΜν–‘–ρΝ–ΒΡΕύκΡΜν–‘¥σ¥σΧαΗΏ. ΧΊ±π «Ήι≥… l-Combi-2 ΒΡ Combi-2 ΚΆ r-Combi-2 …±ΨζΜν–‘ΫœΒΆΜρΦΗΚθΈό…±ΨζΜν–‘, ΒΪ”…Εΰ’ΏΉι≥…ΒΡ l-Combi-2 »¥ΨΏ”–ΫœΗΏΒΡ…±ΨζΡήΝΠ. ΜΖΉ¥ΕύκΡΒΡ…±ΨζΡήΝΠ”κœΏ–‘ΕύκΡœύΒ±Μρ…‘≤ν, ΩΦ¬«ΒΫΕύκΡΒΡΚœ≥…≥…±Ψ, ΨΏ”–ΥΪΜν–‘–ρΝ–ΒΡœΏ–‘ΕύκΡΨΏ”–Ϋχ“Μ≤Ϋ―–ΨΩΒΡΦέ÷Β. ¥ΥΆβ, 8 ΧθΕύκΡΕ‘ΗοάΦ œ―τ–‘ΨζΒΡ…±ΨζΜν–‘Ψυ¬‘«Ω”ΎΗοάΦ œ“θ–‘Ψζ, ΧΊ±π «Ωί≤ί―ΩφΏΗΥΨζ.
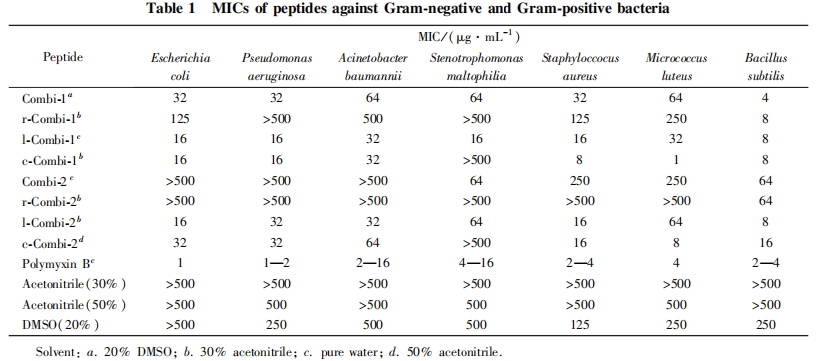
2. 3 ΕύκΡΒΡΕΨ–‘ Β―ιΚΆ»ή―Σ–‘ Β―ι
―ûÅœ ωΕύκΡ÷–…±Ψζ–ßΙϊΫœΚΟΒΡ Combi-1, l-Combi-1 ΚΆ l-Combi-2 Ϋχ––œΗΑϊΕΨ–‘ Β―ι, ΫαΙϊΦϊΆΦ 1.ΕύκΡάύΩΙΨζΥΊ―τ–‘Ε‘’’Εύ’≥ΨζΥΊ B ΥδΨΏ”–Ϋœ«ΩΒΡ…±ΨζΜν–‘(±μ 1), ΒΪΜα“ΐΤπ≤ΩΖ÷’ΐ≥ΘœΗΑϊΒΡΥάΆω. ΧΊ±π «≈®Ε»>80 mg / mL ±, Εύ’≥ΨζΥΊ B Ω…‘λ≥…ΫœΗΏΒΡœΗΑϊΥάΆω¬ . Combi-1 ΒΡœΗΑϊΕΨ–‘Ϋœ–Γ, ‘Ύ≈®Ε»–Γ”ΎΒ»”Ύ80mg / mL ±, Ε‘œΗΑϊΒΡ“÷÷Τ¬ Ψυ≤Μ≥§Ιΐ 22% , ΒΆ≈®Ε» ±ΕΨ–‘ΗϋΒΆ. l-Combi-1 ‘Ύ≈®Ε»–Γ”ΎΒ»”Ύ40 mg / mL ±Ε‘œΗΑϊΒΡ“÷÷Τ¬ ΚήΒΆ, ΒΪ≈®Ε»>80 mg / mL ±, œΗΑϊΕΨ–‘Φ±Ψγ…ΐΗΏ. l-Combi-2 ‘ΎΒΆ≈®Ε» ±“≤”–“ΜΕ®ΒΡœΗΑϊ“÷÷ΤΉς”Ο(≈®Ε»–Γ”ΎΒ»”Ύ80 mg / mL), ΗΏ≈®Ε» ±ΕΨ–‘Ϋœ¥σ. “‘…œΫαΙϊΥΒΟς, Combi-1 ΚΆ l-Combi-1 ‘ΎΫœΒΆ≈®Ε»œ¬ΨΏ”–ΫœΗΏΒΡ…±ΨζΜν–‘«“œΗΑϊΕΨ–‘ΫœΒΆ.
ΕύκΡ Combi-1, l-Combi-1 ΚΆ l-Combi-2 Ε‘ΆΟ―ΣœΗΑϊΒΡ»ή―Σ–‘ΦϊΆΦ 2. Combi-1 ΚΆ l-Combi-2 ‘Ύ≈®Ε»–Γ”ΎΒ»”Ύ125 mg / mL ±Ε‘ΆΟ―ΣœΗΑϊ»ή―Σ–‘Κή–Γ, ΒΪΒ±≈®Ε»…ΐΗΏ ±, »ή―Σ–‘‘ω¥σ; Εχ l-Combi-1 ΚΆ―τ–‘Ε‘’’Εύ’≥ΨζΥΊ B ‘Ύ Β―ι≈®Ε»ΖΕΈßΡΎΜυ±ΨΈό»ή―Σ–‘. Ήέ…œΥυ ω, Combi-1 ΚΆ l-Combi-1 ‘ΎΒΆ≈®Ε»œ¬ΨΏ”–Ϋœ«ΩΒΡ…±ΨζΜν–‘, Ά§ ±œΗΑϊΕΨ–‘ΚΆ»ή―Σ–‘ΫœΒΆ, “ρ¥ΥΨΏ”–Ϋχ“Μ≤ΫΒΡ―–ΨΩΦέ÷ΒΚΆ«±‘ΎΒΡ”Π”ΟΦέ÷Β.
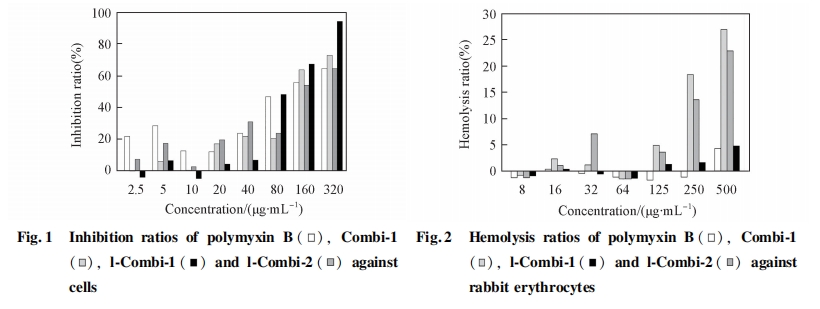
2. 4 ΕύκΡ”κΝΉ÷§ΒΡœύΜΞΉς”Ο
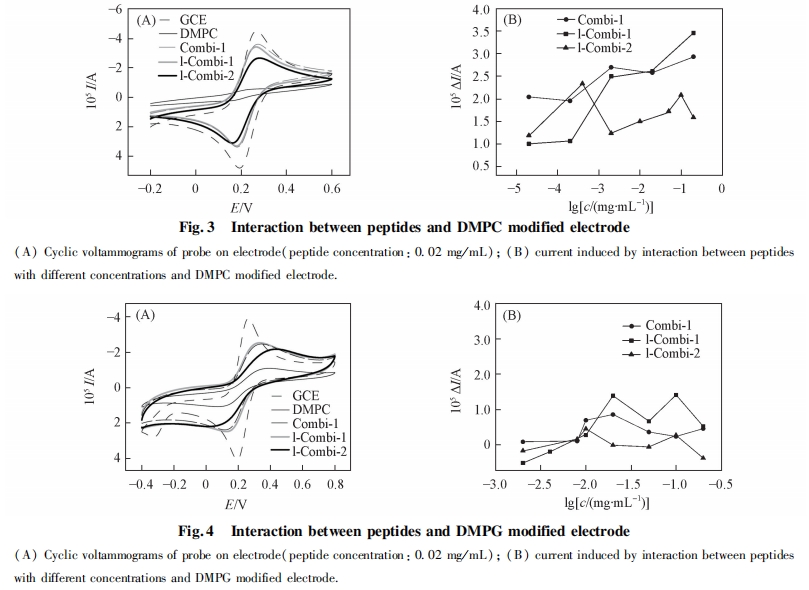
2. 4. 1 ΕύκΡ”κΝΉ÷§ΥΪ≤ψΡΛΒΡœύΜΞΉς”Ο ΙΧΧε÷ß≥≈ΒΡΝΉ÷§ΥΪ≤ψΡΛΈ»Ε®–‘ΚΟ, ΉςΈΣ“Μ÷÷…ζΈοΡΘΡβΡΛ“―±ΜΙψΖΚΒΊ”Π”Ο”ΎΩΙΨζκΡ”κ…ζΈοΡΛΒΡœύΜΞΉς”Ο―–ΨΩ÷–[19 ~ 21]. ±ΨΈΡ≤…”Ο¥ΥΡΛΡΘΡβ…ζΈοΡΛ―–ΨΩΕύκΡ «ΖώΡή‘ωΦ”…ζΈοΡΛΒΡΆ®ΆΗ–‘. ΫΪ DMPC Μρ DMPG –ό Έ”ΎΒγΦΪ…œ, ≤Δ÷Ο”ΎΒγΫβ“Κ÷–≤β ‘. ΝΉ÷§ΨΏ”–ΒγΨχ‘Β–‘, “ρ¥ΥΩ…ΉηΑ≠ΒγΫβ“Κ÷–ΒΡΧΫ’κ K3Fe(CN)6/ K4Fe(CN)6ΒΫ¥οΒγΦΪ±μΟφ. ”κ¬ψ≤ΘΧΦΒγΦΪœύ±», ΧΫ’κΒΡ―θΜ·ΜΙ‘≠ΒγΝςΫœΒΆ. Β±ΝΉ÷§ΥΪ≤ψΡΛΒγΦΪ±Μ÷Ο”ΎΕύκΡ»ή“Κ÷–, »γΙϊΕύκΡ”κΝΉ÷§ΖΔ…ζœύΜΞΉς”Ο, ΙΝΉ÷§ΥΪ≤ψΡΛ≤ζ…ζΩΉΕ¥Μρ’ΏΡΛΖΔ…ζΆΏΫβ, ΝΉ÷§ΥΪ≤ψΡΛΆ®ΆΗ–‘‘ωΦ”, ΧΫ’κΩ…Υ≥άϊΒΫ¥οΒγΦΪ±μΟφ, ¥”Εχ≤ζ…ζΫœ«ΩΒΡ―≠ΜΖΖϋΑ≤ΒγΝς, Ω…Ά®ΙΐΒγΝςΒΡ±δΜ·ά¥ΤάΦέΕύκΡ”κΝΉ÷§ΒΡΉς”Ο≥ΧΕ». ΆΦ 3(A)ΈΣΧΫ’κ K3Fe(CN)6/ K4Fe(CN)6‘Ύ¬ψΒγΦΪΦΑ DMPC –ό ΈΒγΦΪ…œΒΡ―≠ΜΖΖϋΑ≤«ζœΏ. ΧΫ’κ‘Ύ¬ψ≤ΘΧΦΒγΦΪ…œΒΡΒγΝςœλ”ΠΫœΗΏ. Β±ΒγΦΪ±μΟφ–ό Έ”– DMPC ΥΪ≤ψΡΛ ±, ―≠ΜΖΖϋΑ≤ΒγΝςΦ±ΨγΫΒΒΆ, ΥΒΟςΒγΦΪ±μΟφ–ό Έ”–ΝΉ÷§ΥΪ≤ψΡΛ, ΉηΑ≠ΝΥΒγΉ”ΒΡΉΣ“Τ.ΫΪΗΟ DMPC –ό ΈΒγΦΪΫΰ»κΒΫΕύκΡ»ή“Κ÷– 30 min Κσ, ÷Ο”ΎΒγΫβ“Κ÷–≤β ‘, ΖΔœ÷ΧΫ’κΒΡ―≠ΜΖΖϋΑ≤ΒγΝς÷Ί–¬…ΐΗΏ, ΥΒΟςΒγΦΪ±μΟφΒΡ DMPC ΥΪ≤ψΡΛ“―”–ΤΤΥπ, Μρ’Ώ–Έ≥…ΩΉΕ¥, Μρ’ΏΕύκΡ ΙΝΉ÷§ΡΛΖΔ…ζΆΏΫβ. Combi-1,l-Combi-1 ΚΆ lCombi-2 Ε‘ DMPC ΥΪ≤ψΡΛΒΡΤΤΜΒΉς”ΟΦϊΆΦ3(B). ΥφΉ≈ Combi-1 ΚΆ l-Combi-1 ≈®Ε»‘ωΦ”, ―≠ΜΖΖϋΑ≤ΒγΝς‘ω¥σ, ΥΒΟςΧαΗΏΕύκΡ≈®Ε»Ω…ΧαΗΏΕ‘ΝΉ÷§ΡΛΒΡΤΤΜΒΉς”Ο. l-Combi-2 ‘Ύ Β―ι≈®Ε»ΖΕΈßΡΎΕ‘DMPC ΒΡΤΤΜΒΉς”ΟΥφ≈®Ε»±δΜ·≤Μ¥σ. ΝΉ÷§θΘΒ®Φν «≤Η»ιΕ·ΈοœΗΑϊΡΛΒΡ÷Ί“ΣΉιΖ÷, ΕύκΡΕ‘ DMPC ΡΛΒΡΤΤΜΒ±μΟςΕύκΡΩ…ΡήΕ‘’ΐ≥Θ≤Η»ιΕ·ΈοœΗΑϊΡΛΨΏ”–“ΜΕ®ΒΡΤΤΜΒΉς”Ο. ΕύκΡ”κœΗΨζœΗΑϊΡΛΒΡ÷Ί“Σ≥…Ζ÷ DMPG ÷°ΦδΒΡœύΜΞΉς”ΟΦϊΆΦ 4. ”κ DMPC œύ±», ΕύκΡΕ‘ DMPG ΒΡΤΤΜΒΉς”ΟΟςœ‘ΫΒΒΆ(ΆΦ÷–―≠ΜΖΖϋΑ≤ΒγΝςΒΡ‘ω¥σ÷ς“Σά¥Ή‘”Ύ»ήΦΝΕ‘ DMPG ΒΡΤΤΜΒΉς”Ο). ‘Ύ Β―ι≈®Ε»ΖΕΈßΡΎ, ―≠ΜΖΖϋΑ≤ΒγΝςΜυ±Ψ…œΈß»ΤΝψΒψ≤®Ε·(Ωέ≥ΐ»ήΦΝΒΡ”ΑœλΚσ), ±μΟςΕύκΡ≤ΜΡή ΙœΗΨζœΗΑϊΡΛ≤ζ…ζΩΉΕ¥Μρ’ΏΆΏΫβ, ΕύκΡΒΡ…±ΨζΉς”Ο≤ΔΖ«‘¥”ΎΕ‘œΗΨζœΗΑϊΡΛΒΡΤΤΜΒΉς”Ο. Rezansoff Β»[16]±®Βά, Combi-1 ΚΆ Combi-2 ≤ΜΡή‘λ≥…Κ§ PG ΒΡ÷§÷ Χε≤ζ…ζΩΉΕ¥, ΒΪ»¥Ρή¥©ΆΗ¥σ≥ΠΗΥΨζΚΆΫπΜΤ…ΪΤœΧ―«ρΨζΒΡœΗΑϊΡΛ≤ΔΨέΦ·ΒΫœΗΑϊ÷ ÷–, ΆΤ≤βΗΟάύΕύκΡΒΡ…±ΨζΉς”Ο≤ΔΖ«ά¥Ή‘”ΎΕ‘œΗΨζœΗΑϊΡΛΒΡΤΤΜΒ, ΤδΉς”ΟΑ–ΒψΩ…ΡήΈΜ”ΎœΗΑϊΡΎ≤Ω, ¥ΥΫαΙϊΚΆ±ΨΈΡΥυΒΟΫαΙϊ“Μ÷¬.
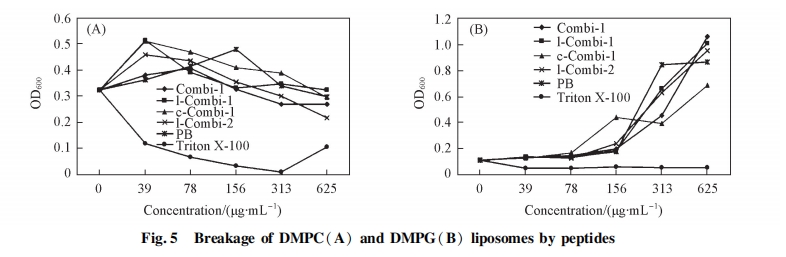
2. 4. 2 ΕύκΡ”κ÷§÷ ΧεΒΡœύΜΞΉς”Ο ÷§÷ Χε“≤ «“Μ÷÷≥ΘΦϊΒΡ…ζΈοΡΛΡΘ–Ά, Ω…”Ο”Ύ―–ΨΩ–ΓΖ÷Ή””κ…ζΈοΡΛΒΡœύΜΞΉς”Ο, ±ΨΈΡάϊ”Ο¥ΥΡΘ–ΆΩΦ≤λΝΥΕύκΡΕ‘…ζΈοΡΛΒΡΤΤΝ―Ής”Ο[22]. ΆΦ 5 œ‘ ΨΝΥΗςΕύκΡΕ‘ DMPC ΚΆDMPG ÷§÷ ΧεΒΡΤΤΝ―Ής”Ο. Combi-1, l-Combi-1, c-Combi-1, l-Combi-2 ΦΑ PB Μυ±Ψ≤Μ“ΐΤπ DMPC ÷§÷ ΧεΒΡΤΤΝ―, Εχ―τ–‘Ε‘’’ Triton X-100 Ω…“ΐΤπΟςœ‘ΒΡ÷§÷ ΧεΤΤΝ―, ΒΦ÷¬ΝΘΕ»±δ–Γ[ΆΦ 5(A)]. “ρ¥Υ, ΕύκΡ≤Δ≤ΜΡήΆ§±μΟφΜν–‘ΦΝ“Μ―υΫΪ DMPC ÷§÷ ΧεΤΤΝ―≥…ΥιΤ§, ¥ΥΫαΙϊ±μΟςΕύκΡ≤Δ≤ΜΡήΫΪœΗΑϊΡΛΤΤΝ―≥…ΥιΤ§, ΕχΩ…Ρή «Ά®Ιΐ–Έ≥…ΩΉΕ¥ ΙΡΛΆ®ΆΗ–‘‘ωΦ”. ΗςΕύκΡ“≤Ά§―υ≤ΜΡή“ΐΤπ DMPG ÷§÷ ΧεΒΡΤΤΝ―[ΆΦ 5(B)]. ÷ΒΒΟΉΔ“βΒΡ «, ΗςΕύκΡ‘Ύ≈®Ε»ΫœΗΏ ±Ψυ≤ΜΆ§≥ΧΕ»ΒΊ“ΐΤπΝΥ DMPG ÷§÷ ΧεΨέΦ·, ¥”Εχ Ι»ή“Κ÷–ΒΡΩ≈ΝΘ±δ¥σ.’βΩ…Ρή «¥χ’ΐΒγΒΡΕύκΡΚΆ¥χΗΚΒγΒΡ DMPG ÷§÷ Χε÷°Φδ«ΩΝ“ΒΡΨ≤ΒγΉς”ΟΥυ÷¬, ¥Υœ÷œσ”κΈΡœΉ[14]ΙΊ”ΎV4 ΒΡ±®Βά“Μ÷¬, Κ…’ΐΒγΒΡ V4 “≤Ω…“ΐΤπ DMPG ÷§÷ ΧεΨέΦ·ΓΘ
2. 5 ΡΘΡβΦΤΥψ
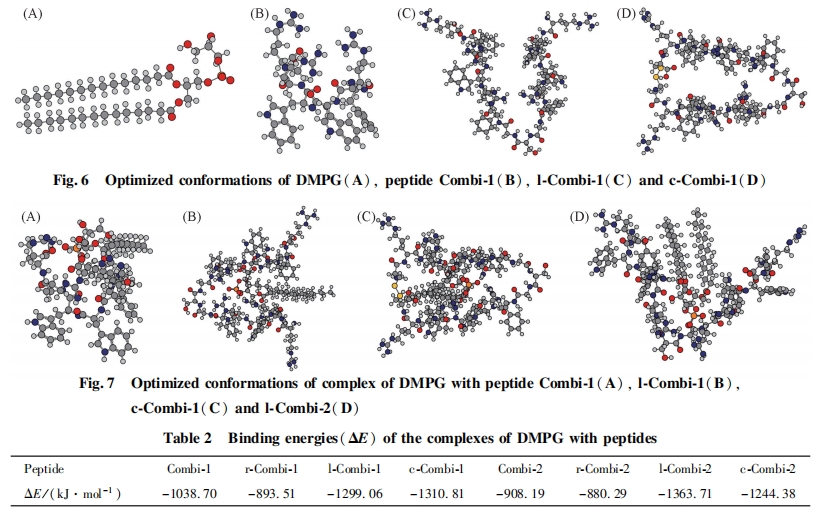
Combi-1, l-Combi-1 ΚΆ l-Combi-2 Υδ≤ΜΡή÷±Ϋ”ΤΤΜΒœΗΨζœΗΑϊΡΛΕχ…±Ψζ, ΒΪ»¥Ω…”κœΗΨζœΗΑϊΡΛΖΔ…ζœύΜΞΉς”Ο, ¥”Εχ¥©ΆΗœΗΑϊΡΛΫχ»κœΗΑϊ÷ . “ρ¥Υ, ±ΨΈΡ―–ΨΩΝΥΕύκΡ”κœΗΨζœΗΑϊΡΛ÷–÷Ί“ΣΒΡΉιΖ÷ DMPG ΒΡœύΜΞΉς”Ο“‘ΧΫΨΩ…±ΨζΜν–‘ΚΆΕύκΡ-ΝΉ÷§œύΜΞΉς”ΟΒΡΙΊœΒ. l-Combi-1 ΚΆ l-Combi-2 Ε‘ΗοάΦ œ“θ–‘ΨζΚΆ―τ–‘ΨζΨυ±μœ÷≥ωΫœΚΟΒΡ…±ΨζΜν–‘. ’β 2 ΧθΕύκΡΨυΚ§”–ΥΪΜν–‘–ρΝ–, « 2 ΧθΨΏ”–ΒΞΜν–‘–ρΝ–ΒΡΕύκΡΆ®ΙΐΦρΒΞΒΡΑ±ΜυΥα≤–ΜυœύΝ§Εχ–Έ≥…, ΒΪ±»œύ”ΠΒΡΕΧΝ¥κΡ±μœ÷≥ωœ‘÷χΧαΗΏΒΡ…±ΨζΜν–‘. ±ΨΈΡ≤…”ΟΦΤΥψΡΘΡβΒΡΖΫΖ®ΦΤΥψΕύκΡ”κ DMPG œύΜΞΉς”Ο ±ΒΡΫαΚœΡήά¥ΤάΦέΕύκΡΚΆœΗΨζœΗΑϊΡΛΒΡΫαΚœ≥ΧΕ». ≤…”Ο Gaussian 09 ÷–ΒΡ PM3ΑκΨ≠―ιΥψΖ®”≈Μ· DMPG ΦΑΗςΕύκΡΒΡΖ÷Ή”ΙΙ–Ά. ≤Έ’’ΈΡœΉ[16,17]Ε‘ Combi-1 ΚΆ Combi-2 ΫαΙΙΒΡ±®Βά, ‘Ύ”≈Μ·Ιΐ≥Χ÷–ΫΪΕύκΡ”κ DMPG Ζ÷Ή”ΒΡΙ«Φή≤ΩΖ÷Ϋχ––ΙΧΕ®“‘ΥθΕΧ”≈Μ· ±Φδ, ΫαΙϊ»γΆΦ 6 Υυ Ψ. ΗυΨίΗςΕύκΡΚΆ DMPG ΒΡΙΙ–Ά”≈Μ·ΒΡΫαΙϊ, ΙΙΫ®ΕύκΡΚΆ DMPG –Έ≥…ΒΡΗ¥ΚœΈο, ≤ΔΕ‘Η¥ΚœΈοΫχ“Μ≤Ϋ”≈Μ·, Η¥ΚœΈοΒΡΙΙ–ΆΦϊΆΦ 7. ΦΤΥψ ±÷ς“ΣΩΦ¬«ΕύκΡΚΆ DMPG Ζ÷Ή”ΒΡΨ≤ΒγΚΆ«βΦϋΫαΚœ, ≤ΔΆ§ ±ΩΦ¬«ΨΓΩ…ΡήΕύΒΡΫαΚœΡΘ Ϋ.“‘ΫαΚœΡήΉνΒΆΈΣ‘≠‘ρ, ΗυΨί Ϋ(1)ΦΤΥψ≥ωΗςΕύκΡ”κ DMPG –Έ≥…ΒΡΗ¥ΚœΈοΚΆΒΞΧε÷°ΦδΒΡΡήΝΩ≤νΒΟΫαΚœΡή, ΐΨίΝ–”Ύ±μ 2[23]. ±μ 2 œ‘ ΨΥυ”–ΕύκΡ”κ DMPG Ζ÷Ή”ΫαΚœΙΐ≥Χ÷–ΒΡΡήΝΩ≤νΨυΈΣΗΚ÷Β, ΥΒΟςΕύκΡ”κDMPG ΒΡœύΜΞΉς”ΟΈΣ ΆΡήΙΐ≥Χ, ΡήΝΩ≤νΒΡΨχΕ‘÷Β‘Ϋ¥σΥΒΟςΕΰ’ΏΫαΚœΒΡΫαΚœΡή‘Ϋ¥σ. œΏ–‘κΡΚΆΜΖΉ¥κΡ‘Ύ”κ DMPG Ζ÷Ή”ΫαΚœ ±±»ΕΧΝ¥κΡΨΏ”–Ηϋ¥σΒΡΫαΚœΡή, ΥΒΟςΗΟάύΕύκΡΗϋ“Ή”κ DMPG Ζ÷Ή”ΖΔ…ζœύΜΞΉς”Ο, ΫχΕχ≤ζ…ζ…±Ψζ–ßΙϊ. DMPG Ζ÷Ή”ΆΖΜυΚ…ΗΚΒγ, “Ή”Ύ”κ¥χ’ΐΒγΒΡΑ±ΜυΥα≤ζ…ζΨ≤ΒγΉς”Ο. ”…ΆΦ 7 Ω…Φϊ, DMPGΒΡΗΚΒγΆΖΜυ‘Ύ”κœΏ–‘κΡΚΆΜΖΉ¥κΡΫαΚœΒΡΙΐ≥Χ÷–, Ω…Ά§ ±”κ 3 Ηω¥χ’ΐΒγΒΡΨΪΑ±Υα≤ζ…ζΨ≤ΒγΉς”Ο, Εχ‘Ύ”κΕΧΝ¥κΡΒΡΫαΚœΙΐ≥Χ÷–÷ΜΡή”κ 2 Ηω¥χ’ΐΒγΒΡΨΪΑ±Υα≤ζ…ζΨ≤ΒγΉς”Ο. ’β «‘λ≥…ΕΧΝ¥κΡΒΡΫαΚœΡή–Γ”ΎœΏ–‘κΡΚΆΜΖΉ¥κΡΒΡ÷ς“Σ‘≠“ρ. ¥ΥΫαΙϊΚΆ Β―ιΥυΒΟ…±ΨζΜν–‘ ΐΨίΜυ±Ψ“Μ÷¬, Φ¥ΨΏ”– 2 ΗωΜν–‘–ρΝ–ΒΡœΏ–‘κΡΚΆΜΖΉ¥κΡ±»ΨΏ”–ΒΞΗωΜν–‘–ρΝ–ΒΡΕΧΝ¥κΡ…±ΨζΜν–‘Ηϋ«Ω. Combi-1 Υδ»ΜΈΣΕΧΝ¥κΡ, ΒΪ”…”ΎΤδΙΙ–ΆΒΡ”Αœλ, ΒΎ 3ΗωΨΪΑ±ΥαΨύΚ…ΗΚΒγΒΡ DMPG Ζ÷Ή”ΆΖΜυœύΕ‘ΫœΫϋ, “ρ¥ΥΫαΚœΡή±»ΤδΥϋΕΧΝ¥κΡΗΏ, …±ΨζΜν–‘“≤Οςœ‘”≈”ΎΤδΥϋΕΧΝ¥κΡ. œΏ–‘κΡΚΆΜΖΉ¥κΡ”κ DMPG Ζ÷Ή”ΒΡΫαΚœΡήœύΫϋ. c-Combi-1 ΚΆ c-Combi-2 ΜΖΉ¥κΡΒΡκΡΝ¥Ϋœ≥Λ,Υυ–Έ≥…ΒΡκΡΜΖΉψΙΜ¥σ, “ρ¥ΥΝΉ÷§Ζ÷Ή”Ω…“‘Άξ»Ϊ≤ε»κκΡΜΖ÷–≤Δ”κ 3 ΗωΨΪΑ±Υα≤ζ…ζΨ≤ΒγΉς”Ο, ΤδΉς”ΟΡΘ Ϋ”κœΏ–‘κΡάύΥΤ, “ρ¥ΥΜΖΉ¥κΡΒΡΜν–‘”κœΏ–‘κΡœύΥΤ.
3 Ϋα ¬έ
…ηΦΤΚœ≥…ΝΥΨΏ”– 2 ΗωΜν–‘–ρΝ–ΒΡœΏ–‘ΚΆΜΖΉ¥ΕύκΡΦΑΨΏ”–ΒΞΗωΜν–‘–ρΝ–ΒΡΕΧΝ¥ΕύκΡ, ―–ΨΩΝΥΥϋΟ«ΒΡ…±ΨζΜν–‘ΓΔ Ε‘’ΐ≥Θ≤Η»ιΕ·ΈοœΗΑϊΒΡΕΨ–‘ΚΆ»ή―Σ–‘ΦΑ”κΝΉ÷§÷°ΦδΒΡœύΜΞΉς”Ο, ≤Δ≤…”ΟΦΤΥψΡΘΡβΒΡΖΫΖ®ΦΤΥψΝΥΕύκΡ”κœΗΨζœΗΑϊΡΛ÷–÷Ί“Σ≥…Ζ÷ΝΉ÷§θΘΗ ”Ά(DMPG)ΒΡΫαΚœΡή, ¥”άμ¬έ…œΫβ ΆΝΥΤδΜν–‘. ΫαΙϊ±μΟς,Κ§ 2 ΗωΜν–‘–ρΝ–ΒΡœΏ–‘ΚΆΜΖΉ¥ΕύκΡ±»Κ§ΒΞΗωΜν–‘–ρΝ–ΒΡΕΧΝ¥κΡΨΏ”–ΫœΗΏΒΡ…±ΨζΜν–‘, Μν–‘ΧαΗΏΖυΕ» ”≤ΜΆ§ΒΡ–ρΝ–Εχ“λ. Ψ≠ΙΐΦΤΥψΡΘΡβ, ΕύκΡΒΡ…±ΨζΜν–‘”κΕύκΡ-ΝΉ÷§ΒΡΫαΚœΡήœ‘ Ψ≥ωΫœΗΏΒΡœύΙΊ–‘. œΏ–‘κΡΚΆΜΖΉ¥κΡ”κ DMPG ΒΡΫαΚœΡήΗΏ”ΎΕΧΝ¥κΡ. ΦΤΥψΡΘΡβΒΡΖΫΖ®ΈΣ―–ΨΩΩΙΨζκΡΒΡ…±ΨζΜν–‘¥”άμ¬έ…œΧαΙ©ΝΥ“ΜΕ®ΒΡ“άΨί. œΏ–‘ΕύκΡΨΏ”–ΫœΗΏΒΡ…±ΨζΜν–‘, …ζ≤ζ≥…±ΨΫœΒΆ, «“Ε‘’ΐ≥Θ≤Η»ιΕ·ΈοœΗΑϊΒΡΕΨ–‘ΚΆ»ή―Σ–‘ΨυΫœΒΆ, “ρ¥ΥΨΏ”–Ϋχ“Μ≤ΫΒΡ―–ΨΩΦέ÷ΒΚΆ«±‘ΎΒΡ”Π”ΟΦέ÷Β. ≤…”ΟΙΧΧε÷ß≥≈ΒΡΝΉ÷§ΥΪ≤ψΡΛΦΑ÷§÷ ΧεΡΘΡβ…ζΈοΡΛ, Ε‘ΕύκΡΒΡΉς”ΟΜζάμΫχ––ΝΥ≥θ≤Ϋ―–ΨΩ. ΫαΙϊ±μΟς, ΕύκΡ Combi-1, l-Combi-1 ΚΆ l-Combi-2 Ω…“‘ ΙDMPC ΡΛ≤ζ…ζΩΉΕ¥Εχ ΙœΗΑϊΡΛΆ®ΆΗ–‘‘ωΦ”. ΕχΕ‘”Ύ DMPG ΡΛ, ΕύκΡ≤ΔΈ¥‘Ύ DMPG ΡΛ…œ≤ζ…ζΟςœ‘ΩΉΕ¥,Εχ «“ΐΤπΝΥΝΉ÷§ΒΡΨέΦ·, “ρ¥ΥœΗΨζœΗΑϊΡΛΩ…Ρή≤Μ «ΗΟάύΕύκΡ…±ΨζΒΡ÷ς“ΣΉς”ΟΑ–Βψ.
Οβ‘π…υΟςΘΚ±ΨΈΡΈΣ––“ΒΫΜΝς―ßœΑΘ§Αφ»®Ιι‘≠Ής’ΏΦΑ‘≠‘”÷ΨΥυ”–Θ§»γ”–«÷»®Θ§Ω…ΝΣœΒ…Ψ≥ΐΓΘΈΡ’¬±ξΉΔ”–Ής’ΏΦΑΈΡ’¬≥ω¥ΠΘ§»γ–η‘ΡΕΝ‘≠ΈΡΦΑ≤ΈΩΦΈΡœΉΘ§Ω…‘ΡΕΝ‘≠‘”÷ΨΓΘ








