
’Σ “Σ: œΗΑϊ¥©ΆΗΜΖκΡΡήΙΜ¥©ΆΗœΗΑϊΡΛΘ§ΧΊ“λ–‘ΒΊΑ–œρœΗΑϊΡΎΑ–±ξΘ§≤ΔΨΏ”–ΫœΚΟΒΡΧεΡΎΈ»Ε®–‘Θ§“ρΕχΨΏ±ΗΚήΚΟΒΡ≥…“©–‘Θ§≤Δ ήΒΫ―–ΨΩ’Ώ‘Ϋά¥‘ΫΕύΒΡΙΊΉΔΓΘΡΩ«ΑΘ§÷ς“Σ”–ΝΫ÷÷ΖΫ ΫΜώΒΟœΗΑϊ¥©ΆΗΜΖκΡΘ§Φ¥¥”Χλ»Μ≤ζΈο÷–ΜώΒΟΚΆΕ‘“―”–ΒΡΜΖκΡΜρœΏ–‘κΡΫχ––Μ·―ß–ό ΈΓΘ±ΨΈΡ÷ς“ΣΕ‘…œ ωΝΫΖΫΟφΫχ––Φρ“ΣΉέ ωΘ§÷ΊΒψΫι…ήΝΫάύœΗΑϊ¥©ΆΗΜΖκΡΧλ»Μ≤ζΈο“‘ΦΑΆ®ΙΐΜ·―ß–ό ΈΖΫΖ®ΒΟΒΫœΗΑϊ¥©ΆΗΜΖκΡΒΡ≤Ώ¬‘Θ§≤ΔΧΫΧ÷œΗΑϊ¥©ΆΗΜΖκΡΒΡΫαΙΙ-Μν–‘ΙΊœΒΦΑΤδœΗΑϊ¥©ΆΗΜζάμΓΘ
ΕύκΡάύ“©Έο «–¬–ΥΒΡ…ζΈο“©Έο―–ΖΔ»»Ο≈Νλ”ρΘ§»Ϊ άΫγ“―Ψ≠Μώ≈ζ…œ –ΒΡΕύκΡάύ“©Έο≥§Ιΐ 50 ΗωΓΘ”κ–ΓΖ÷Ή”“©Έο±»ΫœΘέ1Θ§2ΘίΘ§ΕύκΡάύ“©ΈοΨΏ”–ΫαΚœΟφΗϋ¥σΓΔΉς”ΟΑ–œρ–‘Ηϋ«ΩΓΔΗϋΑ≤»ΪΓΔΗ±Ής”ΟΗϋ–ΓΓΔΚή…Ό“ΐΤπ―œ÷ΊΒΡΟβ“ΏΖ¥”ΠΒ»”≈ΒψΘέ3Θ§4ΘίΘ§“―Ψ≠ΙψΖΚ”Π”Ο”ΎΑ©÷ΔΓΔ–Ρ―ΣΙή≤ΓΓΔ¥ζ–ΜάύΚΆ¥Ϊ»Ψ–‘≤ΓΒ»ΗςάύΦ≤≤ΓΒΡ÷ΈΝΤΓΘ
ΒΪ «Θ§≥ΘΦϊΒΡΕύκΡΖ÷Ή”¥φ‘ΎΈόΖ®Ωγ‘ΫœΗΑϊΡΛΘ§ΟΗΫβΈ»Ε®–‘≤νΚΆΩΎΖΰ…ζΈοάϊ”ΟΕ»ΒΆΒ»Έ ΧβΘέ5ΘίΘ§ΒΦ÷¬¥σΕύ ΐΨΏ”–÷ΈΝΤΉς”ΟΒΡΕύκΡ“©ΈοΚήΡ―Ϋχ»κœΗΑϊΡΎΖΔΜ”“©–ßΘ§«“»ί“Ή‘ΎΧεΡΎΫΒΫβΘέ6ΘίΘ§“ρ¥ΥΘ§ΕύκΡ“©Έο‘Ύ ΒΦ ”Π”Ο÷– ήΒΫΝΥΦΪ¥σΒΡœό÷ΤΓΘΈΣΝΥΩΥΖΰΕύκΡ“©Έο¥φ‘ΎΒΡΈ ΧβΘ§»ΥΟ«ΖΔœ÷≤ΔΖΔ’ΙΝΥ“ΜάύœΗΑϊ¥©ΆΗΜΖκΡΖ÷Ή”Θ§ΥϋΟ«ΨΏ”–¥©ΙΐœΗΑϊΡΛΒΡΡήΝΠΘ§≤ΔΡήΧΊ“λ–‘ΒΊΑ–œρœΗΑϊΡΎΑ–±ξΘ§ΧεΡΎΈ»Ε®–‘ΗΏΘ§ΩΎΖΰ…ζΈοάϊ”ΟΕ»ΚΟΘ§ΗϋΨΏ≥…“©«ΑΨΑΓΘΝμ“ΜΖΫΟφΘ§ΒΑΑΉΜ·―ßΚœ≥…Νλ”ρ»ΓΒΟΒΡ“ΜœΒΝ–÷Ί“ΣΫχ’ΙΘέ7 ΓΪ 15ΘίΘ§¥ΌΫχ―–ΨΩ’ΏΖΔ’ΙΝΥ“ΜœΒΝ–Μ·―ßΚœ≥…ΜΖκΡΒΡΖΫΖ®Θέ16 ΓΪ 20ΘίΘ§ΈΣ―–ΨΩΚΆΗΡ‘λΜΖκΡ¥”ΕχΒΟΒΫœΗΑϊ¥©ΆΗΜΖκΡΒλΕ®ΝΥΦΦ θΜυ¥ΓΘ§”––ßΫβΨωΝΥœΗΑϊ¥©ΆΗΜΖκΡΖ÷Ή”ΒΡΜώ»ΓΈ ΧβΓΘ
±ΨΈΡ÷ΊΒψΫι…ήΡΩ«Α“―Ψ≠ΖΔœ÷ΒΡœΗΑϊ¥©ΆΗΜΖκΡΦΑΤδΆΗΡΛΜζάμΘ§Ά§ ±“≤Φρ ωΗς÷÷ΜώΒΟœΗΑϊ¥©ΆΗΜΖκΡΒΡΜ·―ß–ό Έ≤Ώ¬‘Θ§ΉνΚσΧ÷¬έΗΟΝλ”ρ¥φ‘ΎΒΡΈ ΧβΘ§≤Δ’ΙΆϊœΗΑϊ¥©ΆΗΜΖκΡΒΡ”Π”Ο«ΑΨΑΓΘ
2 Χλ»Μ≤ζΈο÷–ΒΡœΗΑϊ¥©ΆΗΜΖκΡ
ΜΖκΡ «Ή‘»ΜΫγ÷–“ΜάύΙψΖΚ¥φ‘ΎΒΡΧλ»Μ≤ζΈοΘ§Ω…“‘Ά®ΙΐΚΥΧ«ΧεΜρΖ«ΚΥΧ«ΧεΆΨΨΕΚœ≥…Θ§ΨΏ”–ΩΙΨζΓΔ’ρΆ¥ΓΔΩΙ÷ΉΝωΓΔΩΙΟβ“ΏΒ»…ζάμΉς”ΟΓΘΤδ÷–Θ§Ρ≥–©ΜΖκΡΨΏ”–¥©ΆΗœΗΑϊΡΛΒΡΡήΝΠΘ§Φ¥±ΨΈΡΥυ ωΒΡœΗΑϊ¥©ΆΗΜΖκΡΜΖφΏΥΊ( cyclosporine A)ΚΆ÷≤ΈοΜΖκΡ( cyclotides)ΓΘ
2. 1 ΜΖφΏΥΊΦΑΆΗΡΛΜζάμ
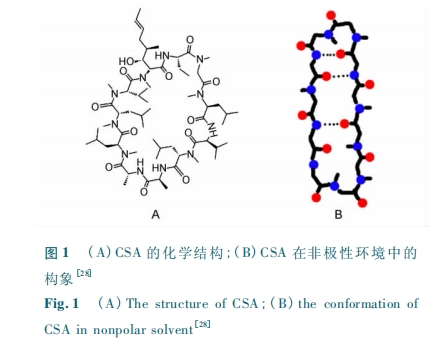
ΜΖ °“ΜκΡ cyclosporine A(CSA)ΜΖκΡ «“Μ÷÷”Ο”Ύ“Τ÷≤ ÷ θΚσΒΡΩΙΟβ“Ώ÷ΈΝΤ“©ΈοΓΘCSA ”Ύ 1969 Ρξ‘Ύ’φΨζ Tolypocladium inflatum ÷–±ΜΖΔœ÷Θ§Ά®ΙΐΖ«ΚΥΧ«ΧεΆΨΨΕΚœ≥…Θέ21ΘίΘ§Κ§”–“ΜΗω D –Ά±ϊΑ±ΥαΚΆ“ΜΗωΖ«Χλ»ΜΑ±ΜυΥαΘ§≤Δ«“‘ΎΕύκΡΙ«Φή…œΚ§”– 7 Ηω N-ΦΉΜυΜ·ΒΡΑ±ΜυΥα≤–Μυ( ΆΦ 1A)ΓΘCSA Ω…“‘¥©ΆΗΝήΑΆœΗΑϊΡΛΘ§”κΝήΑΆœΗΑϊΡΎΒΡ«ΉΜΖΥΊ( cyclophilin) ΫαΚœΘέ22ΘίΘ§Ά®Ιΐ“÷÷ΤΗΤΒςΝΉΥαΟΗ( calcineurin) ΒΡΜν–‘Θ§ ΙΝήΑΆœΗΑϊΒΡΑΉœΗΑϊΫιΥΊ 2 ( IL-2) Ζ÷ΟΎΝΩΦθ…ΌΘ§¥”Εχ“÷÷Τ T œΗΑϊΒΡΦΛΜνΘ§ΤπΒΫ“÷÷ΤΟβ“ΏΒΡΉς”ΟΓΘ―–ΨΩ’ΏΫβΈωΝΥ CSAΒΡΨßΧεΫαΙΙΘέ23Θ§24ΘίΘ§≤Δ”ΟΕΰΈ§ ΚΥ ¥≈ Ι≤ ’ώ ―– ΨΩ ΝΥ CSA‘ΎΦΪ–‘ΚΆΖ«ΦΪ–‘»ήΦΝΜΖΨ≥œ¬ΒΡΕ·Χ§ΫαΙΙΘέ24 ΓΪ 27Θί ( ΆΦ1B)ΓΘ Β―ι±μΟςΘ§CSA ‘ΎΖ«ΦΪ–‘»ήΦΝΚΆΨßΧεΫαΙΙ÷––Έ≥…»ΐΕ‘Ζ÷Ή”ΡΎ«βΦϋΘ§Ά§ ±Θ§”…”Ύ”– 7 ΗωΜΖκΡΙ«Φή…œΒΡ N ΦΉΜυΜ·Θ§Υυ“‘‘Ύ’β÷÷ΙΙœσœ¬ CSA ΒΡΥυ”–«βΦϋΗχΧεΕΦ±ΜΥχΕ®Μρ―Ύ±ΈΘ§”–άϊ”ΎΤδ‘ΎΖ«ΦΪ–‘ΜΖΨ≥œ¬ΒΡ»ήΫβΘ§ΫΒΒΆΤδ‘ΎœΗΑϊΡΛ÷–ΒΡΦΣ≤ΦΥΙΉ‘”…ΡήΓΘ
2. 2 ÷≤ΈοΜΖκΡΦΑΆΗΡΛΜζάμ
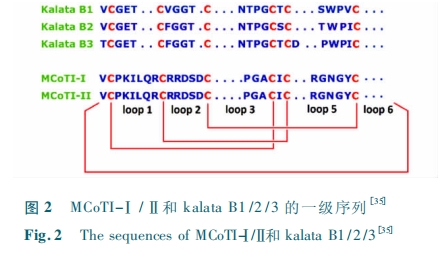
÷≤ΈοΜΖκΡ“≤ «“ΜάύΨΏ”–÷Ί“Σ“©ΈοΦέ÷ΒΒΡΜΖκΡΖ÷Ή”ΓΘ÷≤ΈοΜΖκΡΆ®ΙΐΚΥΧ«ΧεΆΨΨΕΚœ≥…Θ§Α±ΜυΥα≤–Μυ ΐ“ΜΑψ‘Ύ 28 ΓΪ 37Θ§ «ά¥‘¥”Ύ÷≤ΈοΒΡΧλ»Μ≤ζΈοΘέ35ΘίΓΘΡΩ«Α“―Ψ≠ΖΔœ÷÷≤ΈοΜΖκΡΨΏ”–ΚήΕύ…ζΈοΜν–‘Θ§±»»γΩΙœΗΨζΓΔΩΙ≥φΓΔΩΙ≤ΓΕΨΓΔΒΑΑΉΟΗ“÷÷ΤΦΝΒ»Θέ29 ΓΪ 31ΘίΓΘ÷≤ΈοΜΖκΡ÷ς“ΣΖ÷ΈΣΝΫάύ: ΓΑΡΣ±»ΈΎΥΙ–ΆΓ±( the MΔâbius cyclotides)ΚΆΓΑ ÷ομ–ΆΓ±( the bracelet cyclotides)ΓΘΜΙ¥φ‘ΎΟϊΈΣ“»ΒΑΑΉΟΗ“÷÷ΤΦΝΒΡΒΎ 3 ―«άύΘ§’βάύ÷≤ΈοΜΖκΡΫωΑϋά®MCoTI-ΔώΚΆ MCoTI-Δρ ΝΫΗωΜΖκΡΓΘ≤ΜΆ§άύ–ΆΒΡ÷≤ΈοΜΖκΡΕΦΨΏ”–άύΥΤΒΡΫαΙΙ(ΆΦ 2)Θ§ΕύκΡΝ¥ N ΕΥΚΆ C ΕΥ”…θΘΑΖΦϋΜΖΚœΘ§6 ΗωΑκκΉΑ±Υα–Έ≥… 3 Ε‘ΕΰΝρΦϋΘ§Τδ÷– Ε‘ΕΰΝρΦϋ¥”ΝμΆβΝΫΕ‘ΒΡ÷–Φ䥩ΙΐΘ§–Έ≥…ΜΖκΉΑ±ΥαΫΎ( cyclic cystine knotΘ§CCK) ΒΡΫα ΙΙΓΘΧΊ β ΒΡ CCKΫαΙΙ ΙΒΟ÷≤ΈοΜΖκΡΒΡ»»Έ»Ε®–‘ΓΔΜ·―ßΈ»Ε®–‘ΚΆΟΗΈ»Ε®–‘ΚήΗΏΘ§Φ¥±ψΨ≠Ιΐ÷σΖ–“≤»‘»ΜΨΏ±ΗΚήΗΏΒΡ…ζΈοΜν–‘Θέ32ΘίΓΘ÷≤ΈοΜΖκΡΑϋΚ§ 6 ΗωΜΖ”ρ( loop)Θ§Τδ÷–Ρ≥–©ΜΖ”ρ «Ω…±δΒΡΘ§Ι ΕχΩ…“‘‘Ύ÷≤ΈοΜΖκΡ…œΦόΫ”ΨΏ”–…ζάμΜν–‘ΒΡΕύκΡΤ§ΕΈΘ§άϊ”Ο÷≤ΈοΜΖκΡ‘ΎΧεΡΎΒΡΈ»Ε®–‘ΚΆΫœΚΟΒΡ…ζΈοάϊ”ΟΕ»Θ§ΧαΗΏΕύκΡΤ§ΕΈ‘ΎΧεΡΎΒΡΈ»Ε®–‘ΚΆ¥φΝτ ±ΦδΘέ33ΘίΓΘ
Craik Β» Ή¥Έ±®ΒάΝΥΩ…“‘¥©ΙΐœΗΑϊΡΛΒΡ÷≤ΈοΜΖκΡ MCoTI-ΔρΘ§ Τδ Ω… “‘ Ά® Ιΐ ¥σ Αϊ “ϊ Ής ”Ο(macropinocytosis) ±Μ œΗ Αϊ …ψ »ΓΘέ34ΘίΓΘ¥Υ ΚσΘ§CamareroΒ»‘ΎΜνœΗΑϊΥ°ΤΫ…œ÷Λ ΒΝΥ MCoTI-Δώ“≤Ω…“‘¥©ΙΐœΗΑϊΡΛΘέ35ΘίΓΘ≥ΐ MCoTI-ΔρΓΔMCoTI-ΔώΆβΘ§Craik Β»ΖΔœ÷÷≤ΈοΜΖκΡ kalata B1 ΚΆ Νμ “Μ ÷÷ ¥φ ‘Ύ ”Ύ ÷≤ Έο ÷– ΒΡ ΜΖ κΡSTFI-1 ΕΦΩ…“‘¥©ΙΐœΗΑϊΡΛΘέ36ΘίΓΘ
―–ΨΩ±μΟςΘ§œ÷“―ΖΔœ÷ΒΡ÷≤ΈοΜΖκΡά¥‘¥ΒΡ 4 ΗωœΗΑϊ¥©ΆΗΜΖκΡΒΡΩγΡΛΜζάμΗς≤ΜœύΆ§ΓΘMCoTI-ΔρΆ®ΙΐœΗΑϊ÷ςΕ·…ψ»ΓΒΡΖΫ ΫΫχ»κœΗΑϊΓΘ”ΪΙβ≥…œώΗζΉΌΦΦ θ±μΟςΘ§MCoTI-Δρ≥ωœ÷‘ΎΆΧ …–ΓΧε÷–Θ§≤Δ«“œΗΑϊ…ψ»ΓΙΐ≥ΧΕ‘Έ¬Ε»ΟτΗ–Θ§ΥΒΟς MCoTI-Δρ ΒΡΩγΡΛΙΐ ≥Χ « ÷ς Ε· Ιΐ≥ΧΘ§–η“ΣœϊΚΡΡήΝΩΘέ36ΘίΓΘMCoTI-ΔώΒΡΩγΡΛΜζάμ‘ρΫœΈΣΗ¥‘”Θ§ «ΝςΧεœύΡΎΆΧΉς”Ο( fluid-phase endocytosis)ΓΔ“άάΒ÷§÷ ΒΡΡΎΆΧΉς”ΟΚΆΆχΗώΒΑΑΉΫιΒΦΒΡΡΎΆΧΉς”ΟΒ»Ι≤Ά§Ής”ΟΒΡΫαΙϊΘέ35ΘίΓΘΕχ÷≤ΈοΜΖκΡ kalata B1 ”–œΗΑϊΕΨ–‘Θ§≥§Ιΐ“ΜΕ®≈®Ε» ±ΜαΒΦ÷¬œΗΑϊΡΛΤΤΝ―Θ§“ΐΤπœΗΑϊΥά ΆωΓΘ Β ―ι ΖΔ œ÷Θ§kalata B1 ΚΆ ΝΉ ÷§ θΘ ““ ¥Φ ΑΖ( POPE ) ”– œύ ΜΞ Ής ”ΟΘ§Ω… “‘ “ΐ Τπ POPE Άβ Ζ≠( transbilayer movement)Θ§¥”ΕχΒΦ÷¬œΗΑϊΡΛΝΫ≤ύΒΡ≤ΜΕ‘≥ΤΓΘCraik Β»≤¬≤β kalata B1 Ά®Ιΐ”κœΗΑϊΡΛΒΡœύΜΞΉς”ΟΘ§ΗΡ±δœΗΑϊΡΛΒΡ«ζ¬ Θ§¥”Εχ“ΐΤπœΗΑϊΒΡΡΎΆΧΉς”ΟΘέ36ΘίΓΘΝμ“ΜΖΫΟφΘ§kalata B1 ”κœΗΑϊΡΛΒΡ«ΉΚΆ–‘”κ÷§ΖΛœύΙΊΘ§¥χΗΚΒγΒΡΒ®Φν≤Δ≤Μ «œΗΑϊΡΛ”κ kalata B1 ΖΔ…ζ«ΩœύΜΞΉς”ΟΒΡ‘≠“ρΘέ37ΘίΓΘ
÷≤ΈοΜΖκΡœΗΑϊ¥©ΆΗΙΐ≥ΧΒΡ―–ΨΩΜΙ¥Π”ΎΫœ≥θΦΕΒΡΫΉΕΈΓΘ“ΜΖΫΟφΘ§ΤδΫαΙΙ‘ΎΩγΡΛΙΐ≥Χ÷–ΒΡΉς”ΟΜΙ≤ΜΙΜΟς»ΖΓΘ‘Ύ―–ΨΩ÷≤ΈοΜΖκΡΒΡΩγΡΛΙΐ≥Χ ±Θ§ Β―ιΧθΦΰΒΡ≤ν“λΜαΒΦ÷¬≤ΜΆ§ΒΡ Β―ιΫαΙϊΓΘ±»»γ Β―ι÷–―Γ‘ώΒΡœΗΑϊœΒΕ‘ΡΎΆΧΖΫ ΫΒΡΤΪΚΟ≥ΧΕ»≤ΜΆ§ΓΔΥυ”Ο÷≤ΈοΜΖκΡΒΡ≈®Ε»≤ΜΆ§Β»Θ§ΕΦΜαΕ‘ΫαΙϊ≤ζ…ζ”ΑœλΓΘΆ§ ±Θ§Β±«Α÷ΜΡήΆ®ΙΐΗΡ±δ≤–ΜυΒΡΖΫ Ϋά¥ΧΫΨΩΗςΗωΈΜΒψΕ‘’ϊΗωΩγΡΛΙΐ≥ΧΒΡΙ±œΉΘ§ΜΙΈόΖ® Β ±Φύ≤βΜΖκΡΒΡΙΙœσ±δΜ·Ε‘ΩγΡΛΙΐ≥ΧΒΡ”ΑœλΓΘΝμΆβΘ§Ε‘ΩγΡΛΙΐ≥Χ÷–ΒΡœΗΑϊΆΧ …––ΈΣΒΡάμΫβ °Ζ÷”–œόΓΘ≥ΐΕ‘ΆχΗώΒΑΑΉΫιΒΦΒΡΆΧ …Ής”ΟΚΆœΗΑϊΡΛΈ――υΡΎœί( caveolae) ΫιΒΦΒΡΆΧ …Ής”ΟάμΫβΫœΕύΆβΘ§…ζΈο―ßΦ“Ε‘ΤδΥϊάύ–ΆΒΡœΗΑϊΡΎΆΧ––ΈΣΒΡάμΫβ≤Δ≤Μ…ν»κΓΘ’β“≤ΉηΑ≠ΝΥ―–ΨΩ’ΏΕ‘÷≤ΈοΜΖκΡΩγΡΛΙΐ≥ΧΒΡΫχ“Μ≤ΫάμΫβΓΘ“ρ¥ΥΘ§ΖΔ’Ι–¬–ΆΦΦ θ―–ΨΩ÷≤ΈοΜΖκΡΩγΡΛΧΊ–‘ΒΡΫαΙΙ-Μν–‘ΙΊœΒ»‘ «“ΜΗω…–¥ΐΫβΨωΒΡΩΤ―ßΈ ΧβΓΘ
3 »ΥΙΛΗΡ‘λΒΡœΗΑϊ¥©ΆΗΜΖκΡ
œΗΑϊ¥©ΆΗΜΖκΡΨΏ”–ΚήΚΟΒΡ≥…“©«ΑΨΑΘ§’β¥Ό Ι―–ΨΩ’Ώάϊ”ΟΜ·―ßΚœ≥… ÷ΕΈΕ‘ΕύκΡΖ÷Ή”Ϋχ––ΗΡ‘λΘ§“‘ΤΎΜώΒΟΦφΨΏ«Ω…ζάμΜν–‘ΚΆΩγΡΛΡήΝΠΒΡΜΖκΡΖ÷Ή”Θ§…θ÷ΝΜΖκΡΩβΓΘœ¬ΟφΫΪ¥” CSA ΒΡΗΡ‘λΓΔ÷≤ΈοΜΖκΡΒΡΗΡ‘λΚΆœΏ–‘κΡΜΖΜ·Β»»ΐΖΫΟφ≤Ώ¬‘Ϋχ––Ϋι…ήΓΘ
3. 1 Μυ”Ύ CSA ΒΡΗΡ‘λ≤Ώ¬‘
Μυ”Ύ CSA ΒΡœΗΑϊ¥©ΆΗΜΖκΡΒΡ…ηΦΤΥΦ¬ΖΑϋά®ΒςΫΎΜΖκΡΒΡΙΙœσΚΆΕύκΡΙ«ΦήθΘΑΖ N-ΦΉΜυΜ·ΝΫΖΫΟφΓΘ
3. 1. 1 ΜΖκΡΙΙœσ”κΩγΡΛΡήΝΠ
ήΒΫ CSA ‘ΎΦΪ–‘ΚΆΖ«ΦΪ–‘»ήΦΝ÷–ΙΙœσ±δΜ·ΒΡΤτΖΔΘ§―–ΨΩ’ΏΩΣ ΦΙΊΉΔΕύκΡΙΙœσ”κΖ÷Ή”ΩγΡΛΡήΝΠ÷°ΦδΒΡ ΙΊ œΒΘέ38 ΓΪ 40ΘίΓΘLokey Β» œΒ Ά≥ ΒΊ ―– ΨΩ ΝΥ ΜΖ Νυ κΡLeu-Leu-Leu-Leu-Pro-Tyr ΒΡ≤ΜΆ§Ζ«Ε‘”≥“λΙΙΧεΒΡΙΙœσΚΆ Ωγ ΡΛ Ρή ΝΠ ÷° Φδ ΒΡ ΙΊ œΒΘέ41Θί ( ΆΦ 3 )ΓΘ Β ―ι Ι ”ΟCDCl3 ΡΘΡβœΗΑϊΡΛΜΖΨ≥ά¥―–ΨΩΜΖΝυκΡ‘ΎœΗΑϊΡΛ÷–ΒΡΕ·Χ§ΙΙ œσΓΘH /D ΫΜ ΜΜ Β ―ι ‘ρ ”Ο ”Ύ ―– ΨΩ θΘ ΑΖ Φϋ …œNΓΣH Φϋ ‘Ύ »ή ΦΝ ÷– ΒΡ ±© ¬Ε ≥Χ Ε»ΓΘ Β ―ι Ϋα Ιϊ ±μ ΟςΘ§NΓΣHΦϋΒΡ»ήΦΝΩ…ΦΑ–‘( solvent accessibility) ”κΜΖκΡΩγΡΛΡήΝΠΦδΨΏ”–œύΙΊ–‘Θ§»ήΦΝΩ…ΦΑ–‘ΫœΒΆΒΡΖ÷Ή”ΩγΡΛΡήΝΠΗϋ«ΩΓΘ
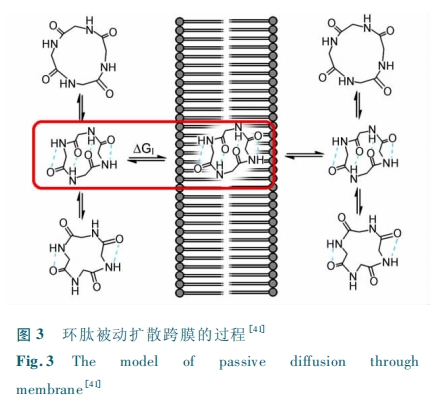
ΈΣΝΥΗϋΦ”Ε®ΝΩΒΊ―–ΨΩ≤Δ‘Λ≤βΜΖκΡ±ΜΕ·ά©…ΔΩγΡΛΒΡΡήΝΠΘ§Lokey ΚΆ Jacobson Β»Χα≥ωΝΥ“Μ÷÷–¬ΒΡ‘Λ≤βΖΫΖ®Θέ42ΘίΓΘΦΌ…ηΜΖκΡ‘ΎœΗΑϊΡΛ÷–ΒΡΙΙœσ(ΒΆΫιΒγΜΖΨ≥ΙΙœσ low-dielectric conformationΘ§LDC) ÷Μ”–“Μ÷÷Θ§ΥϊΟ«÷Η≥ωΘ§Ψ≠ΒδΒΡά©…ΔΡΘ–Ά Pe = KpD / d ÷–ΒΡ Kp”ΠάμΫβΈΣ LDC ‘ΎœΗΑϊΡΛΚΆΥ°œύ÷–ΒΡΖ÷≈δœΒ ΐΘ§Εχ≤Μ «Ά®≥Θ Β―ιΥυ≤βΒΟΒΡΥυ”–ΙΙœσœ¬ΒΡΤΫΨυ÷ΒΓΘΥϊΟ«Χα≥ωΘ§Ω…“‘Ά®ΙΐΖ÷Ή”Ε·ΝΠ―ßΦΤΥψΒΟΒΫ ΠΛGI ( άϊ”ΟΙΪ Ϋ ΠΛGI =Θ≠ Θ“TlnKp )Θ§¥”ΕχΩ…“‘άμ¬έΦΤΥψ≥ω…χΆΗ¬ ΓΘΥϊΟ«÷Η≥ωΘ§’βΗωΡΘ–ΆΒΡ‘Λ≤βΡήΝΠ±»‘Λ≤β«βΦϋ ΐΡΩΚΆ‘Λ≤βΦΪ–‘±μΟφΜΐΗϋΦ”ΉΦ»ΖΓΘΨΓΙήΥϊΟ«ΦΤΥψ≥ωΒΡ ΠΛGIΚΆ Β―ι≤βΒΟΒΡ lnPe≥ œΏ–‘ΙΊœΒΘ§ΒΪ±»άΐœΒ ΐ»¥≤Δ≤Μ“Μ÷¬Θ§“ρΈΣΦΤΥψ÷–ΟΜ”–ΩΦ¬«λΊ–ß”Π;ΝμΆβΘ§ΜΖκΡΖ÷Ή”≥Ώ¥γΚΆ–ΈΉ¥Β»“ρΥΊ“≤ΟΜ”–ΩΦ¬«‘ΎΡΎΘ§≤Δ«“ Β―ι―ι÷ΛΝΩΚή–ΓΘ§ΤδΡΘ–ΆΒΡ’ΐ»Ζ–‘ΜΙ”–¥ΐΦλ―ιΓΘ
Ε‘Ψ≠±ΜΕ·ά©…ΔΩγΡΛΒΡΜΖκΡΕχ―‘Θ§‘Λ≤β≤ΔΆ®ΙΐΜ·―ß–ό ΈΒΡΖΫΖ®ΗΡ±δ LDC ΙΙœσΘ§¥”ΕχΦθ–ΓΜΖκΡ¥”Υ°œύœρœΗΑϊΡΛ«®“Τ÷–ΒΡΦΣ≤ΦΥΙΉ‘”…Ρή±δ «―–ΨΩΒΡΙΊΦϋΒψΓΘΥυ“‘Θ§»œ ΕΜ·―ß–ό ΈΕ‘ΜΖκΡΙΙœσΒΡ”Αœλ «Τδ÷–÷Ί“ΣΒΡΩΤ―ßΈ ΧβΓΘ»ΜΕχΘ§‘Ύœ÷”–ΒΡ±ΜΕ·ά©…ΔΩγΡΛΒΡΜΖκΡ Βάΐ÷–Θ§Τδ≤–ΜυΜυ±ΨΕΦ «≤Μ¥χΒγΚ…≤Δ«“ «Ζ«ΦΪ–‘ΒΡΘ§ΥΒΟς’β÷÷ΩγΡΛ≤Ώ¬‘Ε‘Α±ΜυΥα≤–ΜυΒΡ“Σ«σΫœΗΏΘ§Ε‘ΦΪ–‘ΚΆ¥χΒγΚ…ΒΡ≤–ΜυΒΡ»ί»ΧΕ»ΫœΒΆΓΘ’κΕ‘’βΗωΈ ΧβΘ§Ω…“‘ Β±“ΐ»κ»ί»ΧΕ»Ϋœ¥σΒΡΖ«Χλ»ΜΑ±ΜυΥα“‘ΧαΗΏ±ΜΕ·ά©…Δ≤Ώ¬‘œ¬ΜΖκΡΒΡΕύ―υ–‘;Νμ“ΜΖΫΟφΘ§Ω…“‘άϊ”ΟœΗΑϊΡΎΆβ pH ΜρΟΗΜν–‘ΒΡ≤ν“λΘ§…ηΦΤ pH œλ”ΠΜρΟΗœλ”Π≤–ΜυΘ§‘ΎœΗΑϊΆβΤδΦΪ–‘±Μ―Ύ±ΈΘ§‘ΎœΗΑϊΡΎ»Ξ―Ύ±ΈΘ§ΦΛΜνΜΖκΡΒΡ’ΐ≥Θ…ζάμΜν–‘ΓΘ
3. 1. 2 N-ΦΉΜυΜ·”κΩγΡΛΡήΝΠ
≥ΐΝΥΕύκΡΙΙœσ±δΜ·Ε‘ΩγΡΛΡήΝΠ”–Ι±œΉΘ§ΕύκΡΙ«ΦήΒΡθΘΑΖ N-ΦΉΜυΜ·Ε‘ΩγΡΛΡήΝΠ“≤”–”ΑœλΓΘΙ«ΦήθΘΑΖ N-ΦΉΜυΜ·–ό Έ‘ΎΧλ»Μ≤ζΈο÷–Κή≥ΘΦϊΓΘ‘ΎΧΊΕ®ΈΜ÷Ο“ΐ»κ N-ΦΉΜυΩ…“‘‘ω«ΩΕύκΡ”κ ήΧεΦδΒΡœύΜΞΉς”ΟΓΔ‘ω«ΩΕύ κΡ Ε‘ Α– ±ξ ΒΡ ―Γ ‘ώ –‘ Μρ ΗΡ ±δ ΒΑ ΑΉ ΒΡ Ψέ Φ· ––ΈΣΘέ43 ΓΪ 45ΘίΓΘ
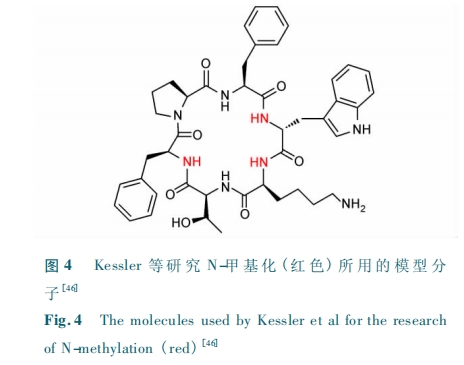
Α¥ ’’ ¥Υ ΥΦ ¬ΖΘ§Kessler Β» ΈΣ ΗΡ …Τ VeberHirschmann ΜΖΝυκΡ( cyclo ( -PFwKTF-) ) ΒΡΩΎΖΰ…ζΈοάϊ”ΟΕ»Θ§œΒΆ≥ΒΊ―–ΨΩΝΥ N-ΦΉΜυΜ·‘ΎΤδ÷–ΒΡΉς”ΟΘέ46Θί(ΆΦ 4)ΓΘΥϊΟ«ΖΔœ÷Θ§‘ΎΧΊΕ®ΈΜ÷Ο“ΐ»κ N-ΦΉΜυΚσΘ§ΜΖκΡ Ζ÷ Ή” ΒΡ ΩΎ Ζΰ …ζ Έο άϊ ”Ο Ε» ¥” Έό Ζ® Φλ ≥ω Χα ΗΏ ΒΫ9. 9% ΓΘΤδ‘≠“ρ « N-ΦΉΜυΜ·‘ωΦ”ΝΥΜΖκΡΖ÷Ή”ΒΡ÷§»ή–‘Θ§ ΙΤδΗϋ»ί“Ή¥©ΙΐœΗΑϊΡΛΓΘ÷°ΚσΘ§Kessler Β»”÷±®ΒάΝΥ…ζ≥ΛΦΛΥΊ“÷÷ΤΦΝάύΥΤΈο MK678 ΒΡ N-ΦΉΜυΩ…“‘ΧαΗΏΩΎΖΰΜν–‘Θ§≤ΔΑΒ ΨΗΟΫαΙϊΩ…Ρή”… N-ΦΉΜυΜ·‘ω«ΩΜΖκΡΩγΡΛΡήΝΠ‘λ≥…Θέ47ΘίΓΘΥϊΟ«”ΟΖ÷Ή”ΡΘΡβΒΡΖΫΖ®ΖΔœ÷ΩΎΖΰΜν–‘ΉνΗΏΒΡΖ÷Ή”‘ΎΥ°œύ÷–ΒΡΙΙœσ”κ CSA ΚήœύœώΓΘΒΪ¥ΥΚσΘ§Kessler ΚΆ Hoffman Β»ΖΔœ÷ΦΉΜυΜ·ΡΩ”κΩγΡΛΡήΝΠ÷°ΦδΟΜ”–±Ί»ΜΝΣœΒΘέ48ΘίΓΘ
Jacobson ΚΆ Lokey Β»Ϋχ“Μ≤ΫœΒΆ≥ΒΊ―–ΨΩΝΥ N-ΦΉΜυΜ·Ε‘ΜΖκΡΙΙœσΚΆΩγΡΛΡήΝΠΒΡ”ΑœλΘέ49Θί ( ΆΦ 5 )ΓΘΥϊΟ«―–ΨΩΝΥΜΖΝυκΡ Leu-Leu-Leu-Leu-Pro-Tyr ΒΡ≤ΜΆ§Ζ«Ε‘”≥“λΙΙΧε‘Ύ ς÷§…œΒΡΦΉΜυΜ·Ζ¥”ΠΓΘΥϊΟ«ΖΔœ÷Θ§“ΜΕ®ΧθΦΰœ¬Θ§Ι“‘Ύ ς÷§…œΒΡΤδ÷– 6 ΗωΙΙ–ΆΒΡΜΖΝυκΡΒΡΦΉΜυΜ·Ζ¥”ΠΨΏ”–«χ”ρ―Γ‘ώ–‘(―Γ‘ώ–‘¥σ”Ύ 95% )ΓΘ‘ΎΨΏ”–«χ”ρ―Γ‘ώ–‘ΒΡΜΖκΡΫχ–– H /D ΫΜΜΜ Β―ι ±ΖΔœ÷Θ§Έ¥ΦΉΜυΜ·ΒΡΜΖκΡΖ÷Ή”ΒΡΥυ”– NΓΣH ±©¬Ε‘Ύ»ή“Κ÷–;Εχ≤ΩΖ÷ΦΉΜυΜ·ΒΡ―ή…ζΈο ÷– Έ¥ ΖΔ …ζ N-ΦΉ Μυ Μ· ΒΡNΓΣH ≤Δ≤Μ±©¬Ε‘Ύ»ή“Κ÷–ΓΘΥϊΟ«÷Η≥ωΘ§…œ ω«χ”ρ―Γ‘ώ–‘Ω…Ρήά¥‘¥”Ύ≤ζΈοΖ÷Ή”ΒΡ”Έάκ NΓΣH ±ΜΈΜΉηΜρΖ÷Ή”ΡΎ«βΦϋœό÷ΤΘ§ΈόΖ®ΦΧ–χΦΉΜυΜ·ΓΘ Β―ι±μΟςΘ§≤ΩΖ÷ΦΉΜυΜ·ΒΡΕύκΡΒΡΩγΡΛΡήΝΠΗϋ«ΩΓΘΥϊΟ«Ά®Ιΐάμ¬έΦΤΥψ÷Η≥ωΘ§«χ”ρ―Γ‘ώ–‘ΦΉΜυΜ·≤ζΈο «Υυ”–―ή…ζΈο÷–ΩγΡΛΡήΝΠΉν«ΩΒΡΘ§“ρΕχ‘ΎΦΪ–‘ΫœΒΆΒΡ»ήΦΝΜΖΨ≥÷–ΥυΫχ––ΒΡΦΉΜυΜ·Ζ¥”Π”–άϊ”Ύ…ζ≥…ΩγΡΛΡήΝΠΉν«ΩΒΡ―ή…ζΈοΓΘΒΪ’β“ΜΦΉΜυΜ·ΖΫΖ®»¥ΈόΖ®ΒΟΒΫΤδΥϊΙΙ–ΆΒΡΉν”≈ΦΉΜυΜ·ΈΜΒψΘ§“≤ΨΆ «ΥΒΘ§ΗΟΦΉΜυΜ·≤Ώ¬‘œ¬ΒΡ«χ”ρ―Γ‘ώ–‘ «Τ䥩ΆΗœΗΑϊΡΛΒΡ≥δΖ÷≤Μ±Ί“ΣΧθΦΰΓΘΥϊΟ«“≤ΖΔœ÷Θ§ΫΪΤδ1ΓΔ3ΓΔ4 ΈΜΒΡΝΝΑ±ΥαΖ÷±πΗΡΈΣΥΩΑ±ΥαΚσΘ§ΤδΩγΡΛΡήΝΠ¥σΖυœ¬ΫΒΘ§ΥΒΟς N-ΦΉΜυΜ·≤Ώ¬‘÷Μ ”Ο”ΎΡ≥–©Α±ΜυΥα≤–ΜυΓΘ”–“βΥΦΒΡ «Θ§ΥϊΟ«÷Η≥ωΘ§‘ΎΗΟ Β―ι÷–ΖΔœ÷ΒΡΦΉΜυΜ· ΈΜ Βψ ”κ «Α ω Kessler Β» ’κ Ε‘ Veber-HirschmannΥυΒΟΒΫΒΡΦΉΜυΜ·ΈΜΒψΘέ46Θί“Μ÷¬Θ§ΥϊΟ«≤¬≤βΤδ÷–ΒΡ Π¬-ΉΣΫ«(Π¬-turn)ΫαΙΙ÷ΗΒΦΝΥΩγΜΖΖ÷Ή”ΡΎ«βΦϋΒΡ–Έ≥…ΓΘ
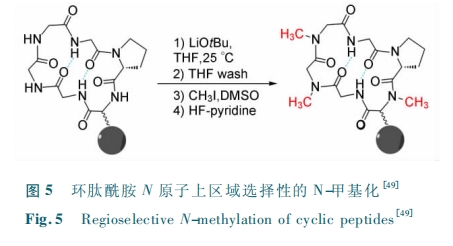
“‘…œΙΛΉς±μΟςΘ§N-ΦΉΜυΜ·Ω…“‘Ά®ΙΐΗΡ±δΜΖκΡ‘ΎΥ°œύ÷–ΒΡΙΙœσά¥ΧαΗΏΤδΩγΡΛΡήΝΠΓΘ‘Ύ«Α»ΥΙΛΉςΒΡΜυ¥Γ…œΘ§Kessler Β»œΒΆ≥ΒΊ―–ΨΩΝΥ N-ΦΉΜυΜ·Ε‘ΜΖκΡΙΙœσΒΡ”ΑœλΘέ50ΘίΓΘΥϊΟ«―Γ‘ώΜΖΝυκΡ cyclo( -D-Ala-Ala5 -) ΉςΈΣ―–ΨΩΕ‘œσΘ§Ζ÷Έω≤ΜΆ§ N-ΦΉΜυΜ·―ή…ζΈο‘ΎΥ°œύ÷–ΒΡΕΰΈ§ΚΥ¥≈ΫαΙΙΓΘΥϊΟ«»œΈΣ N-ΦΉΜυΜ·Μα¥”“‘œ¬»ΐΖΫΟφ”ΑœλΜΖκΡ Π¬-ΉΣΫ«ΫαΙΙΒΡ–Έ≥…Θ§¥”ΕχΒΦ÷¬ΩγΜΖΖ÷Ή”ΡΎ«βΦϋΒΡ≥ωœ÷: ( 1 ) κΡΦϋΒΡΥ≥ΓΔΖ¥ Ϋ; ( 2 ) Ε‘Ι«Φή…œNΓΣH «βΦϋΒΡ―Ύ±ΈΉς”Ο;(3 ) ≈Λ«ζΜΖκΡ‘≠±ΨΒΡΫαΙΙΓΘΥϊΟ«ΖΔœ÷Θ§ Β―ι÷–ΥυΒΟΒΫΒΡ“Μ–©Βδ–ΆΒΡ Π¬-ΉΣΫ«ΫαΙΙ‘Ύ«Α»Υ ΖΔ œ÷ ΒΡ N-ΦΉ Μυ Μ· œΗ Αϊ ¥© ΆΗ ΜΖ κΡ ÷– ”– Ε‘ ”ΠΈοΘέ22Θ§4 6 Θ§47ΘίΓΘΝμΆβΘ§ΥϊΟ«÷Η≥ωΡ≥–©ΫαΙΙΧΊ βΒΡΑ±ΜυΥαΩ…“‘ΤπΒΫ‘ΎΜΖκΡ÷–“ΐ»κ N-ΦΉΜυΜ·Μρ D-–ΆΙΙœσΒΡΉς”ΟΘ§άΐ»γ ΠΝ-N ΦΉΜυΜ·ΒΡΗ§Α±ΥαΚΆΨΏ”–Ε‘≥Τ–‘ΒΡΗ Α±ΥαΓΘ
“‘…œ’β–©ΖΔœ÷Ε‘œΗΑϊ¥©ΆΗΜΖκΡΒΡ…ηΦΤ”–÷ΗΒΦΉς”ΟΘ§ΒΪ «Τδ÷–»‘¥φ‘Ύ“Μ–©Έ ΧβΓΘ±»»γΘ§―–ΨΩœΒΆ≥Εύ «ΜΖΝυκΡΘ§Υυ“‘ΈόΖ®÷ΣœΰΒ±ΜΖ‘ω¥σΚσΘ§ΩγΜΖ«βΦϋ”κ N-ΦΉΜυΜ·÷°ΦδΨΏ”–‘θ―υΒΡ–≠Ά§ΜρΤδΥϊœύΜΞ”ΑœλΓΘΆ§ ±Θ§ΤδΥϊΈΜ÷Ο N-ΦΉΜυΜ·Ε‘ Π¬-ΉΣΫ«ΒΡ–Έ≥…”–‘θ―υΒΡ”Αœλ“≤≤ΜΟςΝΥ;Ά§ ±Θ§ΜΖ‘ω¥σΚσΘ§Μυ”Ύ…Η―ΓΒΡ N-ΦΉΜυΜ·≤Ώ¬‘ΫΪ±δΒΟΗϋΈΣάßΡ―Θ§“ρΈΣ–η“ΣΚœ≥…ΒΡ―ή…ζΈο ΐΝΩ≥ ÷Η ΐ…œ…ΐΓΘΥυ“‘Θ§–η“ΣΖΔ’ΙΩ…“‘ΩλΥΌΒΟΒΫ¥σΝΩœΗΑϊ¥© ΆΗ ΜΖ κΡ ΒΡ N-ΦΉ Μυ Μ· –ό Έ ΖΫ Ζ®ΓΘJacobson ΚΆLokey Β»Θέ49Θί±®ΒάΒΡ―Γ‘ώ–‘ΦΉΜυΜ·ΒΡΙΛΉςΕ‘¥ΥΨΏ”–“ΜΕ®ΤτΖΔ–‘Θ§ΒΪ «ΨύάκΡΩ±ξ Βœ÷ΜΙ”–Ϋœ¥σ≤νΨύΓΘ
3. 2 Μυ”Ύ÷≤ΈοΜΖκΡΒΡΗΡ‘λ≤Ώ¬‘
Μυ”Ύ÷≤ΈοΜΖκΡΒΡœΗΑϊ¥©ΆΗΜΖκΡΒΡ…ηΦΤΥΦ¬Ζ «ΫΪΨΏ”–…ζΈοΜν–‘ΒΡΕύκΡ–ρΝ–ΦόΫ”ΒΫ÷≤ΈοΜΖκΡΙ«Φή…œΓΘΤπ≥θΘ§―–ΨΩ’ΏΫΪΧΊ βΜν–‘–ρΝ–ΦόΫ”ΒΫ÷≤ΈοΜΖκΡ…œ“‘ΤΎΧαΗΏ–ρΝ–ΒΡΧεΡΎΈ»Ε®–‘ΓΘάΐ»γ Daly Β»ΫΪ VEGF-AόΉΩΙΦΝΦόΫ”»κ Kalata BΘέ51ΘίΓΘ÷°ΚσΘ§―–ΨΩ’ΏΖΔœ÷ΦόΫ”ΕύκΡΩ…“‘ΆΗΙΐœΗΑϊΡΛ≤ΔΧαΗΏΩΎΖΰ…ζΈοάϊ”ΟΕ»Θέ33ΘίΓΘάϊ”Ο MCoTI-Δώ ΒΡ Ωγ ΡΛ ΧΊ –‘Θ§Camarero Β» ΫΪ Α– œρHdm2 ΚΆ HdmX ΒΡ ΠΝ ¬ί–ΐ–ρΝ–≤ε»κ MCoTI-ΔώΒΡ 6 Κ≈ΜΖ”ρΘ§ΒΟΒΫ MCo-PMI ΦόΫ”κΡ(ΆΦ 6)ΓΘMCo-PMI ΡήΙΜ“÷÷Τ Hdm2 ΚΆ HdmX Ής”ΟΘ§ΦΛΜν“÷Α©“ρΉ” p53 ΒΡΜν–‘Θέ52ΘίΓΘ‘Ύ–Γ σΡΘ–Ά…œ÷Λ ΒΘ§Β±Ηχ“©ΝΩ‘Ύ 40 mg / kg ±Θ§–Γ σ÷ΉΝω‘ω≥Λœ‘÷χΦθΜΚΓΘΥΒΟςΦόΫ”ΕύκΡ MCoPMI »Ζ ΒΩ…“‘¥©ΙΐœΗΑϊΡΛΘ§Α–œρΑϊΡΎΒΡΑ–±ξΓΘ
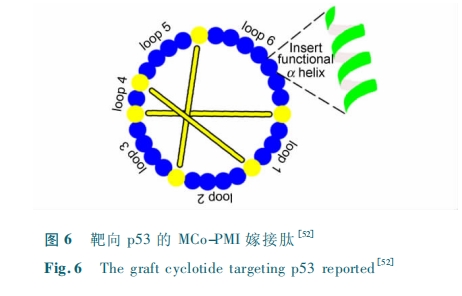
Υδ»ΜΡΩ«Α“―Ψ≠ΖΔœ÷“Μ–©÷≤ΈοΜΖκΡΩ…“‘Ά®ΙΐœΗΑϊΡΛΘ§≤Δ«“Τδ÷–ΒΡΡ≥–©ΜΖκΡ»γ MCoTI ΚΆ Kalata B ΉςΈΣΕύκΡΙ«Φή±Μ”Ο”ΎΦόΫ”ΕύκΡΒΡ―–ΨΩΘ§ΒΪ «”…”Ύ÷≤ΈοΜΖκΡΒΡΩγΡΛΖΫ ΫΕύΈΣœΗΑϊ÷ςΕ·…ψ»ΓΘ§–η“ΣœϊΚΡΡήΝΩΘ§≤Δ«“Ιΐ≥ΧΗ¥‘”Θ§Μζάμ≤ΜΟςΓΘΆ§ ±Θ§ΤδΙΐ≥Χ≤Μœώ±ΜΕ·ά©…Δ“Μ―υΙψΖΚ¥φ‘Ύ”Ύ–ΓΖ÷Ή”“©÷–ΓΘ“ρ¥ΥΘ§÷≤ΈοΜΖκΡΩγΡΛ–ß¬ »‘≤ΜΟς»ΖΘ§Ε‘≤ΜΆ§œΗΑϊΒΡΡΆ ήΕ»“≤≤Μ«ε≥ΰΓΘΙ ΕχΘ§–η“ΣΫχ“Μ≤ΫΗψ«εΫιΒΦ÷≤ΈοΜΖκΡΩγΡΛΒΡΖ÷Ή”Μζ÷Τ;Ά§ ±Θ§ΜΙ–η“ΣœΒΆ≥ΒΊ―–ΨΩΩ…“‘Ϋχ»κœΗΑϊΡΛΒΡ÷≤ΈοΜΖκΡ‘Ύ»ΥΧεΡΎΒΡ“©¥ζΕ·ΝΠ―ßΘ§Ηψ«εΤδΩγΡΛ–ß¬ ΦΑ‘ΎΧεΡΎΒΡΖ÷≤ΦΉ¥ΩωΓΘ‘ΎΕ‘÷≤ΈοΜΖκΡΒΡΩγΡΛΫαΙΙΜυ¥ΓΚΆ“©¥ζΕ·ΝΠ―ß»œ Ε…ν»κΚσΘ§Ω…άϊ”ΟΜ·―ß ÷ΕΈ”≈Μ·ΜΖκΡΫαΙΙΘ§ ΙΤδ‘ΎΧεΡΎΒΡ––ΈΣΗϋΖϊΚœ≥…“©ΒΡ“Σ«σΓΘ
3. 3 Μυ”ΎœΏ–‘κΡΒΡΗΡ‘λ≤Ώ¬‘
ΈΣ ΙœΏ–‘κΡΜΖΜ·ΚσΒΟΒΫΜΖκΡΨΏ”–œΗΑϊ¥©ΆΗΡήΝΠΘ§Ά®≥Θ Ι”ΟΒΡ≤Ώ¬‘Αϋά®≤ύΝ¥ΜΖΜ·ΒΡΓΑΕ© ικΡΓ±≤Ώ¬‘ΚΆ‘ΎΜΖκΡ÷–“ΐ»κœΗΑϊ¥©ΆΗ–ρΝ–ΓΘ
3. 3. 1 Ε© ικΡ
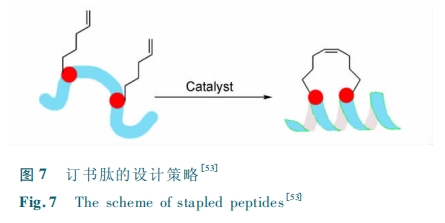
2000 ΡξΘ§Verdine –Γ Ήι Χα ≥ω ΝΥ Ε© ι κΡ ( stapledpeptides)ΒΡΗ≈Ρν(ΆΦ 7)Θ§Φ¥ΫΪ ΠΝ ¬ί–ΐ…œΝΫΗωΑ±ΜυΥα≤–ΜυΒΡ≤ύΝ¥”Ο“ΜΕ®≥ΛΕ»ΒΡΧΦ«βΝ¥œύΝ§Θ§¥”Εχ”––ßΈ»Ε®œΏ–‘κΡΒΡ ΠΝ ¬ί–ΐΫαΙΙΘέ53ΘίΓΘάϊ”ΟΗΟΦΦ θΘ§ΗΟ–ΓΉι‘Ύ2004 Ρξ±®ΒάΝΥ“ΜΧθΑ–œρ BCL-2 ΫιΒΦΒΡœΗΑϊΒρΆωΙΐ≥ΧΒΡΕ© ικΡ( stabilized alpha-helix of BCL-2 domainsΘ§SAHBs)Θέ54ΘίΓΘΥϊΟ«ΖΔœ÷Θ§ΗΟ SAHB Ω…“‘‘ΎΝςΧεœύœΗΑϊΡΎΆΧΫιΒΦœ¬¥©Ιΐ Jurkat ΑΉ―Σ≤ΓœΗΑϊΒΡœΗΑϊΡΛΓΘ÷°Κσ―–ΨΩ’ΏΖΔœ÷≤Δ―–ΨΩΝΥ“ΜœΒΝ–Ω…“‘Ά®ΙΐœΗΑϊΡΛΒΡΕ© ικΡΘέ55 ΓΪ 58ΘίΓΘΫαΚœ N-ΦΉΜυΜ·‘ω«ΩΩγΡΛΡήΝΠΒΡ≤Ώ¬‘Θ§Lin Β»ΫΪ N-ΦΉΜυΜ·“ΐ»κΕ© ικΡ÷–Θ§Ϋχ“Μ≤ΫΧαΗΏΝΥΕ© ικΡΒΡΩγΡΛΡήΝΠΘέ59ΘίΓΘ’βάο–η“Σ÷Η≥ωΘ§Ε© ικΡ‘ΎΥ°œύ÷–ΒΡΫαΙΙΟς»ΖΘ§ Β±ΒΊ“ΐ»κΜ·―ß–ό Έ≤ΜΜαΨγΝ“ΒΊ”ΑœλΤδΫαΙΙΘ§Ι Εχœύ±»ΫαΙΙΕύ±δΒΡΤ’Ά®ΜΖκΡΘ§Ηϋ»ί“Ή‘Ύ±Θ≥÷ΕύκΡ‘≠”–Μν–‘Μυ¥Γ…œΘ§άϊ”Ο N-ΦΉΜυΜ·Β»–ό ΈΜ·―ßΖΫΖ®ΧαΗΏΤδΩγΡΛΡήΝΠΓΘ
3. 3. 2 ΜΖΜ·ΒΡœΗΑϊ¥©ΆΗκΡ
œΗΑϊ¥©ΆΗκΡ ( cell penetrating peptidesΘ§CPP) «“Μ άύ Ρή ΙΜ ¥© Ιΐ œΗ Αϊ ΡΛ ΒΡ œΏ –‘ κΡΘ§Αϋ ά® ¥© ΡΛ κΡ( penetratin )Θέ60ΘίΓΔΉΣ ¬Φ ΦΛ Μν “ρ Ή” ( trans-activator oftranscriptionΘ§Tat ) Τ§ ΕΈΘέ61ΘίΓΔPep-1Θέ62ΘίΓΔΕύ ΨΪ Α± Υα( polyarginines)Θέ63Θί Β»ΓΘCPP Ω… “‘ Ά® Ιΐ œΗ Αϊ ÷ς Ε· …ψ»ΓΘέ64ΘίΜρΖ«ΡήΝΩ“άάΒΒΡΉΣ‘ΥΙΐ≥ΧΘέ65Θ§66ΘίΫχ»κœΗΑϊΘ§≤ΔΡήΫΪ”κ÷°Ι≤ΦέΜρΖ«Ι≤ΦέΝ§Ϋ”ΒΡΒΑΑΉΜρΚΥΥα‘Υ»κœΗΑϊΓΘœΗΑϊ¥©ΆΗκΡ≥Θ¥χ”–œύΒ±ΕύΒΡΨΪΑ±ΥαΘ§±μΟφ¥χ’ΐΒγΘ§ΡήΙΜ”κœΗΑϊΡΛ±μΟφΒΡΗΚΒγΚ…ΖΔ…ζΨ≤ΒγΉς”ΟΘ§‘ω«Ω”κœΗΑϊΡΛΒΡœύΜΞΉς”ΟΓΘ’βάύΕύΨΪΑ±ΥαΒΡ CPP ( arginine richpeptidesΘ§Θ“Θ“P) Ά®Ιΐ”κœΗΑϊΡΛœύΜΞΉς”Ο ΙœΗΑϊΡΛ±δ±ΓΘ§≤ζ…ζΥ≤ ±ΩΉ¥”Εχ¥©ΙΐœΗΑϊΡΛΓΘάϊ”Ο CPP ΡήΙΜΫΪ”κΤδΙ≤ΦέΝ§Ϋ”ΒΡΖ÷Ή”¥χ»κœΗΑϊΒΡΧΊΒψΘ§Pei Β»ΫΪ CPPΙ≤ΦέΒΊΝ§Ϋ”ΒΫΜΖκΡΖ÷Ή”…œΘ§≥…ΙΠ Βœ÷ΝΥΜΖκΡΖ÷Ή”ΩγΡΛΘέ67ΘίΓΘΒΪ «Θ§÷±Ϋ”–ό ΈΒΡ Θ“Θ“P Ζ÷Ή”œΗΑϊ¥©ΆΗΡήΝΠ≤νΘ§”– ±ΨΏ”–œΗΑϊΕΨ–‘Θ§“ΐΤπœΗΑϊΜΒΥάΘέ68 ΓΪ 70ΘίΓΘ
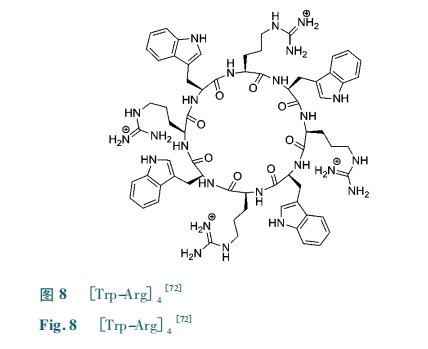
ΈΣΧαΗΏ CPP ΒΡΩγΡΛ–ß¬ Θ§Herce ΚΆ Cardoso Β»ΫΪTat ΚΆΕύΨΪΑ±ΥαΫχ–– ΉΈ≤ΜΖΜ·Θ§Θ“Θ“P ΒΡΜΖΜ· ΙΤδ”κœΗΑϊΡΛΫαΚœ ±ΒΡλΊΦθ–ß”ΠΫΒΒΆΘ§ΧαΗΏΩγΡΛ–ß¬ Θέ71ΘίΓΘΝμΆβΘ§ΜΖ Μ· Κσ κ“ Μυ Φδ Ψύ άκ ΒΡ ‘ω ¥σ “≤ ”– άϊ ”Ύ Ωγ ΡΛΓΘParang Β»Χα≥ωΝμ“Μ÷÷άϊ”Ο CPP ΒΡΥΦ¬Ζ:ΨΏ±ΗΝΫ«Ή–‘«“ΫαΙΙΗ’–‘ΒΡΜΖκΡΩ…ΡήΡήΙΜΆ®ΙΐœΗΑϊΡΛΘέ72ΘίΓΘΥϊΟ«Μυ”Ύ’β“Μ≤¬≤βΫχ––άμ–‘…ηΦΤΚΆ…Η―ΓΘ§ΖΔœ÷ΜΖκΡΘέTrpArgΘί4 (ΆΦ 8)ΚΆΘέTrp-ArgΘί5 ”–ΫœΗΏΒΡΩγΡΛ–ß¬ Θ§≤Δœ‘ Ψ≥ω Ζ« œΗ Αϊ ΡΎ ΆΧ “ά άΒ ( non-endocytosis ) ΒΡ ΧΊ ΒψΓΘΘέTrp-ArgΘί4 ≤ΜΫωΩ…“‘ΫΪΙ≤ΦέΝ§Ϋ”ΒΡ–ΓΖ÷Ή”“©Έο‘Υ»κœΗΑϊΘέ73ΘίΘ§ΜΙΡή”κΝΉΥαΜ·œΏ–‘κΡ–Έ≥…Η¥ΚœΈο≤ΔΫΪ÷°ΥΆ»κΡΛΡΎΘέ74ΘίΓΘ
Pei Β»ΜΙ…η ΦΤ ΝΥ Κ§ CPP Ϋα ΙΙ ΒΞ ‘Σ ΒΡ ΜΖ κΡ Ζ÷ Ή”(ΆΦ 9)Θ§Φ¥‘ΎΜΖ≥Ώ¥γΈΣ 7 ΓΪ 13 Ηω≤–ΜυΒΡΜΖκΡ÷–“ΐ»κ“ΜΕΈ CPP –ΓΤ§ΕΈΑο÷ζΜΖκΡΫχ»κœΗΑϊΘέ75ΘίΓΘ‘Ύ Β―ι÷–Θ§ΥϊΟ«ΖΔ œ÷ ΫΪ Phe-ΠΒ-Arg4 ( Τδ ÷– ΠΒ ΈΣ L-2-ίΝ Μυ ±ϊ Α±Υα)≤ε»κ≤–Μυ ΐΈΣ 7 ΓΪ 13 ΒΡΜΖκΡΚσΘ§ΜΖκΡΨ≠ΡΎΆΧΫχ»κœΗΑϊΒΡΡήΝΠ‘ω«ΩΓΘΗΟ–ρΝ–…θ÷ΝΩ…“‘ΫΪΡ―“‘ΩγΡΛΒΡΝΉΥαΜ·Α±ΜυΥα≤–Μυ¥χ»κΑϊΡΎΓΘ
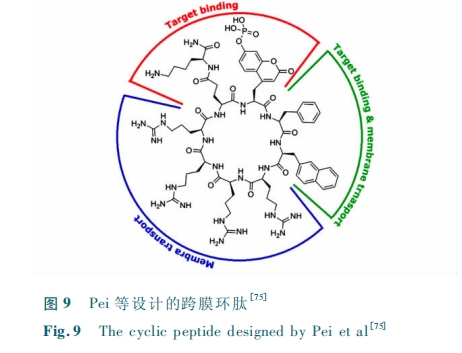
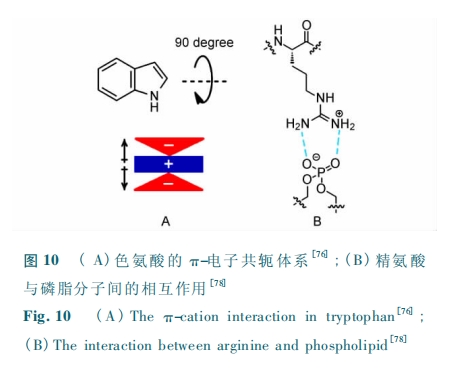
…œ ωΜΖΜ· CPP ΒΡ―–ΨΩΖΔœ÷Θ§’ΐΒγΚ…ΓΔΜΖΜ·ΚΆ ηΥ°Α±ΜυΥαΒΡ“ΐ»κΕΦΜα‘ω«ΩΜΖκΡ”κœΗΑϊΡΛΦδΒΡœύΜΞΉς”ΟΓΘΤδ÷–Θ§ΨΪΑ±ΥαΚΆ…ΪΑ±Υα‘ΎΕύκΡ”κΡΛΦδΒΡœύΜΞΉς”Ο÷–ΨΏ”–÷Ί“ΣΉς”ΟΘέ76Θί(ΆΦ 10)ΓΘ…ΪΑ±ΥαΒΡ≤–ΜυΨΏ”–Π–-ΒγΉ”Ι≤ινΧεœΒΘ§Ω…“‘”κ―τάκΉ”ΖΔ…ζ―τάκΉ”-Π– œύΜΞΉς”ΟΘ§Ι Εχ…ΪΑ±Υα“ΜΑψ¥Π‘ΎΥ°œύ”κœΗΑϊΡΛ÷°ΦδΒΡΫΜΫγ¥ΠΘ§”κΝΉ÷§Ζ÷Ή”¥χ’ΐΒγΚ…ΒΡΚ§ΒΣΦνΜυ¥φ‘ΎœύΜΞΉς”ΟΓΘΨΪΑ±ΥαΒΡκ“Μυ «ΥΪ≥ί«βΦϋΗχΧεΘ§Ω…“‘”κœΗΑϊΡΛ±μΟφΒΡ«βΦϋ ήΧε–Έ≥…ΥΪ÷Ί«βΦϋΘ§”––ßΧαΗΏΤδ”κΡΛΦδΒΡœύΜΞΉς”ΟΘέ77ΘίΓΘ
4 Ϋα¬έ
”κΤ’Ά®œΏ–‘ΕύκΡœύ±»Θ§œΗΑϊ¥©ΆΗΜΖκΡΨΏ”–ΫœΚΟΧεΡΎΈ»Ε®–‘Θ§≤ΔΡήΙΜ¥©ΙΐœΗΑϊΡΛΕχΧΊ“λ–‘ΫαΚœœΗΑϊΡΎΑ–±ξΘ§ΨΏ±ΗΚήΚΟΒΡ≥…“©–‘Θ§“ρ¥ΥœΗΑϊ¥©ΆΗΜΖκΡ“―Ψ≠≥…ΈΣΒ±«Α“©Έο―–ΨΩΒΡ–¬»»ΒψΓΘ±ΨΈΡ¥”Χλ»Μ≤ζΈοά¥‘¥ΚΆ»ΥΙΛΗΡ‘λά¥‘¥ΝΫΖΫΟφΉέ ωΝΥœΗΑϊ¥©ΆΗΜΖκΡΝλ”ρΒΡ―–ΨΩΫχ’ΙΦΑΖΔ’Ι«ΑΨΑΓΘ‘ΎΜ·―ßΚœ≥…ΜώΒΟΥυ–ηΜΖκΡΖ÷Ή”ΒΡΜυ¥Γ…œΘ§Έ“Ο«»‘»Μ–η“ΣΫχ“Μ≤ΫάμΫβΜΖκΡΖ÷Ή”ΒΡΩγΡΛΜζάμΓΔΜΖκΡΖ÷Ή””κ ήΧεΜρΡΛΦδœύΜΞΉς”ΟΒΡΖ÷Ή”Μζ÷ΤΚΆΨΏΧεΙΐ≥ΧΘ§“‘…ηΦΤΓΔΗΡ‘λΒΟΒΫΨΏ”–œΗΑϊ¥©ΆΗΜν–‘ΒΡΜΖκΡ“©ΈοΓΘ
Οβ‘π…υΟςΘΚ±ΨΈΡΈΣ––“ΒΫΜΝς―ßœΑΘ§Αφ»®Ιι‘≠Ής’ΏΦΑ‘≠‘”÷ΨΥυ”–Θ§»γ”–«÷»®Θ§Ω…ΝΣœΒ…Ψ≥ΐΓΘΈΡ’¬±ξΉΔ”–Ής’ΏΦΑΈΡ’¬≥ω¥ΠΘ§»γ–η‘ΡΕΝ‘≠ΈΡΦΑ≤ΈΩΦΈΡœΉΘ§Ω…‘ΡΕΝ‘≠‘”÷ΨΓΘ












