
еЊ вЊ жзСіАаЯђФЩУзЕнвЉЯЕЭГЪЧжИРћгУжзСізщжЏЬиЪтЕФЩњРэВЁРэЬиЕуЃЌгЩФЩУздиЬхАќдижзСіеяСЦвЉЮяЙЙНЈЖјГЩЕФЖджзСізщжЏОпгаАаЯђЖЈЮЛЙІФмЕФвЉЮяЕнЫЭЯЕЭГЁЃЖрыФНщЕМЕФжзСіАаЯђФЩУзЕнвЉЯЕЭГЪЧжзСіАаЯђЕнвЉСьгђНЯаТЕФвЛИібаОПЗНЯђЃЌБОЮФзлЪіСЫИУбаОПЗНЯђЕФЫФИіживЊЗЂеЙРњГЬЃЌЕЅЙІФмАаЯђЁЂЫЋЙІФмАаЯђЁЂжзСіДЉЭИКЭЛЗОГЯьгІаЭАаЯђФЩУзЕнвЉЯЕЭГЁЃВЂНщЩмСЫИїРрЕнвЉЯЕЭГЕФЩшМЦдРэКЭЕфаЭбаОПАИР§ЁЃДЫЭтЃЌЖдФПЧАЖрыФНщЕМЕФФЩУзЕнвЉЯЕЭГДцдкЕФгХЪЦгыВЛзуНјааСЫЗжЮіЃЌ зюКѓЃЌеыЖдЕБЧАжїЖЏАаЯђжзСіЕнвЉЯЕЭГДцдкЕФбаОПРЇОГЃЌЬсГіСЫвЛжжаТаЭжзСіАаЯђЕнвЉВпТд--ЁАЯЕЭГадАаЯђВпТдЁБЃЌ ЫцзХЯрЙибЇПЦКЭЖрбЇПЦНЛВцЕФЗЂеЙЃЌЖрыФНщЕМЕФжзСіАаЯђФЩУзЕнвЉЯЕЭГНЋдкжзСіжЮСЦжаАчбнИќЮЊживЊЕФНЧЩЋЁЃ
жзСіАаЯђФЩУзЕнвЉЯЕЭГЪЧжИРћгУжзСізщжЏЬиЪтЕФЩњРэВЁРэЬиЕуЃЌгЩФЩУздиЬхАќдижзСіеяЖЯЛђжЮСЦвЉЮяЙЙНЈЖјГЩЕФЖджзСізщжЏОпгаАаЯђЖЈЮЛЙІФмЕФвЉЮяЕнЫЭЯЕЭГЃЌСйДВЩЯГЃЙцЛЏСЦвЉЮяЖджзСізщжЏЮоАаЯђадЃЌМгДѓИјвЉМССПГЃЕМжТЖде§ГЃзщжЏбЯжиЕФЖОИБзїгУЃЌЖјНЕЕЭИјвЉМССПЛсв§Ц№жзСіЕФИДЗЂКЭФЭвЉадЃЌгЩгкФЩУздиЬхдкЬсИпвЉЮяЮШЖЈадЁЂИФЩЦвЉЮяЬхФкааЮЊЁЂдіМгЖджзСізщжЏАаЯђадЕШЗНУцЕФгХСМБэЯжЃЌвбЪмЕНСЫбаОПепЕФЙуЗКЙизЂЁЃ
жзСіАаЯђАДЦфЛњРэПЩЗжЮЊШ§РрЃКБЛЖЏАаЯђЁЂЮяРэЛЏбЇАаЯђКЭжїЖЏАаЯђЁЃБЛЖЏАаЯђЪЧвЛжжЛљгкжзСізщжЏЕФEPR(діЧПЩјЭИКЭжЭСє)аЇгІЪЙЕнвЉЯЕЭГАаЯђЗжВМгкжзСізщжЏЕФВпТдЁЃЮяРэЛЏбЇАаЯђЕнвЉЯЕЭГНшжњЬиЖЈЕФЮяРэЛЏбЇЗНЗЈАаЯђгкжзСізщжЏЃЌАќРЈДХАаЯђЁЂPHУєИаЁЂЮТЖШУєИаЕнвЉЯЕЭГЕШЃЌжїЖЏАаЯђЪЧдкБЛЖЏАаЯђЕФЛљДЁЩЯЃЌНшжњжзСізщжЏИпБэДяЕФЬивьадЪмЬхЕФНщЕМзїгУЃЌдіМгЕнвЉЯЕЭГдкжзСізщжЏЁЂЯИАћЛђЯИАћЦїФкЗжВМЕФВпТдЁЃ
жїЖЏАаЯђЕнвЉЯЕЭГгЩгкПЩвдЯджјдіМгвЉЮяБЛжзСіЯИАћЕФЩуШЁСПЃЌдіЧПвЉЮяПЙжзСізїгУЃЌж№НЅГЩЮЊНќФъРДжзСіАаЯђЕнвЉбаОПСьгђЕФШШЕуЃЌИУЯЕЭГвЛАуЪЧНЋАаЯђЗжзгжБНгЛђЭЈЙ§СЌНгБлХМКЯЕНдивЉФЩУзСЃзгБэУцЖјЙЙГЩЁЃгыБЛЖЏАаЯђКЭЮяРэЛЏбЇАаЯђЕнвЉЯЕЭГРрЫЦЃЌГЃгУЕФФЩУздиЬхАќРЈжЌжЪЬхЁЂФЩУзСЃЁЂОлКЯЮяНКЪјЁЂжІзДОлКЯЮяКЭФвХнЕШЃЛСЌНгБлЮЊвЛЖЈЗжзгСПЕФЧзЫЎадДѓЗжзгСДЃЌPEGзюЮЊГЃгУЁЃАаЯђЗжзгвЛАуЮЊгыжзСізщжЏФкЬивьадЪмЬхгаЧзКЯадЕФЮяжЪЃЌжївЊАќРЈПЙЬхЛђПЙЬхЦЌЖЮЁЂЖрыФЁЂаЁЗжзггЊбјЮяжЪЕШЁЃЖрыФНщЕМЕФжзСіжїЖЏАаЯђФЩУзЕнвЉЯЕЭГзїЮЊНќФъРДНЯаТЕФвЛИібаОПЗНЯђЃЌЗЂеЙбИЫйЃЌБОЮФНЋЖдИУЗНЯђНќФъРДЕФживЊНјеЙзївЛзлЪіЁЃ
2 ЖрыФНщЕМжзСіАаЯђЕФЩњРэбЇЛљДЁ
жзСіЕФЩњРэбЇЬиеїЪЧЩшМЦжзСіАаЯђЕнвЉЯЕЭГЕФЛљДЁЁЃЪзЯШЃЌжзСізщжЏЕФвЛИіживЊЩњРэбЇЬиеїЪЧЖдФЩУзПХСЃЕФEPRаЇгІЁЃЕБжзСіЩњГЄЕН 2mm3КѓЃЌгЩгкЯжгаЕФжзСібЊЙмЮоЗЈТњзужзСіПьЫйЩњГЄЫљашгЊбјЃЌвђДЫПЊ ЪМ Гі Яж жз Сі бЊ Йм КЭ жз Сі См АЭ Йм аТ Щњ ЯжЯѓЁЃЕЋЪЧжзСіаТЩњбЊЙмЕФбЊЙмБкМфЯЖНЯПэЧвЭЈЭИадНЯДѓЃЌЖјжзСізщжЏжааФЕФСмАЭЙмвЛАуВЛОпБИе§ГЃЙІФмЃЌдьГЩжзСізщжЏжаСмАЭЛиСїШБЪЇЃЌЕМжТвЛЖЈДѓаЁЕФДѓЗжзгРрЮяжЪШчжЌжЪПХСЃЕШЖджзСізщжЏОпгабЁдёадИпЭЈЭИадКЭжЭСєадЁЃетжжЯжЯѓБЛГЦЮЊЪЕЬхСіЕФEPRаЇгІЁЃ ЦфДЮЃЌжзСіЯИАћвЛАуЛсЙ§ЖШБэДявЛаЉдке§ГЃзщжЏЕЭБэДяЛђВЛБэДяЕФЪмЬхЃЌГЃМћЕФШчвЖЫсЪмЬхЁЂзЊЬњЕААзЪмЬхЁЂЩњГЄвжЫиЪмЬхЁЂбЊЙмЛюадГІыФЪмЬхКЭЕЈФвЪеЫѕЫиЪмЬхЕШЁЃСэЭтЃЌдкжзСібЊЙмБэУцвВЛсБэДявЛаЉЬивьадЪмЬхЃЌШчVEGFЪмЬхЃЌећКЯЫиЁЂФкЦЄЯИАћбЁдёЫиЕШЃЌзюНќдкжзСіСмАЭЙмБэУцвВЗЂЯжСЫвЛаЉЬивьадЪмЬхЃЌШчP32ЪмЬхЁЃДЫЭтЃЌгЩгкжзСіЕФЙЉбЊВЛзуЃЌЮоЗЈМАЪБЧхГ§жзСіЯИАћДњаЛВњЩњЕФЫсадЮяжЪЃЌЕМжТжзСізщжЏФкЕФЫсадЛЗОГЃЌАћЭтPHжЕПЩДя6.0ЁЃСэЭтЙЉбЊВЛзувВЛсЕМжТжзСізщжЏЕФОжВПШБбѕЃЌЖјетгжЛсМгОчжзСіЫсадЛЗОГЕФВњЩњЁЃГ§СЫЩЯЪіЬиеї!жзСізщжЏЛЙОпгаИпМфжЪвКбЙЃЌДцдкЬивьадУИКЭбѕЛЏгІМЄЕШЩњРэЬиеїЁЃ
ЖрыФвЛАугЩ 2-50ИіАБЛљЫсзщГЩЃЌгыЕААзжЪВЛЭЌЃЌЖрыФгЩгкЗжзгСПаЁЃЌвђДЫВЛДцдкИпМЖНсЙЙЁЃЖјЧвЖрыФГ§СЫЬьШЛДцдкаЮЪНЭтЃЌЛЙПЩвдНјааЛЏбЇКЯГЩЃЌЪ§СПХгДѓЃЌНсЙЙЖрбљЃЌБШНЯШнвзевЕНжзСіЪмЬхЕФЬивьадХфЬхЖрыФЁЃХфЬхЖрыФгыЪмЬхНсКЯКѓЃЌгыЖрыФСЌНгЕФФЩУздиЬхвЛАуОЪмЬхНщЕМФкЭЬЕФЗНЪННјШыЯИАћЁЃЖрыФгыЪмЬхЕФНсКЯЛсЕМжТОжВПМЊВМЫЙздгЩФмНЕЕЭЃЌМЬЖјОжВПЯИАћФЄАќЙќФЩУзСЃаЮГЩЗтБеФвХнНсЙЙЃЌЭбРыЯИАћФЄНјШыЯИАћжЪЃЌгыЦфЫћФвХнШкКЯаЮГЩФкКЬхЃЌзюжегыШмУИЬхШкКЯЃЌФЩУзСЃдкШмУИЬхФкЗЂЩњНЕНтЛђЬгРыШмУИЬхНјШыЯИАћжЪЁЃжзСіЯИАћБэУцЕФЪмЬхЭЈГЃЗжЮЊФкЛЏЪмЬхгыЗЧФкЛЏЪмЬхСНРрЃЌФкЛЏЪмЬхПЩНщЕМХфЬхФкЛЏНјШыЯИАћЃЌЖјЗЧФкЛЏЪмЬхЕФХфЬхдђжївЊЗжВМдкЯИАћФЄБэУцЃЌЮоЗЈНјШыЯИАћЁЃгЩгквЉЮяжЛгаНјШыЯИАћжЪВХФмЗЂЛгвЉаЇЃЌвђДЫФкЛЏЪмЬхБШЗЧФкЛЏЪмЬхИќЪЪКЯгУзїжзСіАаЯђФЩУзЕнвЉЯЕЭГЕФНщЕМЪмЬхЁЃ
3 ЖрыФНщЕМЕФжзСіАаЯђФЩУзЕнвЉЯЕЭГ
ЖрыФНщЕМЕФжзСіАаЯђжЮСЦдкНќМИФъФкЕУЕНСЫПьЫйЗЂеЙЃЌЪЧжзСіФкПЦжЮСЦЁЂвЉМСбЇСьгђжазюЛюдОЕФбаОПСьгђжЎвЛЃЌЦфОРњСЫЕЅЙІФмАаЯђЁЂЫЋЙІФмАаЯђЁЂжз,СіДЉЭИЁЂЛЗОГЯьгІаЭАаЯђЕШЗЂеЙЙ§ГЬЃЌЯъМћБэ1ЃЌЯТУцНјааж№вЛНщЩмЁЃ
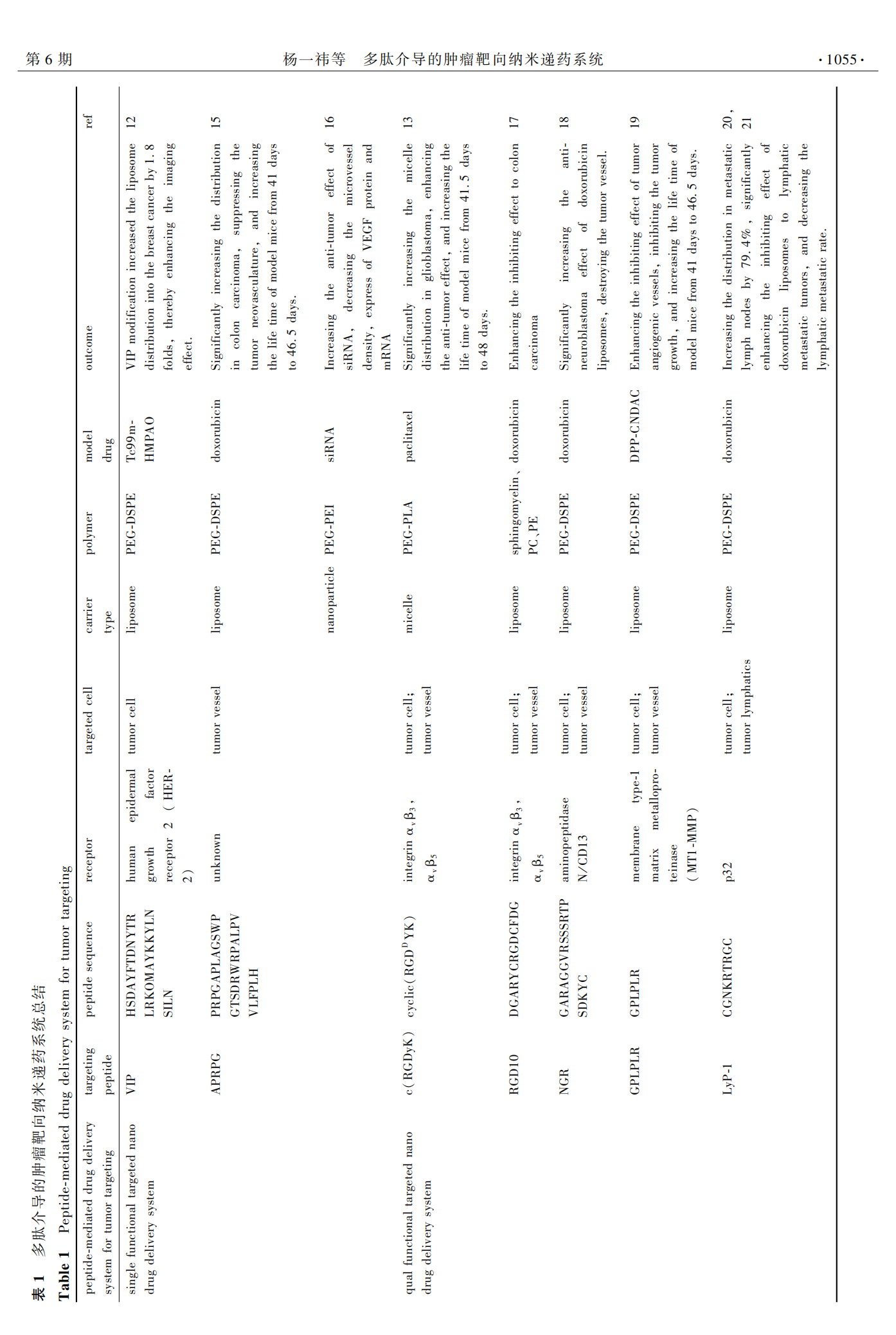
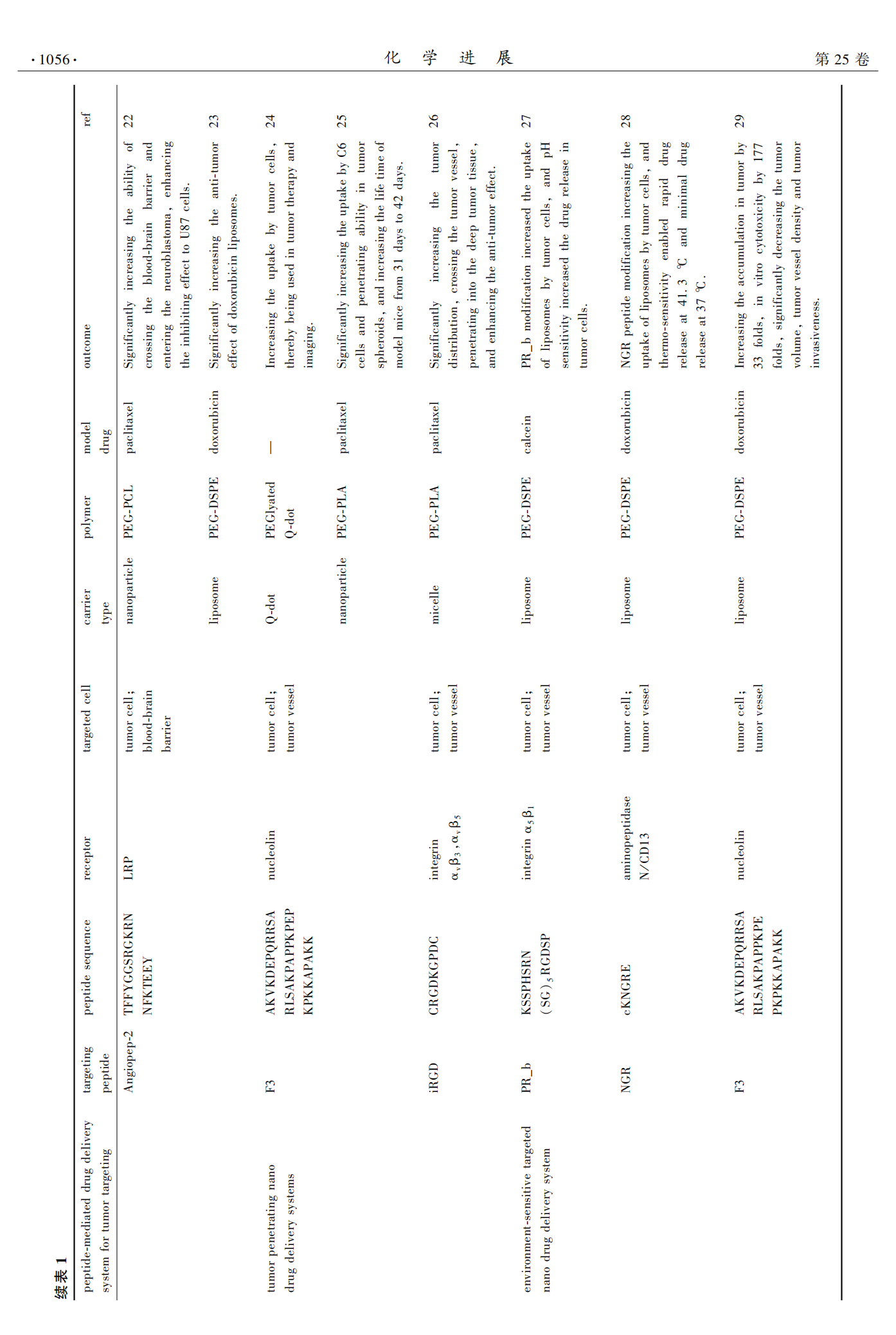
3.1 ЕЅЙІФмАаЯђФЩУзЕнвЉЯЕЭГ
ЕЅЙІФмАаЯђФЩУзЕнвЉЯЕЭГЪЧжИеыЖджзСізщжЏжаЕЅИіАаЕуЕФЕнвЉЯЕЭГЁЃгЩгкжзСізщжЏжажзСіЯИАћЁЂЯИАћЭтЛљжЪЁЂжзСібЊЙмФкЦЄЯИАћЛђжзСіСмАЭЙмФкЦЄЯИАћЕШБэУцОљгаЧјБ№гке§ГЃзщжЏЕФЬивьадЪмЬхБэДяЃЌНЋФмгыИУЪмЬхЬивьадНсКЯЕФАаЯђЗжзгХМКЯЕНЕнвЉЯЕЭГБэУцЃЌЕнвЉЯЕЭГзЂЩфЕНЬхФкКѓЃЌЪзЯШдкEPRаЇгІНщЕМЯТНјШыжзСізщжЏЃЌШЛКѓдкЪмЬхНщЕМзїгУЯТжїЖЏгыАаЯИАћНсКЯЃЌдіМгАаЯИАћЕФвЉЮяЩуШЁСПЃЌЮЊЗРжЙЭјзДФкЦЄЯЕЭГЕФЭЬЪЩЃЌвЛАуВЩгУPEGЛЏЕнвЉЯЕЭГЃЌЪЕЯжвЉЮядкЬхФкЕФГЄбЛЗЁЃР§ШчЃЌдкШЫШщЯйАЉЯИАћЩЯИпБэДявЛжжбЊЙмЛюадГІыФЪмЬхЃЈVIP-RЃЉбаОПепЪЙгУбЊЙмЛюадГІыФЃЈVIPЃЉЃЌвЛжж 28ыФЃЌзїЮЊШщЯйАЉЯИАћАаЯђЗжзгЙВМлаоЪЮЕНжЌжЪЬхБэУцЃЌВЂАќЙќЗХЩфадКЫЫиTc99m-HMPAOЃЌНјааШщЯйАЉЕФЯдЯёеяЖЯЃЌНсЙћЯдЪОЃЌЮоТлжЌжЪЬхЩЯЪЧЗёаоЪЮVIPЃЌЦфдкШщЯйАЉзщжЏЕФЗжВМСПЖМЯджјИпгке§ГЃШщЯйЃЌжЄУїСЫжЌжЪЬхЖдАЉжЂзщжЏЕФБЛЖЏАаЯђадЁЃИќживЊЕФЪЧЃЌVIPаоЪЮЕФжЌжЪЬхдкШщЯйАЉжаЕФЗжВМСПЮЊЮДаоЪЮжЌжЪЬхЕФ1.8БЖЃЌЧвЧАепАаЯђжИЪ§ЃЈШщЯйАЉжаЗжВМСПгые§ГЃШщЯйжаЗжВМСПЕФБШжЕЃЉвВЯджјИпгкКѓепЁЃЯдЪОСЫVIPжЌжЪЬхЖдШщЯйАЉЕФжїЖЏАаЯђадЁЃ
3.2 ЫЋЙІФмАаЯђФЩУзЕнвЉЯЕЭГ
ЕЅЙІФмАаЯђФЩУзЕнвЉЯЕЭГЫфНЯБЛЖЏАаЯђжЮСЦжзСігаСЫКмДѓНјеЙЃЌЕЋЦфЖджзСізщжЏЕФАаЯђадШдВЛРэ:ЯыЃЌПЩ Фм ЕФ д вђ гаЃКЃЈ1ЃЉФЩ Уз Ен вЉ ЯЕ ЭГ Ъз ЯШ вЊ ЭЈ Й§EPRаЇгІНјШыжзСізщжЏЃЌШЛКѓВХФмЗЂЛгАаЯђЗжзгЕФНщЕМзїгУЃЌЕМжТгыжзСіЯИАћЕФНгКЯаЇТЪВЛИпЃЛЃЈ2ЃЉЖдФГаЉЬиЪтВПЮЛЕФжзСіЃЌШчФдВПжзСіЃЌАаЯђаЇТЪЕЭЁЃ ЕнвЉЯЕЭГвЊНјШыФдВПжзСіЪзЯШвЊЯШЭЈЙ§бЊФдЦСеЯЃЈBBBЃЉЛђепбЊФджзСіЦСеЯЃЈBBTBЃЉЃЌетДѓДѓНЕЕЭСЫЦфЖдФджзСіЕФАаЯђаЇТЪЁЃЮЊНјвЛВНдіМгФЩУзЕнвЉЯЕЭГЖджзСізщжЏЕФАаЯђадЃЌбаОПепЩшМЦСЫЖржжЫЋЙІФмАаЯђФЩУзЕнвЉЯЕЭГЃЌвЛАуВЩгУФмЭЌЪБАаЯђСНИіАаЕуЕФЖрыФЗжзгЛђепВЩгУСНИіАаЯђВЛЭЌАаЕуЕФЖрыФЗжзгЭЌЪБаоЪЮдкФЩУздиЬхБэУцЙЙНЈЖјГЩЁЃФПЧАГЃМћЕФЫЋЙІФмАаЯђФЩУзЕнвЉЯЕЭГгавдЯТШ§РрЁЃ
3.2.1 жзСібЊЙм/жзСіЯИАћЫЋЙІФмАаЯђФЩУзЕнвЉЯЕЭГ
ДѓСПбаОПБэУїЃЌдкжзСібЊЙмБэУцБэДягавЛаЉЧјБ№гке§ГЃбЊЙмЕФЬивьадЪмЬхЃЌЭЈГЃетаЉЪмЬхвВЭЌЪБдкжзСіЯИАћБэУцИпБэДяЃЌШчећКЯЫиЁЂКЫШЪЕААзЕШЃЌВЩгУЦфХфЬхЖрыФаоЪЮЕФФЩУзЕнвЉЯЕЭГОпгаЭЌЪБАаЯђжзСібЊЙмКЭжзСіЯИАћЕФЙІФмЁЃЖджзСібЊЙмЕФАаЯђадПЩдіМгЕнвЉЯЕЭГдкжзСібЊЙмИННќЕФжЭСєСПЃЌДгЖјдіМгЦфНјШыжзСізщжЏЕФЗжВМСПЃЌНјЖјдкжзСіЯИАћБэ Уц Ъм Ьх ЕФ Нщ ЕМ ЯТ ЗЂ Лг ПЙ жз Сі ЯИ Аћ Щњ ГЄ зїгУЁЃР§ШчЃЌRGDыФЃЌвЛРрКЌгаОЋАБЫс-ИЪАБЫс-ЬьЖЌАБЫсЃЈArg-Gly-AspЃЉЕФЖЬыФЃЌЪЧећКЯЫиЕФвЛжжХфЬхЖрыФЁЃZhanЕШжЦБИСЫRGDаоЪЮЕФзЯЩМДМНКЪјгУгкЩёОНКжЪСіЕФАаЯђжЮСЦЃЌгыЮДаоЪЮНКЪјЯрБШЃЌЦфЖдU87ЩёОНКжЪСіЯИАћЕФЬхЭтЩњГЄвжжЦзїгУЬсИпСЫ2.5БЖЃЌдкЬхФкЩёОНКжЪСізщжЏЗжВМЯджјдіМгЃЌВЂНЋ КЩ Сі Ту Ъѓ ЕФ Щњ Дц жм Цк Дг41.5Ьь бг ГЄ жС48ЬьЁЃ
3.2.2 жзСіСмАЭЙм/жзСіЯИАћЫЋЙІФмАаЯђФЩУзЕнвЉЯЕЭГ
жзСізщжЏжажзСіСмАЭЙмЕФЩњГЩЖджзСіЗЂЩњСмАЭзЊвЦЦ№зХМЋДѓДйНјзїгУЃЌбаОПБэУїдкжзСіСмАЭЙмКЭжзСіЯИАћБэУцБэДягавЛаЉЙВгаЕФЬивьадЪмЬхЃЌРћгУЦфХфЬхаоЪЮЕФФЩУзЕнвЉЯЕЭГОпгаЭЌЪБЩБЩЫжзСіЯИАћКЭЦЦЛЕжзСіСмАЭЙмЕФзїгУЃЌДгЖјвжжЦжзСіЩњГЄВЂвжжЦжзСіЗЂЩњСмАЭзЊвЦЁЃШчp32ЪмЬхЪЧБэДядкЖржжжзСіЯИАћКЭжзСіСмАЭЙмЩЯЕФЪмЬхЃЌLyP-1ЮЊЦфХфЬхЖрыФЁЃYanЕШжЦБИСЫLyP-1аоЪЮЕФАЂЫижЌжЪЬхгУгкСмАЭзЊвЦжзСіЕФАаЯђжЮСЦЃЌЪЕбщНсЙћЯдЪОЃЌЦфЭЌЪБОпгаАаЯђжзСіЯИАћКЭжзСіСмАЭЙмЕФЙІФмЃЌгыЮДаоЪЮжЌжЪЬхЯрБШЃЌЦфЖдСмАЭзЊвЦжзСіЕФвжжЦаЇЙћЯджјдіЧПЃЌВЂЯджјНЕЕЭСЫжзСіЕФСмАЭзЊвЦТЪЃЌЪЙСмАЭНсзЊвЦТЪДг33.3%НЕЕЭЮЊ16.7%ЃЌїФСмАЭНсзЊвЦТЪДг66.7%НЕЕЭЮЊ0
3.2.3 бЊФдЦСеЯ/жзСіЯИАћЫЋЙІФмАаЯђФЩУзЕнвЉЯЕЭГ
BBBЕФДцдкПЩЮЌГжФдзщжЏжаЮЂЛЗОГЕФЮШЖЈЃЌЕЋвВЕМжТСЫ100%ЕФДѓЗжзгвЉЮявдМА98%ЕФаЁЗжзгвЉЮяФбвдШыФдЃЌДгЖјЪЙФдВПМВВЁЕФвЉЮяжЮСЦГЩЮЊвЛДѓФбЬтЁЃФЩУзЕнвЉЯЕЭГНјШыФдВПжзСіЪзЯШашвЊПчдНBBBШыФдЃЌШЛКѓдйНјШыФджзСіЁЃBBBАаЯђЕнвЉЯЕЭГПЩдіМгвЉЮяШыФдСПЃЌЕЋЖдФджзСіЮожїЖЏбЁдёадЃЌЖјФджзСіЯИАћЕЅЙІФмАаЯђЕнвЉЯЕЭГдђФбвдПчдНBBBШыФдЁЃНЋBBBАаЯђЗжзгКЭжзСіЯИАћАаЯђЗжзгЭЌЪБаоЪЮЛђепНЋBBBКЭжзСіЯИАћЕФЙВЭЌАаЯђЗжзгаоЪЮЕНФЩУзЕнвЉЯЕЭГБэУцЙЙНЈЕФЫЋЙІФм(ЫЋМЖ)АаЯђЕнвЉЯЕЭГПЩОпгаПчдНBBBКЭАаЯђжзСіЯИАћЕФЫЋжиЙІФмЁЃдіМгЖдФдВПжзСіЕФАаЯђадЁЃШчЕЭУмЖШжЌЕААзЃЈLRPЃЉЪЧвЛжжBBBКЭЩёОНКжЪСіЯИАћБэУцЕФЙВгаЪмЬхЃЌбаОПепНЋЦфХфЬхЖрыФAngiopep-2аоЪЮЕНзЯЩМДМФЩУзСЃБэУцгУгкЩёОНКжЪСіЕФАаЯђжЮСЦЃЌAngiopep-2ЕФаоЪЮдіМгСЫФЩУзСЃдкФдВПКЭЩёОНКжЪСіЕФЗжВМСПЃЌВЂЪЙзЯЩМДМФЩУзСЃЖджзСіЕФЩњГЄвжжЦТЪДг36.1%ЬсИпжС65.6%ЃЌЪЙКЩФдСіТуЪѓЕФЩњДцжмЦкДг30ЬьбгГЄжС37ЬьЁЃ
3.3 жзСіДЉЭИФЩУзЕнвЉЯЕЭГ
ЧАСНРржзСіАаЯђФЩУзЕнвЉЯЕЭГДѓДѓЭЦНјСЫжзСіАаЯђжЮСЦЕФбаОПНјГЬЃЌЕЋЪЧЃЌДгЦфОВзЂИјвЉШыбЊЕНгыжзСіЯИАћЗЂЩњНгКЯЕФЙ§ГЬжаЃЌШдЪмЕНСНДѓЦСеЯЕФжЦдМЁЊЁЊжзСібЊЙмЦСеЯКЭжзСіЛљжЪЦСеЯЁЃжзСібЊЙмЦСеЯЪЧжИгЩгкбЊЙмБкЕФДцдкЃЌбЊЙмБкПзОЖДѓаЁВЛвЛЃЌжзСіФкИпМфжЪвКбЙЕШвђЫиЕМжТЕФЕнвЉЯЕЭГДгбЊЙмПчбЊЙмБкНјШыжзСіетвЛЙ§ГЬгіЕНЕФеЯАЁЃжзСіЛљжЪЦСеЯЪЧжИгЩгкжзСіздЭтжмЯђжааФж№НЅдіИпЕФМфжЪвКбЙЁЂжзСіМфжЪЯЫЮЌзшжЭЕШвђЫиЕМжТЕФЕнвЉЯЕЭГДгжзСібЊЙмИННќДЉЙ§жзСіМфжЪНјШыжзСізщжЏФкВПетвЛЙ§ГЬгіЕНЕФеЯАЁЃ габаОПБэУїЃЌетСНДѓЦСеЯЕФДцдкЪЙПЙ жз Сі вЉ дк жз Сі Фк зю дЖ Ні Фм ЕН Дя Ор Ры бЊ Йм40-50um(ЯрЕБгкдМ10ИіЯИАћжБОЖ)ЕФЮЛжУЃЌДѓВПЗжжзСіЯИАћдђЮоЗЈНгДЅЕНвЉЮяЁЃзюНќгабаОПепЭЈЙ§ЖрыФЩИбЁММЪѕЩИбЁГівЛРрОпгажзСібЊЙмДЉЭИадКЭжзСізщжЏДЉЭИадЕФЖрыФЃЌетРрЖрыФПЩНщЕМгыЦфЙВМлСЌНгЕФвЉЮяЗжзгЛђФЩУзЕнвЉЯЕЭГДЉЭИжзСібЊЙмБкВЂЩјЭИНјШыжзСіФкВПЃЌЗжВМЕНећИіжзСізщжЏжаЃЌетРрЖрыФБЛГЦЮЊ"жзСіДЉЭИыФ"ЁЃжзСіДЉЭИыФаоЪЮЕНФЩУзЕнвЉЯЕЭГБэУцМДПЩЙЙНЈГЩЮЊжзСіДЉЭИФЩУзЕнвЉЯЕЭГЁЃ ШчгаБЈЕРЯдЪОЭЈЙ§ЪЩОњЬхеЙЪОММЪѕЩИбЁГіЕФRGDбмЩњЖрыФiRGDЃЌГ§СЫОпгаДЋЭГRGDыФЖджзСібЊЙмКЭжзСіЯИАћАаЯђадЕФЬиЕуЭтЃЌЛЙОпгаДЉЭИжзСібЊЙмКЭжзСізщжЏЕФФмСІЃЛДЋЭГRGDЖрыФжЛФмНЋЕнвЉЯЕЭГАаЯђжСжзСібЊЙмДІЃЌЖјiRGDЖрыФдђФмНщЕМЕнвЉЯЕЭГДЉЭИбЊЙмВЂЩјЭИНјШыжзСізщжЏФкВПЃЌКѓепдкжзСіВПЮЛЕФХЈЖШПЩДяЧАепЕФ10БЖЃЌвжжЦжзСіЩњГЄЕФзїгУвВгаЯджјЬсИпЁЃФПЧАжзСіДЉЭИФЩУзЕнвЉЯЕЭГвбБЛГЩЙІгІгУгквШЯйАЉЁЂШщЯйАЉЁЂКЭЧАСаЯйАЉЕШжзСіЕФАаЯђжЮСЦЁЃ
3.4 ЛЗОГЯьгІаЭАаЯђФЩУзЕнвЉЯЕЭГ
ЩЯЪіМИРрФЩУзЕнвЉЯЕЭГЭЈЙ§БэУцаоЪЮАаЯђЖрыФЃЌКмКУЕиЪЕЯжСЫЯђжзСізщжЏЕФгааЇАаЯђЕнвЉЃЌЕЋЪЧдкжзСіВПЮЛЕФвЉЮяЪЭЗХШдДцдкЮЪЬтЁЃКмЖрФЩУзЕнвЉЯЕЭГдкжзСіВПЮЛФбвдгааЇЪЭЗХвЉЮяЃЌЛђепдкжзСіЯИАћФкЪЭвЉЪБМфЁЂЫйТЪЛђЗНЪНВЛЕБЃЌдьГЩСЫвЉЮяЕЭаЇЛђепРЫЗбЁЃгЩгкжзСіВПЮЛОпгагыЧјБ№гке§ГЃзщжЏЕФЮЂЛЗОГЃЌШчЕЭPHЁЂЮТЖШНЯИпЁЂШБбѕЁЂДцдкЬивьадУИЕШЁЃжзСіЮЂЛЗОГЯьгІаЭЕнвЉЯЕЭГдкЙ§ШЅЖўЪЎФъРявбгаНЯДѓНјеЙЃЌбаОПжївЊМЏжагкPHУєИагыЮТЖШУєИааЭЯЕЭГЃЌНЋетаЉЕнвЉЯЕЭГБэУцаоЪЮжзСіАаЯђЖрыФЗжзгКѓЃЌЙЙНЈГЩЛЗОГЯьгІаЭАаЯђФЩУзЕнвЉЯЕЭГЃЌПЩЪЙЦфЭЌЪБОпгажзСіжїЖЏАаЯђадФмКЭжзСіЮЂЛЗОГУєИаадФмЃЌИФЩЦвЉЮяЪЭЗХааЮЊЃЌЬсИпвЉаЇЁЃ
3.4.1 PHУєИааЭАаЯђФЩУзЕнвЉЯЕЭГ
КмЖрФЩУзЕнвЉЯЕЭГдкжзСізщжЏжаЪЭвЉЫйТЪЙ§Т§ЃЌЛђепгааЉвЉЮядкЧПЫсЛЗОГжаВЛЮШЖЈЁЂвзЪЇЛюЁЃЭЈЙ§ЩшМЦPH-УєИааЭФЩУзЕнвЉЯЕЭГЃЌЪЙЦфдкШѕЫсадЛЗОГжаБфЕУВЛЮШЖЈЃЌДгЖјдкжзСіЯИАћМфвКЁЂФкКЬхЛђепдчЦкШмУИЬхжаМгЫйЪЭЗХвЉЮяЃЌдіМгвЉЮяЪЭЗХСПЃЌВЂБЃжЄЦфдкЕНДяЭэЦкШмУИЬхЧАНЋФкШнЮяЪЭЗХЕНЯИАћжаЃЌзюДѓЯоЖШЕиБЃГжвЉЮяЛюадЁЂдіЧПвЉаЇЁЃИУРрЕнвЉЯЕЭГвбв§Ц№баОПепКмДѓЕФаЫШЄЁЃGargЕШбЁгУдкжзСіЯИАћКЭжзСібЊЙмБэУцЬивьадБэДяЕФећКЯЫиa5B1ЕФАаЯђЖрыФЗжзгPR_bаоЪЮЕНPHУєИаОлввЖўДМЛЏжЌжЪЬхБэУцЃЌPR_b ЕФаоЪЮДѓДѓдіМгСЫжЌжЪЬхБЛжзСіЯИАћЕФЩуШЁЃЌPHУєИаадФмЕФМгШыгждіМгСЫЦфдкжзСіЯИАћФкЕФвЉЮяЪЭЗХЫйТЪЁЃMouraЕШНЋжзСіДЉЭИыФF3аоЪЮЕН PHУєИааЭжЌжЪЬхБэУцЙЙНЈСЫPHУєИааЭАаЯђжЌжЪЬхЃЌЦфдкЬхФкжзСіВПЮЛаюЛ§СПЪЧЦеЭЈжЌжЪЬхЕФ 11 БЖЃЌЪЙАЂУЙЫиЖджзСіЯИАћКЭФкЦЄЯИАћЕФЯИАћЖОадЗжБ№ЬсИпСЫ177КЭ 162БЖЃЌВЂЯджјНЕЕЭСЫжзСіДѓаЁЁЂбЊЙмУмЖШКЭжзСіЧжЯЎадЁЃ
3.4.2 ЮТЖШУєИааЭАаЯђФЩУзЕнвЉЯЕЭГ
ЮТЖШУєИааЭЕнвЉЯЕЭГЪЧжИЭЈЙ§ЮТЖШБфЛЏРДПижЦвЉЮяЪЭЗХЕФЕнвЉЯЕЭГЁЃДѓВПЗжЪЕЬхСіЖМБШжмЮЇЕФе§ГЃзщжЏЮТЖШИпЃЌРћгУИУдРэЩшМЦЮТЖШУєИааЭЕнвЉЯЕЭГПЩдіМгЕнвЉЯЕЭГдкжзСіВПЮЛЕФвЉЮяЪЭЗХЃЌдйећКЯжзСіжїЖЏАаЯђадФмЃЌМДПЩЙЙНЈГЩЮЊЮТЖШУєИааЭАаЯђФЩУзЕнвЉЯЕЭГЁЃNegussieЕШЙЙНЈЕФЛЗзДNGRЖрыФаоЪЮЕФЮТЖШУєИааЭжЌжЪЬхЃЌПЩжїЖЏЪЖБ№жзСібЊЙмЛђепжзСіЯИАћБэУцИпБэДяЕФCD13/АБыФУИNЪмЬхЖј БЛ Щу ШЁ Нј Шы ЯИ АћЁЃ вЉ Юя Ьх Эт ЪЭ ЗХ Ъд бщ Яд ЪОNGRЖрыФаоЪЮЕФЮТЖШУєИааЭжЌжЪЬхдк41.3ЩуЪЯЖШЪБПЩПьЫйЪЭЗХвЉЮяЃЈ4SФкЪЭЗХГЌЙ§ 75%ЃЉЖјдк37ЩуЪЯЖШдђЪЭЗХМЋЩйЁЃ
4 ЖрыФНщЕМжзСіАаЯђЕнвЉЯЕЭГЕФгХЪЦгыВЛзу
гыгЮРывЉЮяКЭжзСіБЛЖЏАаЯђЕнвЉЯЕЭГЯрБШЃЌЖрыФНщЕМЕФжзСіАаЯђЕнвЉЯЕЭГгЩгкПЩжїЖЏЪЖБ№жзСізщжЏЬивьадИпБэДяЕФЪмЬхЖјЯдЪОГіИќКУЕФжзСіАаЯђадЃЌЦфдкжзСізщжЏжЭСєСПКЭжзСіЯИАћЩуШЁСПОљПЩЯджјдіМгЁЃСэЭтЃЌЦфдкПЫЗўжзСіЖрвЉФЭвЉадЗНУцвВЯдЪОГівЛЖЈгХЪЦЁЃгыАаЯђЗжзг-вЉЮяХМКЯЮяЯрБШЃЌЖрыФНщЕМЕФжзСіАаЯђЕнвЉЯЕЭГОпгаАаЯђИпаЇадЕФгХЪЦЁЃЧАепвЛИіАаЯђЗжзгжЛПЩНЋвЛИівЉЮяЗжзгАаЯђжСАаЯИАћЃЌЖјКѓепЦНОљвЛИіАаЯђЗжзгПЩаЏДјДѓСПвЉЮяЗжзгАаЯђжСАаЯИАћЃЌАаЯђЗжзгРћгУТЪЕУЕНМЋДѓЬсИпЁЃгыЕЅПЫТЁПЙЬхНщЕМЕФжзСіАаЯђЕнвЉЯЕЭГЯрБШЃЌЖрыФНщЕМЕФжзСіАаЯђЕнвЉЯЕЭГОпгавзжЦБИЁЂЕЭУтвпдадЁЂЮШЖЈадКУКЭвзДЋЫЭЕШгХЪЦЁЃгЩгкЖрыФЗжзгСПБШЕЅПЙЕЭ1ЁЊЁЊ2ИіЪ§СПМЖЃЌЛљБОВЛДцдкЕААзжЪИпМЖНсЙЙЃЌЖджЦБИЙЄвеЕФвЊЧѓЃЈШчГЌЩљ.ИпЮТ.гаЛњШмМСЕШЃЉдЖЕЭгкЕЅПЙЁЃСэЭтгЩгкЖрыФЗжзгСПЕЭЃЌЫљвдЖрыФНщЕМЕФЕнвЉЯЕЭГдкЬхФкПЩЛљБОБмУтЕЅПЙЫљУцСйЕФИпУтвпдадЕФЮЪЬтЃЌВЂЧвБЛЭјзДФкЦЄЯЕЭГЪЖБ№ЧхГ§ИХТЪЕЭЁЂвзгкдкжзСізщжЏФкДЋЕнЩјЭИЁЃ
ЖрыФНщЕМЕФФЩУзЕнвЉЯЕЭГШдДцдквдЯТвЛаЉВЛзуЁЃЫфШЛФЩУзЕнвЉЯЕЭГОЖрыФаоЪЮКѓПЩИГгшЦфжзСіжїЖЏАаЯђадФмЃЌЕЋЪЧетвВдіМгСЫЦфБЛЭјзДФкЦЄЯЕЭГЕФВЖЛёМИТЪЃЌвђДЫЭљЭљЖрыФаоЪЮЕФЕнвЉЯЕЭГдкИЮдрЁЂЦЂдрЕФЗжВМДѓгкЮДаоЪЮЕнвЉЯЕЭГЃЌГЄЦкИјвЉвздьГЩЖдИЮЦЂЙІФмЕФЫ№КІЁЃжзСібЊЙмЕФПзЯЖТЪКЭДѓаЁЫцзХжзСіРраЭКЭЗЂВЁЮЛжУЕФВЛЭЌЖјВЛЭЌЃЛжзСізщжЏБэДяЕФЬивьадЪмЬхвВОГЃБэЯжГіИіЬхВювьадЃЌЩѕжСЭЌвЛИіЬхЕФВЛЭЌЮЛжУЁЂВЛЭЌНзЖЮЕФжзСівВДцдкВювьЃЌМДжзСізщжЏДцдквьжЪадЃЌетДѓДѓдіМгСЫЖрыФНщЕМЕнвЉЯЕЭГЗЂЛгвЉаЇЕФВЛШЗЖЈадЁЃСэЭтФПЧАЫљВЩгУЕФАаЯђЖрыФЗжзгМИКѕШЋВПЮЊLаЭЖрыФЃЌЖјЬхФкДцдкЖржжРраЭЕФЖрыФНЕНтУИЃЌвђДЫКмЖрАаЯђЗжзгдкЬхФквзБЛНЕНтЃЌЕМжТЕнвЉЯЕЭГЪЇШЅАаЯђадФмЁЃДЫЭтЃЌШчБэ1ЫљЪОЃЌЫфШЛЖрыФЕФаоЪЮПЩВЛЭЌГЬЖШЕидіМгФЩУзЕнвЉЯЕЭГЖджзСіЕФАаЯђаЇТЪЃЌЕЋЪЧЦфдкжзСіВПЮЛЕФОјЖдЗжВМСПШдКмЕЭЃЌШчVIPаоЪЮЕФжЌжЪЬхдкжзСіВПЮЛЕФЗжВМСПНіеМзмИјвЉСПЕФ0.2%ЃЌвђДЫЖрыФНщЕМЕФжзСіАаЯђФЩУзЕнвЉЯЕЭГШдгаД§НјвЛВНбаОПЃЌвдЬсИпЦфАаЯђаЇТЪЁЃ
5 змНсКЭеЙЭћ
ОЙ§баОПШЫдБЕФВЛаИХЌСІЃЌЖрыФНщЕМЕФжзСіАаЯђФЩУзЕнвЉЯЕЭГЯђзХЖрЙІФмЁЂжЧФмЛЏЕФЗНЯђЗЂеЙЃЌвбШЁЕУСЫКмЖрбаОПГЩЙћЃЌдкжзСіЕФАаЯђеяЖЯКЭжЮСЦЗНУцЯдЪОГіКмДѓЕФгІгУЧБСІЁЃЕЋЪЧгЩгкжзСіЕФЬиЪтадКЭИДдгадЃЌЯжгаЕФЕнвЉЯЕЭГШдЮоЗЈПЫЗўЬхФкДЋЕнЙ§ГЬжагіЕНЕФЫљгаЦСеЯВЂИпаЇвжжЦжзСіЩњГЄЁЃ
вЛЗНУцЃЌДг"ЪБМф" НЧЖШРДНВЃЌЕнвЉЯЕЭГДгИјвЉЕНЗЂЛгвЉаЇЕФећИіЬхФкЙ§ГЬУцСйЖржиЦСеЯЃЌАќРЈдкбЛЗЯЕЭГЁЂжзСізщжЏКЭАаЯИАћШ§ИіДЋЕнЙ§ГЬЕФЦСеЯЁЃШчдкбЛЗЯЕЭГжаУцСйЭјзДФкЦЄЯЕЭГЭЬЪЩЁЂУИНЕНтЕШЦСеЯЃЌдкжзСізщжЏДЋЕнЙ§ГЬжаУцСйжзСібЊЙмБкЁЂжзСіЛљжЪзшАЁЂИпМфжЪвКбЙЕШЦСеЯЃЌдкАаЯИАћДЋЕнЙ§ГЬжаУцСйЯИАћЩуШЁЁЂШмУИЬхЬгвнЁЂвЉЮяЪЪЪБЪЭЗХЕШЦСеЯЃЌФПЧАОјДѓВПЗжбаОПОљжЛжТСІгкНтОіЦфжавЛжжЛђМИжжЦСеЯЮЪЬтЁЃЕЋЪЧЃЌжзСіАаЯђжЮСЦЕФзюжеЪЕЯжЃЌашвЊЭЌЪБНтОіЕнвЉЙ§ГЬжаЫљгіЕНЕФЫљгаЦСеЯЁЃ
СэвЛЗНУцЃЌДг"ПеМф"НЧЖШРДНВЃЌжзСіЯИАћВЂВЛЪЧЙТСЂДцдкЕФЃЌжзСіЮЂЛЗОГЖдгкжзСіЕФЩњГЄгызЊвЦгаМЋДѓгАЯьЃЌШчжзСіИЩЯИАћЁЂжзСіаТЩњбЊЙмЁЂжзСіаТЩњСмАЭЙмЁЂжзСіЯрЙиОоЪЩЯИАћЁЂЯИАћЭтЛљжЪЕШЃЌетаЉЖМЪЧжзСіЗЂЩњЁЂЗЂеЙКЭзЊвЦЕФ"ЩњЬЌбЇ"вђЫиЁЃ етаЉвђЫигыАЉЯИАћЯрБШЃЌзмЬхРДЫЕвХДЋНЯЮШЖЈЃЌОпгаКмЩйЕФФЭвЉадВњЩњПЩФмЁЃ ЦЦЛЕжзСіЩњГЄЗЂеЙЫљвРРЕЕФЮЂЛЗОГЃЌЖдЪЕЯжжзСіЕФАаЯђжЮСЦжСЙиживЊ
злЩЯЃЌеыЖдФПЧАжзСіАаЯђФЩУзЕнвЉЯЕЭГгіЕНЕФРЇОГЃЌЮв УЧ Ьс Гі вЛ жж аТ аЭ жз Сі Аа Яђ Ен вЉ Вп ТдЁЊЁЊ"ЯЕЭГадАаЯђ"ВпТдЃЌЗЂеЙ"ЯЕЭГадАаЯђ"ФЩУзЕнвЉЯЕЭГЃЌЪЙЦфОпгаШчЯТЙІФмЃКДг"ЪБМф"НЧЖШЩЯЃЌФмдкЬхФкЮШЖЈДцдкВЂПЫЗўЬхФкВуВуЦСеЯНјШыАаВПЮЛИпаЇЪЭЗХвЉЮяЃЛДг"ПеМф"НЧЖШЩЯЃЌдкАаЯђЩБЩЫжзСіЯИАћЕФЭЌЪБЃЌЦЦЛЕЦфРЕвдЩњДцЕФжзСіЮЂЛЗОГЃЌзюжеЪЕЯжЖджзСіЕФ"ЯЕЭГадАаЯђ"жЮСЦЁЃЦфПЩФмЕФЪЕЯжЭООЖгавдЯТШ§жжЁЃ
ЃЈ1ЃЉЙІФмећКЯ ЖдДЋЭГФЩУзЕнвЉЯЕЭГНјааЙІФмЛЏаоЪЮЃЌНЋЕнвЉЯЕЭГЕФПеМфЮШЖЈадЁЂАаЯђЖрыФЮШЖЈадЁЂжзСібЊЙмБкКЭжзСіЛљжЪЩјЭИадЁЂжзСіЛЗОГУєИаадЁЂАаЯИАћАаЯђадЕШЖржжЙІФмећКЯЕНвЛжжЕнвЉЯЕЭГЃЌЪЙЦфОпгаЭЌЪБПчдНЖржжЕнвЉЦСеЯЕФФмСІЃЛЭЌЪБЃЌНЋПЙжзСіЯИАћЁЂжзСіИЩЯИАћЁЂжзСібЊЙм/ kСмАЭЙмЕШЕФвЉЮяЭЌЪБАќдидкЕнвЉЯЕЭГжаЃЌЪЙЦфОпгаЩБЩЫжзСіЯИАћВЂЦЦЛЕжзСіЮЂЛЗОГЕФФмСІЁЃ
ЃЈ2ЃЉ СЊКЯИјвЉ ЭЈЙ§аоЪЮВЛЭЌАаЯђЗжзгАќдиВЛЭЌвЉЮяЗжБ№жЦБИеыЖджзСізщжЏжажзСіЯИАћЃЌжзСіИЩЯИАћЁЂжзСібЊЙм /kСмАЭЙмЕШВЛЭЌАаЯИАћЕФАаЯђФЩУзЕнвЉЯЕЭГЃЌВЂИГгшЭЌЪБПчдНЖржжЕнвЉЦСеЯЕФФмСІЃЌНЋетаЉЕнвЉЯЕЭГСЊКЯИјвЉЁЃ
ЃЈ3ЃЉаТаЭЖрЙІФмВФСЯЩшМЦ ЭЈЙ§КЯРэЛЏЩшМЦЃЌжЦБИГіОпгаЭЌЪБПчдНЖржжЕнвЉЦСеЯФмСІЕФЖрЙІФмВФСЯЃЌжЦБИЕнвЉЯЕЭГЁЃШчгабаОПепЩшМЦСЫвЛжжНсЙЙМђЕЅ ЕЋ Оп га Нє Ум Аќ ЙќsiRNAЁЂШм УИ Ьх Ьг внЁЂЪЭ ЗХsiRNAЕНЯИАћжЪЁЂЮоЖОНЕНтЕШЖржжЙІФмгквЛЬхЕФаТВФСЯЃЌШєЖдЦфНјааНјвЛВНгХЛЏЃЌгаЭћжЦБИГіНсЙЙМђЕЅЙІФмЖрбљЕФаТаЭВФСЯгыФЩУздиЬхЁЃ
ЩЯЪіШ§жжЭООЖжаЃЌЕквЛжжЭООЖЪЧЭЈЙ§ећКЯПчдНЖржжЕнвЉЦСеЯЕФЙІФмЃЌВЂАќдиЖржжвЉЮяЃЌжЦБИГіЖрЙІФмЖрАаБъЕФвЛжжЕнвЉЯЕЭГЃЌДЫЕнвЉЯЕЭГНсЙЙИДдгЃЌжЦБИЗБЫіЃЌНЯФбЪЕЯжЃЌВЂЧввздьГЩАаЯђЗжзгКЭвЉЮяЕФРЫЗбЃЛЕкЖўжжЭООЖПЩеыЖдВЛЭЌАаЯИАћЗжБ№жЦБИВЛЭЌАаЯђЗжзгКЭвЉЮяЕФЕнвЉЯЕЭГЃЌСЊКЯИјвЉЃЌДЫЗНЗЈПЩааадДѓДѓдіМгЃЌЕЋЖдУПжжЕнвЉЯЕЭГНјааЙІФмећКЯШдНЯФбЪЕЯжЃЛЕкШ§жжЭООЖЬсЙЉЕФВФСЯжЦБИМђЕЅЃЌЙІФмЖрбљЃЌЕЋЪЧЦфКЯРэЛЏЩшМЦНЯРЇФбЃЌашвЊПЦбаШЫдБЕФНјвЛВНХЌСІЁЃ"ЯЕЭГадАаЯђ"етвЛФПБъЕФЪЕЯжШЮжиЕРдЖЃЌашвЊжзСібЇЁЂЗжзгЩњЮябЇЁЂЯИАћЩњЮябЇЁЂВФСЯбЇЁЂвЉМСбЇЕШбЇПЦИїСьгђПЦбаШЫдБЕФЙВЭЌХЌСІЁЃжзСіЗЂЩњЗЂеЙЕФЛњжЦашвЊЩюШыбаОП!ЗЂЯжЬивьадИпЕФаТаЭжзСіБъжОЮяЃЌЮЊжзСіАаЯђЕнвЉЯЕЭГЕФЩшМЦЬсЙЉРэТлЛљДЁЃЛеыЖджзСіАаЕуЃЌРћгУМЦЫуЛњИЈжњЩшМЦЛђЪЩОњЬхеЙЪОММЪѕЕШЩИбЁГіжїЖЏЪЖБ№ФмСІЧПЁЂЮШЖЈадКУЁЂзщжЏЩјЭИадЧПЕФАаЯђЗжзгЃЛеыЖджзСіЯИАћКЭжзСіЮЂЛЗОГЬиЕуЃЌЩшМЦНсЙЙМђЕЅЁЂЖджзСіЛЗОГОпгаИпЯьгІадФмЕФжЧФмЛЏаТВФСЯЃЛРћгУаТВФСЯЩшМЦжЦБИГіЖрЙІФмЁЂжЧФмЛЏЕФжзСіАаЯђЕнвЉЯЕЭГЃЛЖдФЩУзЕнвЉЯЕЭГгыЩњЮяЬхжЎМфЕФЯрЛЅзїгУНјааЯЕЭГЛЏбаОП!АќРЈФЩУзЕнвЉЯЕЭГдкЬхФкбЊвКЃЌжзСізщжЏКЭЯИАћФкЕФЖЏСІбЇааЮЊЃЌвдевГіФЩУзЕнвЉЯЕЭГвдМАЩњЮяЬхжагАЯьвЉаЇЗЂЛгЕФИїИівђЫиЃЌЗЂЯжИївђЫижЎМфЕФЯрЛЅЙиСЊвдМАЯожЦЦфЗЂЛгвЉаЇЕФЙиМќЯоЫйвђЫиЕШЃЌетаЉЪ§ОнЖдЁАЯЕЭГадАаЯђЁБЕФЪЕЯжжСЙиживЊЃЌПЩДѓДѓМђЛЏ"ЯЕЭГадАаЯђ"ЕнвЉЯЕЭГЫљБиашЕФЙІФмЃЌЮЊЦфЩшМЦЬсЙЉПЦбЇжИЕМЁЃФЩУзЕнвЉЯЕЭГгыЩњЮяЬхжЎМфЯрЛЅзїгУЕФбаОПШБЗІвВЪЧФПЧАжЦдМжзСіАаЯђФЩУзЕнвЉЯЕЭГЗЂеЙЕФживЊдвђЃЌШдашвЊДѓСІПЊеЙЯрЙиЕФбаОПЁЃЯраХЫцзХЯрЙибЇПЦСьгђКЭЖрбЇПЦНЛВцЕФЗЂеЙЃЌЮвУЧЛсЩшМЦжЦБИГіИќЮЊЖрЙІФмЁЂжЧФмЛЏЕФЁЂЯЕЭГадАаЯђ"ФЩУзЕнвЉЯЕЭГ"ЃЌЪЕЯжЖджзСіЕФИпаЇАаЯђжЮСЦЁЃ
Утд№ЩљУїЃКБОЮФЮЊаавЕНЛСїбЇЯАЃЌАцШЈЙщдзїепМАддгжОЫљгаЃЌШчгаЧжШЈЃЌПЩСЊЯЕЩОГ§ЁЃЮФеТБъзЂгазїепМАЮФеТГіДІЃЌШчашдФЖСдЮФМАВЮПМЮФЯзЃЌПЩдФЖСддгжОЁЃ




