
’Σ“Σ …ζΈοΖ÷Ή”Ή‘ΉιΉΑΕ‘…ζΈοΧε”–÷Ί“Σ“β“ε, άϊ”Ο…ζΈοΖ÷Ή”ΙΙ÷ΰΨΏ”–ΙΠΡή–‘ΒΡ”––ρΉιΉΑΧε“Μ÷± «»ΥΟ«ΙΊΉΔΒΡΫΙΒψ. κΡΖ÷Ή” «“Μάύ÷Ί“ΣΒΡΉιΉΑΜυ‘Σ, κΡΒΡ≥§Ζ÷Ή”Ή‘ΉιΉΑΩ…–Έ≥…Εύ÷÷Ρ…ΟΉΜρΈΔΟΉ≥ΏΕ»ΒΡΫαΙΙ, ≤ΔΩ…”Π”Ο”ΎΡή‘¥ΓΔ“Ϋ“©Β»Νλ”ρ. »γΚΈ Βœ÷κΡΉ‘ΉιΉΑΫαΙΙΒΡΨΪΉΦΒςΩΊ“‘ΦΑΨΪΉΦΒςΩΊκΡΉ‘ΉιΉΑ Βœ÷ΙΠΡήΜ·, «ΡΩ«ΑΗΟΝλ”ρΟφΝΌΒΡ–¬Χτ’Ϋ. κΡΒΡΉ‘ΉιΉΑ «Μυ”ΎΖ«Ι≤ΦέΦϋΝΠΒΡ–≠Ά§Ής”Ο Βœ÷ΒΡ, Ά®ΙΐΗς÷÷“ρΥΊΒςΫΎ’β–©Ζ«Ι≤ΦέΦϋΝΠΒΡΉς”Ο, « Βœ÷Ή‘ΉιΉΑΫαΙΙΒςΩΊΚΆΙΠΡήΜ·ΒΡΙΊΦϋ. Υδ»ΜΉ‘ΉιΉΑΫαΙΙΒςΩΊΩ…“‘Ά®ΙΐΗΡ±δΆβ≤ΩΜΖΨ≥ΒςΩΊ, ΒΪ «Ά®ΙΐΨΪ»ΖΖ÷Ή”…ηΦΤΓΔΉιΉΑΜυ‘ΣΖ÷Ή”ΦδΒΡœύΜΞΉς”ΟΒςΩΊΩ…“‘ΗϋΚΟΒΊ Βœ÷ΫαΙΙΒΡΨΪΉΦΒςΩΊ; ≤Δ”–άϊ”ΎΫχ“Μ≤ΫΆ®Ιΐ“ΐ»κΙΠΡή–‘Ζ÷Ή”ΉςΈΣΉιΉΑΜυ‘Σ, Βœ÷Ή‘ΉιΉΑΧεΒΡΙΠΡήΜ·. ±ΨΈΡΫΪ’κΕ‘κΡΉ‘ΉιΉΑΧεΒΡΫαΙΙΒςΩΊ“‘ΦΑΙΠΡήΜ·ΝΫΗωΖΫΟφΕ‘œύΙΊ―–ΨΩΫχ––Ήέ ω.
…ζΈοΖ÷Ή”Ή‘ΉιΉΑ «…ζΟϋΒΡΜυ¥Γ, Υϋ‘Ύ…ζΈοΧε÷–Τ’±ι¥φ‘Ύ, ¥”ΦρΒΞΒΡ÷§÷ Ζ÷Ή”ΉιΉΑ–Έ≥…ΝΉ÷§ΥΪΖ÷Ή”≤ψΓΔκΡΝ¥’έΒΰ–Έ≥…ΒΑΑΉ÷ ΫαΙΙ“‘ΦΑ DNA ΥΪ¬ί–ΐΫαΙΙ, ΒΫΗϋΈΣΗ¥‘”ΒΡœΗΑϊΤςΓΔœΗΑϊΓΔΉι÷·ΤςΙΌΒ», ΕΦ «”……ζΈοΖ÷Ή”‘Ύ≤ΜΆ§≥ΏΕ»…œΖ÷ΦΕΉ‘ΉιΉΑΙΙΫ®Εχ≥…ΒΡ, ’β–©ΗΏΕ»–≠ΒςΉ‘ΉιΉΑΧεœΒΈΣ…ζΟϋΧε Βœ÷ΤδΙΠΡή–‘ΚΆΜν–‘ΧαΙ©ΝΥ”–άϊΒΡ±Θ’œ. …ζΈοΖ÷Ή”Ή‘ΉιΉΑΙΐ≥Χ «‘ΎΕ·ΝΠ―ß”κ»»ΝΠ―ßΩΊ÷Τœ¬Ή‘ΖΔ–Έ≥…”––ρΨέΦ·ΧεΒΡΙΐ≥Χ. ΗΟΙΐ≥Χ÷–, Ης÷÷Ζ«Ι≤ΦέΦϋΝΠΑϋά®«βΦϋΝΠΓΔΨ≤ΒγΝΠΓΔ ηΥ°Ής”ΟΓΔΠ–-Π–Ής”Ο“‘ΦΑΖΕΒ¬ΜΣΝΠΦδΒΡ–≠Ά§Ής”Ο «ΨωΕ®Ή‘ΉιΉΑΧε–ΈΟ≤ΚΆΙΠΡήΒΡΙΊΦϋ[1]. ή…ζΈοΧεœΒΤτΖΔ, άϊ”Ο…ζΈοΖ÷Ή”ΉςΈΣΉιΉΑΜυ‘ΣΙΙ÷ΰΗς÷÷≥ΏΕ»“‘ΦΑ–ΈΟ≤ΒΡΡ…ΟΉΫαΙΙ, “Μ÷± ήΒΫ»ΥΟ«ΙψΖΚΙΊΉΔΚΆ―–ΨΩ[2]. κΡΖ÷Ή” «“Μ÷÷ΫœΈΣ≥Θ”ΟΒΡΉιΉΑΜυ‘Σ, Υϋ”…ΦΗΗωΜρΕύΗωΑ±ΜυΥα–ρΝ–ΙΙ≥…, ≤ΔΨΏ”–ΚήΕύ”≈ Τ±»»γ…ζΈοΦφ»ί–‘ΓΔ…ζΈοΫΒΫβ–‘ΓΔΫαΙΙ“Ή±ύΦ≠–‘ΓΔΒΆΟβ“Ώ‘≠–‘Β»[3ΓΪ5]. κΡΖ÷Ή”Ω…Ή‘ΉιΉΑ–Έ≥…Εύ÷÷Ρ…ΟΉΜρΈΔΟΉ≥ΏΕ»ΒΡΫαΙΙ, ≤ΔΩ…”Π”Ο”Ύ…ζΈο“Ϋ“©ΓΔΡ…ΟΉΩΤΦΦΓΔΡή‘¥Β»ΕύΗωΝλ”ρ[6ΓΪ9].
ΥφΉ≈ΩΤΦΦΒΡΖΔ’Ι, ΙΒΟκΡΖ÷Ή”Ή‘ΉιΉΑΒΡ―–ΨΩ“≤ΟφΝΌ–¬ΒΡΧτ’Ϋ: ≤ΜΫω÷ΜΨ÷œό”ΎΉιΉΑΧεΡ…ΟΉΫαΙΙ(“‘œ¬Φρ≥ΤΈΣΓΑΉιΉΑΫαΙΙΓ±)ΒΡΒΞ“ΜΒςΩΊ, Ηϋ“ΣΫΪœύΙΊ―–ΨΩΆΊ’ΙΈΣάϊ”ΟκΡΖ÷Ή”Ζ÷ΦΕΉ‘ΉιΉΑΙΙΫ®Η¥‘”ΫαΙΙΒΡΙΠΡήΧεœΒ[10,11], Φ¥ Βœ÷κΡΉ‘ΉιΧεΡ…ΟΉΫαΙΙΒΡΨΪΉΦΒςΩΊ(“‘œ¬Φρ≥ΤΈΣΓΑΫαΙΙΒςΩΊΓ±)“‘ΦΑΨΪΉΦΒςΩΊκΡΉ‘ΉιΉΑ Βœ÷ΙΠΡήΜ·. “ρ¥Υ, ±ΨΈΡΫΪ¥”’βΝΫΗωΖΫΟφΕ‘œύΙΊ―–ΨΩΫχ––Ήέ ω.
2 κΡΖ÷Ή”Ή‘ΉιΉΑΒΡΫαΙΙΒςΩΊ
Ης÷÷Ζ«Ι≤ΦέΦϋΝΠ, Αϋά®«βΦϋΓΔ ηΥ°Ής”ΟΓΔΨ≤ΒγΉς”ΟΓΔΠ–-Π–Ε―Μΐ“‘ΦΑΖΕΒ¬ΜΣΝΠΒΡ–≠Ά§Ής”Ο «ΨωΕ®κΡΖ÷Ή”Ή‘ΉιΉΑΫαΙΙΚΆ–‘÷ ΒΡΙΊΦϋ[1,12]. Ά®ΙΐΒςΩΊΉιΉΑΜυ‘ΣΒΡΖ÷Ή”ΫαΙΙ“‘ΦΑΉιΉΑΜΖΨ≥“ρΥΊ(Αϋά® pHΓΔΈ¬Ε»ΓΔ≈®Ε»ΓΔΆβ≥ΓΒ»)Ω…“‘ΒςΩΊ’β–©Ζ«Ι≤ΦέΦϋΝΠΒΡœύΜΞΉς”Ο, ΫχΕχ Βœ÷Ε‘Ή‘ΉιΉΑΙΐ≥ΧΒΡ»»ΝΠ―ßΚΆΕ·ΝΠ―ßΩΊ÷Τ[12]. «βΦϋΉς”ΟΨΏ”–ΗΏΕ»―Γ‘ώ–‘ΚΆΖΫœρ–‘, «”’ΒΦ…ζΈοΖ÷Ή”≥Λ≥Χ”––ρΫαΙΙ–Έ≥…ΒΡΙΊΦϋ–‘“ρΥΊ. κΡΖ÷Ή”Κ§”––μΕύ«βΦϋ–Έ≥…ΈΜΒψ, Αϋά®κΡΝ¥Ι«Φή…œΒΡθΘΑΖΜυΆ≈“‘ΦΑ≤ύΝ¥…œΒΡΑ±ΜυΚΆτ»Μυ, “ρ¥Υ«βΦϋ‘Ύ–Έ≥…ΚΆΈ»Ε®κΡΝ¥ΒΡΕΰΦΕΫαΙΙΚΆΒΑΑΉ÷ ΒΡ’έΒΰΙΙœσ÷–ΤπΒΫ÷Ί“ΣΉς”Ο. ηΥ°Ής”Ο «ΝΫ«Ή–‘…ζΈοΖ÷Ή”Ή‘ΉιΉΑΒΡ÷ς“Σ«ΐΕ·ΝΠ, ηΥ°Ής”Ο≤ΜΨΏ”–ΖΫœρ–‘, ‘Ύ…ζΈοΧε÷–, ”…”ΎΥ°Ζ÷Ή”ΒΡ¥φ‘Ύ, ηΥ°Ής”ΟΆυΆυΑιΥφΉ≈«βΦϋΉς”Ο–≠Ά§”ΑœλκΡΖ÷Ή”ΒΡΉ‘ΉιΉΑ. Ψ≤ΒγΉς”ΟΚΆΠ–-Π–Ε―ΜΐΉς”ΟΖ÷±πΕ‘Κ…Βγ–‘ΒΡΚΆΨΏ”–ΖΦœψΜΖάύΒΡκΡΖ÷Ή””–Οςœ‘”Αœλ. ΒΪ «”κ±ΫΜΖΒΡ ηΥ°Ής”Ο≤ΜΆ§ΒΡ «, Π–-Π–Ής”Ο÷–ΒΡ±ΫΜΖΩ…“‘–Έ≥…”––ρΒΡΕ―ΜΐΫαΙΙ. ΖΕΒ¬ΜΣΝΠ «“Μ÷÷÷Ί“Σ«“Τ’±ι¥φ‘ΎΒΡΖ«Ι≤ΦέΦϋΝΠ, ΒΪΥϋΆυΆυ–η“Σ”κΤδΥϊΖ«Ι≤ΦέΦϋΝΠ–≠Ά§”ΑœλΉ‘ΉιΉΑΙΐ≥Χ.
κΡ≥§Ζ÷Ή”Ή‘ΉιΉΑΒΡΫαΙΙΜ·“‘ΦΑΙΠΡήΜ·ΕΦ «Μυ”Ύ’β–©Ζ«Ι≤ΦέΦϋΝΠΒΡ–≠Ά§Ής”Ο Βœ÷ΒΡ; Ζ¥÷°, »γΚΈΆ®ΙΐΗς÷÷“ρΥΊΒςΫΎ’β–©Ζ«Ι≤ΦέΦϋΝΠΒΡΉς”Ο, ≥…ΈΣ»ΥΟ« Βœ÷ΉιΉΑΫαΙΙ”––ßΒςΩΊΒΡΙΊΦϋ. ΡΩ«Α, Ή‘ΉιΉΑΧεΫαΙΙΒςΩΊΒΡΖΫ Ϋ÷ς“Σ”–ΝΫ÷÷: (1)Ά®ΙΐΗΡ±δΆβ≤ΩΜΖΨ≥ΒςΩΊ; (2)Ά®ΙΐΉιΉΑΜυ‘ΣΖ÷Ή”ΦδΒΡœύΜΞΉς”ΟΒςΩΊ.
2.1 Άβ≤ΩΜΖΨ≥ΒςΩΊ
κΡΖ÷Ή”ΒΡΉ‘ΉιΉΑ «‘Ύ»»ΝΠ―ßΚΆΕ·ΝΠ―ß–≠Ά§ΩΊ÷Τœ¬ΒΡΙΐ≥Χ: »»ΝΠ―ß…œ, κΡΖ÷Ή””κ»ήΦΝΦδΒΡΖ«Ι≤ΦέΦϋœύΜΞΉς”ΟΨωΕ®ΝΥΉιΉΑΧεΒΡ»»ΝΠ―ßΈ»Ε®ΫαΙΙ, ΒΪ «”…”ΎΖ«Ι≤ΦέΦϋΦδ»θΒΡœύΜΞΉς”Ο, ‘Ύ≤ΜΆ§ΒΡ»ήΦΝΜΖΨ≥÷–, Φ¥‘Ύ≤ΜΆ§ pHΓΔΈ¬Ε»ΓΔΕ‘άκΉ”Β»Ε·ΝΠ―ß“ρΥΊ”Αœλœ¬, κΡΖ÷Ή”Ω…“‘Ά®Ιΐ≤ΜΆ§ΒΡΕΰΦΕΫαΙΙ(±»»γ Π¬-’έΒΰΚΆ ΠΝ ¬ί–ΐ)ΙΙ÷ΰ≤ΜΆ§≥ΏΕ»ΒΡΫαΙΙ, Αϋά®Ρ…ΟΉΙή[13]ΓΔΡ…ΟΉœΥΈ§[14,15]ΓΔΈΔ«ρ[16]“‘ΦΑΈΔΟΉΦΕΒΡœΥΈ§ χΫαΙΙΒ». Ης÷÷Ε·ΝΠ―ß“ρΥΊΩ…“‘”––ßΒΊΗΡ±δκΡΖ÷Ή””κ»ήΦΝΖ÷Ή”ΒΡΉς”Ο, ¥”Εχ”ΑœλκΡΉ‘ΉιΉΑΧεΒΡ–ΈΟ≤, Ε‘ΉιΉΑΕ·ΝΠ―ßΙΐ≥Χ“ύ”–÷Ί“ΣΒςΩΊΉς”Ο[17,18].
άΐ»γ, Kim Β»[19]±®ΒάΝΥΕΰκΡΕΰ±Ϋ±ϊΑΖΥα(FF)‘Ύ≤ΜΆ§Υ°ΜΖΨ≥÷––ΈΟ≤”κ FF-Υ°Ζ÷Ή”ΦδœύΜΞΉς”ΟΒΡΙΊœΒ: XRD ΫαΙϊ±μΟςΡ…ΟΉΙή”κΡ…ΟΉœΏΒΡΨßΧεΫαΙΙ «“Μ÷¬ΒΡ, Εχ“ΐΤπFF –ΈΟ≤≤Μ“Μ÷¬ΒΡ‘≠“ρ‘Ύ”ΎΥυ–Έ≥…ΨßΧε÷– FF ”κΥ°Ζ÷Ή”œύΜΞΉς”ΟΒΡ«χ±π. ’βΥΒΟς FF ”κΥ°Ζ÷Ή”Ής”Ο≥ΧΕ»≤ΜΆ§, Μα÷±Ϋ””ΑœλΉ‘ΉιΉΑΧεΒΡ–ΈΟ≤. “ρ¥Υ, ‘ωΦ”»ή“ΚάκΉ”«ΩΕ», άκΉ”ΒΡΥ°Κœ–ß”ΠΜα”κ FF ΒΡΥ°ΚœΉς”ΟœύΨΚ’υ, Ήν÷’ΒΦ÷¬FF Υ°Κœ≥ΧΕ»ΒΡΗΡ±δ, ¥”ΕχΩ…“‘”––ßΒΊΒςΩΊ FF –ΈΟ≤ΒΡΉΣ±δ . ΝμΆβ , Ά®Ιΐ‘ω¥σΜΖΨ≥ ΣΕ»Μρ‘ωΦ”ΧεœΒ÷–Υ°Κ§ ΝΩ[20ΓΪ23], “ύΩ…”’ΒΦκΡΡ…ΟΉΙή…ζ≥ΛΈΣΕύΦΕΫαΙΙ. Ά®ΙΐΒςΫΎΥ°»ή“Κ pH[24]ΚΆΈ¬Ε»[25], Ω…“‘ΜώΒΟ≤ΜΆ§–ΈΟ≤ΒΡΉ‘ΉιΉΑΧε. Xu Β»[26]“ΐ»κ““κφ‘ωΦ”Υ°»ή“ΚΒΡ ηΥ°–‘, Ω…“‘”––ß”ΑœλΝΫ«Ή–‘Ι―κΡΖ÷Ή””κΥ°Ζ÷Ή”ΦδΒΡ«βΦϋΉς”Ο, ¥”ΕχΗΡ±δΥυ–Έ≥…œΥΈ§ΒΡ–ΈΟ≤.
ΦρΕχ―‘÷°, ΉςΈΣ“Μ÷÷ΫœΈΣΙψΖΚΚΆ≥Θ”ΟΒΡΒςΩΊ ÷ΕΈ, ΗΟΖΫΖ®÷ς“ΣΆ®ΙΐΗΡ±δ»ήΦΝΜΖΨ≥Αϋά® pHΓΔάκΉ”«ΩΕ»ΓΔ≈®Ε»ΓΔΈ¬Ε»Β»Άβ≤Ω“ρΥΊά¥ΗΡ±δΉιΉΑΖ÷Ή””κ»ήΦΝΦδΒΡΖ«Ι≤ΦέΦϋœύΜΞΉς”Ο, Ά®ΙΐΉ‘ΉιΉΑΙΐ≥ΧΒΡ»»ΝΠ―ßΚΆΕ·ΝΠ―ßΩΊ÷Τ Βœ÷κΡΖ÷Ή”ΉιΉΑΫαΙΙΒΡΗΡ±δΚΆΒςΩΊ[12].
2.2 ΉιΉΑΜυ‘ΣΖ÷Ή”ΦδΒΡœύΜΞΉς”ΟΒςΩΊ
Υδ»ΜΫωΆ®ΙΐΗΡ±δΜυ‘ΣΖ÷Ή”ΒΡΆβ≤ΩΜΖΨ≥ά¥ΗΡ±δΉ‘ΉιΉΑΫαΙΙΒΡΖΫΖ®ΫœΈΣΤ’ ΚΆΦρΒΞ, ΒΪΗΟΖΫΖ®Ά§ ±“≤¥φ‘ΎΫœ¥σΒΡΨ÷œό–‘, Φ¥ΈόΖ® Βœ÷ΨΪΉΦΒςΩΊ. ΕχΆ®ΙΐΧΊΕ®ΒΡΖ÷Ή”…ηΦΤ[27ΓΪ32], “ύΜρΩΊ÷ΤΝΫ÷÷ΜρΝΫ÷÷“‘…œΒΡΉιΉΑΜυ‘ΣΦδΒΡœύΜΞΉς”Ο, Ω…“‘Ηϋ”––ßΒΊ Βœ÷Ε‘ΉιΉΑΧεΫαΙΙΒΡΨΪΉΦΒς ΩΊ[33ΓΪ35].
2.2.1 «βΦϋ÷ςΒΦ
«βΦϋΝΠ «–Έ≥…≤ΔΈ»Ε®ΒΑΑΉ÷ /κΡΕΰΦΕΠ¬-’έΒΰΫαΙΙΒΡΙΊΦϋΉς”ΟΝΠ, “ύ «”’ΒΦΒΑΑΉ÷ –Έ≥…ΒμΖέάύœΥΈ§ΒΡ÷ς“Σ“ρΥΊ. Xu Β»[36,37]Ά®Ιΐ…ηΦΤ≤ΜΆ§ΒΡκΡΖ÷Ή”–ρΝ–ά¥ΒςΩΊκΡΒΡΉ‘ΉιΉΑ. άΐ»γ, Ε‘Ω…–Έ≥…¬ί–ΐœΥΈ§ΫαΙΙΒΡΙ―κΡΖ÷Ή” I4K2 ΒΡΖ÷Ή”–ρΝ–Ϋχ––Βς’ϊ, ΒΟΒΫΒΡ–¬Ζ÷Ή” KI4K Ω…–Έ≥…Ρ…ΟΉΙήΫαΙΙ(ΆΦ 1a)[38]. ΗΡ±δ I3K Ζ÷Ή”÷– I –ρΝ–“‘ΦΑ K –ρΝ–ΒΡ ÷–‘, “ύΩ…ΒΟΒΫΨΏ”–≤ΜΆ§ ÷–‘ΫαΙΙΒΡœΥΈ§, œΥΈ§ΒΡ ÷–‘»ΓΨω”Ύ K –ρΝ–ΒΡ–‘÷ (ΆΦ 1b)[39].

Yan Β»[40]Ά®ΙΐœρΕ଻ֹΆι÷–“ΐ»κΈΔΝΩ»ήΦΝ(““¥ΦΓΔN,N-ΕΰΦΉΜυΦΉθΘΑΖΓΔ±ϊΆΣΓΔΥ°)ΒΡΖΫΖ®, ―–ΨΩΝΥ«βΦϋΉς”ΟΕ‘ΕΰκΡ(FF)Ή‘ΉιΉΑΒΡΒςΩΊΡήΝΠ. ”…”Ύ“ΐ»κΒΡΈΔΝΩ»ήΦΝΚ§ΝΩΫœΒΆ, Ω…“‘ΫΪΈΔΝΩ»ήΦΝΖ÷Ή”Β±Ής»ή÷ Ζ÷Ή”, ’β–©ΈΔΝΩ»ή÷ Ζ÷Ή””κ FF Ζ÷Ή”ΖΔ…ζΙ≤ΉιΉΑ, ¥”ΕχΉςΈΣ÷ςΒΦ“ρΥΊά¥ΒςΩΊΕΰκΡΒΡΉ‘ΉιΉΑ––ΈΣ. ΫαΙϊΖΔœ÷«βΦϋΉς”ΟΝΠ‘Ύ FF œΥΈ§Μ·Ιΐ≥Χ÷– «ΙΊΦϋΒΡ”’ΒΦ“ρΥΊ, ΧμΦ”ΒΡΨΏ”–≥…«βΦϋΡήΝΠΒΡΈΔΝΩ»ήΦΝΩ…“‘”––ßΒΊ”Αœλ FF Ζ÷Ή”÷– CΘΫO ΚΆ NΓΣHΒΡ«βΦϋΉς”Ο; «βΦϋΒΡΖΫœρ–‘Ω…“‘”’ΒΦ FF Ζ÷Ή”‘Ύ≥Λ≥ΧΖΫœρ…œΒΡ”––ρ≈≈Ν–, Ήν÷’ΒΦ÷¬Ρ…ΟΉœΥΈ§“‘ΦΑΡ…ΟΉ¥χΫαΙΙΒΡ–Έ≥….
Xu Β»[41]άϊ”Ο≤ΜΆ§ΒΡΚΥή’Ε‘ΕύκΡΫχ––ΝΥΖ÷Ή”…ηΦΤΚΆΗΡ–‘, ÷°ΚσΫΪΒΟΒΫΒΡΚΥή’-κΡΖ÷Ή”ΝΫΝΫΜλΚœ, Ω…“‘ΒΟΒΫΆ§œΥΈ§ΫαΙΙΒΡΡΐΫΚ, ΗΟΡΐΫΚΨΏ”–ΚήΚΟΒΡ…ζΈοΦφ»ί–‘«“Ε‘ΒΑΑΉΟΗ K±μœ÷≥ωΚήΚΟΒΡΩΙΥ°Ϋβ–‘, ‘ΎΥυ–Έ≥…ΒΡœΥΈ§ΫαΙΙ÷–, ≤ΜΆ§ΫαΙΙΒΡΚΥή’-κΡΖ÷Ή”ΦδΒΡ«βΦϋΚΆ ηΥ°–≠Ά§Ής”Ο « ΙΧεœΒΈ»Ε®ΒΡΙΊΦϋ“ρΥΊ.
2.2.2 Ψ≤ΒγΝΠΚΆΠ–-Π–Ής”Ο÷ςΒΦ
“ΜΑψ«ιΩωœ¬, ηΥ°Ής”ΟΜα”’ΒΦΒΑΑΉ÷ Ζ÷Ή”ΨέΦ·, ΒΪ «Υυ–Έ≥…ΒΡΨέΦ·ΧεΈ»Ε®–‘Ϋœ≤ν, ‘ΎΧεΆβΜρΧεΡΎΒΡœΓ ΆΉς”ΟΕΦΜα ΙΨέΦ·ΧεΖΔ…ζΫβΉιΉΑ. ΫϋΡξά¥, άϊ”ΟΕΰ‘ΣΉιΖ÷±»»γΒΑΑΉ/κΡΚΆ…ζΈοΨέΚœΈοΦδΒΡ«ΩΨ≤ΒγΉς”Ο, Ω…“‘Ή‘ΉιΉΑ–Έ≥…Ρ…ΟΉ‘ΊΧε, ¥”ΕχΧαΗΏΒΑΑΉ÷ ΨέΦ·ΧεΒΡΈ»Ε®–‘, ήΒΫ»ΥΟ«ΙψΖΚΙΊΉΔ. Yan Β»[42]άϊ”Ο»Υ―Σ«εΑΉΒΑΑΉ(HSA)ΚΆ¥χ”–Ζ¥ΒγΚ…ΒΡΑ±ΜυΥαάύΨέΚœΈο(Ψέ-L-άΒΑ±Υα, PLL)ΦδΒΡΨ≤ΒγΉς”ΟΉ‘ΉιΉΑ–Έ≥…«ρ–Έ“©Έο‘ΊΧε(ΆΦ 2). «ρΧεΒΡΝΘΨΕΩ…Ά®Ιΐ HSA ΚΆ PLL ≈®Ε»“‘ΦΑ pH Β»“ρΥΊΫχ––ΒςΫΎ. –Έ≥…ΒΡΈΔ«ρ‘ΊΧεΦ»Ω…ΗΚ‘ΊΥ°»ή–‘ΒΡ–ΓΖ÷Ή”(Αϋά®»ΨΝœΖ÷Ή”)“‘ΦΑ…ζΈο¥σΖ÷Ή”(±»»γΤœΧ―ΨέΧ«ΓΔΒΑΑΉ÷ Β»), “ύΩ…ΗΚ‘ΊΖ«Υ°»ή–‘ΒΡΖ÷Ή”±»»γΡα¬όΚλ»ΨΝœΖ÷Ή”, ¥”ΕχΩ…“‘Η≥”η’β÷÷Μυ”ΎΒΑΑΉ÷ ΒΡ…ζΈο≤ΡΝœ≤ΜΆ§ΒΡ–‘÷ , ”Π”Ο‘Ύ≤ΜΆ§Νλ”ρ. άΐ»γ, ΫΪΙβΟτΦΝΗΚ‘ΊΒΫΈΔ«ρ÷–, ΫΪΈΔ«ρ±μΟφάϊ”ΟΨέ““Εΰ¥Φ–ό Έ(PEG Μ·), Ω…”Ο”Ύ÷ΉΝωΒΡΙβΕ·ΝΠ÷ΈΝΤ[43].
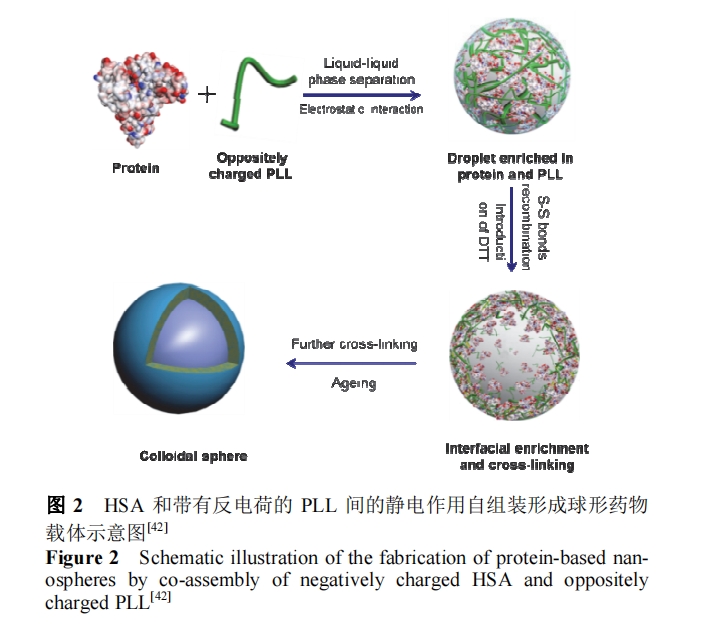
άϊ”ΟΕΰκΡ”κΏ≤ΏχΖ÷Ή”Ι≤ΉιΉΑΙΙ÷ΰΕύΩΉ«ρ–ΈΫαΙΙ: ‘ΎΥα–‘ΧθΦΰœ¬, ΕΰκΡΖ÷Ή”÷–ΑΖΜυ÷ Ή”Μ· ΙΕΰκΡ¥χ”–’ΐΒγΚ…[FF]ΘΪ, ΕχΏ≤ΏχΖ÷Ή”÷–Μ«ΥαΜυΒΡ»Ξ÷ Ή”Μ· Ι÷°¥χ”–ΗΚΒγΚ…[H4TPPS]2Θ≠, [FF]ΘΪ”κ[H4TPPS]2Θ≠Ζ÷Ή”ΦδΒΡΨ≤ΒγΉς”Ο ΙΏ≤ΏχΖ÷Ή”–Έ≥…”––ρΒΡ J ΨέΦ·ΫαΙΙ, ΫχΕχ–Έ≥…κΡ-Ώ≤ΏχΡ…ΟΉΑτ, ’β–©Ρ…ΟΉΑτΫχ“Μ≤Ϋ‘Ύ ηΥ°Ής”Οœ¬–Έ≥…ΕύΩΉ(Εύ«Μ “)«“ΨΏ”–ΗΏΥ°Μ·≥ΧΕ»ΒΡ«ρ–ΈΫαΙΙ(ΆΦ 3a ΚΆ 3b). ”…”ΎΏ≤ΏχΖ÷Ή”ΒΡ“ΐ»κ, ΈΔ«ρΩ…Έϋ ’ΙβΡή, “ρ¥ΥΩ…άϊ”ΟΗΟΈΔ«ρ≤ΕΜώΙβΡή, ‘ΎΈΔ«ρ÷–ΖΔ…ζΙβ¥ΏΜ·Ζ¥”Π, ‘ΎΥ°»ή“Κ÷–¥ΏΜ·ΜΙ‘≠Ϋπ τ―Έ÷Τ±ΗΈόΜζΜρ”–Μζ≤ΡΝœ. άΐ»γ, ‘≠ΈΜ’’…δΈΔ«ρ 5 min, ±ψΩ…‘ΎΈΔ«ρ±μΟφ–Έ≥…‘Φ 2 nm ΒΡ Pt Ρ…ΟΉΝΘΉ”[44].
Ά®ΙΐΗΡ±δΕΰκΡΒΡ–‘÷ Ω…“‘”––ßΒςΩΊΉ‘ΉιΉΑΫαΙΙ, ”ΟL-Lys-L-Lys (KK)¥ζΧφ FF ”κΏ≤ΏχΙ≤ΉιΉΑΚσ, KK-Ώ≤ΏχΖ÷Ή”ΦδΒΡΨ≤ΒγΉς”ΟΚΆ«βΦϋΉς”ΟΓΔ“‘ΦΑΏ≤Ώχ-Ώ≤ΏχΖ÷Ή”ΦδΒΡΠ–-Π–Ής”Ο–≠Ά§”’ΒΦΏ≤ΏχΖ÷Ή”–Έ≥…ΨΏ”– J ΨέΦ·ΫαΙΙΒΡ KK-Ώ≤ΏχΡ…ΟΉΑτ. ‘ΎΕΧ≥ΧΒΡΖΕΒ¬ΜΣΝΠΉς”Οœ¬, Ρ…ΟΉΑτΨέΦ·≥…ΕύΦΕΒΡ≥Λ≥ΧœΥΈ§ χΫαΙΙ, Ρ…ΟΉΑτΒΡΫχ“Μ≤ΫΨέΦ·Ω…”ΟOnsager άμ¬έ÷–ΒΡΤΫΕ·λΊΚΆΉΣΕ·λΊ±δά¥Ϋβ Ά(ΆΦ3a ΚΆ3c). Ήν÷’–Έ≥…ΒΡœΥΈ§ χΫαΙΙΨΏ”–ΚήΚΟΒΡΙβ¥ΏΜ·Μν–‘ΚΆΙβΈ»Ε®–‘, Ω…”Ο”Ύ¥ΏΜ·ΜΙ‘≠…ζ≥…PtΡ…ΟΉ«ρΜρPtΡ…ΟΉœΏ[45]. ΫαΚœ»Ϊ‘≠Ή”Ζ÷Ή”Ε·ΝΠ―ßΡΘΡβ(MD)“‘ΦΑΚΡ…ΔΝΘΉ”Ε·ΝΠ―ßΡΘΡβ(DPD), œΗΜ·―–ΨΩΝΥΏ≤Ώχ”κΝΫ÷÷≤ΜΆ§ΒΡΕΰκΡ–Έ≥…≤ΜΆ§Ρ…ΟΉΫαΙΙΒΡ‘≠“ρ: Υδ»Μ FF ”κ KK ΕΦΜα”’ΒΦΏ≤Ώχ–Έ≥… JΨέΦ·ΒΡΡ…ΟΉΑτΫαΙΙ, ΒΪ «”…”Ύ FF Ζ÷Ή”ΒΡ«Ω ηΥ°–‘ Ι FFΗϋ«ψœρ”Ύ≤ε»κΏ≤Ώχ J ΨέΦ·ΧεΡΎ≤Ω, Εχ«ΉΥ°ΒΡ KK Ζ÷Ή”‘ρ±ΜΙΧΕ®‘ΎΏ≤Ώχ J ΨέΦ·ΧεΒΡ±μΟφ, ¥”Εχ‘ω«ΩΝΥΏ≤ΏχΡ…ΟΉΑτΒΡΖΫœρ–‘, ≤Δ¥Ό ΙΡ…ΟΉΑτΕ®œρ…ζ≥Λ≥…œΥΈ§ χΫαΙΙ[46].
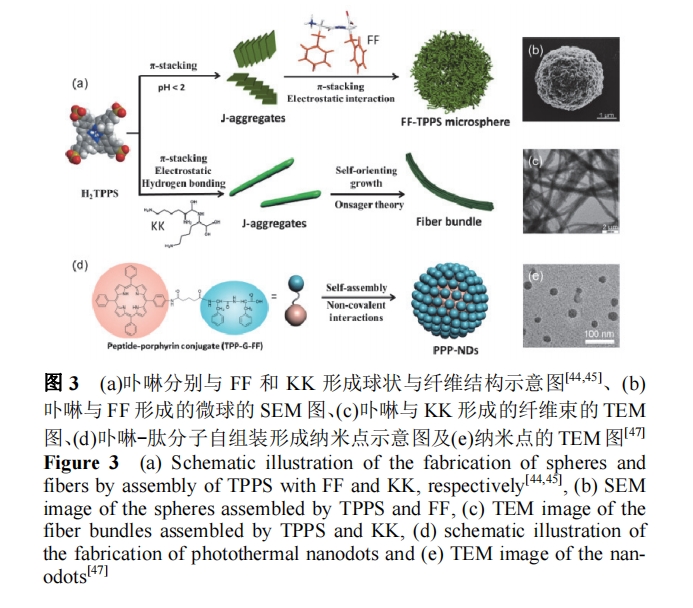
“‘…œ «Ώ≤ΏχάύΖ÷Ή””κ≤ΜΆ§ΒΡΙ―κΡΖ÷Ή”Ι≤ΉιΉΑ, Ά®ΙΐΖ÷Ή”ΦδΉς”ΟΝΠΒΡ–≠Ά§“‘–Έ≥…≤ΜΆ§ΒΡΉιΉΑΫαΙΙ. Εχ…ηΦΤΫΪΏ≤ΏχΚΆΕΰκΡΖ÷Ή”Ά®ΙΐΙ≤ΦέΦϋΚœ≥…ΈΣ“ΜΗωΖ÷Ή”Κσ, ‘ρΩ…“‘–Έ≥…”–»ΛΒΡΡ…ΟΉΒψ, Ώ≤ΏχΒΡΠ–-Π–Ής”Ο“‘ΦΑ’ϊΗωΖ÷Ή”ΒΡ ηΥ°–ß”Π «–Έ≥…ΒΡΡ…ΟΉΒψΒΡ÷ς“Σ«ΐΕ·ΝΠ. κΡΖ÷Ή”÷–ΒΡΒγΚ…ΕΥΜυ”––ßΒΊΖά÷ΙΝΥΏ≤ΏχΖ÷Ή”ΙΐΩλΒΡΠ–Ε―Μΐ, ¥”ΕχΤπΒΫΝΥΈ»Ε®Ρ…ΟΉΒψΒΡΉς”Ο(ΆΦ 3d ΚΆ 3e)[47].
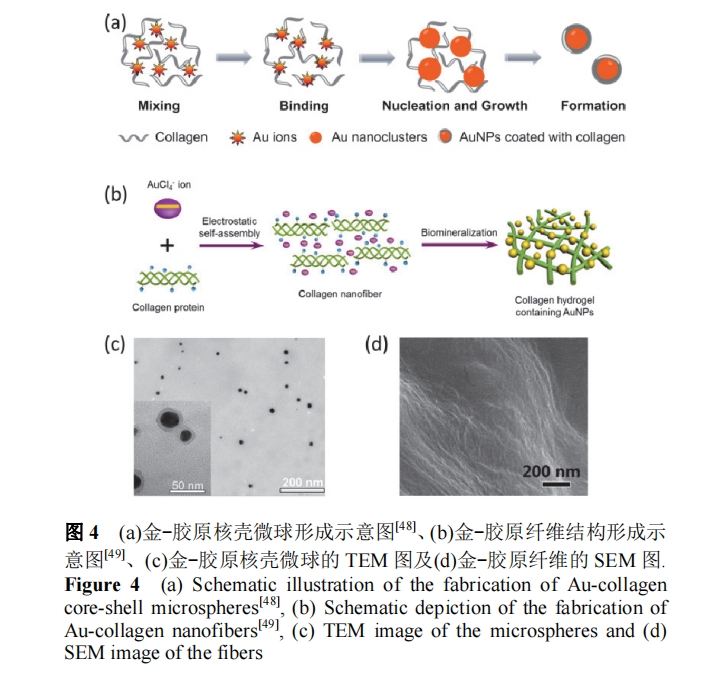
‘ΎΈ¬ΚΆΒΡΧθΦΰœ¬( “Έ¬ΓΔΥ°»ή“Κ÷–)Ω…÷Τ±ΗΈ»Ε®ΒΡΫπ-ΫΚ‘≠ΚΥΩ«ΈΔ«ρ, ÷Τ±ΗΙΐ≥Χ÷–ΟΜ”–Φ”»κΤδΥϊΜΙ‘≠ΦΝΚΆΈ»Ε®ΦΝ. Ϋπ‘≠Ή””κΫΚ‘≠ΒΑΑΉΖ÷Ή”ΦδΒΡΨ≤ΒγΝΠ“‘ΦΑœύΑιΥφΒΡτ«(Μυ)Η§Α±ΥαΒΡ‘≠ΈΜΜΙ‘≠Ής”Ο «–Έ≥…Ϋπ-ΫΚ‘≠ΚΥΩ«ΈΔ«ρ÷ς“Σ‘≠“ρ(ΆΦ 4a ΚΆ 4c). Ϋχ“Μ≤Ϋάϊ”Ο’β–©Ϋπ-ΫΚ‘≠ΚΥΩ«ΈΔ«ρΒΡ≤ψ≤ψΉ‘ΉιΉΑ–Έ≥…±ΓΡΛΩ…“‘”––ßΒΊ”Π”Ο”ΎœΗΑϊΒΡπΛΗΫ“‘ΦΑ…ζ≥Λ[48]. Ά§―υάϊ”ΟΫΚ‘≠ΒΑΑΉΚΆ[AuCl4]Θ≠άκΉ”ΦδΒΡΨ≤ΒγΉς”ΟΩ…”’ΒΦΫΚ‘≠ΒΑΑΉ–Έ≥…œΥΈ§ΫαΙΙ, ‘Όάϊ”Ο‘≠ΈΜΩσΜ·Ζ¥”Π‘ΎœΥΈ§±μΟφ…ζ≥… Au Ω≈ΝΘ, ¥”Εχ–Έ≥…ΨΏ”–Φτ«–±δœΓΦ¥Ω…ΉΔ…δ–‘÷ ΒΡΥ°ΡΐΫΚ(ΆΦ 4b ΚΆ 4d)[49].
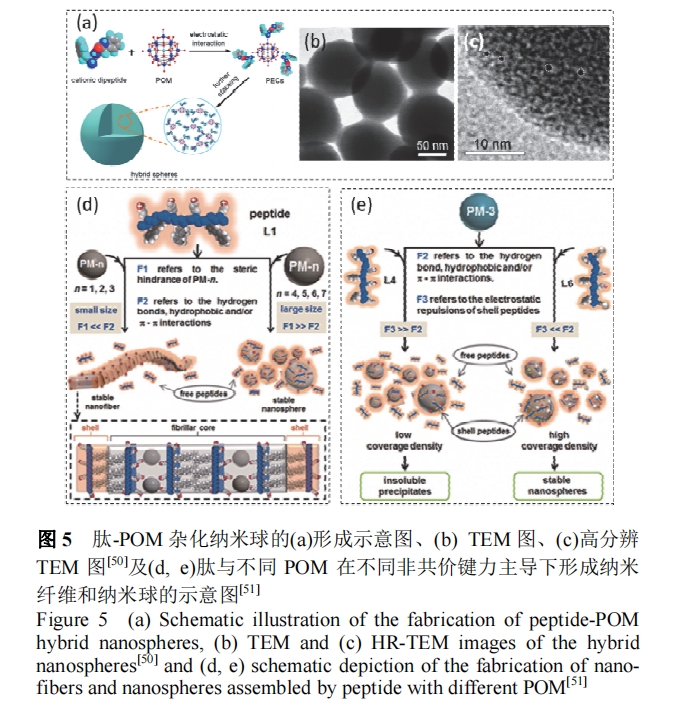
ΕύΫπ τ―θ¥Ί(POM) «“Μ÷÷≥Θ”ΟΒΡΨΏ”–¥ΏΜ·ΓΔΒγ―ßΓΔΙβ―ßΒ»–‘÷ ΒΡΈόΜζ‘”Μ·ΨέάκΉ”. Yan Β»[50]Χα≥ωΫΪ POM“ΐ»κκΡΉ‘ΉιΉΑ÷–, ‘ΎΨ≤ΒγΝΠΒΡ”’ΒΦœ¬, κΡΑϋΙϋ POM –Έ≥…Ά≈¥Ί, Ά≈¥ΊΕύΦΕΉ‘ΉιΉΑ–Έ≥…ΝΘΨΕ‘Φ 150 nm ΒΡ«ρΉ¥ΫαΙΙ(ΆΦ5aΓΪ5c). LiΒ»[51]Ϋχ“Μ≤ΫΧΫΨΩΝΥκΡΖ÷Ή””κPOMΖ÷Ή”–‘÷ Ε‘Ή‘ΉιΉΑΉν÷’–ΈΟ≤ΒΡ”Αœλ, ΫαΙϊΖΔœ÷: ‘ΎΖ«Ι≤ΦέΦϋ–≠Ά§Ής”Οœ¬, Ϋœ¥σΒΡ POM ‘ρ”’ΒΦκΡ–Έ≥…Ρ…ΟΉΈΔ«ρΫαΙΙ; Εχ‘ΎΈΜΉη–ß”Π”Αœλœ¬, Ϋœ–ΓΒΡ POM Μα”’ΒΦκΡ–Έ≥…œΥΈ§ΫαΙΙ(ΆΦ 5d ΚΆ 5e). ”…”Ύ POM ΒΡ“ΐ»κ, Υυ–Έ≥…ΒΡκΡ‘”Μ·œΥΈ§±μΟφ¥χ”–ΙΐΝΩΒΡ’ΐΒγΚ…“‘ΦΑ¥σΝΩΩ…“‘”κΨζœΗΑϊΉς”ΟΒΡ≥…ΦϋΈΜΒψ, ¥”Εχ”––ßΒΊ‘ω«ΩΝΥκΡΒΡΩΙΨζ–ßΙϊ[52].
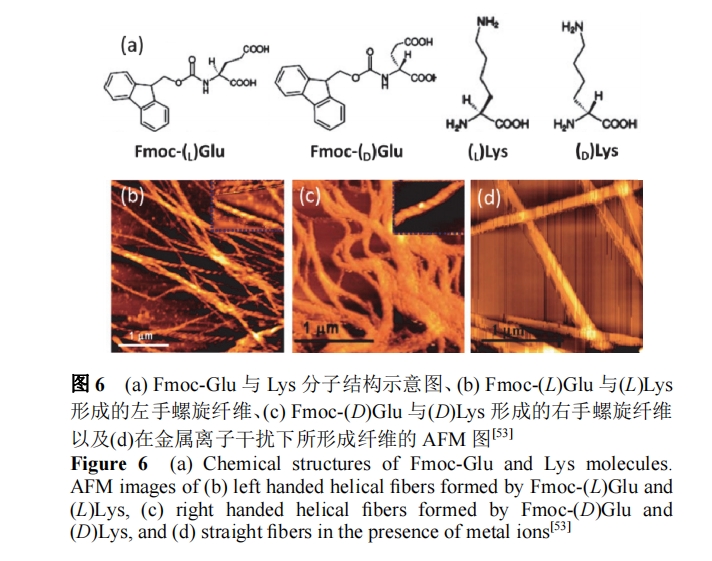
≥ΐΝΥΆ®Ιΐ“ΐ»κΩΆΧεΖ÷Ή”(‘≠Ή”ΓΔΨέάκΉ”)ΒςΩΊΉ‘ΉιΉΑΫαΙΙ, άϊ”ΟΝΫ÷÷ΜρΕύ÷÷¥χ”–œύΖ¥ΒγΚ…ΒΡΑ±ΜυΥα, “ύΩ…¥οΒΫ”––ßΒςΩΊΒΡΡΩΒΡ. Banerjee Β»[53]ΫΪ ÷–‘ΒΡ Fmoc-Ι»Α±Υα(Glu)”κ ÷–‘ΒΡάΒΑ±Υα(Lys)Ι≤ΉιΉΑ, ΫαΙϊΖΔœ÷, ‘ΎΨ≤ΒγΉς”Οœ¬, Fmoc-(L)Glu”κ(L)LysΩ…–Έ≥…Ήσ ÷¬ί–ΐΫαΙΙΒΡœΥΈ§, Εχ Fmoc-(D)Glu ”κ(D)Lys ‘ρ–Έ≥…”“ ÷¬ί–ΐΫαΙΙΒΡœΥΈ§, ±μΟςΉιΉΑΜυ‘ΣΒΡ ÷–‘–‘÷ ΨωΕ®ΝΥ≥§Ζ÷Ή”ΫαΙΙΒΡ ÷–‘–‘÷ . ΒΪ «œρΧεœΒΧμΦ”Ϋπ τάκΉ”±»»γ Ca2ΘΪΜρ Mg2ΘΪ, ‘ρΜα ΙœΥΈ§ΒΡ ÷–‘¬ί–ΐΫαΙΙΉΣ±δΈΣ≥ΘΦϊΒΡΖ« ÷–‘ΫαΙΙ, ’β «”…”ΎΫπ τάκΉ”Ω…“‘”––ßΒΊΤΝ±ΈΑ±ΜυΥαΦδΒΡΨ≤ΒγΉς”Ο, ¥”ΕχΗΡ±δœΥΈ§ΒΡΫαΙΙ(ΆΦ 6).
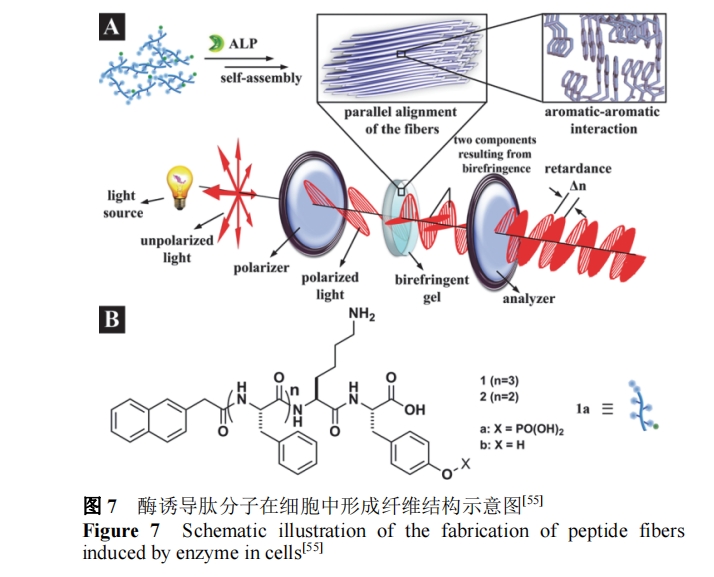
Xu ―–ΨΩΉι[54]±®ΒάΝΥ“ΜœΒΝ–άϊ”ΟΖ÷Ή”ΦδΠ–-Π–Ε―ΜΐΉς”Ο–Έ≥…ΒΡΡΐΫΚΧεœΒ. ΥϊΟ«άϊ”Ο≤ΜΆ§ΒΡ±ΫΜΖάύΜυΆ≈Αϋά®ή≈ΜυΓΔήΧΜυΓΔίΝΜυΒ»Ε‘Ι―κΡΖ÷Ή”Ϋχ––…ηΦΤ, ÷°ΚσΫΪΝΫ÷÷≤ΜΆ§ΗΡ–‘ΒΡκΡΖ÷Ή”Ϋχ––Ι≤ΉιΉΑ–Έ≥…œΥΈ§ΫαΙΙ, ΧΫΧ÷ΝΥ≤ΜΆ§±ΫΜΖΜυΆ≈Ε‘œΥΈ§ΫαΙΙΒΡ”Αœλ, ΫαΙϊ±μΟς÷Μ”–Ζ÷Ή”ΦδΠ–-Π–Ής”Ο”κ«βΦϋΉς”Ο¥οΒΫΤΫΚβΒΡΧεœΒ≤≈Ω…“‘–Έ≥…ΡΐΫΚΫαΙΙ. ΗΟΉιΜΙάϊ”ΟΟΗ”’ΒΦκΡΆ®ΙΐΠ–-Π–Ής”Ο–Έ≥…Ηςœρ“λ–‘ΒΡΡΐΫΚ, ΗΟΡΐΫΚΕ‘Ιβ”–ΚήΚΟΒΡΤΪ’ώ–ßΙϊ(ΆΦ 7)[55].
2.2.3 Ι≤ΦέΦϋΉς”Ο”’ΒΦ
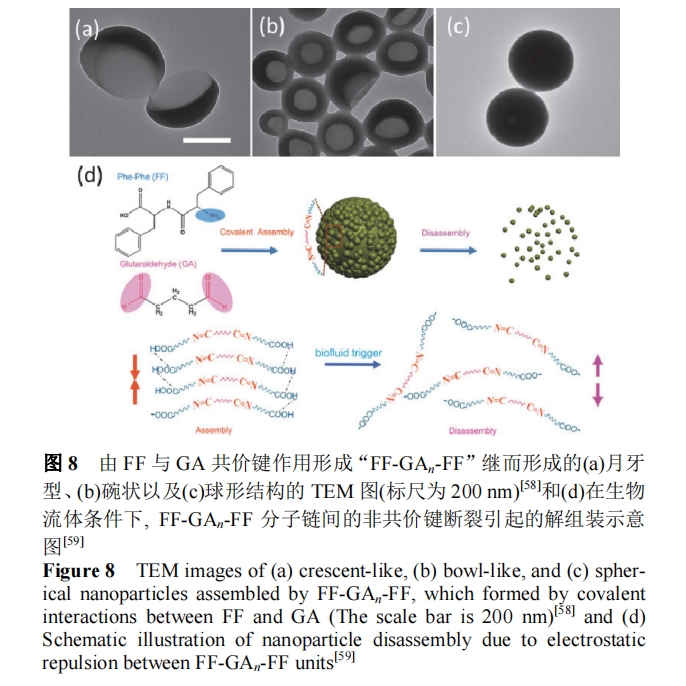
…ηΦΤΚœ ΒΡΖ÷Ή”, ‘ΎΉ‘ΉιΉΑΙΐ≥Χ÷–άϊ”ΟΖ÷Ή”ΦδΙΠΡήΜυΆ≈ΦδΒΡΙ≤ΦέΦϋœύΜΞΉς”Ο, ΙΕΰ‘ΣΜρΕύ‘ΣΉιΖ÷Ϋχ––ΓΑ»ΎΚœΓ±Κσ, ‘Ό‘ΎΖ«Ι≤ΦέΦϋœύΜΞΉς”ΟΒΡ«ΐΕ·œ¬, Ω…ΒςΩΊ≤ΜΆ§Ρ…ΟΉΫαΙΙΒΡ–Έ≥…. ΕΰκΡ(FF)Ζ÷Ή”‘ΎΗΏΈ¬œ¬ΜαΖΔ…ζΜΖΜ·Ζ¥”Π, ΆΥΜπΚσΩ……ζ≥…Ρ…ΟΉ¥χΫαΙΙ. “ΐ»κΝμ“ΜΉιΖ÷ΦΉθΘΑΖΚσ, ΦΉθΘΑΖ”κ FF ΦδΒΡ Schiff ΦνΖ¥”ΠΜα¥Ό Ι FF ΜΖΜ·ΫαΙΙΒΡ…ζ≥…, ¥”ΕχΩΊ÷ΤΡ…ΟΉ¥χΫαΙΙΉΣ±δΈΣΗϋΚώΒΡΤΫΑεΫαΙΙ[56]. Εχ‘Ύ FF ΧεœΒ÷–“ΐ»κΈλΕΰ»©Ζ÷Ή”Κσ, ‘ρ”…”ΎΕΰκΡ(FF)Ζ÷Ή”÷–Α±Μυ”κΈλΕΰ»©(GA)Ζ÷Ή”÷–»©ΜυΦδΒΡSchiffΦνΖ¥”Π…ζ≥…ΓΑ―ΤΝεΓ±–ΆΕΰκΡ(FF-GAn-FF)[57], Ϋχ“Μ≤Ϋ‘Ύ”ΆΥ°ΫγΟφ…œΩΊ÷Τ FF-GAn-FF ≥…ΚΥΚΆ…ζ≥ΛΥΌ¬ , Φ¥Ω…ΜώΒΟ≤ΜΆ§–ΈΟ≤Ω≈ΝΘ, Αϋά®‘¬―ά–ΆΓΔΆκΉ¥“‘ΦΑ«ρ–ΈΫαΙΙ(ΆΦ 8aΓΪ8c)[58]. –Έ≥…ΒΡΡ…ΟΉ«ρΩ…“‘”––ßΗΚ‘Ί“©Έο, Ϋχ––œύΙΊ…ζΈο÷ΈΝΤ. άΐ»γ, Fei ΚΆ Li Β»[59]ΫΪΩΙ…ζ―ΣΒΡ“©ΈοΑϋΗ≤‘Ύ FF-GA Ρ…ΟΉ«ρ÷–, ‘Ύ…ζΈοΝςΧε(pH)ΒΡ¥ΧΦΛœ¬, FF-GAn-FF Ζ÷Ή”Ν¥ΦδΒΡΖ«Ι≤ΦέΦϋ±ΜΩλΥΌΤΤΜΒ(œλ”Π ±Φδ5 s“‘ΡΎ), ¥”Εχ ΆΖ≈≥ω“©Έο≤Δ¥οΒΫ÷Ι―ΣΒΡΡΩΒΡ(ΆΦ 8d).
Ήέ…œΥυ ω, άϊ”ΟΝΫ÷÷ΜρΝΫ÷÷“‘…œΒΡΉιΉΑΜυ‘ΣΦδΒΡœύΜΞΉς”ΟΩ…“‘ΧαΗΏΉ‘ΉιΉΑΫαΙΙΒΡΨΪΉΦ–‘, Ηϋ”–άϊ”ΎΆ®ΙΐΧΊΕ®ΒΡΖ÷Ή”…ηΦΤ, Βœ÷Ή‘ΉιΉΑΧεΒΡΙΠΡήΜ·.
3 κΡΖ÷Ή”Ή‘ΉιΉΑΒΡΙΠΡήΜ·
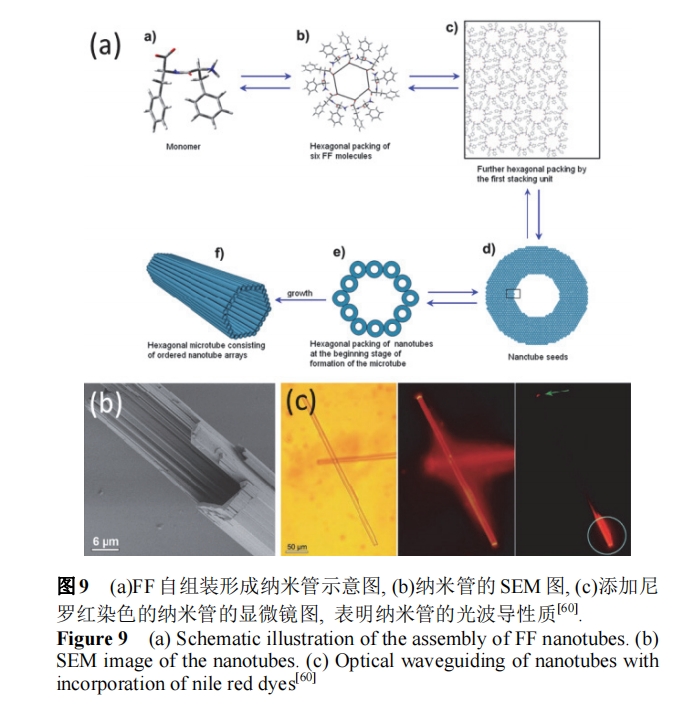
Έό¬έΚΈ÷÷–ΈΟ≤ΓΔΫαΙΙΒΡκΡΉ‘ΉιΉΑΧε, ΤδΙΠΡήΜ·ΒΡ Βœ÷≤≈ «»ΥΟ«»’“φΙΊΉΔΒΡ÷ΊΒψ. ”––©κΡ–ρΝ–ΜρΉιΉΑΫαΙΙ±Ψ…μΨΏ”–ΙΠΡή–‘, άΐ»γΖ÷Ή” Ε±πΓΔΙβ≤®ΒΦ“‘ΦΑΒγΒΦΒ». ±»»γFFΖ÷Ή”ΉιΉΑ–Έ≥…ΒΡΡ…ΟΉΙήΨΏ”–Ιβ≤®ΒΦ–‘÷ (ΆΦ9)[56,60]. Εχ¥σΕύκΡΖ÷Ή”±Ψ…μΈόΙΠΡήΜ·, –η“Σ“ΐ»κΙΠΡήΜ·ΒΡΖ÷Ή”, ±»»γΙβΟτΦΝΒ»”κκΡΖ÷Ή”–≠Ά§Ής”Ο, ¥”Εχ Βœ÷Ή‘ΉιΉΑΧεΒΡΙΠΡήΜ·.
3.1 ΡΘΡβΖ¬…ζΙβΚœ≥…œΒΆ≥
Ή‘»ΜΙβΚœ≥…œΒΆ≥ΡήΫΪΧΪ―τΡήΗΏ–ßΉΣΜ·ΈΣΜ·―ßΡή, ΡΘΡβΚΆ¥¥Ϋ®’βάύœΒΆ≥ΈΣ»ΥΟ«Ηϋ¥σ≥ΧΕ»ΒΊάϊ”ΟΧΪ―τΡήΧαΙ©ΝΥΜζ”ω. ‘ΎΉ‘»ΜΫγ÷–ΒΡΙβΚœ≥…œΒΆ≥÷–, Ήν”––ß Βœ÷Ιβ≤ΕΜώ“‘ΦΑΡήΝΩΉΣ“ΤΒΡΖΫ ΫΦ¥ «άϊ”ΟΒΑΑΉ÷ /κΡ”κΨΏ”–ΖΔ…ΪΜυΆ≈ΒΡΓΔΙΠΡή–‘ΒΡΖ÷Ή”Ι≤ΉιΉΑ–Έ≥…ΒΡΉ‘ΉιΉΑΧε, Εχ»γΚΈΆ®ΙΐΨΪΉΦΒΡ»ΥΙΛΒςΩΊ, ά¥‘ω«ΩΙβ≤ΕΜώΓΔΒγΚ…Ζ÷άκΚΆ¥ΏΜ·Ζ¥”ΠΒΡ≥÷–χ–‘, «ΙΙΫ®ΡΘΡβΙβΚœ≥…œΒΆ≥ΒΡΙΊΦϋΩΤ―ßΈ Χβ.
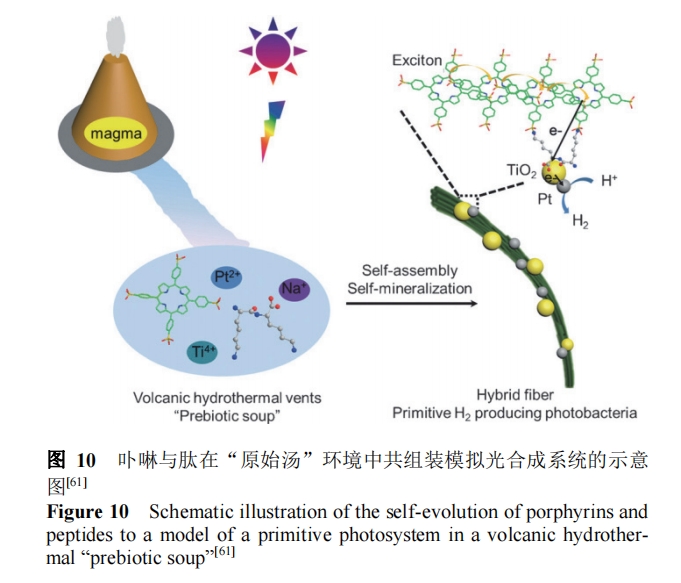
YanΒ»[61]άϊ”ΟκΡ”κΙΠΡή–‘Ζ÷Ή”Ι≤Ή‘ΉιΉΑά¥ΡΘΡβΙβΚœ≥…œΒΆ≥ΖΫΟφΩΣ’ΙΝΥ“ΜœΒΝ–ΙΛΉς. ΕΰκΡ”κΏ≤ΏχΖ÷Ή”Ή‘ΉιΉΑ–Έ≥…ΒΡœΥΈ§ χΧεœΒΚήΚΟΒΡΡΘΡβΝΥ¬Χ…ΪΧε÷–Ψζ¬ΧΥΊΒΡΉι÷·ΡΘ Ϋ, œΥΈ§ χ÷–ΒΡ J ΨέΦ·ΫαΙΙ‘ω«ΩΝΥΙβΈϋ ’ΚΆΡήΝΩ¥ΪΒίΡήΝΠ. ‘ΎΡΘΡβΒΡάύΥΤ¬ΫΒΊΜπ…Ϋ»»“ΚΒΡΓΑ‘≠ ΦΧάΓ±Φ¥Υα–‘ pHΘΫ2.0ΓΔ»» 70 ΓφΓΔΗΜΚ§ΩσΈο÷ (NaΘΪ, Ti4ΘΪ, Pt2ΘΪ)ΒΡΜΖΨ≥÷–, œΥΈ§ χΩ…ΉςΈΣΩσΜ·ΡΘΑε‘≠ΈΜ…ζ≥… TiO2 ΚΆ Pt Ρ…ΟΉΩ≈ΝΘ, ‘Ύ‘”Μ·œΥΈ§ χ…œ–Έ≥…ΝΥ≤ΕΙβΒΞ‘Σ(Ώ≤Ώχ)ΓΔΖ¥”Π÷––Ρ(TiO2)ΚΆ¥ΏΜ·÷––Ρ(Pt)ΒΡΗΏ–ß≈ΦΚœ, ¥”Εχ”––ßΒΊ Βœ÷ΝΥΩ…ΗΏ–ß≥÷–χ≤ζ«βΒΡΖ¬…ζœΒΆ≥(ΆΦ 10). ΗΟΙΛΉςΆ®ΙΐΫαΙΙ…ηΦΤάϊ”ΟκΡ”κΙΠΡή–‘Ζ÷Ή”Ι≤ΉιΉΑ’β“ΜΦρΒΞΖΫ Ϋ, ≤ΜΫω‘ΎΏ≤ΏχΒΡΉι÷·ΫαΙΙ…œΡΘΡβΝΥ¬Χ…ΪΧε, “≤ΡΘΡβΝΥΙβΚœ≤ζ«βœΗΨζΒΡΜυ±ΨΙΛΉς‘≠‘ρ.
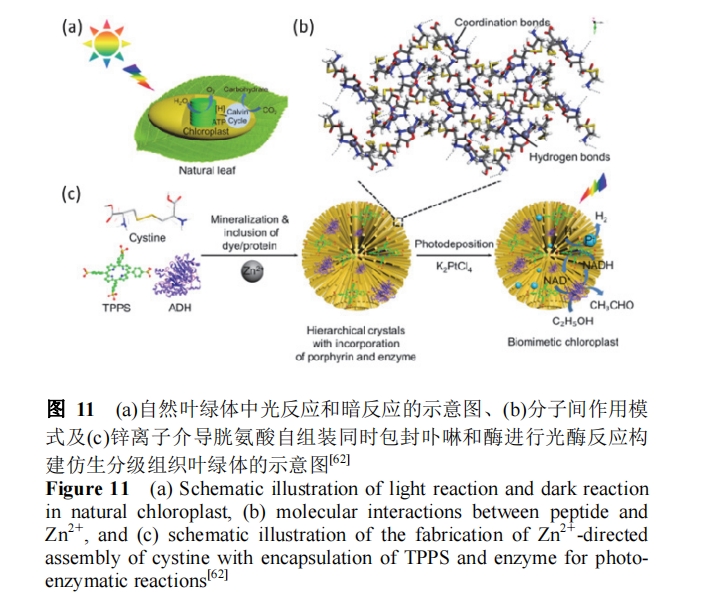
ΝμΆβ, άϊ”ΟκΉΑ±Υα-Ϋπ τάκΉ”ΩσΜ·ΒΡΉ‘ –‘“ύΩ…“‘ΡΘΡβΙΙΫ®¬Χ…ΪΧεΒΡΖ÷ΦΕΉι÷·ΫαΙΙ: Ϋπ τάκΉ”Ω…“‘Ά®Ιΐ≈δΈΜΚΆ«βΦϋΉς”ΟΫιΒΦκΉΑ±ΥαΩσΜ·–Έ≥…Ζ÷ΦΕ”––ρΈΔ«ρ, ΫαΙΙ…œάύΥΤ”Ύ“Ε¬ΧΧεΜυΝΘΒΡΕ―Βΰ. ‘ΎΈΔ«ρ–Έ≥…Ιΐ≥Χ÷–, “ΐ»κΏ≤ΏχΚΆ““¥ΦΆ―«βΟΗΖ÷±πΉςΈΣΙβ¥ΏΜ·ΦΝΚΆΟΗ¥ΏΜ·ΦΝ, ΈΔ«ρΩ…“‘Ά®Ιΐ≈δΈΜΚΆΨ≤ΒγΉς”ΟΑϋΖβ’βΝΫ÷÷ΩΆΧεΖ÷Ή”, ΙΥϋΟ«ΗΫΉ≈≈≈≤Φ‘ΎΈΔ«ρ÷–ΒΡΡ…ΟΉΑτΫαΙΙ…œ, «“±Υ¥ΥΝΎΫϋ, ¥”Εχ Βœ÷ΝΥΗΟΧεœΒΒΡΙβΟΗ≈ΦΝΣΖ¥”Π, ΗΟΙΛΉς‘ΎΫαΙΙ…œΡΘΡβΝΥ“Ε¬ΧΧεΜυΝΘΒΡΖ÷ΦΕΉι÷·ΫαΙΙ, ΙΠΡή…œΡΘΡβΝΥ“Ε¬ΧΧε÷–ΙβΖ¥”ΠΚΆΑΒΖ¥”ΠΒΡ≈ΦΝΣ, ‘ω«ΩΝΥΙβ¥ΏΜ·»ΦΝœ…ζ≥…ΒΡ≥÷–χ–‘ΆΦ 11)[62].
ΗυΨίκΡΖ÷Ή”Ή‘ΉιΉΑΧεΒΡΫαΙΙΧΊΒψ, ΜΙΩ…“‘Ζ¬…ζ±»»γΙβ¥ΏΜ·≤ζ―θ. ”…”ΎκΡΖ÷Ή”Ή‘ΉιΉΑΒΡΕύ―υ–‘ΚΆΩ…ΩΊ–‘, ‘ΎΡΘΡβ…ζΈοΧεœΒ(Έό¬έ «ΫαΙΙΖ¬…ζ, ΜΙ «ΙΠΡήΖ¬…ζ)ΖΫΟφΕΦ”–Κή¥σ”≈ Τ, ÷ΒΒΟ»ΥΟ«…ν»κΧΫΨΩ.
3.2 ÷ΉΝω÷ΈΝΤ
άϊ”ΟΜ·―ß“©ΈοΒΡΕΨ–‘ «÷ΈΝΤ÷ΉΝω≥Θ”ΟΒΡΖΫ Ϋ÷°“Μ. Ά®ΙΐΖ÷Ή”…ηΦΤΩ…“‘”––ßΒΊΫΪΜ·―ß“©ΈοΑϋ‘ΊΒΫκΡΉ‘ΉιΉΑΧε÷–. Li Β»[63]άϊ”ΟΟΗœλ”Π–‘ΒΡ ςΉ¥–ΆκΡΖ÷Ή”Ν§Ϋ”Μ·―ß“©Έο Dox, …ηΦΤΒΡΖ÷Ή”Ω…Ή‘ΉιΉΑ–Έ≥…±μΟφ¥χΗΚΒγΚ…ΒΡ«ρ–ΆΝΘΉ”, ”…”Ύ ηΥ°Ής”Ο, Dox ΜυΆ≈Φ·÷–‘ΎΝΘΉ”ΡΎ≤Ω, “ρ¥Υ”––ßΫΒΒΆΝΥ Dox Ε‘…ζΈοΧεΒΡΕΨ–‘Ής”Ο. ‘ΎΟΗΒΡ¥ΧΦΛœ¬, ΧεœΒΖΔ…ζΫβΉιΉΑΚσ ΆΖ≈≥ω Dox, ¥”Εχ¥οΒΫ÷ΈΝΤΒΡΡΩΒΡ.
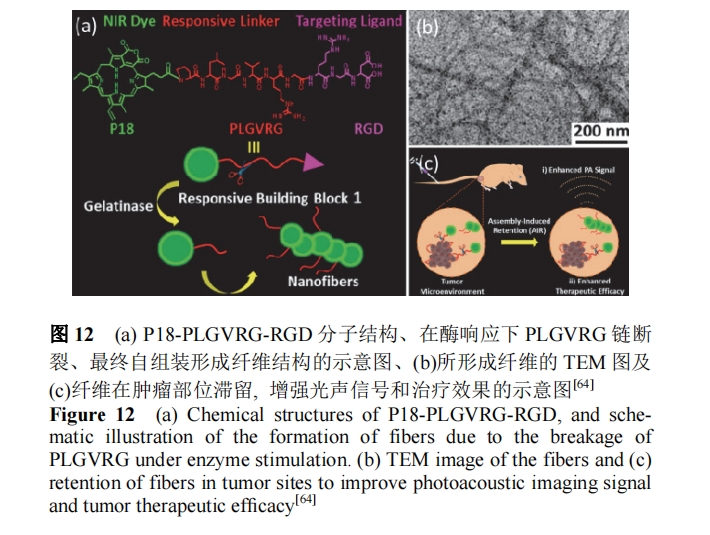
Wang Β»[64]…ηΦΤΝΥ“Μ÷÷œλ”Π–‘ΒΡΓΔ”…κΡ”κΚλΉœΥΊΝ§Ϋ”–Έ≥…ΒΡ–ΓΖ÷Ή”«ΑΧε P18-PLGVRGRGD. κΡ Ν¥(PLGVRGRGD)Ω…±Μ÷ΉΝωΈΔΜΖΨ≥÷–ΒΡΟςΫΚΟΗ―Γ‘ώ–‘ΒΊ«–Εœ, ΜώΒΟ≤–ΝτΒΡ ηΥ°–‘Ζ÷Ή”(P18-PLG)Ω…Ή‘ΉιΉΑ–Έ≥…Ρ…ΟΉœΥΈ§(ΆΦ12aΚΆ12b). œΥΈ§ΫαΙΙΩ…―”≥Λ‘Ύ÷ΉΝω≤ΩΈΜΒΡ÷ΆΝτ, ¥”ΕχΧαΗΏ÷ΉΝω≤ΩΈΜΒΡΙβ…υ–≈Κ≈ΚΆ÷ΈΝΤ–ßΙϊ(ΆΦ 12c). άύΥΤΒΡ, άϊ”Ο÷ΉΝωΈΔΜΖΨ≥…ηΦΤœλ”Π–‘Ζ÷Ή”ΓΔΩΊ÷ΤΖ÷Ή”‘Ύ÷ΉΝωΜΖΨ≥÷–ΒΡΉ‘ΉιΉΑΩ…ΈΣ÷ΉΝω’οΕœΚΆ÷ΈΝΤΒΡΖΔ’ΙΧαΙΑ–¬ΒΡΥΦ¬ΖΚΆΖΫΖ®[65].
ΙβΕ·ΝΠΚΆΙβ»»÷ΈΝΤ «“Μ÷÷ΙβΗ®÷ζΖ««÷»κΒΡ÷ΉΝω÷ΈΝΤΖΫ Ϋ, ‘Ύ÷ΈΝΤ÷ΉΝωΓΔΤΛΖτ≤ΓΚΆΈΔ…ζΈοΗ–»ΨΒ»Φ≤≤Γ÷–”–Ή≈÷Ί“Σ”Π”Ο. ΙβΕ·ΝΠΚΆΙβ»»÷ΈΝΤΨΏ”–≤ΌΉςΦρΒΞΓΔ―Γ‘ώ–‘ΗΏΓΔΕΨΗ±Ής”Ο–ΓΒ»”≈ Τ, ΫϋΡξά¥ΒΟΒΫΝΥ―ΗΥΌΖΔ’Ι, “―”–“Μ–©“©Έο±Μ≈ζΉΦ”Ο”ΎΝΌ¥≤”Π”Ο. Ά®Ιΐ“ΐ»κΚœ ΒΡΙβΟτΦΝ”κκΡΙ≤ΉιΉΑ[66], “ΜΖΫΟφΩ… Βœ÷Ή‘ΉιΉΑΧεΫαΙΙΒΡΨΪΉΦΒςΩΊ, Νμ“ΜΖΫΟφ, ”–άϊ”ΎΧαΗΏ“©ΈοΒΡ…ζΈοΜν–‘“‘ΦΑ…ζΈοΦφ»ί–‘.
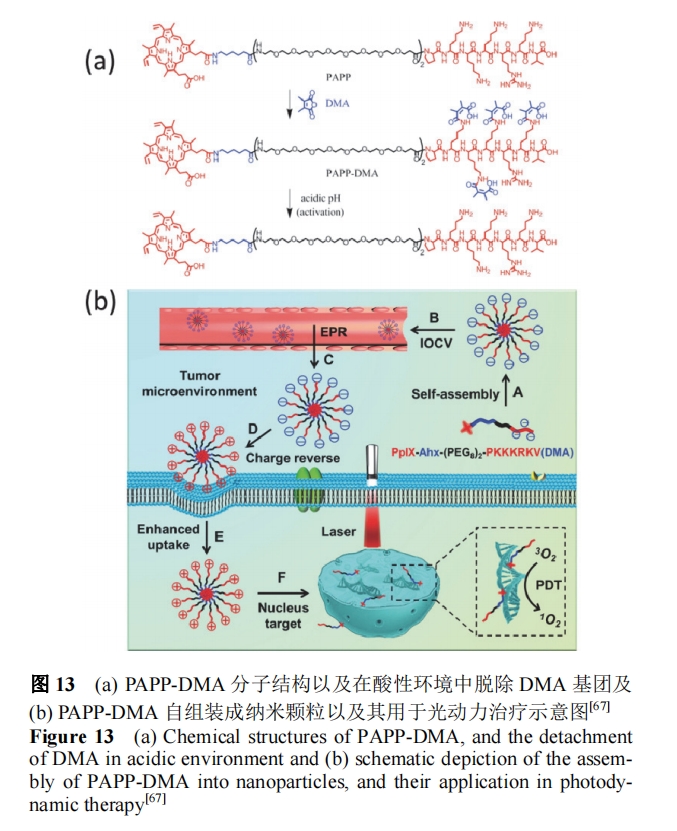
Han Β»[67]…ηΦΤΫΪΥατϊΗΡ–‘ΒΡΓΔΨΏ”–ΚΥΥαΑ–œρ–‘ΒΡκΡ”κΏ≤ΏχΖ÷Ή”Ά®Ιΐ PEG Ι≤ΦέΦϋœύΝ§(PAPP-DMA), ΗΟΖ÷Ή”Ω…–Έ≥…±μΟφ¥χΗΚΒγΚ…ΒΡΡ…ΟΉΩ≈ΝΘ. ΝΘΉ”Ϋχ»κΥα–‘ΒΡ÷ΉΝωΈΔΜΖΨ≥Κσ, ”…”Ύ DMA ΜυΆ≈¥” PAPP-DMA Ζ÷Ή”…œΆ―»Ξ, ΙΝΘΉ”±μΟφΒγΚ…ΖΔ…ζΖ¥ΉΣ, ΧαΗΏΝΥ÷ΉΝωœΗΑϊΕ‘ΝΘΉ”ΒΡ…ψ»ΓΡήΝΠ. κΡΕ‘ΚΥΒΡΑ–œρ–‘¥Ό ΙΝΘΉ”Ϋχ»κœΗΑϊΚΥ≤Δ‘ΎΚΥΡΎ Βœ÷ΙβΕ·ΝΠΙΠΡή(ΆΦ 13).
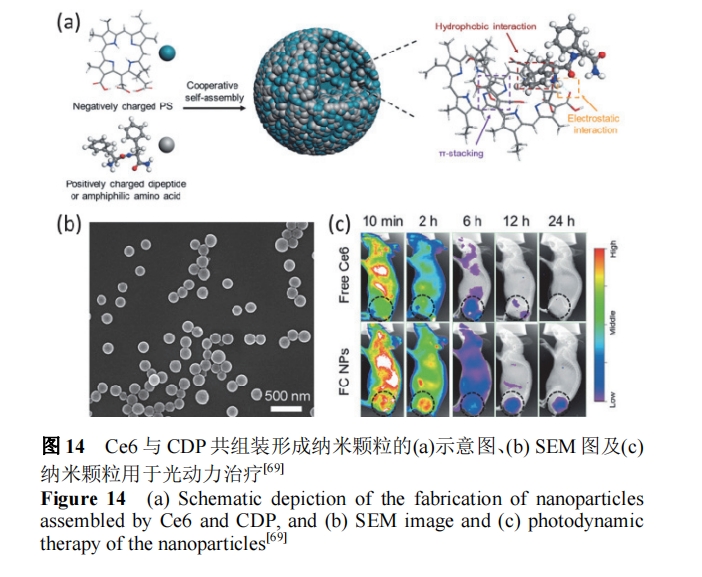
Yan Β»[68]άϊ”Ο CDP(―τάκΉ”Μ·ΒΡ FF Ζ÷Ή”)”κ GA Ζ÷Ή”ΦδΖΔ…ζ Schiff ΦνΖ¥”ΠΩ…ΒςΩΊ–Έ≥…«ρ–ΈΩ≈ΝΘ, ‘ΎΩ≈ΝΘ±μΟφΩ…Ϋχ“Μ≤ΫΆ®ΙΐΨ≤ΒγΉς”Ο–ό ΈΙβΟτΦΝΖ÷Ή”Εΰ«βΏ≤Ζ‘(Ce6)ΚΆΗΈΥΊ(Hep)Ζ÷Ή”, Φ¥Ω…ΜώΒΟΤΫΨυΝΘΨΕΈΣ 100 nmΓΔ±μΟφΒγ ΤΈΣΘ≠25 mV ΒΡΩ≈ΝΘ, Ω≈ΝΘΩ…“‘ΚήΚΟΒΊ±Μ÷ΉΝωœΗΑϊ…ψ»Γ≤ΔΨΏ”–ΫœΚΟΒΡΙβΕ·ΝΠ÷ΈΝΤ–ßΙϊ. ΩΦ¬«ΒΫ GA Ζ÷Ή”Ε‘…ζΈοΧεΒΡΕΨ–‘, ΥϊΟ«ΫΪΧεœΒΫχ––ΗΡΫχ: ÷±Ϋ”“ΐ»κ Ce6”κ CDP Ι≤ΉιΉΑ–Έ≥…Έ»Ε®ΒΡΒΞΖ÷…ΔΡ…ΟΉΩ≈ΝΘ. ΉιΉΑ–Έ≥…ΒΡΙβΟτΦΝΡ…ΟΉΩ≈ΝΘΝΘΨΕΩ…ΒςΓΔ‘Ί“©ΝΩΗΏΓΔΕ‘“©ΈοΕύ÷Ίœλ”Π–‘ ΆΖ≈(pHΓΔ±μΟφΜν–‘ΦΝ“‘ΦΑΟΗœλ”Π), ≤Δ«“ΨΏ”–‘ω«ΩΒΡœΗΑϊ…ψ»ΓΚΆ÷ΉΝωΑ–œρΗΜΦ·ΒΡΧΊΒψ, ΙΤδ‘ΎΧεΡΎΆβΙβΕ·ΝΠΩΙ÷ΉΝω÷ΈΝΤ÷–ΤπΒΫΝΥΟςœ‘–ßΙϊ, Ω… Βœ÷“Μ¥ΈΗχ“©ΓΔ“Μ¥ΈΙβ’’, ±ψΩ…¥οΒΫΦΗΚθΆξ»Ϊ«ε≥ΐ–Γ σ÷ΉΝωΒΡ–ßΙϊ(ΆΦ14)[69].
Yan Β»[47]ΜΙάϊ”ΟΜ·―ßΦϋΝ§Ϋ”ΒΡΏ≤Ώχ-ΕΰκΡΗ¥ΚœΖ÷Ή”Ή‘ΉιΉΑ–Έ≥…ΨΏ”–ΚήΚΟΒΡΙβ»»–ßΙϊΒΡΡ…ΟΉΒψ. Ρ…ΟΉΒψΫαΙΙ÷–Ώ≤ΏχΠ–-Π–Ής”ΟΥυ–Έ≥…ΒΡ J ΨέΦ·ΫαΙΙΩ…“‘”––ßΒΊ“÷÷Τ”ΪΙβΖΔ…δ“‘ΦΑΒΞœΏΧ§―θΒΡ≤ζ…ζ, ¥”Εχ Ι’ϊΗωΡ…ΟΉ‘ΎΙβ’’ΧθΦΰœ¬ΨΏ”–ΚήΗΏΒΡΙβ»»ΉΣΜΜ–ß¬ , ΫχΕχ”Ο”Ύ÷ΉΝωΒΡΙβ»»÷ΈΝΤ÷–. άϊ”Ο‘≠ΈΜΩσΜ·Ζ¥”Π÷Τ±ΗΒΡΑϋΚ§ Au Ω≈ΝΘΒΡΩ…ΉΔ…δΒΡΥ°ΡΐΫΚ, Ω…ΉςΈΣ“©Έο‘ΊΧεΗΚ‘Ί“©ΈοΚσ÷±Ϋ”±ΜΉΔ…δ≤Δ±ΘΝτ‘Ύ÷ΉΝωΡΎ≤Ω, Ϋχ––”––ßΒΡΙβΕ·ΝΠ÷ΈΝΤ[49]. ΝμΆβ, ”…”ΎΫπΡ…ΟΉΩ≈ΝΘ±Ψ…μΨΏ”–ΚήΚΟΒΡΙβ»»–ßΙϊ, “ρ¥Υ, ’β÷÷ΫΚ‘≠-Ϋπ‘”Μ·Υ°ΡΐΫΚ“ύΩ…”Ο”Ύ÷ΉΝωΒΡΙβ»»÷ΈΝΤ“‘ΦΑΙβ»»-ΙβΕ·ΝΠΝΣΚœ÷ΈΝΤ÷–[70].
3.3 “ΐ»κΤδΥϊΙΠΡή–‘Ζ÷Ή”
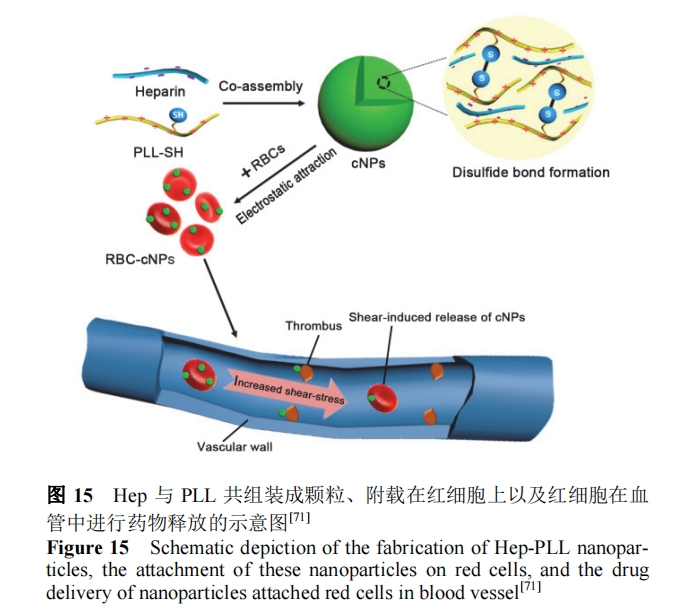
―ΣΥ®“Μ÷± «Άΰ–≤»ΥάύΫΓΩΒΒΡ–Ρ―ΣΙήΦ≤≤Γ, ΗΈΥΊ(Hep) «≥Θ”ΟΒΡ“Μ÷÷”––ßΒΡΩΙΡΐ“©Έο, ΒΪ «ΗΟ“©Έο÷±Ϋ”ΒΡΨ≤¬ωΉΔ…δΜα≤ζ…ζ≤Γάμ≥ω―ΣΒ»Η±Ζ¥”Π, Υυ“‘Τδ”Π”Ο“Μ÷± ήΒΫœό÷Τ. Yan Β»[71]ΫΪ Hep “ΐ»κέœΜυΜ·ΒΡ PLL Ή‘ΉιΉΑΧεœΒ÷–, Ϋη÷ζ”Ύ Hep ”κ PLL ΦδΒΡΨ≤ΒγΉς”Ο÷Τ±ΗΡ…ΟΉΩ≈ΝΘ, ÷°ΚσΫΪΩ≈ΝΘΈϋΗΫ‘ΎΚλœΗΑϊ±μΟφ, ”Ο”Ύ―ΣΙήΒΡΩΙΥ®÷ΈΝΤ≤Δ»ΓΒΟΝΥΝΦΚΟ–ßΙϊ(ΆΦ 15).
“ΐ»κΙΠΡή–‘ΟΗΖ÷Ή””’ΒΦΩ… Βœ÷κΡΉ‘ΉιΉΑ“‘ΦΑΉ‘ΉιΉΑΧε‘Ύ…ζΈοΧεœΒ÷–ΒΡ”Π”Ο[72ΓΪ74]. Xu Β»[75,76]‘ΎΗΟΖΫΟφΉωΝΥœΒΝ––‘ΙΛΉς. άΐ»γ, ‘ΎΟΗΒΡΆ―ΝΉΥαΉς”Οœ¬, Ω…”’ΒΦΙ―κΡ‘ΎœΗΑϊ÷––Έ≥…œΥΈ§ΫαΙΙ, ¥”Εχ“÷÷Τ÷ΉΝωœΗΑϊΒΡΜν –‘[77,78]. ΝμΆβ, ΗΟΉιΫΪ D-Α±ΜυΥαΜρΧ«ή’“ΐ»κκΡΖ÷Ή”…œ, Ω…“‘”––ßΒΊΧαΗΏκΡΥυ–Έ≥…ΡΐΫΚΒ÷ΩΙΒΑΑΉΟΗ K ΒΡΥ°ΫβΡήΝΠ[79,80].
ΤδΥϊ“Μ–©ΨΏ”–ΙβΓΔΒγΓΔ¥≈ΒΡΖ÷Ή”“ύΩ…“ΐ»κκΡΖ÷Ή”Ή‘ΉιΉΑΧεœΒ÷–, ≤Δ”––ßΒΊ‘ω«ΩΧεœΒΒΡ–‘Ρή, ΈΣκΡΉ‘ΉιΉΑΒΡΙΠΡήΜ·ΧαΙ©ΝΥ”–άϊ÷ß≥≈.
4 ΉήΫα”κ’ΙΆϊ
κΡ≥§Ζ÷Ή”Ή‘ΉιΉΑ‘Ύ÷ΎΕύΫΜ≤φΝλ”ρ, Αϋά®Μ·―ßΓΔ≤ΡΝœΓΔ“‘ΦΑ…ζΈοΩΤ―ß, ΕΦ”–÷Ί“ΣΒΡ―–ΨΩ“β“ε. κΡΖ÷Ή”Ω…Ή‘ΉιΉΑ–Έ≥…ΙήΓΔœΏΓΔΩ≈ΝΘΓΔœΥΈ§Β»Εύ÷÷¥”Ρ…ΟΉ÷ΝΈΔΟΉ≥ΏΕ»ΒΡ≤ΡΝœ, ’β–©≤ΡΝœ‘Ύ…ζΈο“Ϋ“©÷–ΨΏ”–ΙψΖΚ”Π”Ο«ΑΨΑ. ”…”ΎκΡΉ‘ΉιΉΑΙΐ≥Χ «‘ΎΗς÷÷Ζ«Ι≤ΦέΦϋΑϋά®«βΦϋΓΔΠ–-Π–Ε―ΜΐΓΔ ηΥ°Ής”ΟΓΔΨ≤ΒγΝΠ“‘ΦΑΖΕΒ¬ΜΣΝΠΒΡ–≠Ά§Ής”Οœ¬ Βœ÷ΒΡ, “ρ¥Υ, ΚœάμΒΊΒςΫΎ’β–©ΝΠΒΡœύΜΞΉς”Ο, ±ψΩ…¥”Ε·ΝΠ―ßΚΆ»»ΝΠ―ß…œΕ‘Ή‘ΉιΉΑΧεΫαΙΙΫχ––ΒςΩΊ, ¥”Εχ Βœ÷Ή‘ΉιΉΑΧεΙΠΡήΒΡΕύ―υΜ·.
Υδ»ΜΆ®ΙΐΒςΩΊΉιΉΑΜΖΨ≥“ρΥΊ(Αϋά® pHΓΔΈ¬Ε»ΓΔ≈®Ε»ΓΔΆβ≥ΓΒ»)Ω…“‘ΚήΚΟΒΊΗΡ±δΧεœΒ÷–Ζ«Ι≤ΦέΦϋΒΡœύΜΞΉς”Ο, ΒΪ «ΗΟΖΫΖ®Ιΐ”ΎΒΞ“Μ«“≤Μάϊ”ΎΉ‘ΉιΉΑΧεΙΠΡήΜ·ΒΡ Βœ÷. ΕχΆ®ΙΐΒςΩΊΉιΉΑΜυ‘ΣΒΡΖ÷Ή”ΫαΙΙΓΔ“ύΜρ…ηΦΤΝΫ÷÷(ΦΑ“‘…œ)ΉιΉΑΜυ‘ΣΦδΒΡΙ≤ΉιΉΑΫΪΗϋ”–άϊ”ΎΜώΒΟΫαΙΙΩ…ΒςΒΡΉ‘ΉιΉΑΧε, Ά§ ±“ΐ»κΙβΟτΦΝΓΔΜ·“©ΓΔΟΗΒ»ΙΠΡή–‘Ζ÷Ή””κκΡΖ÷Ή”Ϋχ––Ι≤ΉιΉΑ, Ω…“‘”––ßΧαΗΏκΡΉ‘ΉιΉΑΒΡ–‘Ρή, Βœ÷≤ΡΝœΙΠΡήΒΡΕύ―υΜ·. άΐ»γ, Ά§―υ «άϊ”ΟΕΰκΡ”κΏ≤ΏχΖ÷Ή”Ϋχ––Ι≤ΉιΉΑ, ΒΪ «Ά®ΙΐΗΡ±δΕΰκΡΖ÷Ή”ΒΡ–‘÷ , ±ψΩ…ΜώΒΟ≤ΜΆ§ΫαΙΙΒΡΉ‘ΉιΉΑΧε, ΕχΏ≤ΏχΒΡ“ΐ»κΗ≥”η≤ΡΝœΙβ≤ΕΜώΓΔ“‘ΦΑΙβΟτΒ»ΧΊ–‘, Ι≤ΡΝœΩ…“‘”––ßΒΊ”Π”Ο”Ύ≤ζ«βΓΔΙβΕ·ΝΠ÷ΈΝΤΒ»Νλ”ρ[44,45].
‘ΎΚσ–χΕ‘κΡΖ÷Ή”Ή‘ΉιΉΑΒΡ―–ΨΩ÷–, ≤ΜΡή÷ΜΨ÷œό”ΎΕ‘Ή‘ΉιΉΑΧε–ΈΟ≤ΫαΙΙΒΡΒΞ“ΜΒςΩΊ, Ηϋ–η“ΣΫχ“Μ≤ΫΆΊ’Ι: (1)ΉΔ÷Ί»γΚΈ Βœ÷ΨΪΉΦΒςΩΊ, Αϋά®‘ΎΧΊ β≥ΏΕ»…œΒΡΩΊ÷ΤΓΔΕ‘ΧΊ βΙΠΡήΒΡΒςΩΊ. ‘ΎΖ÷Ή”…ηΦΤΙΐ≥Χ÷–, œΗ–Γ“ρΥΊΒΡ“ΐ»κΜρΗΡ±δ, ΕΦΩ…ΡήΕ‘Ή‘ΉιΉΑΧεΒΡ–ΈΟ≤ΚΆΙΠΡή≤ζ…ζΨό¥σ”Αœλ. άϊ”ΟΕύ÷÷ ÷ΕΈ±»»γΖ÷Ή”Ε·ΝΠ―ßΡΘΡβ, ¥”Εύ≥ΏΕ»Ϋ«Ε»άμΫβ’β–©œΗ–Γ“ρΥΊΕ‘ΧεœΒΡΎΖ«Ι≤ΦέΦϋœύΜΞΉς”ΟΝΠΒΡΗΡ±δ[81], Ω…“‘Ηϋ”––ßΒΊ Βœ÷ΨΪΉΦΒςΩΊΒΡΡΩΒΡ. (2)”κ¥ΥΆ§ ±, “ΣΙΊΉΔΙΠΡήΜ·ΒΡΉ‘ΉιΉΑΧε‘ΎΗ¥‘”ΜΖΨ≥±»»γ…ζάμΜΖΨ≥÷–ΒΡΉιΉΑ/ΫβΉιΉΑΚΆΈ»Ε®–‘Β»Έ Χβ. “ΜΖΫΟφ”–÷ζ”Ύ…ν»κάμΫβ…ζΈοΖ÷Ή”‘ΎΗ¥‘”ΜΖΨ≥œ¬ΒΡΉς”ΟΜζ÷Τ; Νμ“ΜΖΫΟφ“≤ΈΣκΡΉ‘ΉιΉΑΧεœΒ‘Ύ…ζΈο“Ϋ“©ΓΔ¬Χ…ΪΡή‘¥Β»ΕύΗωΝλ”ρΒΡ”Π”ΟΧαΙ©Ηϋ”––ßΒΡ÷ß≥≈.
Οβ‘π…υΟςΘΚ±ΨΈΡΈΣ––“ΒΫΜΝς―ßœΑΘ§Αφ»®Ιι‘≠Ής’ΏΦΑ‘≠‘”÷ΨΥυ”–Θ§»γ”–«÷»®Θ§Ω…ΝΣœΒ…Ψ≥ΐΓΘΈΡ’¬±ξΉΔ”–Ής’ΏΦΑΈΡ’¬≥ω¥ΠΘ§»γ–η‘ΡΕΝ‘≠ΈΡΦΑ≤ΈΩΦΈΡœΉΘ§Ω…‘ΡΕΝ‘≠‘”÷ΨΓΘ

















