
’Σ“ΣΘΚ÷ΉΝω «”…œΗΑϊΓΔœΗΑϊΆβΜυ÷ ΦΑΈΔΜΖΨ≥Β»Εύ“ρΥΊΉι≥…ΒΡΗ¥‘”œΒΆ≥, ≤ΜΆ§“ρΥΊ‘Ύ÷ΉΝωΒΡΖΔ…ζΚΆΖΔ’Ι÷–ΖΔΜ”ΙΊΦϋΉς”Ο. ÷ΉΝωœΗΑϊΓΔœΗΑϊΆβΜυ÷ ΦΑΈΔΜΖΨ≥ΒΡΧΊ“λ–‘Ζ÷ΈωΕ‘”Ύ÷ΉΝωΒΡΨΪΉΦ’οΕœΚΆΑ–œρ÷ΈΝΤ÷ΝΙΊ÷Ί“Σ. ΕύκΡΧΫ’κΨΏ”–ΧΊ“λ–‘ΗΏΓΔ…ζΈοœύ»ί–‘ΚΟΓΔΉι÷·¥©ΆΗΡήΝΠ«ΩΚΆ“Ή”Ύ÷Τ±ΗΒ»”≈Βψ, “―±ΜΙψΖΚ”Ο”Ύ÷ΉΝωΒΡΧΊ“λ–‘≥…œώ―–ΨΩ. ±ΨΈΡΉέ ωΝΥΕύκΡΧΫ’κΕ‘÷ΉΝωœΗΑϊΓΔΟβ“ΏœΗΑϊΒ»œΗΑϊΑ–ΒψΒΡΧΊ“λ–‘≥…œώ; ≤ΔΫι…ήΝΥ“‘ΫΚ‘≠ΒΑΑΉΓΔœΥΈ§ΒΑΑΉΒ»ΆβΜυ÷ ΒΑΑΉΈΣΑ–ΒψΒΡ÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κΒΡ≥…œώ―–ΨΩ. ±ΨΈΡΜΙΉήΫαΝΥΕ‘÷ΉΝωΈΔΜΖΨ≥÷–»θΥα–‘ΓΔΗΏΟΗΜν–‘Β»“ρΥΊœλ”ΠΒΡ÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κΦΑΤδ…ζΈο≥…œώ”Π”Ο. ΉνΚσ, ±ΨΈΡΉήΫα≤ΔΧ÷¬έΝΥ÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κΥυΟφΝΌΒΡΧτ’Ϋ”κΜζ”ω, ’ΙΆϊΝΥΤδ‘Ύ÷ΉΝωΨΪΉΦ’οΕœΚΆΗω–‘Μ·÷ΈΝΤΝλ”ρΒΡ«ΑΨΑ.
÷ΉΝω «Αϋά®÷ΉΝωœΗΑϊΓΔœΗΑϊΆβΜυ÷ ΦΑΈΔΜΖΨ≥Β»≤ΜΆ§ΉιΖ÷ΒΡΗ¥‘”…ζΜ·œΒΆ≥, ≤ΜΆ§ΉιΖ÷‘Ύ÷ΉΝωΒΡΖΔ…ζΓΔΖΔ’ΙΚΆΉΣ“Τ÷–ΖΔΜ”÷Ί“ΣΉς”Ο[1-2]. ÷ΉΝωΨΏ”–«χ±π”Ύ’ΐ≥ΘΉι÷·ΒΡ≤Γάμ–‘œΗΑϊΆβΜυ÷ (ECM)ΓΔ–¬…ζ―ΣΙήΚΆΝήΑΆΙήΆχ¬γ, “‘ΦΑ“λ≥ΘΒΡœΗΑϊ±μ–Ά[3-4]. Ά§ ±, »±―θΓΔ»θΥα–‘ΚΆΗΏΜυ÷ Ϋπ τΒΑΑΉΟΗ(MMPs)Μν–‘Β»“ρΥΊ «÷ΉΝωΈΔΜΖΨ≥”κ’ΐ≥Θ…ζάμΜΖΨ≥ΒΡ÷Ί“Σ≤ν“λ[5-6]. ÷ΉΝωœΗΑϊΓΔœΗΑϊΆβΜυ÷ ΦΑΈΔΜΖΨ≥ΒΡΉι≥…ΓΔΫαΙΙΚΆ…ζΜ·–‘÷ ΒΡΗΡ±δ“―≥…ΈΣ”Αœλ÷ΉΝωΕύ―υ–‘ΚΆ«÷œ°–‘ΒΡΙΊΦϋ‘≠“ρ, ≤ΔΜα”ΑœλΩΙΑ©“©ΈοΒΡΉι÷·…χΆΗΚΆΑ–œΗΑϊΟτΗ––‘[7⇓-9]. “ρ¥Υ, ÷ΉΝωœΗΑϊΓΔœΗΑϊΆβΜυ÷ ΦΑΈΔΜΖΨ≥ΒΡΩ… ”Μ·Ζ÷ΈωΕ‘÷ΉΝωΒΡ≤ΓάμΖ÷ΈωΓΔ‘γΤΎ’οΕœΦΑ÷ΈΝΤΨΏ”–÷Ί¥σ“β“ε[10-11].
Ζ÷Ή”ΧΊ“λ–‘≥…œώΧΫ’κΒΡΩΣΖΔ“―÷πΫΞ≥…ΈΣ÷ΉΝωΩ… ”Μ·Νλ”ρΒΡ»»Βψ. ΩΙΧεΓΔΕύκΡΚΆΚΥΥα ΧεΒ»ΧΊ“λ–‘Ζ÷Ή” «ΧΫ’κΒΡΚΥ–ΡΉιΦΰ, ”Ο”Ύ÷ΉΝω±ξ÷ΨΈοΒΡΧΊ“λ–‘ Ε±π[12⇓⇓-15]. Ά§ ±, Ν§Ϋ”ΜΖΨ≥ΟτΗ––ΆΉιΦΰΒΡΖ÷Ή”ΧΫ’κΡήΙΜΧΊ“λ–‘ΒΡΖ÷Έω÷ΉΝωΒΡpH ÷Β±δΜ·ΓΔΟΗΜν–‘ΚΆ―θΤχΥ°ΤΫ[16]. Υ≥¥≈–‘Έο÷ ΓΔΖ≈…δ–‘ΚΥΥΊΓΔ”ΪΙβΖ÷Ή”ΚΆΡ…ΟΉΝΘΉ”Β»Έο÷ ΉςΈΣ±®ΗφΜυΆ≈, “―‘Ύ¥≈Ι≤’ώ≥…œώ(MRI)ΓΔΒΞΙβΉ”ΖΔ…δΦΤΥψΜζΕœ≤ψ≥…œώ θ(SPECT)ΓΔ’ΐΒγΉ”ΖΔ…δΕœ≤ψ≥…œώ θ(PET)ΚΆ”ΪΙβ≥…œώ÷–ΙψΖΚ”Π”Ο[17⇓⇓⇓⇓⇓-23]. Ζ÷Ή”ΧΊ“λ–‘≥…œώΧΫ’κ“―≥…ΈΣΦΪΨΏ«±ΝΠΒΡΝΌ¥≤‘λ”ΑΦΝ.
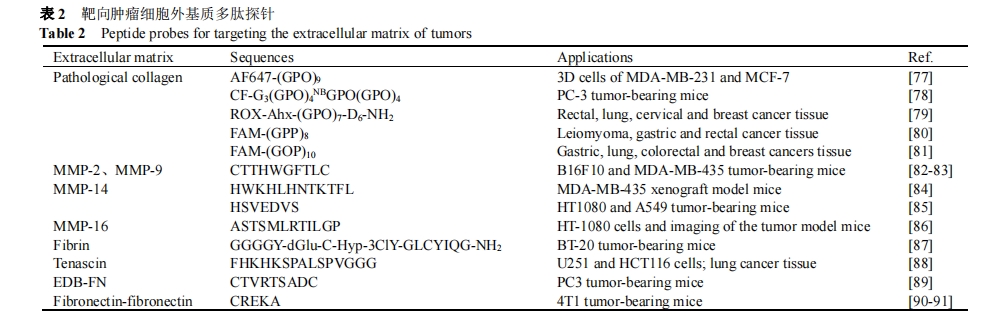
ΕύκΡΧΫ’κΨΏ”–ΧΊ“λ–‘ΗΏΓΔ…ζΈοœύ»ί–‘ΚΟΓΔΉι÷·¥©ΆΗΡήΝΠ«ΩΚΆ“Ή”ΎΚœ≥…–ό ΈΒ»”≈ΒψΕχ±ΜΙψΖΚ”Ο”ΎΖ÷Ή”Υ°ΤΫΒΡ÷ΉΝω≥…œώ―–ΨΩ[24⇓-26]. ÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κΆ®Ιΐ÷±Ϋ””κ÷ΉΝω±ξ÷ΨΈοΫαΚœΜρœλ”Π÷ΉΝωΈΔΜΖΨ≥“ρΥΊΒΡ±δΜ·, Βœ÷÷ΉΝωΒΡΧΊ“λ–‘Φλ≤β(ΆΦ1). Τδ÷–, »Υ±μΤΛ…ζ≥Λ“ρΉ” ήΧε(HER)ΓΔ“ΕΥα ήΧεΚΆ―ΣΙήΡΎΤΛ…ζ≥Λ“ρΉ” ήΧε(VEGFR)Β»œΗΑϊΡΛ ήΧε“―≥…ΈΣΩΣΖΔ÷ΉΝωΑ–œρΕύκΡΧΫ’κΒΡ÷Ί“Σ±ξ÷ΨΈο(±μ1)[27⇓-29]. ΫΚ‘≠ΒΑΑΉΓΔœΥΈ§ΒΑΑΉΒ»œΗΑϊΆβΜυ÷ ΒΑΑΉ‘ρ «Ά®ΙΐΑ–œρΕύκΡΧΫ’κ―–ΨΩ÷ΉΝω«÷œ°ΚΆΉΣ“ΤΒΡΙΊΦϋΑ–Βψ(±μ2)[1,30]. »θΥα–‘ΚΆΗΏΟΗΜν–‘ΒΡΈΔΜΖΨ≥œλ”ΠΒΡΕύκΡΧΫ’κ“≤“―≥…ΈΣ÷ΉΝωΧΊ“λ–‘≥…œώΒΡ÷Ί“ΣΙΛΨΏ(±μ3)[5,31].
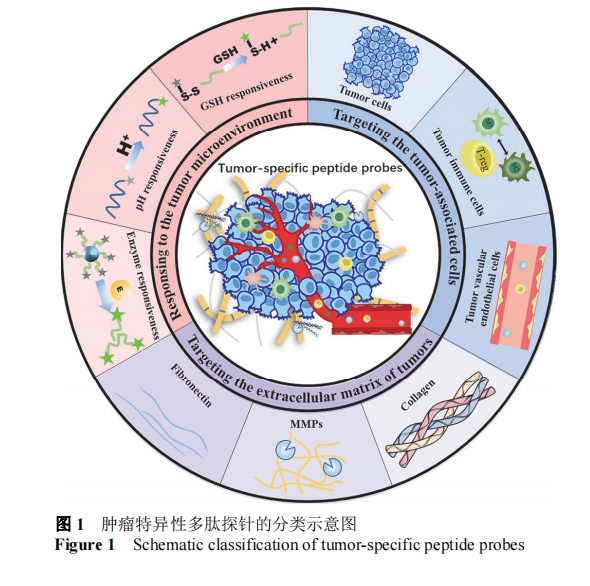
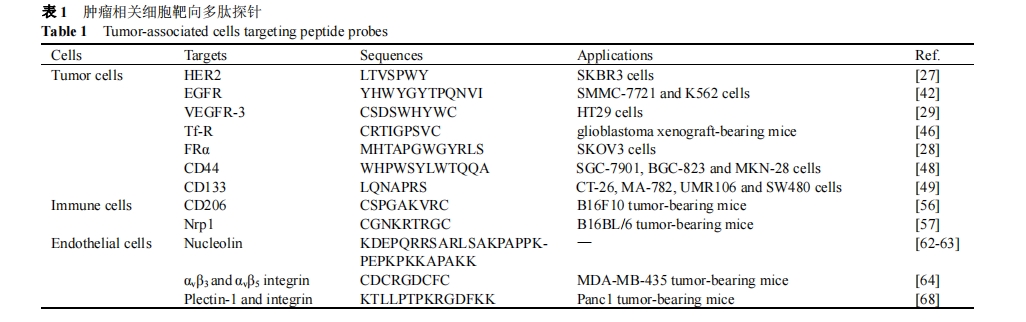
÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κΒΡΩΣΖΔΈΣ÷ΉΝωΒΡΨΪΉΦ≥…œώΧαΙ©ΝΥΗϋΕύΒΡΜζΜαΚΆΩ…Ρή. Έ“Ο«ΫΪ“‘÷ΉΝωœύΙΊœΗΑϊΓΔ÷ΉΝωœΗΑϊΆβΜυ÷ ΒΑΑΉ“‘ΦΑ÷ΉΝωΈΔΜΖΨ≥œλ”Π“ρΥΊ»ΐΗωΖΫΟφΕ‘÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κΫχ––Ζ÷άύΉέ ω. ±ΨΈΡΫΪœΒΆ≥ΒΊΫι…ή÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κΒΡ―–ΨΩΫχ’Ι, ≤ΔΗ≈ ωΤδ‘Ύ…ζΈο≥…œώΝλ”ρΒΡ”Π”Ο.

2 ÷ΉΝωœύΙΊœΗΑϊΑ–œρΕύκΡΧΫ’κ
÷ΉΝωΒΡΖΔ’Ι «ΦΪΤδΗ¥‘”ΒΡΙΐ≥Χ, …φΦΑ≤ΜΆ§άύ–ΆœΗΑϊΒΡΙ≤Ά§Ής”Ο. ÷ΉΝωœΗΑϊ «÷ΉΝωΖΔ’ΙΒΡ÷¥––’Ώ, Τδ‘ω÷≥ΓΔ«®“ΤΒ»Ιΐ≥Χ÷±Ϋ”Ζ¥”≥ΝΥ÷ΉΝωΒΡΖΔ’ΙΫΉΕΈ. Οβ“ΏœΗΑϊΆ®ΙΐΖ÷ΟΎ≤ΜΆ§ΒΡœΗΑϊ“ρΉ”, ÷¥––ΩΙ÷ΉΝωΜρ¥Ό÷ΉΝωΒΡΥΪœρΉς”Ο. ÷ΉΝωΡΎΤΛœΗΑϊΈΜ”Ύ÷ΉΝω―ΣΙήΜρΝήΑΆΙή÷–, ΩΊ÷ΤΈο÷ ”κ÷ΉΝωΉι÷·ΒΡ¥Ϊ δΫΜΜΞ, ≤Έ”κ÷ΉΝωΒΡΉΣ“ΤΚΆά©…Δ[2,32-33]. “ρ¥Υ, ÷ΉΝωœΗΑϊΓΔΟβ“ΏœΗΑϊΚΆ÷ΉΝωΡΎΤΛœΗΑϊΒΡΧΊ“λ–‘Φλ≤β, Ε‘÷ΉΝωΒΡΨΪΉΦ’οΕœΚΆ‘ΛΚσΖ÷ΈωΨΏ”–÷Ί“Σ“β“ε.
2.1 ÷ΉΝωœΗΑϊΑ–œρΕύκΡΧΫ’κ
÷ΉΝωœΗΑϊΒΡΡΛΒΑΑΉ≤Έ”κΒςΩΊ÷ΉΝωΒΡ«÷œ°ΚΆΉΣ“Τ, «÷ΉΝω’οΕœ÷–Ήν≥ΘΦϊΒΡ…ζΈο±ξ÷ΨΈο. HERΓΔ±μΤΛ…ζ≥Λ“ρΉ” ήΧε(EGFR)ΚΆVEGF «Φλ≤β÷ΉΝωœΗΑϊΒΡ÷Ί“ΣΑ–Βψ[34⇓⇓⇓-38]. SioudΒ»[27]ΙΙΫ®ΝΥΑ–œρΒΊΫαΚœHER2ΒΡΕύκΡΧΫ’κGFP-GGG-LTVSPWY. ΗΟΧΫ’κΧΊ“λ–‘ΒΊ≥…œώΗΏ±μ¥οHER2ΒΡSKBR3œΗΑϊ. ChengΒ»[39]ΩΣΖΔΝΥHER2Α–œρΕύκΡRSLWSDFYASASRGP, Ώ≈ΏαίΦ¬Χ(ICG)–ό ΈΒΡκΡΧΫ’κ±Μ”Ο”Ύ–Γ σ“Τ÷≤ΝωΡΘ–ΆΒΡΫϋΚλΆβΕΰ«χ(NIR-II)≥…œώ. ZhangΒ»[40]ΙΙΫ®ΝΥHER2ΚΆSR-BIΒΡΥΪΑ–œρκΡFY-35. œύΫœ”ΎΫωΑ–œρSR-BIΒΡΕύκΡΧΫ’κ, FY-35ΨΏ”–Ηϋ≥ΛΒΡ÷ΉΝω±ΘΝτ ±Φδ. RobertsΒ»[41]Ά®ΙΐmRNA’Ι ΨΦΦ θ…Η―ΓΝΥHER2Α–œρΕύκΡSUPR4. SUPR4Ε‘HER2―τ–‘ΒΡBT-474œΗΑϊΒΡ±μΙέKDΈΣ13Γά2 nmol/L, “―”Ο”ΎSKOv3Κ…Νω–Γ σΒΡΫϋΚλΆβ”ΪΙβ≥…œώ. GuΒ»[42]ΩΣΖΔΝΥΧΊ“λ–‘ Ε±πEGFRΒΡΕύκΡΧΫ’κFITC-YHWYGYTPQNVI. ΗΟΧΫ’κ―Γ‘ώ–‘ΒΊΫαΚœEGFR―τ–‘ΒΡSMMC-7721œΗΑϊ, Εχ”κEGFR“θ–‘ΒΡœΗΑϊΈόΟςœ‘ΫαΚœ. GuΒ»[43]ΩΣΖΔΝΥEGFRΧΊ“λ–‘ΕύκΡSYRRPSQIRY, ”Ο”Ύ÷ΉΝωΡΘ–Ά–Γ σ÷ΉΝωΉΣ“ΤΒΡΦύ≤β.
ZhangΒ»[29]ΩΣΖΔΝΥΕύκΡΧΫ’κFITC-CSDSWHYWC (FITC-P1), ”Ο”ΎVEGFRΒΡΧΊ“λ–‘Φλ≤β. FITC-P1ΒΡœΗΑϊ≥…œώ±μΟςFITC-P1”κ±μ¥οVEGFR-3ΒΡHT29œΗΑϊΧΊ“λ–‘ΫαΚœ, ΒΪ≤ΜΡήΫαΚœEVC304œΗΑϊ. SunΒ»[44]άϊ”ΟΒΆΟήΕ»÷§ΒΑΑΉ ήΧεœύΙΊΒΑΑΉ1ΒΡΧΊ“λ–‘ΕύκΡAngiopep-2–ό ΈΒΡAg2S ΝΩΉ”Βψ, ΙΙΫ®ΝΥΫϋΚλΆβΕΰ«χΖ÷Ή”≥…œώΧΫ’κ”Ο”ΎΡ‘ΫΚ÷ ΝωœΗΑϊΒΡΑ–œρ≥…œώ. p32ΒΑΑΉ‘ΎΕύ÷÷÷ΉΝω÷–ΗΏ±μ¥ο, ”κΑ©÷ΔΒΡΕώ–‘≥ΧΕ»œύΙΊ. YanΒ»[45]Ά®ΙΐΫΪp32Α–œρκΡCGNKRTRGC (LyP-1)”κ…ζΈοΚœ≥…ΒΡGVsΫαΚœ, ΩΣΖΔ≥ω”…LyP-1–ό ΈΒΡΤχΧεΡ“≈ίLyP-1-GVs, ≤Δ Βœ÷ΝΥΚ…Νω–Γ σΒΡ≥§…υ≥…œώ.
“ΕΥα ήΧε(FRΠΝ) «¬―≥≤Α©Φλ≤β÷–≥Θ”ΟΒΡ÷ΉΝω±ξ÷ΨΈο. WangΒ»[28]ΩΣΖΔΝΥFRΠΝΧΊ“λ–‘ΕύκΡΧΫ’κFITC-MHTAPG- WGYRLS (FITC-C7). ‘Ύ÷ΉΝωœΗΑϊ≥…œώΒΡ―–ΨΩ÷–, FITC-C7ΧΊ“λ–‘ Ε±πFRΠΝ±μ¥ο―τ–‘ΒΡ»Υ¬―≥≤Α©œΗΑϊSKOV3, Εχ”κFRΠΝ±μ¥ο“θ–‘ΒΡΗΈΑ©œΗΑϊHepG2ΈόΫαΚœ. ΉΣΧζΒΑΑΉ ήΧε(Tf-R) «»ΥΫΚ÷ ΡΗœΗΑϊΝωΦλ≤β÷–≥Θ”ΟΒΡ÷ΉΝω±ξ÷ΨΈο[46]. Tf-RΒΡΜΖΉ¥Α–œρΕύκΡCRTIGPSVC±Μ”Ο”ΎΫΚ÷ ΡΗœΗΑϊΝω–Γ σΉι÷·÷–Tf-RΒΡΧΊ“λ–‘≥…œώ[47].
CD44ΚΆCD133 «÷ΉΝωΫχ’Ι÷–≥ΘΦϊΒΡΧ«ΒΑΑΉ±ξ÷ΨΈο, “―Ψ≠≥…ΈΣΕώ–‘÷ΉΝωΦλ≤βΒΡ÷Ί“ΣΑ–Βψ[48-49]. LuΒ»[50]ΩΣΖΔΝΥCD44Α–œρΕύκΡΧΫ’κFITC-WHPWSYLWTQQA, ΗΟΧΫ’κ”κΗΏ±μ¥οCD44ΒΡΈΗΑ©œΗΑϊSGC-7901ΚΆBGC-823ΧΊ“λ–‘ΫαΚœ. XuΒ»[51]ΩΣΖΔΝΥCD44 Α–œρΒΡΕύκΡΉ‘ΉιΉΑΧΫ’κ, ”Ο”ΎΑρκΉΑ©ΒΡΈ»Ε®≥…œώ. DBCO–ό ΈΒΡCD44v6Α–œρΕύκΡ Ήœ»”κ÷ΉΝωΫαΚœ; RAPΕύκΡΥφΚσΖΔ…ζΒψΜςΖ¥”Π”κΑ–œρΕύκΡΝ§Ϋ”≤Δ«ΐΕ·Ή‘ΉιΉΑ–Έ≥…Ρ…ΟΉΆχ¬γ. LiΒ»[52]ΩΣΖΔΝΥCD133Α–œρΕύκΡΧΫ’κFITC-LQNAPRS (FITC-LS-7). FITC-LS-7”κCD133ΩΙΧε≥…œώ–Γ σΫα≥ΠΑ©œΗΑϊCT-26, ΝΫ’ΏΦΗΚθ÷ΊΚœΒΡ”ΪΙβ–≈Κ≈±μΟςΝΥFITC-LS-7ΧΊ“λ–‘ΒΊΕ®ΈΜCT-26œΗΑϊ÷–ΒΡCD133.
2.2 Οβ“ΏœΗΑϊΑ–œρΕύκΡΧΫ’κ
Οβ“ΏœΗΑϊ «÷ΉΝωΈΔΜΖΨ≥ΒΡ÷Ί“ΣΉι≥…≤ΩΖ÷, ≤Έ”κ÷ΉΝωΫχ’ΙΒΡ≤ΜΆ§ΫΉΕΈ. Οβ“ΏœΗΑϊΒΡΫΰ»σ «÷ΉΝωΖΔ…ζΚΆΉΣ“ΤΒΡ÷Ί“Σ±ξ÷Ψ, ≥ΘΦϊΒΡΟβ“ΏœΗΑϊΑϋά®÷ΉΝωœύΙΊΨό …œΗΑϊ(TAMs)ΓΔΒςΫΎ–‘TœΗΑϊ(Tregs)ΚΆ ςΆΜΉ¥œΗΑϊΒ». ΥϋΟ«Ά®Ιΐœϊ≥ΐœΗΑϊΕΨ–‘TΝήΑΆœΗΑϊ(CTL)ΫιΒΦΒΡΟβ“ΏΖ¥”Π, ¥ΌΫχ÷ΉΝωΒΡ…ζ≥Λ[32].
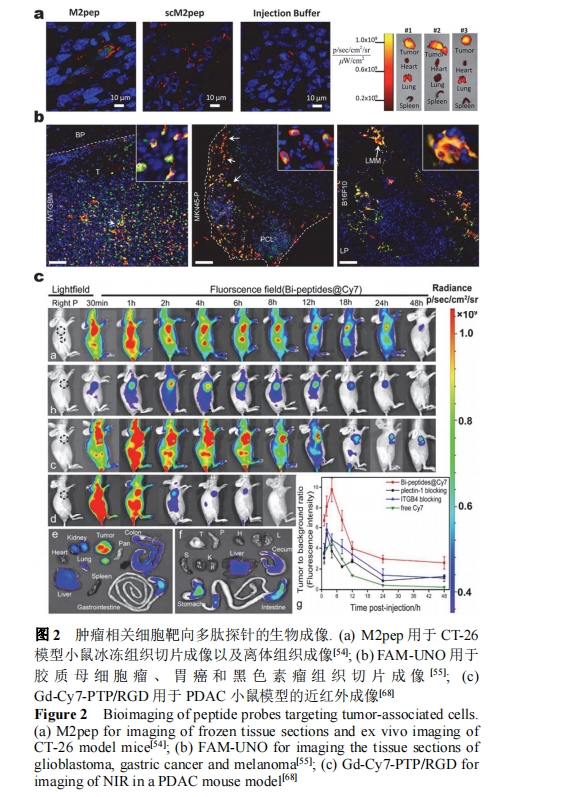
M2–Ά÷ΉΝωœύΙΊΨό …œΗΑϊ”κ÷ΉΝωœΗΑϊΖ÷Μ·≥ΧΕ»œ‘÷χœύΙΊ, «»ιœΌΑ©ΓΔΫΚ÷ ΡΗœΗΑϊΝωΚΆΈΗΑ©Β»Εώ–‘÷ΉΝω‘ω÷≥ΚΆΉΣ“ΤΒΡ÷Ί“Σ±ξ÷ΨΈο[53]. CD206 «M2–ΆΨό …œΗΑϊΧΊ“λ–‘ΒΡΦλ≤βΑ–Βψ, PunΒ»[54]ΙΙΫ®ΝΥCD206ΒΡΑ–œρΕύκΡΧΫ’κAlexaFluor660-YEQDPWGVKWWY (M2pep), ≤Δ”Ο”ΎM2–ΆΨό …œΗΑϊΒΡ≥…œώ―–ΨΩ. TianΒ»[55]ΙΙΫ®[68Ga]Ga-DOTA-M2pepΧΫ’κ, ≤ΔΕ‘B16F10Κ…Νω–Γ σΫχ––ΝΥMicroPET≥…œώΚΆ…ζΈοΖ÷≤Φ―–ΨΩ. Β―ιΫαΙϊ±μΟς, ΧΫ’κΡήΙΜ―ΗΥΌΒΫ¥ο÷ΉΝω≤ΩΈΜ, ≤Δ‘ΎΉΔ…δΚσ1 h‘Ύ÷ΉΝω÷–œ‘ Ψ¥σΝΩΜΐάέ. ‘ΎCT-26Ϋα≥ΠΑ©ΡΘ–Ά–Γ σΒΡάκΧε≥…œώ―–ΨΩ÷–, M2pepΧΊ“λ–‘ΒΊΖ÷≤Φ”ΎΡΘ–Ά–Γ σΒΡ÷ΉΝω≤ΩΈΜ(ΆΦ2a). TeesaluΒ»[56]Ά®Ιΐ …ΨζΧε’Ι ΨΦΦ θ…Η―ΓΝΥΑ–œρCD206ΒΡΕύκΡCSPGAKVRC (UNO). FAM–ό ΈΒΡUNO”κCD206ΩΙΧεΙ≤Ε®ΈΜ≥…œώ–Γ σ»ιœΌΑ©Ήι÷·, ≤Δ”Ο”ΎΫΚ÷ ΡΗœΗΑϊΝωΓΔΈΗΑ©ΚΆΚΎ…ΪΥΊ÷ΉΝωΒΡΉι÷·≥…œώ(ΆΦ2b).
ΒςΫΎ–‘T (Treg)œΗΑϊ”’ΒΦΒΡ÷ΉΝωΈΔΜΖΨ≥÷–ΒΡΟβ“Ώ“÷÷Τ±Μ»œΈΣ «÷ΉΝωΟβ“ΏΧ”“ίΒΡΙΊΦϋΜζ÷Τ, «Α©÷ΔΟβ“Ώ÷ΈΝΤΒΡ÷ς“Σ’œΑ≠. …ώΨ≠ΤΛΥΊ-1 (Nrp1) «―–ΨΩTregsΒΡ÷Ί“Σ±ξ÷ΨΈο, KimΒ»[57]ΙΙΫ®ΝΥNrp1ΒΡΑ–œρΕύκΡΡ…ΟΉΧΫ’κCy5.5-CGNKRTRGC-hNPs (Cy5.5-tLyp1-hNPs). »Υ«ΑΝ–œΌΑ©œΗΑϊDU145ΒΡœΗΑϊ≥…œώΚΆB16BL/6Κ…Νω–Γ σ÷ΉΝωΒΡΒΞœΗΑϊ–ϋ“Κ Β―ι÷ΛΟςCy5.5-tLyp1-hNPs”κTregœΗΑϊΧΊ“λ–‘ΫαΚœ.
ςΆΜΉ¥œΗΑϊ(DCs) «÷ΉΝωΟβ“Ώ÷–Ήν÷Ί“ΣΒΡΩΙ‘≠≥ ΒίœΗΑϊ, MohamadzadehΒ»[58]Ά®Ιΐ …ΨζΧε’Ι ΨΦΦ θ…Η―ΓΝΥDCsΑ–œρΕύκΡ–ρΝ–FYPSYHSTPQRP, ≤Δ”κΝ¥ΟΙ«ΉΚΆΥΊ- Alexa488≈ΦΝΣ”Ο”ΎDCsΒΡΧΊ“λ–‘≥…œώ. CD11c «“Μ÷÷‘ΎDCs ±μΟφΗΏΕ»±μ¥οΒΡΡΛΒΑΑΉ. GahmbergΒ»[59]…Η―Γ≥ωΝΥCD11cΒΡΗΏ«ΉΚΆΝΠΕύκΡP-D2, Τδ–ρΝ–ΈΣGGVTLTYQF- AAGPRDK.
2.3 ÷ΉΝω―ΣΙήΡΎΤΛœΗΑϊΑ–œρΕύκΡΧΫ’κ
‘Ύ÷ΉΝωΈΔΜΖΨ≥÷–, ÷ΉΝω―ΣΙήΒΡ…ζ≥… «÷ΉΝω…ζ≥ΛΚΆΉΣ“ΤΒΡ÷Ί“ΣΧθΦΰ[60]. ÷ΉΝω―ΣΙήΡΎΤΛœΗΑϊΆ®ΙΐΖ÷ΟΎ―ΣΙή…ζ≥…“ρΉ”, ¥ΌΫχ÷ΉΝω―ΣΙήΒΡ…ζ≥…ΦΑ÷ΉΝωœΗΑϊΒΡ’≥ΗΫΚΆΉΣ“Τ[61]. ΚΥ» ΥΊΉςΈΣ÷ΉΝωΡΎΤΛœΗΑϊΒΡ±ξ÷ΨΈο, «Φλ≤β÷ΉΝω―ΣΙή–¬…ζΒΡ÷Ί“ΣΑ–Βψ. RuoslahtiΒ»[62]ΙΙΫ®ΝΥΧΊ“λ–‘ΫαΚœΚΥ» ΥΊΒΡΕύκΡΧΫ’κFITC-KDEPQRRSARLSAKPAPPK- PEPKPKKAPAKK, Ά§ ±, YingΒ»[63]άϊ”ΟœύΆ§ΒΡΑ–œρΕύκΡΙΙΫ®ΝΥCdTeΝΩΉ”Βψ-ΕύκΡΧΫ’κ, ”Ο”Ύ»Υ»ιœΌΑ©œΗΑϊMDA-MB-435ΒΡΜνœΗΑϊ≥…œώ.
’ϊΚœΥΊ «Φλ≤β÷ΉΝωΡΎΤΛœΗΑϊ«®“ΤΚΆ÷ΉΝω―ΣΙή…ζ≥…ΒΡ÷Ί“Σ…ζΈο±ξ÷ΨΈο. RuoslahtiΒ»[64]Ά®Ιΐ …ΨζΧε’Ι ΨΦΦ θ…Η―ΓΝΥΑ–œρΠΝvΠ¬3ΚΆΠΝvΠ¬5ΒΡΕύκΡCDCRGDCFC. ΠΝvΠ¬3ΩΙΧε”κΧΫ’κΙ≤Ε®ΈΜ≥…œώMDA-MB-435ΡΘ–Ά–Γ σΒΡ÷ΉΝωΉι÷·, ÷ΛΟςΗΟΕύκΡ–ρΝ–ΧΊ“λ–‘ Ε±π’ϊΚœΥΊΠΝvΠ¬3. YangΒ»[65]ΫΪΫϋΚλΆβΚΥΫΜΝΣΨέΚœΫΚ χΡ…ΟΉΝΘΉ”(NIRF-CCPM)”κRGDΕύκΡ≈ΦΝΣ, ≤ΔΆ®ΙΐΖ≈…δ–‘ΚΥΥΊ 111In±ξΦ«, ”Ο”ΎU87÷ΉΝωΡΘ–Ά¬ψ σΒΡΚΥ“Ϋ―ß/Ιβ―ßΥΪΡΘ≥…œώ―–ΨΩ. LiΒ»[66]Χα≥ωΝΥ“Μ÷÷PDA-RGDΡ…ΟΉ≈γΈμΗ®÷ζΙβ»»≥…œώœΒΆ≥, ”Ο”ΎΧεΆβœΗΑϊΦχ±πΚΆΧεΡΎ÷ΉΝωΈΜ÷ΟΚΆ±ΏΫγΒΡΩ… ”Μ·, ÷ΗΒΦ Β ±ΨΪ»Ζ ÷ θΤΎΦδΒΡ÷ΉΝω«–≥ΐ θ. LamΒ»[67]…ηΦΤΝΥΚ§RGDΜυ–ρΒΡOBOCκΡΩβ, ≤Δ…Η―Γ≥ωΧΊ“λ–‘ΕύκΡLXW7. ”κRGDΜΖκΡœύ±», LXW7œ‘ Ψ≥ωΗϋΗΏΒΡ÷ΉΝω…ψ»ΓΚΆΫœΒΆΒΡΗΈ‘ύ…ψ»Γ.
Plectin-1‘Ύ“»œΌΑ©œΗΑϊΒΡ‘ω÷≥ΓΔ«®“ΤΚΆ«÷œ°Ιΐ≥Χ÷–ΨΏ”–÷Ί“ΣΉς”Ο. TianΒ»[68]ΙΙΫ®ΝΥ’ϊΚœΥΊΚΆPlectin-1ΥΪΧΊ“λ–‘ΒΡΕύκΡΧΫ’κGd-Cy7-KTLLPTPKRGDFKK (Gd-Cy7-PTP/RGD). Gd-Cy7-PTP/RGD±Μ”Ο”ΎΗΏΥ°ΤΫ±μ¥οPlectin-1ΚΆ’ϊΚœΥΊΒΡ“»œΌΒΦΙήœΌΑ©(PDAC)–Γ σΡΘ–ΆΒΡ¥≈Ι≤’ώΚΆΫϋΚλΆβΥΪΡΘ≥…œώ, ΥΪ÷ΊΑ–œρ”––ßΧαΗΏΝΥΧΫ’κΕ‘“»œΌΑ©ΒΡΦλ≤βΡήΝΠ(ΆΦ2c). LiuΒ»[69]ΙΙΫ®ΝΥ89Zr±ξΦ«ΒΡ’ϊΚœΥΊΚΆVEGFRΥΪΧΊ“λ–‘ΒΡΕύκΡΧΫ’κ≤Δ”Ο”ΎU87MGΚ…Νω–Γ σΒΡPET≥…œώ.
3 ÷ΉΝωœΗΑϊΆβΜυ÷ Α–œρΕύκΡΧΫ’κ
ECM÷–ΒΑΑΉ÷ Κ§ΝΩΚΆΫαΙΙΒΡ±δΜ·, ΒςΩΊ÷ΉΝωΒΡ«÷œ°ΚΆΉΣ“Τ. ‘Ύ÷ΉΝωΖΔ’ΙΙΐ≥Χ÷–, I–ΆΫΚ‘≠ΒΑΑΉΒΡΫΜΝΣ‘ωΦ”ΝΥECMΟήΕ»ΚΆ”≤Ε», ΈΣ÷ΉΝωΒΡ«÷œ°ΧαΙ©ΓΑΗΏΥΌΆ®ΒάΓ±[70-71]. ÷ΉΝω÷–ΗΏ±μ¥οΒΡMMPsΆ®ΙΐΫΒΫβœΗΑϊΆβΜυ÷ ΒΑΑΉΙΙ≥…ΒΡ…ζάμΤΝ’œ, ¥ΌΫχ÷ΉΝωœΗΑϊΒΡΉΣ“Τ[1,5,31]. Ά§ ±, œΥΈ§ΒΑΑΉΓΔœΥΈ§Ν§Ϋ”ΒΑΑΉ(FN)ΚΆκλ…ζΒΑΑΉ(TN)Β»ΆβΜυ÷ ΒΑΑΉΆ®ΙΐΒςΩΊœΗΑϊΆβΜυ÷ ”κ÷ΉΝωœΗΑϊΒΡ’≥ΗΫΉς”Ο, ≤Έ”κ÷ΉΝωΒΡΖΔ’ΙΙΐ≥Χ[72⇓⇓-75]. ÷ΉΝωœΗΑϊΆβΜυ÷ “―≥…ΈΣ÷ΉΝω≤Γάμ―–ΨΩΚΆ‘γΤΎ’οΕœΒΡ÷Ί“ΣΑ–Βψ.
3.1 ≤Γ±δΫΚ‘≠ΒΑΑΉΑ–œρΕύκΡΧΫ’κ
÷ΉΝωœΗΑϊΆβΜυ÷ “λ≥Θ÷ΊΥήΤΎΦδ≤ζ…ζΒΡ≤Γ±δΫΚ‘≠ΒΑΑΉ, “―÷πΫΞ≥…ΈΣ―–ΨΩ÷ΉΝω«÷œ°ΚΆΉΣ“ΤΒΡΙΊΦϋ±ξ÷ΨΈο. 2005Ρξ, YuΒ»[76]÷ΛΟς”…Η§Α±Υα(Pro)-τ«Η§Α±Υα(Hyp)-Η Α±Υα(Gly)÷ΊΗ¥–ρΝ–Ήι≥…ΒΡΫΚ‘≠ΡΘΡβκΡ(GPO)n‘ΎΒΞΝ¥ ±Ε‘ΟςΫΚΨΏ”–«Ω«ΉΚΆΝΠ. AF647–ό ΈΒΡΕύκΡΧΫ’κAF647-(GPO)9±Μ”Ο”Ύ»Υ»ιœΌΑ©œΗΑϊMDA-MB-231ΚΆMCF-7ΒΡ3DœΗΑϊΡΘ–ΆΒΡΫΚ‘≠ΒΑΑΉ≥…œώ[77]. Ε‘”Ύ¥σΝΩ≤ζ…ζ≤Γ±δΫΚ‘≠ΒΑΑΉΒΡMDA-MB-231œΗΑϊΡΘ–Ά, AF647-(GPO)9ΧΫ’κ¥σΝΩΗΜΦ·; ΕχMCF-7œΗΑϊ‘ρΈόΟςœ‘”ΪΙβ–≈Κ≈(ΆΦ3a). »ΜΕχ, (GPO)nΦΪ“Ή–Έ≥…»ΐ¬ί–ΐΫαΙΙ, ¥”Εχ ß»ΞΕ‘≤Γ±δΫΚ‘≠ΒΑΑΉΒΡΫαΚœΡήΝΠ. YuΒ»[78]ΩΣΖΔΝΥΝΐ ΫΫΚ‘≠‘”ΫΜκΡΧΫ’κCF-G3(GPO)4NBGPO(GPO)4 (CF-NB(GPO)9), ”Ο”Ύ“÷÷ΤΤδ»ΐ¬ί–ΐΫαΙΙΒΡ–Έ≥…. ΗΟΧΫ’κ÷––ΡœθΜυή–ΜυΝΐ ΫΜυΆ≈(NB)‘ΎΙβ¥ΧΦΛœ¬Ά―¬δ, ±δΈΣCF-(GPO)9. ΫϋΚλΆβ”ΪΙβΜυΆ≈IRDye800CW±ξΦ«ΒΡΝΐ ΫΧΫ’κ”Ο”ΎPC-3ΡΘ–Ά–Γ σΧεΡΎ≤Γ±δΫΚ‘≠ΒΑΑΉΒΡ≥…œώ―–ΨΩ(ΆΦ3b). ≥…œώΫαΙϊ÷ΛΟς, ΧΫ’κ‘ΎΙβ¥ΧΦΛΚσ, Ά®ΙΐΫαΚœ≤Γ±δΫΚ‘≠ΒΑΑΉ Βœ÷‘ΎΡΘ–Ά–Γ σ÷ΉΝω≤ΩΈΜΧΊ“λ–‘Μΐάέ.
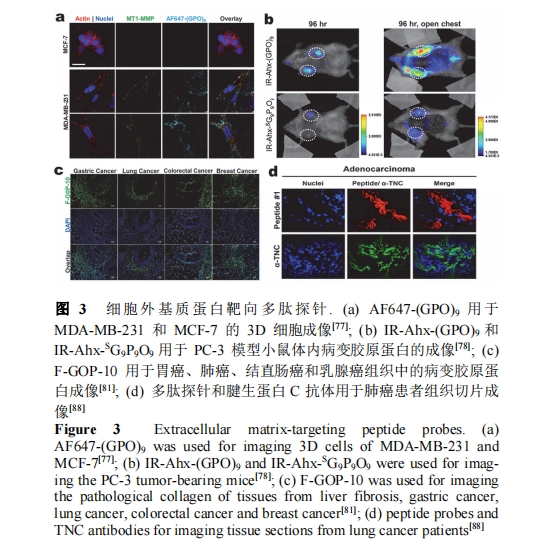
XiaoΒ»[79]Ά®ΙΐΨ≤Βγ≈≈≥β≤Ώ¬‘, ΙΙΫ®ΝΥ “Έ¬ΒΞΝ¥ΒΡΕύκΡΧΫ’κROX-Ahx-(Gly-Pro-Hyp)7-(Asp)6-NH2, ≤Δ”Ο”Ύ÷ΉΝω≤ΓάμΉι÷·÷–≤Γ±δΫΚ‘≠ΒΑΑΉΒΡ”ΪΙβ≥…œώ. XiaoΒ»[80] Ι”ΟProΧφ¥ζ(Gly-Pro-Hyp)n–ρΝ–÷–ΒΡHyp, ΙΙΫ®ΝΥ4 Γφ ±»‘ «Έ»Ε®ΒΞΝ¥ΫαΙΙΒΡΕύκΡΧΫ’κFAM-(Gly-Pro-Pro)8 (FAM-GPP). FAM-GPP±Μ”Ο”ΎΤΫΜ§ΦΓΝωΓΔΈΗΑ©ΚΆ÷±≥ΠΑ©ΒΡΉι÷·≥…œώ. Ά®ΙΐΫΜΜΜ(Gly-Pro-Hyp)n–ρΝ–÷–ProΚΆHypΒΡΈΜ÷Ο, XiaoΒ»[81] Ή¥ΈΙΙΫ®ΝΥΆξ»ΪΒΞΝ¥ΒΡ≤Γ±δΫΚ‘≠ΒΑΑΉΑ–œρΧΫ’κFAM-(Gly-Hyp-Pro)10 (F-GOP-10), Βœ÷ΈΗΑ©ΓΔΖΈΑ©ΓΔΫα÷±≥ΠΑ©ΚΆ»ιœΌΑ©Β»÷ΉΝωΉι÷·÷–≤Γ±δΫΚ‘≠ΒΑΑΉΒΡΑ–œρ≥…œώ(ΆΦ3c).
3.2 Μυ÷ Ϋπ τΒΑΑΉΟΗΑ–œρΕύκΡΧΫ’κ
MMPsΒςΩΊ÷ΉΝωΒΡ«÷œ°ΚΆΉΣ“Τ, “―≥…ΈΣ÷ΉΝωΦλ≤β÷–÷Ί“ΣΒΡœΗΑϊΆβΜυ÷ Α–Βψ. WeberΒ»[82]Ά®Ιΐ …ΨζΧε’Ι ΨΦΦ θ≥…ΙΠ…Η―Γ≥ωΜΖκΡyCTTHWGFTLC (CTT), ”Ο”ΎMMP-2ΚΆMMP-9ΒΡΧΊ“λ–‘ Ε±π. AndersonΒ»[83]Ά®Ιΐ“ΐ»κΆ§ΈΜΥΊ±ξ«©64Cu-DOTA, ΙΙΫ®ΝΥmicroPET≥…œώΧΫ’κ64Cu-DOTA-CTT. 64Cu-DOTA-CTTΕ‘MMP-2ΚΆMMP-9ΨΏ”–ΗΏ«ΉΚΆΝΠ, ≥…ΙΠ”Ο”ΎΚ…Νω–Γ σΒΡmicroPETΧεΡΎ≥…œώ. ChenΒ»[84]ΙΙΫ®ΝΥMMP-14ΧΊ“λ–‘ΒΡΕύκΡΧΫ’κCy5.5-HWKHLHNTKTFL (Cy5.5-MT1-AF7p), ≤Δ Βœ÷ΝΥΧΫ’κCy5.5-MT1-AF7pΕ‘MDA-MB-435“Τ÷≤Νω–Γ σΒΡΧεΡΎ≥…œώ. FangΒ»[85]Ά®Ιΐ …ΨζΧε’Ι ΨΦΦ θ…Η―Γ≥ωMMP-14ΧΊ“λ–‘ΒΡΕύκΡΧΫ’κCy5.5-HSVEDVS (Cy5.5-HS7). ”κCy5.5-MT1-AF7pœύ±», Cy5.5-HS7ΨΏ”–ΗϋΗΏΒΡMMP-14«ΉΚΆΝΠ, «“Cy5.5-HS7’Ιœ÷≥ωΗϋ≥ΛΒΡΧεΡΎ≥…œώΑκΥΞΤΎ. FangΒ»[86]ΙΙΫ®ΝΥΑ–œρMMP-16ΒΡΝΩΉ”Βψ-ΕύκΡΧΫ’κQD@MT3-AF4pΦΑΕ‘’’ΧΫ’κQD@MT-scr. œύ±»”ΎQD@MT-scr»Ψ…ΪΒΡHT-1080œΗΑϊΈόΟςœ‘”ΪΙβ, QD@MT3-AF4p»Ψ…ΪΒΡHT-1080œΗΑϊœ‘ Ψ«ΩΝ“ΒΡ”ΪΙβ, ±μΟςΤδΕ‘MMP-16ΙΐΝΩ±μ¥οΒΡHT-1080œΗΑϊΒΡΧΊ“λ–‘.
3.3 ΤδΥϊ÷ΉΝωœΗΑϊΆβΜυ÷ ΒΑΑΉΒΡΑ–œρΕύκΡΧΫ’κ
œΥΈ§ΒΑΑΉΚΆκλ…ζΒΑΑΉCΕ‘÷ΉΝω―ΣΙήΒΡ…ζ≥…”–¥ΌΫχΉς”Ο, ≥…ΈΣ÷ΉΝωΧΊ“λ–‘Φλ≤βΒΡ–¬–ΥΑ–Βψ. GrüllΒ»[87]ΙΙΫ®ΝΥœΥΈ§ΒΑΑΉΧΊ“λ–‘ΒΡΕύκΡΧΫ’κ111In-DOTA-GGGGY- dGlu-C-Hyp-3ClY-GLCYIQG-NH2 (111In-Epep), ≤Δ”Ο”ΎBT-20Κ…Νω–Γ σΒΡSPECT/CT≥…œώ. 111In-EpepΧΊ“λ–‘ΒΊΑ–œρ÷ΉΝωΡΘ–Ά–Γ σΒΡœΥΈ§ΒΑΑΉΗΏ≥ΝΜΐ«χ”ρ, ≤Δœ‘ Ψ≥ωΟςœ‘ΒΡ≥…œώ–≈Κ≈. ΕύκΡΧΫ’κFHKHKSPALSPVGGGΕ‘κλ…ζΒΑΑΉCΨΏ”–ΗΏ«ΉΚΆΝΠ, “―”Ο”ΎΝΌ¥≤÷ΉΝω«–Τ§ΒΡΧΊ“λ–‘≥…œώ[88](ΆΦ3d).
œΥΈ§Ν§Ϋ”ΒΑΑΉΒΡBΫαΙΙ”ρ(EDB-FN) «÷ΉΝωΧΊ“λ–‘≥…œώΒΡ≥ΘΦϊΑ–Βψ. LuΒ»[89]ΙΙΫ®ΝΥEDB-FNΒΡΧΊ“λ–‘ΕύκΡΧΫ’κCy5-CTVRTSADC (Cy5-ZD2). Cy5-ZD2±Μ”Ο”Ύ«ΑΝ–œΌΑ©œΗΑϊPC3Κ…Νω–Γ σΚΆΝΦ–‘«ΑΝ–œΌ‘ω…ζ–Γ σΒΡΧεΡΎ”ΪΙβ≥…œώ. ”κΝΦ–‘«ΑΝ–œΌ‘ω…ζœύ±», Cy5-ZD2Ε‘«ΑΝ–œΌ÷ΉΝω±μœ÷≥ωΗϋ«ΩΒΡΫαΚœΡήΝΠ. LuΒ»[90-91]Ϋχ“Μ≤ΫΙΙΫ®ΝΥΑ–œρœΥΈ§Ν§Ϋ”ΒΑΑΉ-œΥΈ§ΒΑΑΉΗ¥ΚœΈοΒΡΕύκΡΧΫ’κCy5.0-PEG-CREKA, ≤ΔΖ÷±π”κœΥΈ§Ν§Ϋ”ΒΑΑΉΩΙΧεΚΆœΥΈ§ΒΑΑΉΩΙΧεΙ≤Ε®ΈΜ»Ψ…Ϊ4T1÷ΉΝωΉι÷·.
4 ÷ΉΝωΈΔΜΖΨ≥œλ”Π–ΆΕύκΡΧΫ’κ
÷ΉΝωΈΔΜΖΨ≥ΨΏ”–«χ±π”Ύ’ΐ≥Θ…ζάμΜΖΨ≥ΒΡ»θΥα–‘ΚΆΗΏΟΗΜν–‘, Ά§ ±÷ΉΝωΈΔΜΖΨ≥÷–ΡΎ‘¥–‘Ι»κΉΗ κΡ(GSH)±μ¥οΝΩΙΐΗΏ, ’β–©ΧΊ’ςΈΣ÷ΉΝωΒΡΧΊ“λ–‘Φλ≤βΧαΙ©ΝΥάμœκΑ–Βψ[5,31,92]. Μυ”Ύ÷ΉΝωΈΔΜΖΨ≥ΒΡΧΊ’ς, pHœλ”ΠΓΔΟΗœλ”ΠΚΆ―θΜ·ΜΙ‘≠œλ”ΠΒΡ÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κΧεœΒ±ΜœύΦΧΩΣΖΔ. ÷ΉΝωΈΔΜΖΨ≥œλ”Π–ΆΕύκΡΧΫ’κΆ®Ιΐ”ΪΙβΓΔ¥≈Ι≤’ώ“‘ΦΑPETΒ»≥…œώΖΫΖ®, Βœ÷÷ΉΝωΉΣ“ΤΓΔ«÷œ°ΚΆΖ÷ΤΎΒΡΨΪΉΦΦλ≤β.
4.1 pHœλ”Π–ΆΕύκΡΧΫ’κ
÷ΉΝωΈΔΜΖΨ≥ΒΡœ‘÷χΧΊ’ς÷°“Μ «»θΥα–‘ΒΡpH, ΡήΙΜΉςΈΣ÷ΉΝωΧΊ“λ–‘Φλ≤βΒΡΑ–Βψ[5,93]. ‘Ύ÷ΉΝωΈΔΜΖΨ≥÷–, ”…”Ύ÷ΉΝωœΗΑϊΒΡΖΠ―θ–‘Χ«ΫΆΫβ, »ιΥα‘Ύ÷ΉΝω«χ”ρΒΡ¥σΝΩΜΐάέ‘λ≥…÷ΉΝωΈΔΜΖΨ≥≥ œ÷»θΥα–‘ΒΡpH. ΒΆpH÷Βœλ”ΠΒΡ≤ε»κκΡ(pHLIPs)ΚΆΉιΑ±ΥαpHœλ”ΠΧΫ’κ“―±ΜΩΣΖΔ”Ο”Ύ÷ΉΝωΒΡΧΊ“λ–‘≥…œώ.
4.1.1 pHLIPsœλ”ΠΧεœΒ
pHLIPsΑϋά®ΦΪ–‘Ρ©ΕΥΚΆΚ§”–ΧλΕ§Α±Υα≤–ΜυΒΡ÷–―κΩγΡΛΫαΙΙ”ρ. pHLIPs‘Ύ÷––‘pHœ¬”κœΗΑϊΡΛΦδΒΡœύΜΞΉς”ΟΚή»θ; Εχ‘Ύ÷ΉΝωΒΡ»θΥα–‘pH÷Βœ¬, ΩγΡΛΫαΙΙ”ρ÷–Υα–‘Α±ΜυΥα≤–ΜυΒΡ÷ Ή”Μ·ΒΦ÷¬pHLIPs–Έ≥…ΠΝ-¬ί–ΐΙΙœσ, ¥”ΕχΨΏ”–ΝΥ≤ε»κ÷ΉΝωœΗΑϊΡΛΒΡΡήΝΠ[94]. AndreevΒ»[95]ΙΙΫ®ΝΥpHLIPsΧΫ’κAAEQNPIYWARYADWLFTTPLL- LLDLALLVDADEGTCG, ≤Δ”Ο”Ύ÷ΉΝωΒΡΧΊ“λ–‘≥…œώ. ΉΣ“Τ–‘ΚΎ…ΪΥΊΝωœΗΑϊœΒM4A4ΚΆΖ«ΉΣ“Τ–‘»Υ»ιœΌΒΦΙήΑ©œΗΑϊNM2C5÷ΉΝω–Γ σΡΘ–ΆΒΡΜνΧε≥…œώΫαΙϊ÷ΛΟς, ÷ΉΝω÷–pHLIPsΒΡΜΐάέ”κ÷ΉΝωΒΡ«÷œ°–‘ΫτΟήœύΙΊ. ReshetnyakΒ»[96]Ά®Ιΐ Ι”ΟLysΚΆAsn»Γ¥ζ‘≠–ρΝ–ΒΡAsp, Ζ÷±πΙΙΫ®±δΧεΧΫ’κACEQNPIYWARYANWLFTTPLLLL- NLALLVDADEGTG (N-pHLIP)ΚΆACEQNPIYWARYA- KWLFTTPLLLLKLALLVDADEGTG (K-pHLIP). AspΒΡ»Γ¥ζΒΦ÷¬ΧΫ’κ≤ε»κ÷ΉΝωœΗΑϊΡΛΡήΝΠΫΒΒΆ, ΫχΕχ”ΑœλΧΫ’κΕ‘÷ΉΝωΒΡΧΊ“λ–‘.
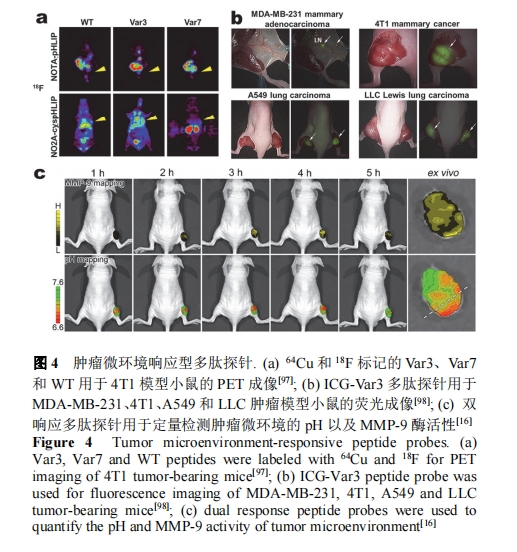
Εύ÷÷pHLIPs±δΧε–ρΝ–±ΜΩΣΖΔ“‘ΧαΗΏ‘≠ ΦΧΫ’κΒΡpHœλ”ΠΥΌ¬ ΚΆ‘Ύ÷ΉΝω÷–ΒΡΜΐάέΝΩ. LewisΒ»[97]÷Τ±ΗΝΥpHLIPs±δΧεΧΫ’κVar3 (ACDDQNPWRAYLDLLFPTD- TLLLDLLW)ΓΔVar7 (ACEEQNPWARYLEWLFPTET- LLLEL)ΚΆpHLIPs‘≠ ΦΧΫ’κWT (ACEQNPIYWARY- ADWLFTTPLLLLDLALLVDADEGT). Var3ΚΆVar7¥”œΏ–‘ΫαΙΙΉΣ±δΒΫΠΝ¬ί–ΐΫαΙΙΥυ–ηΒΡpK±»WTΗϋΗΏ, «“Var3ΚΆVar7ΒΡΡΛ≤ε»κΥΌ¬ ‘ΕΗΏ”ΎWT. ‘Ύ64CuΚΆ18F±ξΦ«ΧΫ’κΒΡ4T1÷ΉΝωΡΘ–Ά–Γ σPET≥…œώ÷–, Var3ΚΆVar7ΧΫ’κΕ‘”Ύ÷ΉΝωΒΡΧΊ“λ–‘…ψ»ΓΗΏ”ΎWTΧΫ’κ, «“Var7ΧΫ’κΒΡ―Σ“Κ«ε≥ΐΥΌ¬ ΉνΩλΓΔ‘Ύ÷ΉΝω≤ΩΈΜ–≈Κ≈ΜΐάέΉνΕύ(ΆΦ4a). ICG-Var3±ΜΫχ“Μ≤Ϋ”Ο”ΎMDA-MB-231ΓΔ4T1ΓΔA549ΚΆLLCΒ»÷ΉΝωΡΘ–Ά–Γ σΒΡ”ΪΙβ≥…œώ―–ΨΩ[98]. ≥…œώΫαΙϊ÷ΛΟςICG-Var3ΧΊ“λ–‘ Ε±π÷ΉΝω≤ΩΈΜ, ≤ΔΉΦ»Ζ Ε±π÷ΉΝω±Ώ‘ΒΓΔ≤Γ‘νΚΆΩΩΫϋ‘≠ΖΔ÷ΉΝωΈΜΒψΒΡΈΔΉΣ“ΤΝήΑΆΫα(ΆΦ4b).
4.1.2 ΉιΑ±ΥαΕύκΡΧεœΒ
ΉιΑ±ΥαΕύκΡΧεœΒΡήΙΜΧΊ“λ–‘ΒΊœλ”Π÷ΉΝωΈΔΜΖΨ≥pH (6.5~7.0), ΉιΑ±ΥαΒΡΏδΏρΜυΆ≈‘Ύ÷ΉΝωΈΔΜΖΨ≥œ¬”…ΈόΒγΚ…ΉΣ±δΈΣ’ΐΒγΚ…ΜυΆ≈, Βœ÷Ε‘÷ΉΝωΒΡΑ–œρΦλ≤β. Μυ”Ύ¥Υ‘≠άμ, StuppΒ»[99]ΙΙΫ®ΝΥΑϋΚ§H6–ρΝ–ΚΆΝΫ«Ή–‘ΕύκΡ–ρΝ–(PAs)ΒΡpHœλ”Π–ΆΉ‘ΉιΉΑΕύκΡΧΫ’κPA1ΚΆPA2, ΝΫ÷÷ΕύκΡΧΫ’κΖ÷±πΉ‘ΉιΉΑ≥…œΥΈ§Ή¥ΚΆ«ρ–Έ. PA1ΚΆPA2Ε‘MDA-MB-231÷ΉΝωΡΘ–Ά–Γ σάκΧε≥…œώΒΡΫαΙϊ±μΟς, œΥΈ§Ή¥ΧΫ’κ±»«ρ–ΈΧΫ’κΨΏ”–ΗϋΗΏΒΡ÷ΉΝωΧΊ“λ–‘. Β―ιΫαΙϊ÷ΛΟςΉ‘ΉιΉΑΕύκΡΧΫ’κΒΡ–ΈΧ§Μα”ΑœλΧΫ’κΕ‘÷ΉΝωΒΡΑ–œρ–ßΙϊ.
4.2 ΟΗœλ”Π–ΆΕύκΡΧΫ’κ
MMPsΚΆΉι÷·ΒΑΑΉΟΗΆ®ΙΐΫΒΫβ÷ΉΝωECM, ¥ΌΫχ÷ΉΝωœΗΑϊΒΡΉΣ“ΤΚΆ÷ΉΝω―ΣΙήΒΡ…ζ≥…. ‘Ύ÷ΉΝωΈΔΜΖΨ≥÷–ΗΏ±μ¥οΒΡMMPsΚΆΉι÷·ΒΑΑΉΟΗ“―Ψ≠≥…ΈΣ÷ΉΝωΧΊ“λ–‘Φλ≤βΒΡΑ–Βψ. MMPsΚΆΉι÷·ΒΑΑΉΟΗΒΡœλ”Π–ΆΕύκΡΧΫ’κ“―±Μ”Ο”Ύ÷ΉΝωΒΡΧΊ“λ–‘≥…œώ.
4.2.1 Μυ÷ Ϋπ τΒΑΑΉΟΗœλ”Π–ΆΕύκΡΧΫ’κ
MMP-2Ά®ΙΐΒςΫΎΕύ÷÷œΗΑϊ–≈Κ≈Ά®¬Ζ”ΑœλΉ≈÷ΉΝωΒΡΫΰ»σΓΔΉΣ“ΤΦΑ‘ΛΚσ. NaganoΒ»[100]…ηΦΤΝΥΈόΜ«Μυ”ΪΙβΜυΆ≈–ό ΈΒΡMMP-2œλ”Π–ΆΧΫ’κ(BODIPY)650/665-PLGLAG (BODIPY-MMP), ≤ΔΙΙΫ®Κ§”–Μ«Μυ”ΪΙβΜυΆ≈ΒΡSulfoCy5-PLGLAG (SulfoCy5-MMP)ΉςΈΣΕ‘’’ΧΫ’κ. HT-1080–Γ σ“Τ÷≤ΝωΡΘ–ΆΒΡΫϋΚλΆβ≥…œώΫαΙϊ÷ΛΟς, BODIPY-MMPΧΫ’κΨΏ”–±»SulfoCy5-MMPΗϋ≥ΛΒΡ÷ΉΝωΆΘΝτ ±ΦδΚΆΗϋΗΏΒΡ–≈‘κ±». WangΒ»[101]ΙΙΫ®ΝΥΑϋΚ§MMP-2œλ”ΠκΡGPLGVRGKΚΆ…ώΨ≠ΤΛΥΊ-1 (Nrp-1)Α–œρκΡCRGDKΒΡΡ…ΟΉΡ“≈ίN-G-C, Βœ÷ΝΥHT29÷ΉΝωΡΘ–Ά–Γ σΒΡΧΊ“λ–‘ΫϋΚλΆβ≥…œώ.
YangΒ»[102]ΩΣΖΔΝΥΨΏ”–÷ΉΝωœΗΑϊ¥©ΆΗΡήΝΠΒΡMMP-2œλ”Π–Ά¥≈–‘Ρ…ΟΉΧΫ’κ. ΗΟΧΫ’κ”…Κλ…Ϊ”ΪΙβΒΑΑΉmCherryΓΔΒΆΖ÷Ή”ΝΩ”ψΨΪΒΑΑΉΓΔMMP-2ΒΡΧΊ“λ–‘ΒΉΈοκΡPLGVRΚΆΨέΉιΑ±Υα(His6)Ήι≥…. ΡχΧζ―θΧεΡ…ΟΉΩ≈ΝΘ(MIONs)Ά®ΙΐΡχάκΉ”ΚΆHis6÷°ΦδΒΡρϋΚœΉς”Ο, Κœ≥…ΝΥΉ‘ΉιΉΑΕύκΡΧΫ’κrCCMH. ΧΫ’κrCCMH‘ΎΗΏ±μ¥οMMP-2ΒΡHT-1080Κ…Νω–Γ σ÷– Βœ÷ΝΥΧεΡΎ≥…œώ. ZhangΒ»[103]÷Τ±ΗΝΥ“‘ ς÷ΠΉ¥¥σΖ÷Ή”ΨέθΘΑΖ-ΑΖ(PAMAM)ΈΣΚΥ–ΡΓΔPEGΈΣΆβΩ«ΒΡMMP-2œλ”ΠΧΫ’κ. ΧΫ’κΒΡPEG≤ψΆ®Ιΐœλ”ΠMMP-2ΒΡΟΗ«–Ής”Ο”κPAMAMΖ÷άκ, Βœ÷MCF-7ΚΆL02œΗΑϊ≥…œώ“‘ΦΑ÷ΉΝωΡΘ–Ά–Γ σΒΡΧεΡΎ≥…œώ.
MMP-14‘ΎΫΚ÷ Νω÷–Ιΐ±μ¥ο, Εχ‘Ύ’ΐ≥Θ¥σΡ‘÷–±μ¥οΩ…“‘Κω¬‘≤ΜΦΤ, «ΫΚ÷ ΝωΦλ≤βΒΡ…ζΈο±ξ÷ΨΈο. Warram Β»[104]ΙΙΫ®ΝΥΨΏ”–MMP-14œλ”Π–ρΝ–RSCitG-HPhe-YLYΚΆMMP-14ΫαΚœ–ρΝ–ΈΣHWKHLHNTKTFLΒΡPET/ΫϋΚλΆβΥΪΡΘ≥…œώΕύκΡΧΫ’κ. U87ΫΚ÷ Νω–Γ σΡΘ–ΆΒΡΫϋΚλΆβ”ΪΙβ-PETΥΪΡΘ≥…œώΫαΙϊ÷ΛΟς, ΕύκΡΧΫ’κΆ®Ιΐœλ”ΠMMP-14 Βœ÷ΫΚ÷ ΝωΒΡΧΊ“λ–‘≥…œώ.
4.2.2 Ήι÷·ΒΑΑΉΟΗœλ”Π–ΆΕύκΡΧΫ’κ
Ήι÷·ΒΑΑΉΟΗBΚΆΉι÷·ΒΑΑΉΟΗS≤Έ”κ÷ΉΝωœΗΑϊΆβΜυ÷ ΒΡ“λ≥ΘΫΒΫβ, ¥ΌΫχ÷ΉΝω–¬…ζ―ΣΙήΒΡ–Έ≥…ΚΆ÷ΉΝωΒΡΉΣ“Τ, ”κΖΈΑ©ΓΔ»ιœΌΑ©Β»÷ΉΝωΒΡΖΔ’ΙΟή«–œύΙΊ. YoonΒ»[105]Ά®ΙΐGFLG–ρΝ–Ν§Ϋ”«ηΜ·ΟΗCyAΚΆCyB, ΙΙΫ®ΝΥΉι÷·ΒΑΑΉΟΗBœλ”Π–ΆNIR”ΪΙβΕύκΡΧΫ’κCyA-P-CyB. ShabatΒ»[106]Μυ”ΎGFLG–ρΝ–Κœ≥…ΝΥΖ÷Ή”ΡΎΒγΚ…ΉΣ“Τ(ICT)ΦΛΜνΜζ÷ΤΚΆ”ΪΙβΙ≤’ώΡήΝΩΉΣ“Τ(FRET)ΦΛΜνΜζ÷ΤΒΡΉι÷·ΒΑΑΉΟΗBœλ”ΠΒΡΕύκΡΧΫ’κ. ΝΫ÷÷ΧΫ’κΒΡ4T1÷ΉΝωΡΘ–Ά–Γ σΧεΡΎ”ΪΙβ≥…œώ±μΟς, ΝΫ÷÷ΧΫ’κ‘Ύ±ΜΉι÷·ΒΑΑΉΟΗBΟΗ«– ±Ψυ±μœ÷≥ω”ΪΙβ‘ω«Ω, ΒΪICTΧΫ’κ‘ΎOFFΉ¥Χ§œ¬ΒΡΫϋΚλΆβ”ΪΙβΟςœ‘ΒΆ”ΎFRETΧΫ’κ. ≥…œώΫαΙϊ÷ΛΟςICTΧΫ’κ Βœ÷ΝΥΗϋΗΏΒΡ–≈‘κ±».
GarrisonΒ»[107]ΫΪœλ”ΠΉι÷·ΒΑΑΉΟΗSΒΡΕύκΡΝ§Ϋ”Έο(CSLs)”κN-(2-τ«±ϊΜυ)-ΦΉΜυ±ϊœ©θΘΑΖ(HPMA)œύΝ§, ÷Τ±Η≥ωΩ…Ν―ΫβΒΡΙ≤ΨέΈοCSCs. CSCs÷–ΒΡCSLs”…DOTAρϋΚœΈοΓΔΉι÷·ΒΑΑΉΟΗSœλ”Π–ρΝ–PMGLPΓΔ«ε≥ΐ–ρΝ–G-(D)S-SD(S)“‘ΦΑΝ§Ϋ”ΜυΆ≈ΥΡΗω≤ΩΖ÷Ήι≥…. 177Lu–ό ΈΒΡCSCs±Μ”Ο”Ύ»Υ“»œΌœΌ≈ί…œΤΛΑ©(HPAC)ΡΘ–Ά–Γ σΒΡSPECT/CT≥…œώ, ΫαΙϊ±μΟςCSCsΆ®Ιΐœλ”Π÷ΉΝωΈΔΜΖΨ≥÷–ΒΡΉι÷·ΒΑΑΉΟΗS, Βœ÷÷ΉΝωΒΡΧΊ“λ–‘≥…œώ.
4.3 ―θΜ·ΜΙ‘≠œλ”Π–ΆΕύκΡΧΫ’κ
÷ΉΝωΈΔΜΖΨ≥≥ œ÷ΗΏ―θΜ·ΜΙ‘≠Υ°ΤΫ, ÷±Ϋ””Αœλ÷ΉΝωœΗΑϊ¥ζ–Μ, ¥Ό Ι÷ΉΝωœΗΑϊΒΡ‘ω÷≥ΚΆ«®“Τ[5,31]. GSH «ΒςΩΊœΗΑϊ―θΜ·ΜΙ‘≠ΤΫΚβΒΡ÷ς“ΣΖ÷Ή”, ‘Ύ÷ΉΝωΉι÷·÷–ΒΡΚ§ΝΩ‘ΕΗΏ”Ύ’ΐ≥ΘΉι÷·. “ρ¥Υ, Μυ”Ύ÷ΉΝωΈΔΜΖΨ≥÷–GSHΒΡΗΏΥ°ΤΫ±μ¥ο, ―θΜ·ΜΙ‘≠œλ”ΠΒΡΕύκΡΧΫ’κ±Μ…ηΦΤ≤Δ”Ο”Ύ÷ΉΝωΒΡΧΊ“λ–‘≥…œώ. ΕΰΝρΦϋΫαΙΙΝ§Ϋ”ΒΡΕύκΡΧΫ’κ‘ΎΗΜΚ§GSHΒΡ÷ΉΝωΈΔΜΖΨ≥œ¬ΖΔ…ζΕœΝ―, ’β“ΜΖ¥”Π≥…ΈΣ÷ΉΝωΦλ≤βΒΡ–¬≤Ώ¬‘. ChoiΒ»[108]Ά®ΙΐΕΰΝρΦϋΫΪΙβΟτΦΝ”κ÷ΉΝω±ξ÷ΨΈοEGFRΒΡΑ–œρΕύκΡYHWYGYTPQNVI (GE11)Ν§Ϋ”“‘ΙΙΫ®ΕύκΡΧΫ’κRedoxT. »ΐ“θ–‘»ιœΌΑ©–Γ σΒΡΧεΡΎ≥…œώ÷ΛΟς, ΧΫ’κ‘Ύ–Γ σ÷ΉΝω≤ΩΈΜΧΊ“λ–‘Μΐάέ.
4.4 Εύ÷Ίœλ”Π–ΆΕύκΡΧΫ’κ
÷ΉΝω «“ΜΗωΗ¥‘”ΒΡ…ζΈοΧεœΒ, Ε‘÷ΉΝωΈΔΜΖΨ≥÷–Εύ÷÷“λ≥ΘΧΊ’ςΒΡΆ§ ±Φλ≤βΡήΙΜ”––ßΒΊΧαΗΏ÷ΉΝωΦλ≤βΒΡΧΊ“λ–‘ΚΆΉΦ»Ζ–‘[109]. ÷ΉΝωΈΔΜΖΨ≥ΒΡΕύ÷Ίœλ”ΠΕύκΡΧΫ’κΧεœΒ±ΜΩΣΖΔ, “‘ Βœ÷÷ΉΝωΒΡΨΪΉΦΦλ≤β. MMP-2ΚΆMMP-7‘ΎΗΈΑ©œΗΑϊ÷–ΒΡ±μ¥οΥ°ΤΫΗΏ”Ύ’ΐ≥ΘΗΈœΗΑϊ. TangΒ»[110]Ά®ΙΐΑκκΉΑ±Υα≤–ΜυΫΪΆ§ ±œλ”ΠMMP-2ΚΆMMP-7ΒΡΕύκΡ–ρΝ–GPLGVRG-VPLSLTMGΝ§Ϋ”‘ΎΫπΡ…ΟΉΝΘΉ”±μΟφ, ΙΙΫ®ΝΥMMP-2ΚΆMMP-7ΥΪœλ”ΠΒΡΫπΡ…ΟΉΝΘΉ”ΕύκΡΧΫ’κ. ογœΒ≈δΚœΈοBCTOT-Eu111ΚΆ7-Α±Μυ-4-ΦΉΜυœψΕΙΥΊ(AMC)Ζ÷±π–ό Έ‘ΎΕύκΡΒΡNΕΥΚΆCΕΥ. ‘Ύ350 nmΒΡΒΞ≤®≥ΛΦΛΖΔœ¬, ΧΫ’κΨΏ”–449 nm (AMC)ΚΆ613 nm (BCTOT-Eu111)ΝΫΗωΆξ»ΪΖ÷ΩΣΒΡΖΔ…δΖε. ΗΟΧΫ’κΕ‘»Υ’ΐ≥ΘΗΈœΗΑϊHL7702ΚΆ»ΥΗΈΑ©œΗΑϊHepG2ΒΡœΗΑϊ≥…œώ÷ΛΟς, ΕύκΡΧΫ’κΆ®ΙΐΆ§ ±œλ”Π÷ΉΝωœΗΑϊΖ÷ΟΎΒΡMMP-2ΚΆMMP-7, ΧΊ“λ–‘ Ε±π»ΥΗΈΑ©œΗΑϊ.
Μυ”Ύ÷ΉΝωΈΔΜΖΨ≥÷–Υα–‘pHΚΆΗΏΜν–‘MMPsΒΡΧΊ–‘, pHΚΆMMPsΥΪ÷Ίœλ”ΠΒΡΕύκΡΧΫ’κ±ΜΩΣΖΔ≤Δ”Ο”Ύ÷ΉΝωΒΡΦλ≤β. GaoΒ»[16]…ηΦΤΝΥΥΪœλ”ΠΒΡ±»¬ ΧΫ’κ”Ο”Ύ÷ΉΝωΈΔΜΖΨ≥pHΚΆMMP-9Μν–‘ΒΡΕ®ΝΩΦλ≤β. ΗΟΧΫ’κ «”…pHΟτΗ–»ΨΝœANNAΓΔMMP-9œλ”ΠΕύκΡGGKGPLGLPGΓΔΫϋΚλΆβ»ΨΝœCy5.5“‘ΦΑΥΡ―θΜ·»ΐΧζΡ…ΟΉΩ≈ΝΘΉι≥…ΒΡ”ΪΙβΙ≤’ώΡήΝΩΉΣ“Τ(FRET)œΒΆ≥. ΧΫ’κ±Μ”Ο”Ύ»ΥΫα≥ΠΑ©LS180–Γ σ÷ΉΝωΡΘ–ΆΒΡΫϋΚλΆβΚΆ¥≈Ι≤’ώΥΪΡΘ≥…œώ. ΫαΙϊ÷ΛΟςΝΥMMP-9‘Ύ÷ΉΝωΈΔΜΖΨ≥÷–ΒΡΗΏ±μ¥ο‘Ύ ±ΦδΚΆΈΜ÷Ο…œΕΦ”κpHΒΡ“λ≥ΘΟή«–œύΙΊ, ≤Δ«“MMP-9ΚΆpHΒΡ–≠Ά§Ής”ΟΩΊ÷ΤΝΥΕώ–‘÷ΉΝωΒΡ“λ÷ –‘«÷œ°(ΆΦ4c).
JiangΒ»[111]…ηΦΤΝΥΆ§ ±œλ”ΠpHΚΆMMPsΒΡΜνœΗΑϊ¥©ΆΗκΡΧΫ’κdtACPPD. ΗΟΧΫ’κ”…Ψέ―τάκΉ”ΒΡœΗΑϊ¥©ΆΗκΡR9 (CPP)ΓΔ¥χΗΚΒγ“‘―Ύ±ΈCPPΡΎΜ·ΙΠΡήΒΡpHœλ”ΠκΡΚΆMMP-2œλ”ΠΕύκΡΉι≥…, Τδ÷–MMP-2œλ”ΠΕύκΡ≤ε»κΒΫpHœλ”ΠκΡΚΆœΗΑϊ¥©ΆΗκΡR9÷°Φδ, –Έ≥…ΓΑΖ÷Ή”ΡΎΖΔΦ–ΫαΙΙΓ±. dtACPPD‘Ύ…ζάμΜΖΨ≥÷–¥χΗΚΒγΚ…; Εχ‘Ύ÷ΉΝωΈΔΜΖΨ≥÷–, ΕύκΡΧΫ’κΆ§ ±œλ”Π»θΥα–‘pHΚΆMMP-2, ±δΈΣ≤Μ¥χΒγΜρ’ΐΒγΚ…ΒΡ–Έ ΫΚσ±Μ÷ΉΝωœΗΑϊ…ψ»Γ. dtACPPDΧΫ’κΒΡ…ώΨ≠ΫΚ÷ Νω–Γ σΡΘ–ΆΧεΡΎ≥…œώ÷ΛΟς, ΧΫ’κœλ”Π÷ΉΝωΈΔΜΖΨ≥ΒΡpHΚΆMMPsΚσ, ‘Ύ–Γ σ÷ΉΝω≤ΩΈΜΧΊ“λ–‘Μΐάέ. WangΒ»[112]…ηΦΤΝΥΆ§ ±œλ”Π÷ΉΝωΈΔΜΖΨ≥»θΥα–‘pHΚΆMMPsΒΡΉ‘ΉιΉΑΕύκΡΧΫ’κP-S-H, pHœλ”Π–ρΝ–(HLA)2HHLAHLAHΚΆMMP-2œλ”Π–ρΝ–GPLGIAGQC”κPEGΡ©ΕΥ≈ΦΝΣ. »Υ…ώΨ≠ΫΚ÷ ΝωU87œΗΑϊ≥…œώΚΆU87÷ΉΝω–Γ σΧεΡΎ≥…œώΫαΙϊ÷ΛΟς, P-S-H‘Ύœλ”Π÷ΉΝωœΗΑϊΗΏ±μ¥οΒΡMMP-2ΚΆ÷ΉΝω»θΥα–‘pHΚσΖΔ…ζ÷ΊΉι, ÷ΊΉιΚσΒΡP-S-H Ε±π»Υ…ώΨ≠ΫΚ÷ ΝωU87œΗΑϊ≤Δ‘ΎU87÷ΉΝω–Γ σΧεΡΎΧΊ“λ–‘Μΐάέ.
5 Ϋα¬έ”κ’ΙΆϊ
ΕύκΡΧΫ’κ”…”ΎΧΊ“λ–‘ΗΏΓΔ…ζΈοœύ»ί–‘ΚΟΚΆ“Ή”Ύ÷Τ±ΗΒ»”≈ Τ, ‘Ύ÷ΉΝωΒΡΧΊ“λ–‘…ζΈο≥…œώ÷–ΦΪΨΏ«±ΝΠ. “‘œΗΑϊΓΔœΗΑϊΆβΜυ÷ ΚΆ÷ΉΝωΈΔΜΖΨ≥Β»Εύ÷÷“ρΥΊΈΣΑ–Βψ, ÷ΉΝω±ξ÷ΨΈοΑ–œρ–ΆΚΆ÷ΉΝωΈΔΜΖΨ≥œλ”Π–ΆΒΡ÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κ±ΜœύΦΧΩΣΖΔ. Υ≥¥≈–‘Έο÷ ΓΔΖ≈…δ–‘ΚΥΥΊΚΆ”ΪΙβΖ÷Ή”ΙΠΡήΜ·ΒΡ÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κ‘ΎMRIΓΔSPECTΓΔPETΚΆ”ΪΙβ≥…œώ÷–ΙψΖΚ Ι”Ο, “―≥…ΈΣ÷ΉΝω‘ΎœΗΑϊΓΔΉι÷·ΚΆΜνΧε≤ψΟφΧΊ“λ–‘≥…œώΦλ≤βΒΡ÷Ί“ΣΙΛΨΏ. Τδ÷–, SomatostatinΒ»ΕύκΡ“―”Π”Ο”ΎΝΌ¥≤―–ΨΩ, «“68Ga PSMA-11Β»÷ΤΦΝ“―±ΜFDA≈ζΉΦΈΣ÷ΉΝωΒΡ’οΕœΦΝ(±μ4)[113-114]. Ψ≠ΙΐΕύΡξΒΡ―–ΨΩ, ÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κ“―»ΓΒΟΝν»Υ÷θΡΩΒΡΫχ’Ι, Ά§ ±¥φ‘Ύ–μΕύΒΡΜζ”ωΚΆΧτ’Ϋ.

÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κΨΏ”–≥ω…ΪΒΡ÷ΉΝω≥…œώΡήΝΠ, ”–Άϊ≥…ΈΣ÷ΉΝωΒΡ ÷ θΒΦΚΫΙΛΨΏ. ΕύκΡΧΫ’κΖ÷Ή”ΝΩΫœ–Γ, ‘Ύ»ΥΧε÷–ΒΡΑκΥΞΤΎΕΧ, ¥ζ–ΜΥΌΕ»Ωλ. ’β“ΜΧΊΒψ Ι÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κΡή‘Ύ ÷ θΙΐ≥Χ÷–Ϋχ––Φ¥ ±ΉΔ…δΚΆ ÷ θΒΦΚΫ, ΧαΗΏΝΥ ÷ θ–߬ ; »ΜΕχ, ’β“ΜΧΊΒψ“≤‘λ≥…ΝΥ ÷ θ¥ΑΩΎΤΎΕΧΒΡΈ Χβ. “ρ¥Υ, ΧαΗΏ÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κΒΡΈ»Ε®–‘ΚΆ…ζΈοΩ…”Ο–‘≥…ΈΣ±ΨΝλ”ρΒΡΙΊΦϋΧτ’Ϋ. ΗΏΈ»Ε®–‘ΚΆΩμ ÷ θ¥ΑΩΎΤΎΫΪ Ι÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κΒΡΝΌ¥≤ ÷ θΒΦΚΫ≥…ΈΣΩ…Ρή.
ΟφΕ‘≤ΜΆ§÷ΉΝωάύ–ΆΦδΒΡ≤ν“λ–‘“‘ΦΑ–¬–Υ÷ΉΝωΑ–ΒψΒΡ≤ζ…ζ, Α–ΒψΒΡΕύ―υ–‘≥…ΈΣ÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κΒΡΝμ“ΜΧτ’Ϋ. –¬Α–ΒψΒΡΧΊ“λ–‘ΕύκΡΒΡ…Η―Γ «ΧαΗΏΕύκΡΧΫ’κΕύ―υ–‘ΒΡ÷Ί“ΣΜΖΫΎ. –¬Α–ΒψΕύκΡΧΫ’κΒΡΩΣΖΔΫΪΆΤΕ·≤ΜΆ§÷÷άύ÷ΉΝωΒΡΨΪΉΦ’οΕœ. Ά§ ±, Μυ”Ύ–¬Α–ΒψΒΡ÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κΒΡ…ζΈο≥…œώ”κΟβ“ΏΝΤΖ®Β»–¬–Ά÷ΉΝω÷ΈΝΤΖΫΖ®ΒΡΝΣ”Ο, ΡήΙΜΈΣ÷ΉΝω’οΝΤ“ΜΧεΜ·ΖΫΖ®ΒΡΩΣΖΔΧαΙ©–¬ΤθΜζ.
Ήή÷°, ΥφΉ≈≤ΡΝœΩΤ―ßΓΔΖ÷Ή”…ζΈο―ßΓΔ÷ΉΝω“©άμ―ßΒ»―ßΩΤΒΡΩγ―ßΩΤΖΔ’Ι, Έ“Ο«œύ–≈÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κΒΡ…ζΈο≥…œώΫΪ≥…ΈΣ÷ΉΝωΝΌ¥≤’οΕœΒΡ÷Ί“ΣΖΫΖ®. Ά§ ±, ÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κΫΪ÷π≤ΫΆΜΤΤΉηΑ≠, Ϋχ»κ÷ΉΝωΒΡΝΌ¥≤”Π”Ο, ΈΣ÷ΉΝωΒΡΨΪΉΦ÷ΈΝΤΧαΙ©ΙΛΨΏ. ÷ΉΝωΧΊ“λ–‘ΕύκΡΧΫ’κΒΡΖΔ’Ι, ΫΪΖΰΈώ”Ύ÷ΉΝωΒΡΨΪΉΦ’οΕœΚΆΗω–‘Μ·÷ΈΝΤ, Ϋχ“Μ≤ΫΧα…ΐ»Υάύ…ζΟϋΒΡ≥ΛΕ»ΚΆ÷ ΝΩ.
Οβ‘π…υΟςΘΚ±ΨΈΡΈΣ––“ΒΫΜΝς―ßœΑΘ§Αφ»®Ιι‘≠Ής’ΏΦΑ‘≠‘”÷ΨΥυ”–Θ§»γ”–«÷»®Θ§Ω…ΝΣœΒ…Ψ≥ΐΓΘΈΡ’¬±ξΉΔ”–Ής’ΏΦΑΈΡ’¬≥ω¥ΠΘ§»γ–η‘ΡΕΝ‘≠ΈΡΦΑ≤ΈΩΦΈΡœΉΘ§Ω…‘ΡΕΝ‘≠‘”÷ΨΓΘ










