
摘 要:肿瘤微环境在肿瘤的发生、发展和转移过程中起着至关重要的作用,因此靶向调控微环境为发展肿瘤精准治疗的新策略提供了机遇。纳米技术的快速发展为传统药物的增效减毒提供了契机,已有一系列纳米药物用于肿瘤临床治疗。近年来,分子自组装领域的快速发展为智能纳米药物的研发提供了新机遇。多肽作为生物相容性高、序列可设计、易修饰、功能多样化的生物分子,可组装构建结构多样和功能集成的纳米药物系统。本文综述了利用多肽自组装超分子体系实现药物对肿瘤微环境的响应释放和高效递送,并对其通过调控微环境中的血管、成纤维细胞和胞外基质等组分,改变肿瘤赖以生存的“土壤”,并与抗肿瘤细胞治疗有机结合的最新进展进行了介绍。针对肿瘤异质性和复杂性的难题,构建表/界面性质可控的纳米药物系统,发展基于肿瘤微环境调控与联合治疗的肿瘤综合治疗方案,将是未来重要的发展方向之一。
恶性肿瘤的发病率和死亡率高、诊疗难度大、易复发和转移[1],现有的放化疗、靶向治疗、免疫治疗及纳米药物均无法有效降低恶性肿瘤的死亡率,研发新型治疗药物迫在眉睫。肿瘤组织包括肿瘤细胞及其周围的间质细胞和细胞外基质,共同构成了肿瘤微环境[2]。肿瘤细胞与微环境的关系犹如“种子”和“土壤”,被肿瘤细胞驯化的间质细胞协同细胞外基质为肿瘤细胞提供适宜生存、转移和耐药的微环境,不仅加速了肿瘤的恶性进展,还构成阻碍药物输运的重要屏障,严重影响抗肿瘤药物的疗效[3, 4]。与肿瘤细胞相比,肿瘤组织的间质细胞与基质所占比例高、遗传背景相对稳定、与药物接触机率高[5],因此,靶向肿瘤微环境的治疗成为遏制肿瘤的新策略。
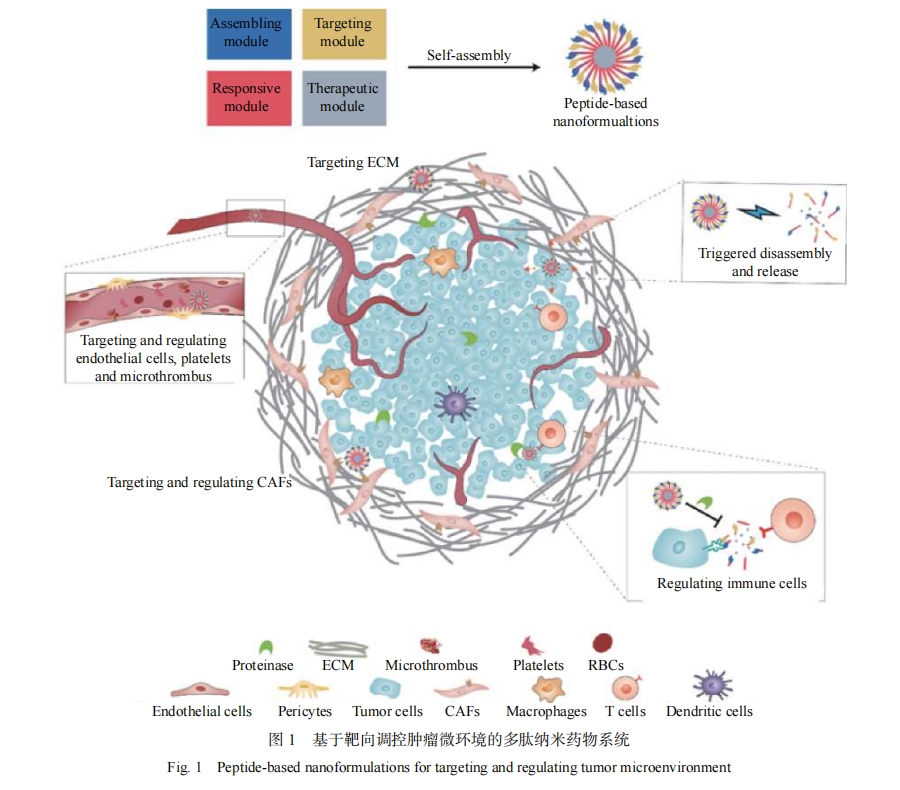
纳米技术的发展为传统药物的增效减毒提供了契机,一系列纳米药物已用于肿瘤临床治疗[6]。基于新型载体的抗肿瘤药物研发是目前的热点之一[7]。近年来,分子自组装领域的快速发展为智能纳米药物研发提供了新的机遇,该技术将不同功能的分子以非共价键组装成高度有序的纳米体系,是构建结构多样、功能集成的纳米药物的有效策略[8]。生物分子多肽序列中氨基酸残基具有不同的化学结构,其可以利用肽链间氢键作用以及氨基酸残基之间的各种非共价键的作用有效实现分子自组装[9]。基于多肽及其衍生物在结构设计上精确可控的特性,可将具有不同生物功能的多肽分子通过可控组装进行模块化功能集成,构建多肽纳米药物[10]。基于多肽自组装构建的抗肿瘤纳米药物包含两个层次的内容:一是以多肽自组装体作为载体输运和递送药物分子;二是以抗肿瘤活性短肽为组装基元构建多肽药物的纳米剂型[5, 11-13]。
1 靶向调控肿瘤血管系统相关成分
为了运输营养和排出代谢废物,肿瘤微环境中含有大量血管。肿瘤血管主要由内皮细胞及附近的周细胞和基底膜构成[15]。内皮细胞为血管管腔的主体;周细胞包裹在血管外,为内皮细胞提供结构支持和促进血管成熟[16]。肿瘤血管新生是指肿瘤组织为了在快速增殖过程中获得足够的氧气供给和营养物质,肿瘤细胞通过释放多种促血管生长因子,进而过表达相应受体的内皮细胞发生增殖和迁移,在已有血管的基础上新生出更多的毛细血管,从而满足能量需求[17]。和正常组织血管不同的是肿瘤血管生长迅速,导致其具有形态学上的不规则性[15];同时由于内皮细胞和周细胞的连接不紧密,增加了血管渗透性―即实体瘤的高渗透长滞留效应(EPR效应)[18],但这也在一定程度上为肿瘤转移创造了条件[19]。
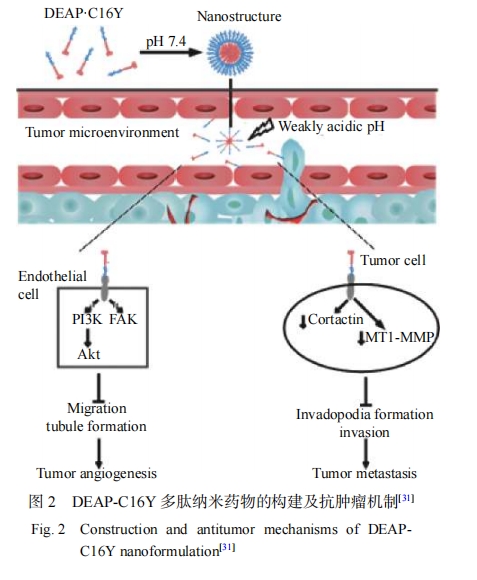
化疗是抗肿瘤治疗的主要手段之一,然而化疗药物触发的血管重建与破裂是导致肿瘤复发和转移的关键原因[33]。大量研究表明,3种细胞(包括肿瘤细胞、血管周围的巨噬细胞和内皮细胞)的密度和乳腺癌转移的风险挂钩。化疗药物明显影响了肿瘤组织中血管周围的巨噬细胞密度,在新增的巨噬细胞中,受体酪氨酸激酶Tie2相关巨噬细胞(Tie2 associated macrophages, TAMs)的比例尤其多。敲除巨噬细胞上Tie2受体后血管重建和肿瘤复发的概率大幅度减少[34]。因此,抑制Tie2的功能是减少肿瘤复发和转移风险的重要策略。在众多具有Tie2抑制功能的小分子抑制剂中,短肽NLLMAAS具有强大的抗肿瘤活性。然而,短肽NLLMAAS是疏水性多肽,生物利用度差;此多肽序列对抗肿瘤活性有着高度保守性,改变其氨基酸顺序和对其侧链和两端进行任何修饰都将使其失去抗肿瘤活性[35]。以上特性都严重增加了对其改造并提高成药性的难度,因此我们考虑基于自组装技术构建多肽纳米药物,提高其未来临床应用的可能性。
我们将抗肿瘤活性疏水肽NLLMAAS改造成两亲性分子[36],自组装构建具有肿瘤微酸性环境和酶双重响应的多肽纳米药物。两亲性组装基元为PEG1000-K(DEAP)-AAN-NLLMAAS,其亲水部分为PEG1000,用于增加纳米体系的体内半衰期。疏水部分包括3个功能模块:(1)肿瘤微环境特异性高表达的豆荚蛋白酶(legumain)的特异性底物片段AAN-X作为酶响应模块;(2)功能分子DEAP在生理环境中呈现疏水性,在pH约6.8的微酸性环境中质子化带正电荷,作为肿瘤微酸性pH响应模块;(3)疏水性抗肿瘤活性肽NLLMAAS作为效应模块。此多肽纳米药物一方面可提高疏水性抗肿瘤活性肽在血液循环中的稳定性和生物利用度;另一方面,将NLLMAAS序列隐藏在其疏水核区域,从而避免暴露在纳米结构表面以减少机体血管功能异常的副作用;通过对肿瘤微酸性环境和酶的双重响应性,产生特异性解聚变构释放抗肿瘤活性肽NLLMAAS,且不改变氨基酸序列,以确保其抗肿瘤活性。在乳腺癌肿瘤模型中,我们发现此多肽纳米药物通过肿瘤原位抑制Tie2功能,减少了化疗后血管重建和破裂等异常现象,与对照组相比,降低约97%的化疗后肺部转移,并减小副作用,最终有效控制肿瘤的恶性发展,实现更加高效、长效、安全的肿瘤治疗。
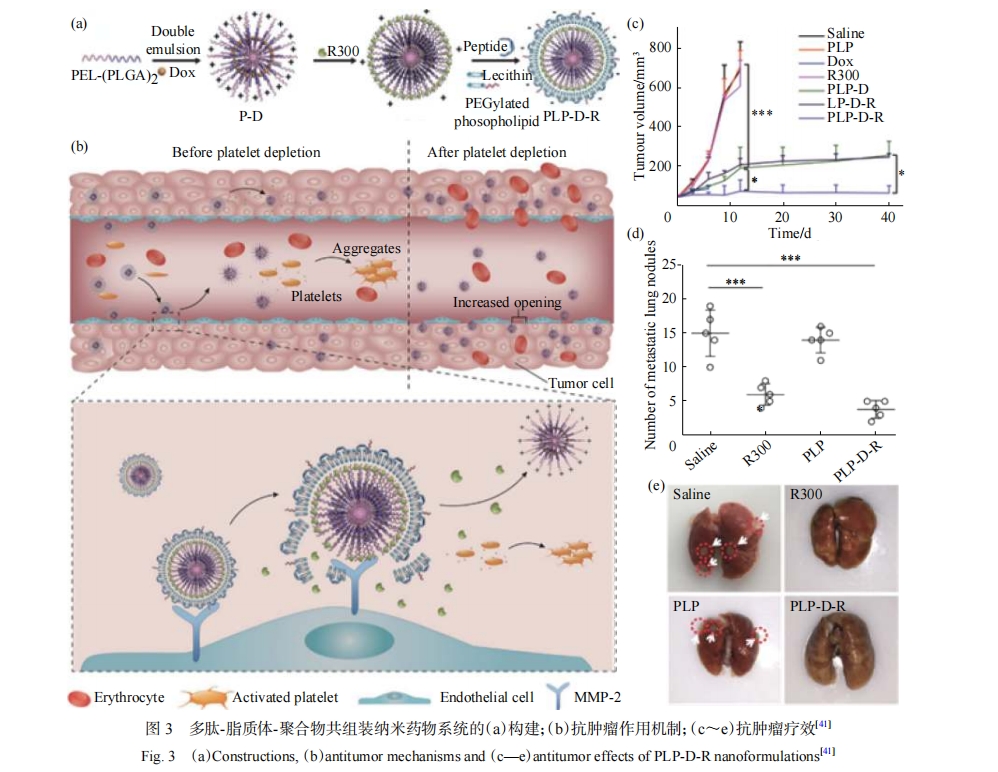
此外,肿瘤相关血小板已经被证实在肿瘤转移过程中发挥关键作用,它们可以刺激肿瘤细胞获得侵袭特性,释放转化生长因子(TGF-β)[46],在转移至远处病灶过程中结合至循环肿瘤细胞表位,避免被免疫系统中的自然杀伤细胞(NK细胞)清除[47],或将主要组织相容性复合体(MHC)Ⅰ类蛋白转移至肿瘤细胞表面。与肿瘤细胞的异质性不同,血小板性质相对稳定,因此展示出作为诊疗靶点的优良特性。Zhang等[48]利用多肽序列CREKA(Cys-Arg-Glu-Lys-Ala)能够特异性与肿瘤血管壁上的纤维蛋白-纤连蛋白复合物(微血栓)结合的特点,通过薄膜法制备表面修饰CREKA的卵磷脂/DSPE杂合脂质体包载替卡格雷,竞争性抑制肿瘤相关血小板上P2Y12受体[49],并抑制TGF-β释放。与生理盐水组相比,实现了75%的肺部转移抑制率。
2 靶向调控免疫细胞
肿瘤相关巨噬细胞是肿瘤微环境中免疫细胞的主要和主导性成分[50, 51]。微环境中的巨噬细胞会根据环境刺激选择性分化为M1型或者M2型巨噬细胞,这两种表型的生物标记分子不尽相同[52]。M1型细胞为免疫激活型细胞,通过释放γ-干扰素(IFN-γ)和Notch信号通路介导抗肿瘤免疫活性[53]。在缺氧的肿瘤微环境中,巨噬细胞会倾向于分化为M2型,其高表达抗炎性细胞因子如TGF-β和IL-10,M2型巨噬细胞和肿瘤细胞间的相互作用还会激活STAT3信号通路,促进形成免疫抑制性肿瘤微环境,使肿瘤细胞逃脱免疫系统的监视和清除[54]。在大多数癌症中,较低的M1与M2型巨噬细胞比例与预后呈负相关[55]。此外,还有报道表明TAM是化疗和放疗过程中产生耐受性的关键因素[56]。针对肿瘤相关巨噬细胞的治疗策略以抑制巨噬细胞募集,降低TAM存活率,增强TAM向M1型细胞分化,或者抑制M2型细胞的促肿瘤活性为主[57]。Conde等[58]设计了以金纳米粒为核体,表面修饰小干扰RNA(siRNA)和多肽的杂合纳米体系,利用M2pep(YEQDPWGVKWW)特异性靶向至肺癌相关巨噬细胞,同时结合小干扰RNA降低M2 TAM中VEGF的表达,抑制肿瘤血管新生和侵袭。在作者构建的小鼠肺癌原位模型中,长期给以低剂量制剂显著降低TAM在肺部肿瘤组织的募集,肿瘤抑制率约为95%,生存期延长约75%,展示出良好的治疗效果。

在肿瘤微环境中存在多种T细胞亚群,它们分别具有抑制和促进肿瘤生长的作用[3]。CD8+ T细胞(CTL)通过促进肿瘤细胞凋亡具有强大的肿瘤杀伤能力,因此肿瘤组织的CTL细胞比例和预后呈正相关[54];CD4+ T细胞(Th)通过释放促炎细胞因子如白细胞介素-2和IFN-γ增强其他细胞的免疫活性[65];肿瘤微环境中CD4+CD25+FOXP3+ T细胞(Treg)种群比例的增加表明肿瘤免疫抑制微环境的产生,同时Treg能够诱导单核粒细胞向M2型分化[66]。然而,肿瘤在恶性增生过程中进化出多种机制逃脱机体的免疫反应,细胞程序性死亡受体-1(PD-1)是在T细胞表面表达的免疫检查点受体,许多实体瘤通过过表达细胞程序性死亡受体-1的配体(PD-L1),抑制激酶信号通路,从而降低T细胞的增殖与活力,逃脱免疫系统的攻击[67]。
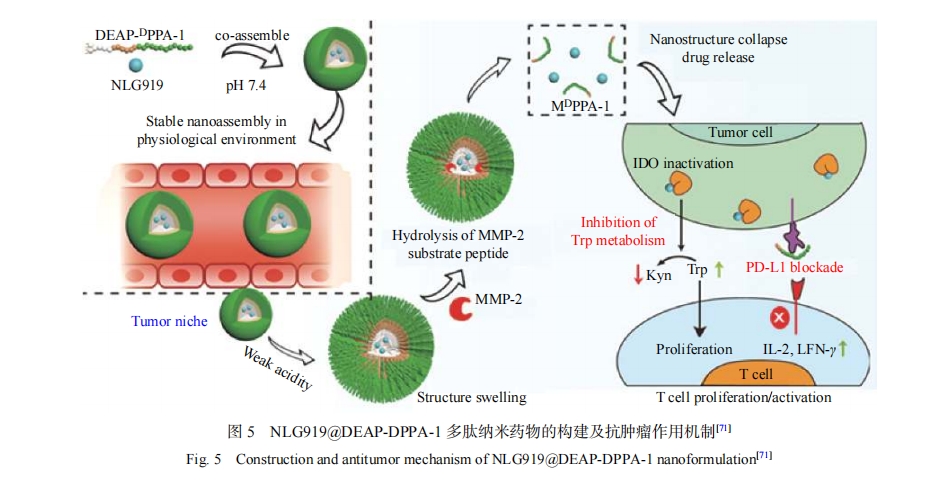
阻断免疫检查点的免疫疗法为治愈肿瘤患者提供了希望,PD-L1和吲哚胺-(2, 3)-双加氧酶(IDO)是肿瘤免疫治疗的重要靶点[68, 69]。免疫检查点抗体药物疗效显著,但它们同时给患者带来了严重甚至持续性的不良反应,尤其是多药联合应用导致的不良反应率更高。其中一个重要原因是抗体类药物的免疫原性很高,同时抗体药物还存在研发周期长、制备成本高和组织渗透率低等问题[70]。与抗体药物相比,多肽药物的组织渗透率高、免疫原性低、受体结合率高,但体内半衰期很短,严重制约了其临床应用。
3 靶向调控肿瘤相关成纤维细胞(CAFs)
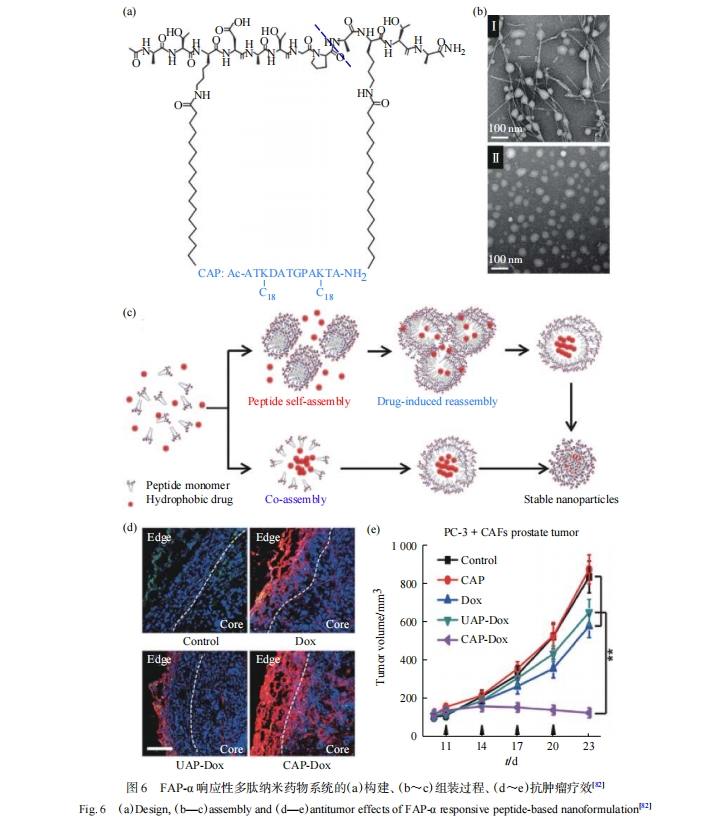
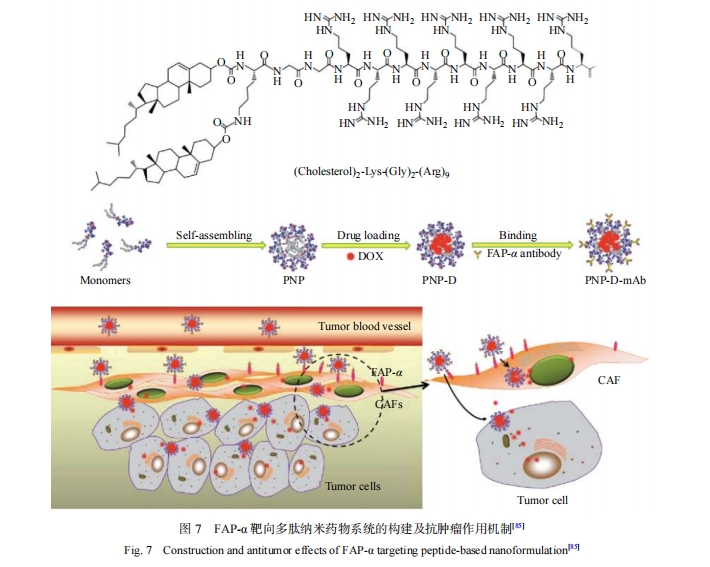
4 靶向调控细胞外基质的纳米药物系统
细胞外基质(ECM)是一种包含胶原、弹性蛋白、纤连蛋白、透明质酸、糖蛋白以及蛋白聚糖的三维结构[86],用以支撑细胞和维护体系水分及pH的动态平衡[87]。由于肿瘤细胞的异质性、组织乏氧以及炎性反应,导致了以胶原交联沉积为代表的细胞外基质重构现象,表现为基质的密度和刚性增加[88]。重构的细胞外基质一方面促进血管新生、肿瘤增殖和迁移,另一方面致密的细胞外基质和肿瘤细胞的堆叠增大了组织间质压,极大限制了药物渗透进入深层组织和穿透血管的能力,增加了肿瘤组织的耐药性[89]。CAFs在肿瘤微环境中合成并分泌大量细胞外基质的主要成分,因此主导塑造高度纤维化的致密生物屏障,在基质丰富的实体瘤中严重限制着纳米药物的瘤内递送。
Ⅳ型胶原(Collagen IV)在血管基底膜成分中占50%左右[93]。Langer等[94]通过噬菌体筛选技术设计出多肽序列(HWGSLRA),体外实验展示出对Collagen IV的特殊亲和力,并构建了基于FDA批准的生物安全性材料的胶束型紫杉醇药物递送系统,表面修饰多肽特异性结合组织中Ⅳ型胶原。体内实验证明,该载药系统对于创伤后血管具有良好的靶向性并可实现长达12 d的缓控释效果。Langer等表示该体系日后可以应用于包括心脑血管疾病和癌症在内的一系列血管类疾病进行药物递送和治疗。
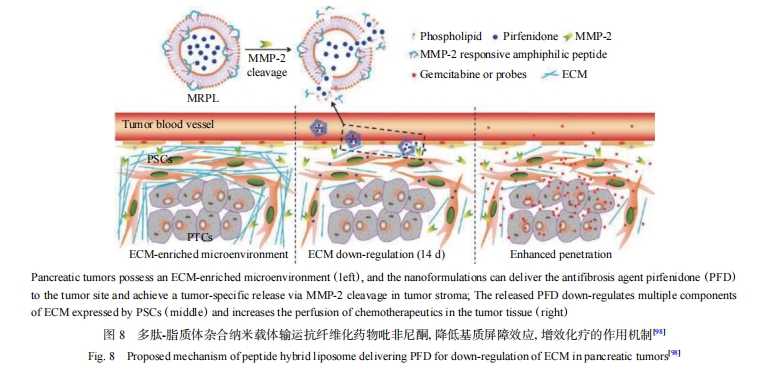
5 总结与展望
针对恶性肿瘤治疗难度大、易复发和转移等临床挑战,发展基于自组装生物纳米材料靶向调控肿瘤微环境的创新策略,为实现肿瘤的综合性精准治疗提供了科学依据,将是未来重要的发展方向之一。通过纳米技术改善和重塑肿瘤微环境,可实现抑制肿瘤恶性表型,提高肿瘤治疗效果。基于多肽和高生物相容性分子精准自组装技术,构建表/界面性质可控的纳米药物系统,可实现药物在体内多靶点、多层次、多模式的肿瘤靶向递送和可控响应释放;揭示生物纳米材料组装调控规律,及其影响肿瘤微环境病理效应的关键纳米参数;发展基于肿瘤微环境调控的纳米抗肿瘤综合治疗策略。
聚焦人类健康与疾病,智能诊疗技术已逐渐成为快速捕获各类疾病的分子表型,认识其在疾病发生、发展过程中的动态演化规律,实现对疾病的早期预防、诊断和治疗的关键技术。充分利用多肽分子的结构特性和生物功能特性等优势,基于模块化设计的概念,可以通过对多肽单体的设计、修饰和组装实现不同功能多肽分子的模块化生物功能性集成,构筑具有系列生物功能的多肽纳米药物系统。它一方面可以兼顾多肽的生物相容、生物可降解等特性;另一方面,多肽超分子组装体能够在不同的生物环境中进行可控组装和解聚的变构过程,因此,多肽纳米药物系统具有生物功能多样化和利于变构的明显优势。综合利用疾病微环境的病理、生理特点,精准构筑多肽纳米药物系统,使其在肿瘤微环境中实现可控变构和功能性,将有助于我们更好地认识生命体的生理与病理过程等,研究诸多与人类健康和疾病相关的科学问题,有望成为实现对疾病精准诊断和治疗的一个重要突破口。
免责声明:本文为行业交流学习,版权归原作者及原杂志所有,如有侵权,可联系删除。文章标注有作者及文章出处,如需阅读原文及参考文献,可阅读原杂志

电话:0551-65177703 邮箱:pb@peptidesbank.com 地址:安徽省合肥市四川路868号云谷创新园A6栋3层
合肥肽库生物(Taikubio)只为有资质的科研机构、医药企业基于科学研究或药证申报的用途提供医药研发服务, 不为任何个人或者非科研性质的、非用于药证申报使用等其他用途提供服务。