
еЊвЊ БОЮФвдШ§ДњОлЙШАБЫсыФРрЪїжІзДЗжзг(G3-Glu)ЮЊДѓЗжзгв§ЗЂМС, в§ЗЂ N-єШЛљ-L-БНБћАБЫс-ЛЗФкЫсєћ(NCA-Phe)ЕФПЊЛЗОлКЯЗДгІ, жЦБИОлЙШАБЫсЪїжІзДДѓЗжзг-ОлБНБћАБЫсЧЖЖЮЙВОлЮя. ЧЖЖЮЙВОлЮяЭЈЙ§здзщзАаЮГЩвдОлБНБћАБЫсСДЖЮЮЊКЫ, ОлЙШАБЫсЪїжІзДДѓЗжзгЮЊПЧЕФНКЪј. НЋПЙжзСівЉЮяАЂУЙЫиИКдиЕНИпЗжзгНКЪјжа, баОПЦфвЉЮяЪЭЗХадФмМАЬхЭтПЙжзСіаЇЙћ. НсЙћБэУї, ЙВОлЮяНКЪјОпгаСМКУЕФЩњЮяЯрШнад. дивЉНКЪјОпгавЉЮяЛКЪЭаЇЙћ, вЉЮяГжајЪЭЗХЪБМфПЩДя 60 h. дивЉНКЪјЕФЬхЭтПЙжзСіЪЕбщБэУїЦфЖдИЮАЉЯИАћ HepG2 ОпгаКмКУЕФЩБУ№аЇЙћ, ЙВХрбј 48 h КѓЖдАЉЯИАћЕФЩБЫРТЪПЩИпДя 75%.
здзщзАдкаТаЭЙІФмВФСЯЕФЙЙжўжавбЯдЪОГіОоДѓЕФЧБСІ[1, 2]. КЯГЩЖрыФЗжзгЭЈЙ§здзщзАаЮГЩЕФВФСЯдкЦфНсЙЙЁЂаЮУВКЭадФмЩЯОпгаЮоПЩБШФтЕФгХЪЦ[3]. КЯГЩЖрыФздзщзАВФСЯВЛНіПЩвдаЮГЩЧђаЮЁЂАєзДЁЂЯпадМАФвХнЕШВЛЭЌЕФНсЙЙКЭаЮЬЌ[4~7], ВЂЧвЛЙОпгаИїжжЬивьадЕФЮяРэЁЂЛЏбЇЛђЩњЮябЇЙІФм[4, 8, 9]. вдЬьШЛАБЛљЫсЮЊдСЯЕФКЯГЩЖрыФ, гЩгкЦфСМКУЕФЩњЮяЯрШнадКЭЩњЮяНЕНтад, вбГЩЮЊвЛРрживЊЕФЩњЮявНгУВФСЯ, дкМВВЁеяжЮКЭзщжЏаоИДЕШЩњЮявНбЇСьгђЗЂЛгзХживЊЕФзїгУ. РћгУыФРрДѓЗжзгздзщзАЙЙНЈЕФвЉЮя/ЛљвђДЋЪфдиЬхВФСЯПЩБЛИГгшгХдНЕФжЧФмЛЗОГЯьгІКЭАаЯђЙІФмад[10~12]; ЖрыФздзщзАЫЎФ§НКдкзщжЏаоИДжаЯдЪОГіКмКУЕФзщжЏдйЩњгеЕМаЇЙћ[13~15].
ыФРрЪїжІзДДѓЗжзгГ§СЫОпгаЦеЭЈЪїжІзДДѓЗжзгЬиеїШчЙцећадЁЂИпЖШжЇЛЏЁЂБэУцИпУмЖШЙйФмЭХЁЂФЩУзГпЖШЁЂЗжзгСПЕЅвЛЕШЭт, ЛЙОпгаРрЫЦЕААзЕФНсЙЙ, вдМАДѓСПЭтЮЇЙйФмЭХИГгшЕФСМКУЫЎШмад[16]. ЛљгкыФРрЪїжІзДДѓЗжзгЫЋЧзадЧЖЖЮЙВОлЮяздзщзАЙЙНЈЕФНКЪјгыДЋЭГЕФЯпаЮЫЋЧзадЧЖЖЮЙВОлЮяздзщзАаЮГЩЕФИпЗжзгНКЪјЯрБШ, ВЛНіОпгаИќИпЕФЮШЖЈад, ЦфЭтЮЇОпгаИќЖрПЩЙЉаоЪЮЕФЙйФмЭХ, гаРћгкНјвЛВННјаажЧФмЁЂАаЯђЕШЙІФмЕФаоЪЮ. Р§Шч, ЪїжІзДДѓЗжзгЧЖЖЮОлКЯЮядкЯрааЮЊЩЯгыЯпаЮЧЖЖЮОлКЯЮяОЭДцдкУїЯдВювь[17]; ЭЈЙ§ЭтЮЇЕФЪїжІзДЗжзгвдИФЩЦздзщзАЬхЕФШмНтадФм, ДгЖјИФБфСЫздзщзАЬхЕФЮяРэЁЂЛЏбЇЬиад[18]; Рћ гУ dendron-like/linear/dendron-like ЧЖЖЮОлКЯПЩ ЙЙжўаЮЬЌОљвЛЕФздзщзАдиЬх, ВЂгУзївЉЮяЛКЪЭЕФдиЬх[19].
БОЮФЭЈЙ§ЗЂЩЂ-ЪеСВЯрНсКЯЕФЗНЗЈКЯГЩШ§ДњОлЙШАБЫсЪїжІзДДѓЗжзг(G3-Glu)[20], вдЪїжІзДДѓЗжзгКЫжаЕФАБЛљв§ЗЂ N- єШ Лљ -L- БНБћАБЫс - ЛЗФкЫсєћ(NCA-Phe)ЕФПЊЛЗОлКЯ[21]КЯГЩОлЙШАБЫсЪїжІзДДѓЗжзг-ОлБНБћАБЫсЫЋЧзадЧЖЖЮЙВОлЮя, ЭЈЙ§здзщзАаЮГЩНКЪј. вдЩЈУшЕчзгЯдЮЂОЕ(SEM)ЁЂЭИЩфЕчзгЯдЮЂОЕ(TEM)БэеїСЫЙВОлЮяНКЪјЕФНсЙЙаЮУВ. НЋЪшЫЎадПЙжзСівЉЮяАЂУЙЫиИКдиЕНздзщзАНКЪјжа, баОПСЫдивЉНКЪјЕФвЉЮяЪЭЗХааЮЊ, ЬхЭтЯИАћЩуШЁвдМАЖдИЮАЉЯИАћ HepG2 ЕФЩБУ№аЇЙћ.
2 ЪЕбщВПЗж
2.1 ЪЕбщЪдМС
ЪхЖЁбѕєЪЛљ-ЙШАБЫс(Boc-Glu-COOH), ЙШАБЫсЫЋмаѕЅ(H-Glu(OBzl)-OBzl), 1-ввЛљ-(3-ЖўМзЛљАБЛљБћЛљ)ЬМЖўбЧАЗ(EDC), 1-єЧЛљБНВЂШ§пђ(HOBT), N,N-ЖўвьБћЛљввАЗ(DIEA), Ш§ЗњввЫс(TFA), мабѕєЪЛљ-БНБћАБЫс(N-Cbz-Phe), ЫФЧтпЛрЋ, ЖўТШМзЭщ, е§МКЭщ, ввЫсввѕЅ, ввДМ, NaHCO3, NaHSO4, NaCl, ЮоЫЎ MgSO4, DMEM(ИпЬЧ)ЯИАћХрбјЛљЕШ.
2.2 вЧЦї
КЫДХЙВеёВЈЦзвЧ(NMR, Bruker AV-400); ИЕСЂвЖКьЭтЙтЦзвЧ(FTIR, Necolet PE Spectrometer); ЪБМфЗЩаажЪЦз(TOF, Bruker Autoflex III); ГЌЩљВЈЧхЯДЦї(KQ-300DE); ЩЈУшЕчзгЯдЮЂОЕ(SEM, JSM-5900LV); ЭИЩфЕчзгЯдЮЂОЕ(TEM, JEM-100CX); ЖЏЬЌЙтЩЂЩфвЧ(DLS, Malvern Zetasizer Nano ZS); МЄЙтЙВОлНЙЩЈУшЯдЮЂОЕ(CLSM, Leica TCP SP5).
2.3 ОлЙШАБЫсШ§ДњЪїжІзДДѓЗжзг(G3-Glu)ЕФКЯГЩ
2.3.1 ЙШАБЫсЖўДњ(G2-Glu)ЕФКЯГЩ
Boc-Glu-COOH КЭЙ§СПЕФ H-Glu(OBzl)-OBzl дкЕЊЦјБЃЛЄЯТ, ЭЈЙ§ HOBT/EDC/DIEA ДпЛЏЫѕКЯ, дк CH2Cl2 жаГЃЮТЗДгІ 24 h. гУБЅКЭ NaHCO3 ШмвКЁЂNaHSO4 ШмвКЁЂБЅКЭ NaCl ШмвКЗДИДЯДЕгВњЮя. ЖдВњЮяХЈЫѕКѓдк CH2Cl2/е§МКЭщжажиНсОЇ, Й§ТЫИЩдяКѓЕУЕНВњЮя 1, ШчЭМ 1.
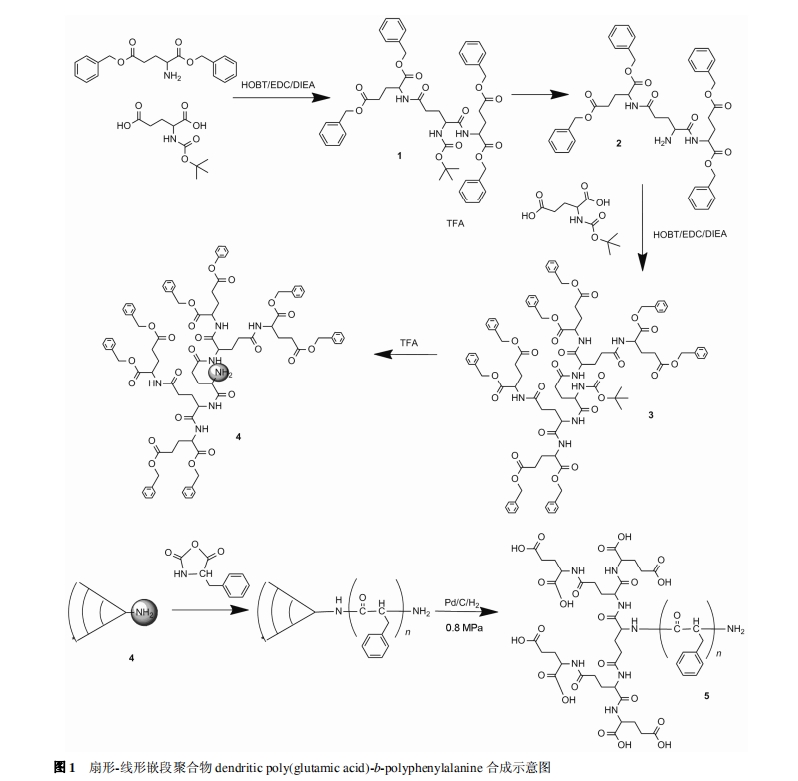
2.3.2 Ш§ДњОлЙШАБЫсЪїжІзДДѓЗжзг(G3-Glu)ЕФКЯГЩ
ЙШАБЫсЖўДњ(G2-Glu)дкЕЊЦјБЃЛЄЯТ, гУ TFA ЭбГ§ Boc БЃЛЄ, МѕбЙГ§ШЅ TFA, ЕУЕНВњЮя 2. ВњЮя 2 дкЕЊЦјБЃЛЄЯТМгШыЕН Boc-Glu-COOH жа, ЭЈЙ§ HOBT/ EDC/DIEA ДпЛЏЫѕКЯ , ГЃЮТЗДгІ 24 h. гУБЅКЭNaHCO3 ШмвКЁЂNaHSO4 ШмвКЁЂБЅКЭ NaCl ШмвКЗДИДЯДЕгЪ§ДЮ. РћгУЙшНКжљЙ§жљЗжРы, ЕУЕНОлЙШАБЫсШ§ДњЪїжІзДДѓЗжзг(G3-Glu)(ВњЮя 3, ЭМ 1).
2.4 ЙВОлЮяЕФжЦБИ
2.4.1 ДѓЗжзгв§ЗЂМС G3-Glu-NH2 ЕФжЦБИ
ОлЙШАБЫсШ§ДњЪїжІзДДѓЗжзг(G3-Glu)дкЕЊЦјЕФБЃЛЄЯТ, гУ TFA ЭбГ§ Boc БЃЛЄ, МѕбЙГ§ШЅ TFA ЕУЕНВњЮя 4. НЋВњЮя 4 дк NaOH ДМШмвКжаЕїНк pH жЕ, ГфЗжНСАш, а§ИЩШмМС, НЋЙЬЬхШмгк CH2Cl2, ТЫГ§ЙЬЬх, НЋТЫвКа§ИЩД§гУ.
2.4.2 N-єШЛљ-L-БНБћАБЫс-ЛЗФкЫсєћ(NCA-Phe)ЕФКЯГЩ
ГЦШЁЮоЫЎИЩдяЕФмабѕєЪЛљ-БНБћАБЫс(Cbz-Phe), дкЕЊЦјБЃЛЄЯТШмгк 20 mL ЮоЫЎ THF жа, Щ§ЮТжС 40 Ёц; НЋ SOCl2 ЕЮШыЩЯЪіЗДгІЬхЯЕ, ЗДгІ 4 h. АбЗДгІвКМгШыЙ§СПЮоЫЎе§МКЭщжа, ЕЭЮТОВжУ 12 h. НЋЕУЕНЕФАзЩЋГСЕэгУЮоЫЎввЫсввѕЅ/ЮоЫЎе§МКЭщЗДИДжиНсОЇ 3 ДЮ, ецПеИЩдяЕУЕНАзЩЋеызДОЇЬх.
2.4.3 ЧЖЖЮЙВОлЮяЕФКЯГЩ
АДееФІЖћБШ 1:10 ЕФБШР§, зМШЗГЦШЁИЩдяДІРэКѓЕФДѓЗжзгв§ЗЂМСКЭ L-Phe-NCA ЭЖШыЗДгІЦПжа, ГщецПеКѓЭЈШыЕЊЦјБЃЛЄ. МгШы DCM/DMF ЛьКЯШмМС, ЪвЮТЗДгІ 48 h, ЕУЕНВњЮя 5. дкбЙСІдМЮЊ 0.8 MPa ЕФИпбЙИЊжа, вд Pd/C ЮЊДпЛЏМС, МгШы H2, ЪвЮТЗДгІ 24 h, ЭбШЅ OBzl. Й§ТЫЗжРы, МѕбЙГ§ШЅШмМСКЭмаДМ.
2.5 СйНчНКЪјХЈЖШЕФВтЖЈ
вдмХЮЊгЋЙтЬНеыВтЖЈздзщзАНКЪјЕФСйНчНКЪјХЈЖШ, дкЙЬЖЈЕФгЋЙтМЄЗЂВЈГЄЯТ, ВтЖЈ I338 КЭ I335 ДІЕФгЋЙтЮќЪежЕ.
2.6 ЬхЭтвЉЮяЪЭЗХ
НЋЧЖЖЮЙВОлЮяШмгкМзДМжа, дкГЌЩљЬѕМўЯТЛКТ§ЕЮМгЕНШЅРызгЫЎжа, ОВжУ, МѕбЙГ§ШЅМзДМ. АДееБШР§НЋЧЖЖЮЙВОлЮяКЭАЂУЙЫиХфГЩМзДМШмвК, дкГЌЩљЬѕМўЯТЛКТ§ЕЮМгЕНШЅРызгЫЎжа, дк 4 ЁцЯТЭИЮі 24 h, РфЖГИЩдяКѓБИгУ.
зМШЗГЦШЁвЛЖЈСПЕФдивЉНКЪј, ШмгкСМШмМСжа, ВтЖЈИУШмвКдкВЈГЄ 485 nm ДІЕФгЋЙтЮќЪежЕ, вРОнБъзМЮќЪеЧњЯпМЦЫудивЉНКЪјжаАЂУЙЫиЕФСП.
ОЋШЗГЦШЁдивЉНКЪјШмгк PBS ЛКГхШмвКжа(pH 7.4), ХфГЩ 1 mg/mL ШмвК. ЩшжУ 3 зщбљ, дкНиСєЗжзгСПЮЊ2000 Da ЕФЭИЮіДќжаМгШы 1 mL ЕФЛКГхШмвК, жУгк 25 mL 37 ЁцЕФ PBS жа. ИљОнВЛЭЌЪБМф, ШЁГі 1 mL ЪЭЗХНщжЪ, ЭЌЪБВЙГф 1 mL PBS ШмвК. ВтЖЈНщжЪдкВЈГЄ 485 nm ДІЕФгЋЙтЮќЪежЕ, ЛцжЦдиАЂУЙЫиНКЪјЕФЬхЭтЪЭЗХЧњЯп. ВЂВтЖЈЖдеезщбЮЫсАЂУЙКЭАЂУЙЫиЕФЪЭЗХЧњЯп.
2.7 ЯИАћЖОадЪЕбщ
НЋ 3T3 ЯИАћНгжжгк 3 Пщ 96 ЯИАћХрбјПзАх(T = 12 h, 1ЁС104Иі/Пз; t = 24 h, 5ЁС103Иі/Пз; t = 48 h, 3ЁС103Иі/Пз). Хрбј 24 h Кѓ, МгШыПеАзНКЪј, ХЈЖШЗжБ№ЮЊ 150, 100 КЭ 50 µg/mL, УПИіХЈЖШЩшжУ 3 ИіЦНаабљ, ВЂЩшжУЖдеезщ. 3T3 ЯИАћдкХрбјЛљжаЗжБ№Хрбј 12ЁЂ24 КЭ 48 hКѓ, гУ PBS ЛКГхШмвК(pH 7.4)ГхЯДКѓВЂИќЛЛаТЯЪЕФХрбјЛљ, МгШы CCK-8, МЬајХрбј 2 h, дкУИБъвЧВтЖЈ 490 nm ДІЕФЮќЙтжЕ, МЦЫуЯИАћДцЛюТЪ.
2.8 ЬхЭтЯИАћЩуШЁдивЉНКЪј
ШЁ HepG2 ЯИАћ, МгХрбјвКЯЁЪЭ, АД 1 ЁС 104 Иі/ПзЕФЯИАћУмЖШНгжжгкВЃСЇХрбјУѓжа, Д§ЯИАћЬљБкЩњГЄКѓ, МгШыдивЉНКЪј, АЂУЙЫиЕФХЈЖШЮЊ 10 µg/mL. ЯИАћХрбј2 hКѓ, гУМЄЙтЙВОлНЙЯдЮЂОЕ(CLSM)ЙлВьЬхЭтЯИАћЩуШЁдивЉНКЪјЕФЧщПі. МЄЗЂЙтВЈГЄЮЊ 485 nm, ЩЂЩфЙтВЈГЄЮЊ 595 nm.
2.9 ЬхЭтПЙжзСіаЇЙћ
ШЁ HepG2 ЯИАћ, АДШЁЕуВтЖЈЪБМфдкУППзМгХрбјвКЯЁЪЭ t = 12 h, 1 ЁС 104 Иі/Пз; t = 24 h, 5 ЁС 103 Иі/Пз; t = 48 h, 3 ЁС 103 Иі/Пз. МгШыдивЉНКЪј, ПижЦАЂУЙЫиЕФжеХЈЖШЗжБ№ЮЊ 15, 10 КЭ 5 µg/mL. ЗжБ№Хрбј 12ЁЂ24 КЭ48 h Кѓ, гУ PBS ЛКГхШмвКЧхЯД 3 ДЮ, жУЛЛШыаТЯЪЕФХрбјвК, МгШы CCK-8 ВЂЧсЮЂе№ЕД, МЬајХрбј 2 h, дкУИБъвЧ 490 nm ВтЖЈЮќЙтЖШ, МЦЫуЯИАћДцЛюТЪ.
3 НсЙћгыЬжТл
СНЧзадВЛЖдГЦЭиЦЫНсЙЙЕФыФРрЪїжІзДЧЖЖЮОлКЯЮя, ЭЈЙ§вдШ§ДњЙШАБЫсЩШаЮЗжзг G3(Glu)-NH2 ЮЊДѓЗжзгв§ЗЂ NCA-Phe ЕФПЊЛЗОлКЯКЯГЩ, ШчЭМ 1 ЫљЪО. РћгУДПЛЏЙ§ЕФ G3(Glu)-NH2 дкбЯИёЮоЫЎЕФЬѕМўЯТв§ЗЂNCA ЕФПЊЛЗОлКЯ. РћгУ 1H NMR ЖдКЯГЩЙ§ГЬжаЕФживЊВњЮяНјааНсЙЙБэеї.
ЭМ 2(a)ЮЊЕЅЬх NCA-Phe(CDCl3 ЮЊШмМС)1H NMR ЭМЦз, ИљОнВњЮяЕФЬиеїЗхЙщЪєМАЛ§ЗжУцЛ§жЄУїСЫNCA-Phe ЕФКЯГЩ, ЛЏбЇЮЛвЦдк 0.5 КЭ 2.0 жЎМфЕФЮЂШѕЮќЪеЗхЮЊЮДГ§ОЁЕФЫФЧтпЛрЋШмМСаХКХЗх. ЭЈЙ§ FT-IRБэеї, NCA-Phe дк 1856 КЭ 1776 cm−1 ДІГіЯжСЫЫсєћНсЙЙЕФЬиеїЮќЪе, НјвЛВНжЄУїСЫ NCA-Phe ЕФКЯГЩ. ШчЭМ 2(b)ЫљЪОЮЊ G3-Glu(d6-DMSO), дк ІФ 1.75~2.75 ppmжЎМфГіЯжСЫ G3-Glu ЕФЙЧМмЮќЪе; ІФ 5.1 ppm ЙщЪєЮЊOBzl БЃЛЄжа−CH2-O−ЧтЕФёюКЯСбЗж; ІФ 7.2~7.4 ppm жЎМфЮЊ OBzl БЃЛЄжаБНЛЗЩЯЧтЕФаХКХ; ЛЏбЇЮЛвЦ 8 ppmГіЯжСЫ−NH−ЕФЮќЪе. РћгУДѓЗжзгв§ЗЂМСЕФАБЛљв§ЗЂNCA-Phe ЕФПЊЛЗОлКЯ, ЭбШЅ OBzl БЃЛЄКѓ, дк CD3ODжаЕФЧтЦзШчЭМ 2(c)ЫљЪО. КьЭтЙтЦзНсЙћЯдЪО, дкЧзЫЎЦЌЖЮЕФЩШаЮЙШАБЫсЭбШЅмаѕЅБЃЛЄжЎКѓ, гЮРыЬЌєШЛљжаЕФ−OH ЩьЫѕЗх 3550~3500 cmЈC1 ЕФЮќЪеУїЯддіЧП. ЭЌЪБ, ЪБМфЗЩаажЪЦзНсЙћЯдЪОдк m/z 2409.23 ДІЕФаХКХзюЧП, етгыЩшМЦКЯГЩЧЖЖЮЗжзгСПЯрЗћ; ДЫЗжзгСПВтЖЈбЁгУ DHB ЮЊЛљжЪ.
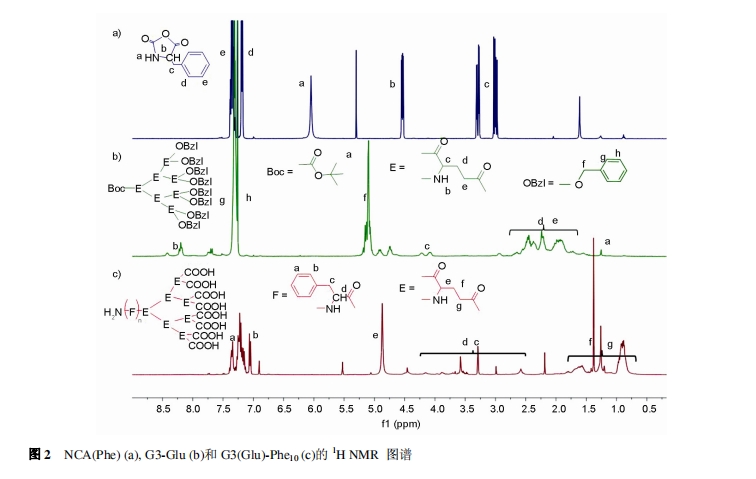
ЩШаЮ G3(Glu)ЦЌЖЮЭтЮЇгЕгаДѓСПЕФєШЛљ, ГЪЯжГіНЯЧПЕФЧзЫЎад; ЖјОлБНБћАБЫсЦЌЖЮдђГЪЯжГіЪшЫЎадФм. НЋСНЧзЕФОлКЯЮяШмгкСМШмМС, ВЂж№ЕЮМгШыЕНШЅРызгЫЎжа, ЭЈЙ§ЧзЪшЫЎзїгУаЮГЩздзщзАЬх, ЪшЫЎЦЌЖЮЕФОлБНБћАБЫсЧвДцдкІа-ІаЖбЕўЕФЙВщюзїгУ[22], ШчЭМ 3 ЫљЪО. ЪшЫЎадЕФАЂУЙЫиЭЈЙ§ЧзЪшЫЎзїгУПЩвддиШыздзщзАНКЪјЕФФкКЫ.
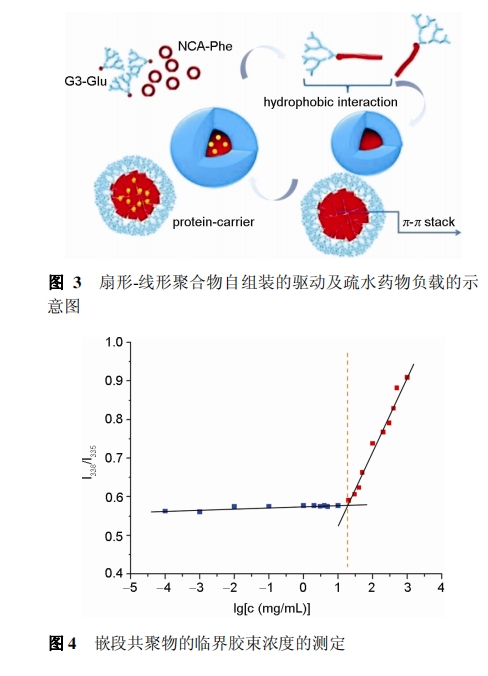
вдмХЮЊгЋЙтЗжзгЬНеы, баОПЧЖЖЮЙВОлЮяздзщзАНКЪјЕФСйНчНКЪјХЈЖШ. мХЫљДІЛЗОГЕФМЋадИФБфЪБ, гЋЙтЬиеїЗЂЩфЦзЕФЮЛвЦЗЂЩњБфЛЏ. здзщзАНКЪјжа, мХЗжЩЂдкКЫФк, ЛЗОГМЋадЗЂЩњБфЛЏЪБ, гЋЙтЮќЪеЗхДг 335 nm КьвЦЕН 338 nm. ЕБЧЖЖЮЙВОлЮяХЈЖШЕЭгкСйНчНКЪјХЈЖШЪБ, I338/I335 жЕЛљБОБЃГжВЛБф; ЕБХЈЖШДяЕНСйНчНКЪјХЈЖШЪБ, I338/I335 жЕЫцОлКЯЮяХЈЖШдіМгЖјГЪЯжЭЛБфЕФЧїЪЦ. ЭЈЙ§ЯпадФтКЯ, МЦЫуЕУЕНЕФСйНчНКЪјХЈЖШЮЊ19.50 ІЬg/mL(ЭМ 4).
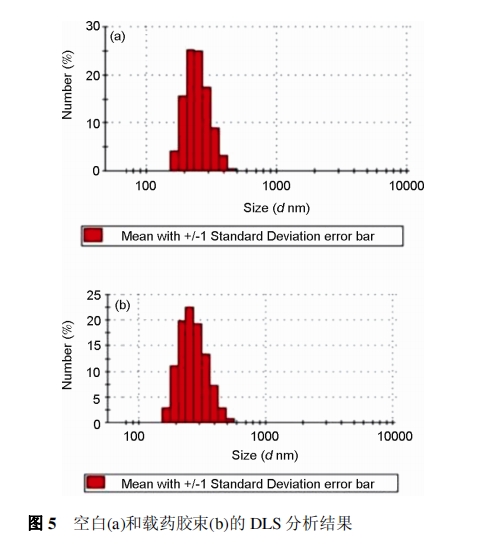
ЖЏЬЌЙтЩЂЩфЗжЮі(DLS)баОППеАзНКЪјМАдивЉНКЪјЕФСЃОЖЗжВМ. 50 ІЬg/mL ПеАзНКЪјдкЫЎШмвКжаСЃОЖЗжВМЧщПіШчЭМ 5(a)ЫљЪО, НсЙћЯдЪОздзщзАНКЪјдкЫЎжаОпгаНЯКУЕФЕЅЗжЩЂад, PDI жЕЮЊ 0.320. дивЉКѓЕФНКЪјСЃОЖЮДГіЯжУїЯддіДѓ(ЭМ 5(b)), PDI жЕЮЊ 0.394. НКЪјдивЉЧАКѓСЃОЖЮДГЪЯжГіДѓЕФБфЛЏдвђЮЊ: ЪшЫЎЕФАЂУЙЫидіШнгкздзщзАЬхЕФЪшЫЎКЫФкВП, ЕЋЭЌЪБвВЪЙЫЎШмвКЖдНКЪјећЬхЧзЪшЫЎзїгУСІдіЧП, бЙЫѕаЇгІдіДѓ; ЭЌЪБАЂУЙЫиЁЂОлБНБћАБЫсжЎМфДцдкЯрЛЅзїгУ, гаРћгкЬхЛ§бЙЫѕ[23].
здзщзАНКЪјЕФаЮУВРћгУЭИЩфЕчОЕКЭЩЈУшЕчОЕЙлВь. ЭЈЙ§ TEM ЙлВьПеАзКЭдивЉНКЪј, ЗЂЯжНКЪјдивЉЧАКѓНсЙЙгаНЯУїЯдЕФВювь(ЭМ 6). ПеАзНКЪјЮЊЧђаЮ(ЭМ6(a)), аЮзДЙцдђЁЂЗжЩЂадСМКУ; ИКдиАЂУЙЫиКѓ(ЭМ 6(b)), НКЪјГіЯжУїЯдЕФКЫ-ПЧНсЙЙ, етПЩФмЪЧвђЮЊАЂУЙЫиОпгаКмЧПЕФЪшЫЎадКЭЙВщюНсЙЙ, ВЂЧвДцдкгкНКЪјЕФЪшЫЎКЫжа, гАЯьСЫНКЪјФкКЫЕФЮяРэЛЏбЇаджЪМАПеМфНсЙЙ, ЕМжТУїЯдЕФКЫ-ПЧБпНч[22, 23]. SEM жа(ЭМ 6(c)), ЧЖЖЮЙВОлЮядк 100 ІЬg/mL ЕФХЈЖШЯТздзщзАаЮГЩЕФПеАзНКЪјСЃОЖДѓдМдк 80~100 nm жЎМф, ЗжЩЂСМКУ.
ХЈЖШЮЊ 100 ІЬg/mL ЪїжІзДДѓЗжзгЧЖЖЮЙВОлЮяНКЪјжаЪшЫЎАЂУЙЫиЕФзюДѓдивЉСПдМЮЊ 15%. дивЉНКЪјЕФЬхЭтвЉЮяЪЭЗХдк PBS жаНјаа, вдЪшЫЎадвЉЮяАЂУЙЫиКЭЧзЫЎадвЉЮябЮЫсАЂУЙЫиЮЊЖдеебљ(ЭМ 7). дивЉНКЪјдк 12 h ЪБвЉЮяЕФРлЛ§ЪЭЗХСПдМЮЊ 30%, ЕБЪЭЗХЪБМфЮЊ 60 h ЪБ, вЉЮяЕФРлЛ§ЪЭЗХСПДяЕН 80%. гыбЮЫсАЂУЙЫиЯрБШ, НКЪјЖдвЉЮяОпгаУїЯдЕФЛКЪЭзїгУ. здгЩЕФЪшЫЎАЂУЙЫидкЭИЮідкжагаЛКТ§ЮіГіЕФЯжЯѓ, ВЛвзШмгк PBS ЛКГхШмвК, дкЪЭЗХПМВьЕФЪБМфЗЖЮЇФкЛљБОВЛЪЭЗХ. баОПНсЙћБэУїдивЉНКЪјОпгаЛКЪЭаЇЙћ.

НКЪјЯИАћЖОадЕФНсЙћШчЭМ 8 ЫљЪО. ЭЈЙ§ 3 ИіХЈЖШЬнЖШ(50, 100 КЭ 150 ІЬg/mL)МА 3 ИіЪБМфЕу(12ЁЂ24 КЭ48 h)ЕФМьВтЦРМлЗЂЯж, аЁЪѓ 3T3 ГЩЯЫЮЌЯИАћЕФДцЛюТЪОљЮДГіЯжУїЯдНЕЕЭ, ЫЕУїНКЪјЖд3T3ЯИАћУЛгаУїЯдЕФЯИАћЖОад, ОпгаКмКУЕФЩњЮяЯрШнад.
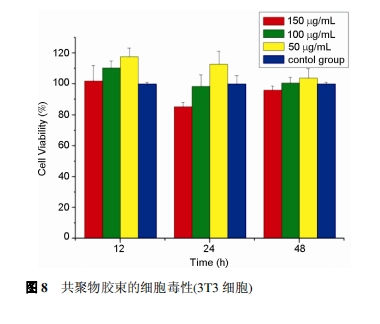
АЂУЙЫижЛгаНјШыжзСіЯИАћЕФЯИАћКЫВХФмЗЂЛгвЉаЇ. ЮЊСЫбаОПдивЉНКЪјЪЧЗёОпгаПЙжзСіаЇЙћКЭЯИАћФкЛКЪЭзїгУ, ЭЈЙ§МЄЙтЩЈУшЙВОлНЙЯдЮЂОЕ(CLSM)ЙлВьСЫИЮАЉЯИАћ HepG2 ЖддивЉНКЪјЕФЭЬЪЩ.
МЄЙтЙВОлНЙНсЙћШчЭМ 9 ЫљЪО. ЭМ 9(a)КЭЭМ 9(b)ЮЊбЮЫсАЂУЙЫиКЭАЂУЙЫигыЯИАћЙВХрбј 2 h, АЂУЙЫидкЯИАћФкЕФЗжВМНсЙћ. ЭМ 9(c)ЮЊдиАЂУЙЫиНКЪјдкЯИАћФкЗжВММАЪЭЗХаЇЙћ, дкЭМ 9(c2)жаПЩвдПДГідигаАЂУЙЫиЕФНКЪјФЩУзПХСЃОлМЏдкЯИАћКЫжмЮЇВЂЯђЯИАћКЫФкЪЭЗХАЂУЙЫи, ЯИАћКЫФкГіЯжНЯЧПЕФКьЩЋгЋЙт. ЖјдкЭМ 9(a2)жа, бЮЫсАЂУЙЫиДѓСПНјШыЯИАћКЫ, ЯдЪОГіЧПЕФКьЩЋгЋЙт. ЭМ 9(b2)ЯдЪО, АЂУЙЫигЩгкЦфЫЎШмадВю, ВЛШнвзНјШыЯИАћ, Ыљвд 2 h КѓЯИАћФкВПЛљБОУЛгаАЂУЙЫи. дигаАЂУЙЫиЕФНКЪјЭЈЙ§ЯИАћФкЭЬЕФаЮЪННјШыЕНЯИАћЪЭЗХГіИКдиЕФвЉЮя, ВЛНіЦ№ЕНСЫЖдАЂУЙЫиЕФдіШнзїгУ, ЭЌЪБОпгаЛКЪЭаЇЙћ.
дкВЛЭЌ HepG2 ЯИАћУмЖШЕФШмвКжа, МгШыдивЉНКЪј, АЂУЙЫиХЈЖШЗжБ№ЮЊ 15, 10 КЭ 5 µg/mL. ЗжБ№Хрбј12ЁЂ24 КЭ 48 h Кѓ, ЦРМлдивЉНКЪјЕФЬхЭтПЙжзСіаЇЙћ(ЭМ 10). НсЙћЯдЪО, дивЉНКЪјОпгаНЯКУЕФЬхЭтПЙжзСіаЇЙћ. ЙВХрбј 48 h Кѓ, жзСіЯИАћЕФЛюадНіЮЊ 40%. ВЛЭЌвЉЮяХЈЖШЯТ, дивЉНКЪјгыжзСіЯИАћЙВХрбј 48 hЗЂЯж(ЭМ 11), ЕБвЉЮяХЈЖШЮЊ 15 µg/mL ЪБ, дивЉНКЪјЯдЪОГіНЯИпЕФПЙжзСіаЇЙћ, жзСіЯИАћЕФЩБУ№ТЪИпгк75%.
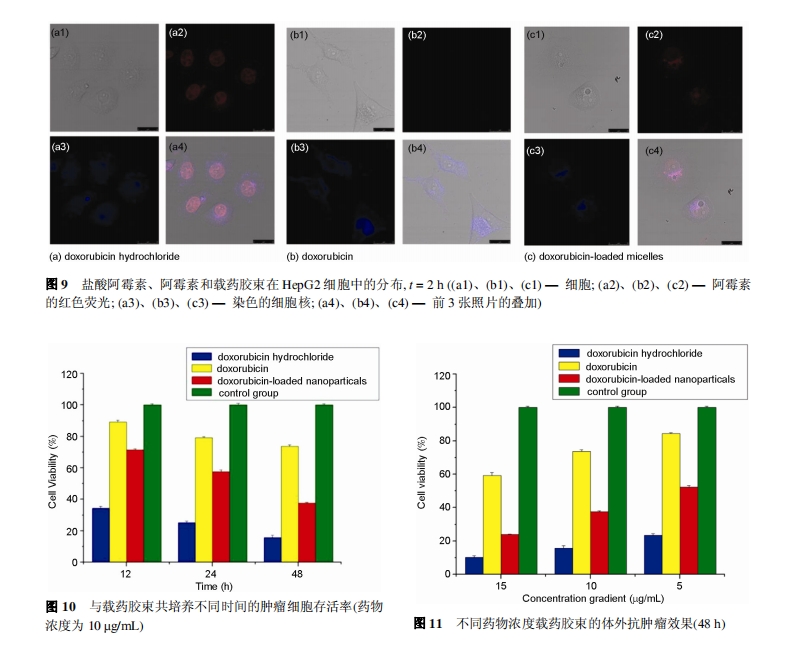
ЭМ 12 ЮЊ HepG2 жзСіЯИАћдкгыбЮЫсАЂУЙЫи(a)ЁЂАЂУЙЫи(b)ЁЂдивЉНКЪј(c)МАПеАзЖдеезщ(d)ЙВХрбј 48h ЪБЕФЙтОЕееЦЌ. ЭМ 12(a)ЯдЪОбЮЫсАЂУЙЫиЕМжТДѓСПЕФжзСіЯИАћЫРЭі, аќИЁдкХрбјЛљжа, ХрбјЛљЕзВПЛљБОУЛгаИНзХЩњГЄЕФжзСіЯИАћ; ЭМ 12(b)жагаЩйСПЫРЭіЕФжзСіЯИАћаќИЁгкХрбјЛљжа, ЕЋЕзВПЛЙгаДѓСПЕФЯИАћЬљБкЩњГЄ, ГЪЯжСМКУЕФЯИАћаЮЬЌ; ЭМ 12(c)жаЯдЪОСЫдигаАЂУЙЫиНКЪјЕФПЙжзСіаЇЙћУїЯдКУгкАЂУЙЫи,гаДѓСПаќИЁЕФЫРЭіжзСіЯИАћКЭЩйСПЬљБкЩњГЄЕФжзСіЯИАћ.
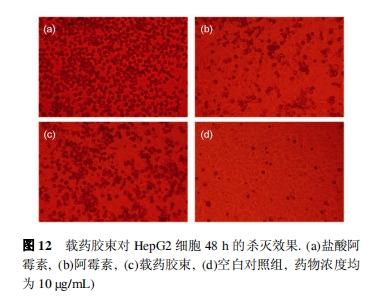
вдОлЙШАБЫсЪїжІзДДѓЗжзг-ОлБНБћАБЫсЧЖЖЮЙВОлЮяЮЊздзщзАЕЅдЊЙЙНЈЕФНКЪј, ОпгаСМКУЕФЩњЮяЯрШнад. гыЕфаЭЕФЯпаЮИпЗжзгздзщзАдивЉНКЪјЯрБШ, гЩВЛЖдГЦЭиЦЫНсЙЙЕФЧЖЖЮОлКЯаЮГЩздзщзАНКЪј, Г§СЫЧзЪшЫЎзїгУЭт, ЭЌЪБЛЙаЭЌСЫЙВщюзїгУЁЂПеМфаЇгІЕШзїгУ, ЯдЪОГіСМКУЕФЮШЖЈадЁЂЛКЪЭМАЬхЭтПЙжзСіаЇЙћ. здзщзАНКЪјЭтЮЇДѓСПЕФЛЏбЇЛюадЙйФмвВЮЊНјвЛВНЙІФмЛЏаоЪЮЬсЙЉСЫПЩФмад.
4 НсТл
БОЮФЭЈЙ§ДѓЗжзгв§ЗЂМСКЯГЩСЫОлЙШАБЫсЪїжІзДДѓЗжзг-ОлБНБћАБЫсЧЖЖЮЙВОлЮя, ЙВОлЮяздзщзАГЩЮЊИпЗжзгНКЪј. ЙВОлЮяНКЪјОпгаСМКУЕФЩњЮяЯрШнад. дивЉНКЪјОпгавЉЮяЛКЪЭаЇЙћ, вЉЮяГжајЪЭЗХЪБМфПЩДя60 h. дивЉНКЪјЕФЬхЭтПЙжзСіЪЕбщБэУїЦфЖдИЮАЉЯИАћHepG2 ОпгаКмКУЕФЩБУ№аЇЙћ, ЙВХрбј 48 h КѓЖдАЉЯИАћЕФЩБЫРТЪПЩИпДя 75%. ЭЈЙ§ЖдетРрыФРрЪїжІзДДѓЗжзгНКЪјЕФЙІФмЛЏ, ПЩЭћИГгшЦфжЧФмЁЂАаЯђЕШЙІФм, зїЮЊаТаЭЕФвЉЮяЪЭЗХдиЬх.
Утд№ЩљУїЃКБОЮФЮЊаавЕНЛСїбЇЯАЃЌАцШЈЙщдзїепМАддгжОЫљгаЃЌШчгаЧжШЈЃЌПЩСЊЯЕЩОГ§ЁЃЮФеТБъзЂгазїепМАЮФеТГіДІЃЌШчашдФЖСдЮФМАВЮПМЮФЯзЃЌПЩдФЖСддгжО










