ыФЁЂЕААзжЪКЭКЫЫсЕШЩњЮяЗжзгЭЈГЃФбвдЭЈЙ§БЛЖЏРЉЩЂДЉЙ§ЯИАћФЄЁЃШЛЖјЃЌЯИАћДЉЭИыФ(CPPs)ЁЂЯИОњЕААзЖОЫиЁЂФГаЉецКЫЕААзЁЂВЁЖОвдМАаэЖрКЯГЩвЉЮяЕнЫЭдиЬхФмЙЛвдВЛЭЌЕФаЇТЪНјШыецКЫЯИАћЃЌЫќУЧЭЈГЃВЩгУвЛжжЛђЖржжЛњжЦНјШыЯИАћВЂГѕВНЖЈЮЛгкФкЬхжаЁЃЕЋЪЧЫќУЧШчКЮДЉЙ§ФкЬхФЄНјШыЯИАћНЌ(ФкЬхЬгвн)ШДвРШЛУЛгаЧхЮњЕФбаОПНсЙћЃЌетвВвЛжБЪЧИпаЇвЉЮяЕнЫЭЯЕЭГПЊЗЂЕФжївЊЦПОБЫљдкЁЃДЫЭтЃЌаэЖрЯИОњКЭецКЫЕААзЗжБ№ЭЈЙ§ЫЋОЋАБЫсзЊдЫ(TAT)КЭЗЧГЃЙцЕААзЗжУк(UPS)ЯЕЭГдкЦфздШЛзДЬЌЯТДЉЙ§жЪФЄНјШыжмжЪ/АћЭтПеМфЁЃЭЌбљЃЌетаЉЕААзжЪЪфГіЯЕЭГЕФдЫзїЛњжЦЩаВЛЧхГўЁЃ
2022Фъ1дТЃЌУРЙњЖэКЅЖэжнСЂДѓбЇХсЕТЛЊНЬЪкдкAccounts of Chemical ResearchЩЯЗЂБэЮФеТЃЌНщЩмСЫвЛжжжЎЧАЩаЮДЬсГіЕФЁЂЛљБОЕФПчФЄзЊдЫЛњжЦЁЊЁЊФвХнУШГіКЭЦЦСбЛњжЦ(Vesicle Budding-and-Collapse,VBC)ЃЌВЂЭЈЙ§ЪЕбщбщжЄСЫЯрЙиНсТлЁЃVBCПЩФмЪЧЯИОњTATКЭецКЫUPSЯЕЭГЕФЧ§ЖЏЛњжЦЃЌНЋРДПЩФмЮЊИпаЇЕФвЉЮяЕнЫЭЯЕЭГЕФЩшМЦЬсЙЉддђаджИЕМЁЃ
ЯИАћФЄЪЧвЛжжИпаЇЕФЩњЮяЦСеЯЃЌФмЙЛНЋЯИАћФкЮяжЪАќКЌЦфжаЃЌЭЌЪБАбЭтРДЮяжЪзшЕВдкЭтЁЃЗжзгСПаЁгк500ЧвЪшЫЎадДяЕНКЯРэЦНКтЕФаЁЗжзгФмвдБЛЖЏРЉЩЂЕФЗНЪНДЉЙ§ЯИАћФЄЃЌЖјыФЁЂЕААзжЪКЭКЫЫсЕШЩњЮяДѓЗжзгдђЭЈГЃВЛФмЁЃШЛЖјЃЌвЛаЉЩњЮяЗжзгФмЙЛзджїНјШыВИШщЖЏЮяЯИАћЃЌШчЯИАћДЉЭИыФ(CPPs)ЁЂЗЧыФРрЯИАћДЉЭИЗжзг(CPMs)ЁЂЯИОњЕААзЖОЫиЁЂФГаЉВИШщЖЏЮяЕААзЁЂВЁЖОвдМАКЯГЩвЉЮяЕнЫЭЯЕЭГ(ЭМ1)ЃЌЫќУЧжаЕФДѓЖрЪ§ФмЙЛЭЈЙ§ФкЭЬзїгУНјШыЯИАћЃЌВЂЖЈЮЛгкФкЬхжаЁЃЮЊСЫГЩЙІНјШыАћНЌЃЌЦфжавЛаЉЪЕЬхЫцКѓашвЊзЊдЫДЉЙ§ФкЬхФЄНјШыАћНЌЃЌетвЛЙ§ГЬГЦЮЊФкЬхЬгвнЁЃ
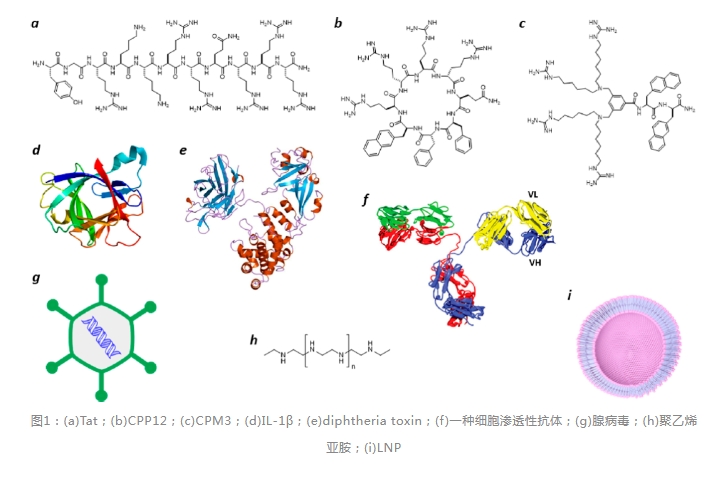
баОПБэУїЃЌЦфЫћЪЕЬхПЩжБНгПчдНЯИАћФЄЛђНјвЛВННјШыФкжЪЭјЃЌВЂФцаазЊдЫДЉЙ§ФкжЪЭјФЄНјШыАћНЌЁЃелЕўЕФЕААзжЪвВПЩвдЗДЗНЯђДЉЙ§жЪФЄЃЌДгАћНЌзЊдЫЕНжмжЪ/АћЭтПеМфЃЌетвЛЙ§ГЬБЛГЦЮЊецКЫЯИАћЕФЗЧГЃЙцЕААзЗжУкЯЕЭГ(UPS)КЭЯИОњМАЯИАћЦїЕФЫЋОЋАБЫсзЊдЫЯЕЭГ(TAT)ЁЃЫљгаетаЉЧщПіЯТЃЌЩњЮяЗжзг/ЪЕЬхБиаыДЉЙ§жЌжЪЫЋВуФЄЁЃЩњЮяЗжзгШчКЮзджїзЊдЫДЉЙ§жЌжЪЫЋВуФЄдкаэЖрСьгђвЛжБЪЧИіУеЭХЃЌЖјЖдзЊдЫЛњжЦШЯЪЖЕФШБЗІМЋДѓЕизшАЯИАћЩјЭИадЩњЮяжЦМСзїЮЊЯТвЛДњжЮСЦвЉЮяЕФЗЂеЙЁЃ
зюНќЃЌPeiЕШЗЂЯжCPPsКЭCPMsФмЙЛЭЈЙ§ШЋаТЕФVBCЛњжЦЪЕЯжФкЬхЬгвн(ЭМ2)ЁЃVBCЛњжЦЪЧвЛжжШЋаТЕФЛњжЦЃЌЩЯЪіаэЖр(ПЩФмЫљга)ЩњЮяЗжзгПЩЭЈЙ§VBCЛњжЦзджїЕиПчжЌжЪЫЋВуФЄзЊдЫЁЃ
ЭЈЙ§VBCЛњжЦЪЕЯжФкЬхЬгвн
ФПЧАЃЌПЦбЇМввбЬсГіЖржжФкЬхЬгвнЛњжЦЃЌАќРЈжЪзгКЃУраЇгІгеЕМЕФЩјЭИСбНтЁЂФЄШкКЯЁЂаЮГЩПзЖДЁЂОжВПФЄЦЦСбКЭVBCЁЃЦфжаVBCЪЧЮЈвЛОЙ§ЪЕбщбщжЄЕФЛњжЦЃЌЪЪгУгквдЩЯУшЪіЕФЫљгаЧщПіЃЌЖјЦфЫћМйЩшЭЈГЃжЛЩцМАФГжжЧщПіЃЌВЂЧвФбвдНтЪЭаэЖрЪЕбщЙлВьНсЙћЁЃ
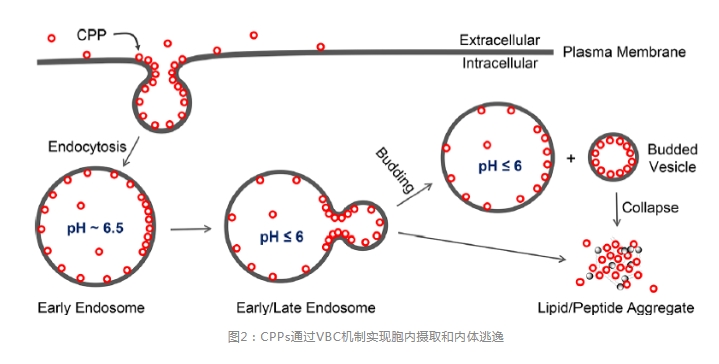
ЭМ2ЪЧЛЗзДCPPsЕФЯИАћЩуШЁКЭФкЬхЬгвнЛњжЦЁЃЛЗзДCPPsжБНггыжЪФЄСзжЌ(вдМАЧБдкЕФЦфЫћФЄГЩЗж)НсКЯЃЌЭЈЙ§ФкЭЬзїгУНјШыЯИАћаЮГЩдчЦкФкЬхЃЌЫцзХдчЦкФкЬхГЩЪьЮЊЭэЦкФкЬхЃЌЦфФкВПж№НЅЫсЛЏЃЌCPPsгыФкЬхФЄЕФЧзКЭСІдіЧПЁЃвђЮЊCPPsЕФОЋАБЫсВрСДдкФкЬхЫсЛЏЙ§ГЬжа(pH6.5-4.5)ВЛЛсНјвЛВНжЪзгЛЏЃЌвђДЫЃЌжЪзгЛЏПЩФмЗЂЩњдкСзжЌЩЯ(ШчЭЗВПСзЫсЛљЭХ)ЁЃОЋАБЫсЕФывЛљФмЙЛЭЌЪБгыСНИіЯрСкЕФСзЫсаЮГЩЫЋГнЧтМќ(ЭМ3a)ЁЃетжжЖРЬиЕФФмСІМгЩЯЖрИіОЋАБЫсВаЛљЕФДцдкЃЌCPPФмЙЛНЋСзжЌНЛСЊЕНИЛКЌCPPЕФжЌжЪгђЁЃСзЫсЕФВПЗжжЪзгЛЏНЋЭЈЙ§МѕЩйОВЕчХХГтНјвЛВНДйНјжЌжЪОлМЏЃЌжЌжЪгђЕФаЮГЩдкжЌжЪгђКЭЦфжмЮЇФЄжЎМфВњЩњЯпеХСІЃЌНјЖјЧ§ЖЏжЌжЪгђУШГіаЮГЩФвХнЁЃдкФвХнУШГіЙ§ГЬжаЃЌУШГіОБВП(Й§ЖЩЬЌ)ГЪИКИпЫЙЧњТЪ(Шчдке§НЛЗНЯђЩЯЭЌЪБОпгае§КЭИКЧњТЪ)ЃЌВЂЧвЯрЖдгкУШГіЪТМўЧАКѓЕФЛљЬЌОпгаНЯИпЕФЪЦФм(ЭМ3b)ЁЃ
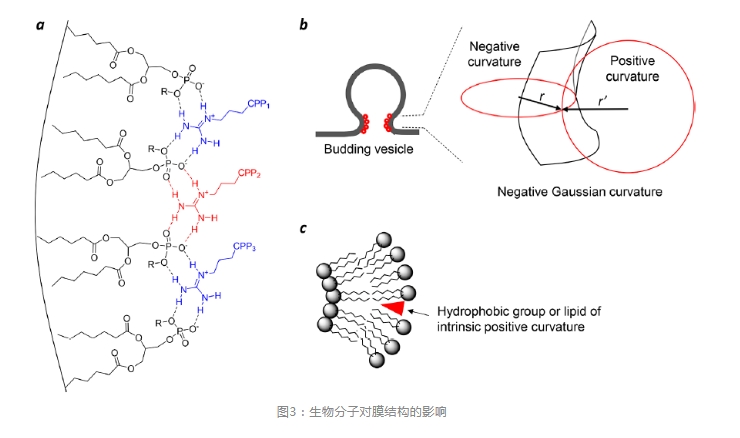
ЮЊСЫДйНјУШГіЪТМўЃЌCPPsгІИУбЁдёадНсКЯЕНУШГіОБВПВЂНЕЕЭФмРнЁЃОпгаНЯИпФкЬхЬгвнаЇТЪЕФCPPsКЭCPMsЭЈГЃГЪСНЧзадЧвЙЙЯѓЪмЯоЁЃИеадЙЙЯѓдіМгСЫCPPs/CPMsгыФкЬхФЄЕФЧзКЭСІЃЌЖјСНЧзаддђгаРћгкдкУШГіОБВПВњЩњИКИпЫЙЧњТЪЁЃдкСзжЌЗжзгжЎМфВхШыЪшЫЎЛљЭХЛсВњЩње§ФЄЧњТЪ(ЭМ3c)ЃЌЖјОЋАБЫсВаЛљПЩвдгыСзжЌЕФЭЗВПСзЫсЛљЭХЭЈЙ§ЧтМќНсКЯВЂОлМЏгеЕМВњЩњИКЧњТЪ(ЭМ3a)ЁЃФкЬхФЄУШГіЙ§ГЬЛђУШГіКѓЃЌаЁФвХнздЗЂЕибИЫйНтЬхГЩыФ/жЌжЪОлКЯЬхЃЌВЂж№НЅШмНтЕНЯИАћвКжаЁЃОЁЙмаЁФвХн(жБОЖдМЮЊ100nm)ПЩФмгЩгкИпЕФФЄЧњТЪКЭ/ЛђИпХЈЖШЕФCPPsЕФДцдкЖјБОжЪЩЯВЛЮШЖЈЃЌЕЋФвХнЦЦСбЕФЧ§ЖЏСІЩаВЛЧхГўЁЃVBCЛњжЦЕФЖРЬижЎДІдкгкЃЌЩњЮяЗжзгдкЭиЦЫбЇвтвхЩЯПчдНФЄЃЌЖјЗЧЮяРэЩЯДЉЙ§ФЄЃЌВЂЧвУПДЮФкЬхЬгвнЪТМўжЎЧАЁЂЦкМфКЭжЎКѓЃЌФкЬхЖМБЃГжЭъећЁЃЯрЗДЃЌЫљгаЦфЫћФЄзЊдЫЛњжЦЖМЩцМАЪЕЬхЮяРэЩЯДЉЙ§ЯИАћФЄЃЌвђДЫашвЊВПЗжЛђШЋВПЦЦЛЕЯИАћФЄЁЃЖдгкВЛЭЌЕФЩњЮяЗжзгЃЌНјШыЯИАћЕФОпЬхЯИНкПЩФмгаЫљВЛЭЌЁЃ
VBCЛњжЦжаЃЌФкЬхЬгвнашвЊФкЬхжаОпгавЛИізюаЁЪ§СПЕФЩњЮяЗжзгЃЌЧвФкЬхЬгвнаЇТЪОпгаХЈЖШвРРЕадЁЃзюНќбаОПЗЂЯжЃЌвЛжжУћЮЊTatЕФЯпадCPPдкХЈЖШЮЊ0.2ЁЂ10ЁЂ20ІЬMХЈЖШЪБЕФЕФФкЬхЬгвнаЇТЪЗжБ№ЮЊ0.08%ЁЂ0.38%ЁЂ0.66%ЁЃетвЛЗЂЯжНтЪЭСЫЮЊЪВУДCPPsЕФАћФкЩуШЁаЇТЪЖдCPPХЈЖШИпЖШУєИаЃЌЧвЫцзХCPPХЈЖШЕФдіМгЖјГЪЗЧЯпаддіМгЃЌвђЮЊЃЌАћФкЩуШЁвВОпгаCPPХЈЖШвРРЕадЁЃPeiШЯЮЊгеЕМвЛДЮVBCЕФзюаЁЩњЮяЗжзгЪ§СПЮЊУПИіФкЬх80-360ИіЗжзгЃЌЯргІЕФФкЬхФкХЈЖШЪЧ2-9ІЬM(МйЩшФкЬхЦНОљжБОЖЮЊ0.5ІЬM)ЃЌЕЋЪЧетИіЪ§зжПЩФмЛсвђЮЊЩњЮяЗжзгЕФаджЪЖјТдЮЂгаЫљВЛЭЌЁЃ
ЯИАћДЉЭИыФ(CPPsЃЉ
ЭЈГЃШЯЮЊЃЌЕЭХЈЖШЪБЃЌCPPsжївЊЭЈЙ§вЛжжЛђЖржжФмСПвРРЕадЕФФкЭЬзїгУНјШыЯИАћЃЌЫцКѓЗЂЩњФкЬхЬгвнЃЌЖјИпХЈЖШЪБЃЌвЛаЉCPPsвВФмвдЗЧФмСПвРРЕадЕФЗНЪНжБНгзЊдЫЭЈЙ§ЯИАћФЄЁЃVBCЕФдчЦкЯпЫїРДздзїепЖдЛЗзДCPP12КЭФЃФтФкЬхФЄГЩЗжЕФДѓЕЅВуФвХн(GUVs)ЕФЬхЭтбаОПЃЌШОСЯБъМЧЕФCPP12ФмНсКЯЕНGUVsЕФЭтВрЧвзюГѕОљдШЗжВМдкGUVФЄЩЯЁЃЫцзХЪБМфЭЦвЦЃЌCPP12ЗжзгОлМЏГЩЧПСвЕФгЋЙтЧјгђЃЌДѓИХЪЧжЌжЪгђЃЌЫцКѓетаЉЧјгђвдаЁХнЕФаЮЪНУШГі(ЛђепЩйВПЗжНјШыGUVЧЛФк)(ЭМ4a)ЁЃдкУШГіжЎЧАЃЌCPP12МЏжадкУШГіОБВП(ЭМ4b)ЃЌШЛКѓЃЌУШГіЕФаЁХнЭпНтГЩаЮзДВЛЙцдђЁЂгЋЙтЧПСвЕФОлМЏЬхЃЌетвЛЙ§ГЬвЊУДгыУШГіЙ§ГЬЭЌЪБЗЂЩњЃЌвЊУДдкУШГіЭъГЩКѓВЛОУЗЂЩњЁЃ
ЮЊСЫЙлВьЛюЯИАћжаЕФVBCЪТМўЃЌзїепгУвЛжжpHУєИаЕФШОСЯ(pHAb)БъМЧCPP12ЃЌетжжШОСЯдкФкЬх/ШмУИЬхЕФЫсадЛЗОГжаЗЂГігЋЙтЃЌЖјдкжаадАћНЌЛђЯИАћЭтПеМфжаВЛЗЂГігЋЙтЁЃгУCPP12pHAb(КьЩЋ)КЭФЄБъМЧЮя(TopFluorБъМЧЕФСзжЌѕЃЫПАБЫс(PSTopFluor))ДІРэHeLaЯИАћЃЌВЂгУЛюЯИАћЙВОлНЙЯдЮЂОЕЪЕЪБГЩЯёЁЃФкЬхЬгвнЪМгкФкЬхФЄЩЯЕФвЛИіаЁФвХнЕФУШЗЂЃЛетИіНзЖЮЃЌУШГіЕФФвХнКЭЪЃгрЕФФкЬхОљЗЂГіКьЩЋ(CPP12pHAb)КЭТЬЩЋгЋЙт(PSTopFluor)(ЭМ4c)ЁЃКьЩЋгЋЙт(CPP12pHAb)ЕФЭЛШЛЯћЪЇКЭТЬЩЋгЋЙт(PSTopFluor)ЕФБЃСєжЄУїСЫЫцКѓаЁФвХнЕФЭпНт(ВаЬхБЉТЖгкАћНЌpH)ЃЌЖјЭъећЕФФкЬхБЃСєСЫКьЩЋКЭТЬЩЋгЋЙтЁЃУПДЮФкЬхЬгвнЪТМўЗЂЩњЗЧГЃбИЫйЃЌЭЈГЃГжајЪБМф<60УыЁЃ
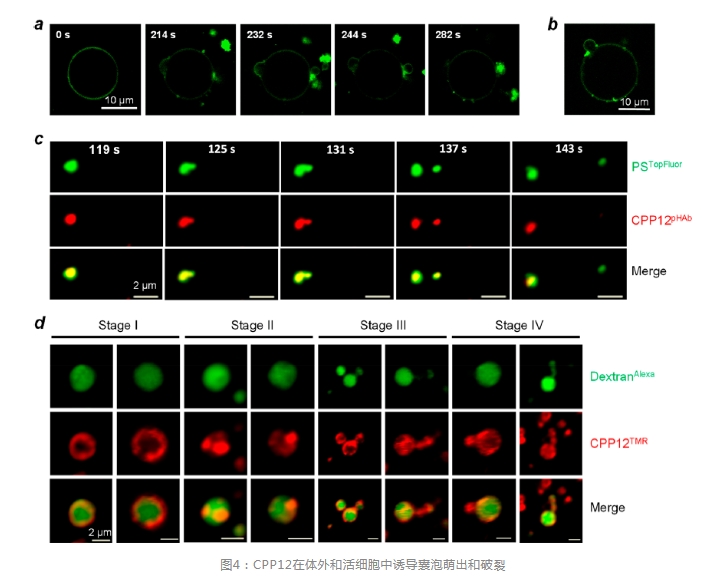
НгЯТРДЃЌзїепгУМЄУИвжжЦМСYM201636дЄДІРэHeLaЯИАћЃЌвдРЉДѓФкЬх(ЦНОљжБОЖДг0.5ІЬmдіМгЕН∼2ІЬm)ЃЌШЛКѓЬэМгЫФМзЛљТоЕЄУї(TMR)БъМЧЕФCPP12(CPP12TMR)КЭФкЬхБъМЧЮя(AlexaFluor488БъМЧЕФЦЯОлЬЧ(DextranAlexa))ЃЌвдЭЈЙ§бгЪБЛюЯИАћЙВОлНЙЯдЮЂОЕЙлВьФкЬхдкОРњVBCЙ§ГЬжаЕФНсЙЙБфЛЏ(ЭМ4d)ЁЃУїЯдЃЌЛюЯИАћжаВЖЛёЕФVBCжаМфЬхгыдчЦкGUVбаОПжаЙлВьЕНЕФЗЧГЃЯрЫЦ(ЭМ4a,b)ЁЃДЫЭтЃЌЭЌВНЗјЩфаЁНЧXЩфЯпЩЂЩфбаОПБэУїЃЌЛЗзДCPPдкШЫЙЄФЄЩЯВњЩњИКИпЫЙЧњТЪЪЧЗЧГЃИпаЇЕФЁЃЮЊСЫЦРЙРVBCЛњжЦЕФЦеБщадЃЌзїепМрВтСЫTat(ЕфаЭЕФЯпадCPPЃЌОпгаЕЭФкЬхЬгвнаЇТЪЃЌЁм0.66%)КЭCPM3(МИКѕФмЖЈСПФкЬхЬгвн)дкHeLaЯИАћжаЕФЬгвнЧщПіЁЃCPM3ДгФкЬхжагеЕМГіЧПСвЕФVBCЪТМўЃЌВЂВњЩњРрЫЦгкCPP12ЕФVBCжаМфЬхЃЌЖјTatНщЕМЕФVBCЪТМўЗЂЩњЕФЦЕТЪвЊЕЭЕУЖр(вВКмФбЙлВьЕН)ЁЃетаЉНсЙћБэУїЃЌФкЬхЬгвнаЇТЪжївЊШЁОігкЩњЮяЗжзгдкФкЬхФЄгеЕМVBCЕФаЇТЪ(ЦЕТЪ)ЁЃ
вЛЯюCPPЮФЯзЕїбаБэУїЃЌЦфЫћCPPsвВФмдкФкЬхКЭ/ЛђЯИАћФЄЩЯгеЕМVBCЁЃР§ШчЃЌдкYM201636ДІРэЕФSaos-2ЯИАћжаЃЌвЛжжЯИАћЩјЭИадЕФЮЂаЭЕААзZF5.3ЪЙФкЬх(КЭШмУИЬх)аЮГЩгыCPP12КЭCPM3геЕМЕФVBCжаМфЬхЗЧГЃЯрЫЦЕФФЄНсЙЙЁЃЩјЭИЫиЁЂОХОлОЋАБЫс(R9)ЕШЯпадИЛКЌОЋАБЫсЕФCPPsКЭRW9ФмЙЛЭЈЙ§геЕМФЄФкЯнКЭаЮГЩЮоЖЈаЮЕФыФ/жЌОлМЏЬхЖјзджїНјШыШЫЙЄФвХн(ШчGUVКЭжЪФЄЧђ(PMSs))ЁЃЭЌВНЗјЩфаЁНЧЖШXЩфЯпЩЂЩфбаОПжЄЪЕСЫЯпадCPPsвВФмдкШЫЙЄФЄЩЯВњЩњИКИпЫЙЧњТЪЁЃ
ЯШЧАСюШЫРЇЛѓЕФНсЙћЯждкПЩвдКЯРэЛЏЃЌВЂЮЊVBCЛњжЦЬсЙЉЖюЭтЕФжЇГжЃК(1)CPPsФмЙЛдЫЫЭВЛЭЌДѓаЁ(ДгаЁЗжзгЕНДѓЕААзжЪ)КЭРэЛЏаджЪЕФЛѕЮяЃЌетаЉЛѕЮягыCPPЭЈЙ§ЙВМлСЌНгЛђЗЧЙВМлНсКЯЃЛ(2)CPPsДйНјЮоЙиСЊДѓЗжзгЛѕЮя(ШчЛЗК§ОЋКЭПЙЬх)ЕФФкЬхЪЭЗХЃЛ(3)ШкКЯаджЌжЪКЭЖрыФДйНјCPPsЕФФкЬхЪЭЗХЃЛ(4)ЬсИпСЫЛЗзДКЭЦфЫћЙЙЯѓЪмЯоЕФCPPsКЭCPMЕФАћФкЩуШЁаЇТЪЁЃШЛЖјЃЌЪЧЗёЫљгаЕФCPPs/CPMsЖМЭЈЙ§VBCЛњжЦРыПЊФкЬхЛђПчФЄзЊдЫШдгаД§ШЗЖЈЁЃ
ЯИОњЖОЫи
ЯИОњЕААзЖОЫиЕФНсЙЙКЭЦфНјШыЯИАћЕФЛњжЦОљОпгаЖрбљадЁЃвЛаЉЖОЫиПЩжБНгЭЈЙ§жЪФЄзЊдЫЕНЯИАћжЪжаЃЛСэвЛаЉЖОЫидђгыЯИАћБэУцЪмЬхНсКЯЃЌЭЈЙ§ФкЭЬзїгУКЭФкЬхЬгвнНјШыЯИАћжЪжаЃЛЛЙгавЛаЉЖОЫиБЛзЊдЫЕНФкжЪЭјЃЌШЛКѓФцаазЊдЫЕНЯИАћжЪжаЁЃШЛЖјЃЌВЛЙмВЩгУФФжжЗНЪННјШыЯИАћЃЌЖОЫидкЕНДяАћНЌжЎЧАБиаыдкЭиЦЫбЇвтвхЩЯДЉЙ§жЌжЪЫЋВуФЄЁЃАзКэЖОЫи(DT)ЕШABРрЯИОњЖОЫиЭЈГЃгЩСНИіЙІФмЕЅдЊзщГЩЃКвЛИіУИВПЗж(AЃЌЪЧЪЕМЪЕФЖОЫи)КЭвЛИіЗЧУИВПЗж(BЃЌЪЧЕнЫЭдиЬх)ЃЌЗЧУИВПЗжФмНщЕМЪмЬхНсКЯ(R-НсЙЙгђ)КЭФЄзЊдЫ(T-НсЙЙгђ)ЁЃЯИАћЩуШЁЪМгкRНсЙЙгђЪЖБ№ЫожїЯИАћЕФБэУцЪмЬхЃЌЕМжТЪмЬх−ЖОЫиИДКЯЮяЕФФкЭЬЃЛФкЬхЕФЫсЛЏЪЙЖОЫиДгЪмЬхЩЯНтРыЃЌВЂгеЕМTНсЙЙгђЕФЙЙЯѓИФБфЃЌШЛКѓTНсЙЙгђВхШыФкЬхФЄаЮГЩРызгДЋЕМПз/ЭЈЕРЁЃЭЈГЃШЯЮЊЃЌAВПЗжеЙПЊВЂДЉЙ§TНсЙЙгђаЮГЩЕФЯСеЭЈЕРЕНДяЯИАћжЪЁЃШЛЖјЃЌЖрФъРДЃЌПз/ЭЈЕРМйЫЕЪмЕНСЫаэЖрЪЕбщЙлВьНсЙћЕФЬєеНЁЃР§ШчЃЌDTПЩвдНЋГЌЮШЖЈЕФЛѕЮяЕААзвдМАЗЧЙВМлНсКЯЕФКЫЫсдЫЫЭЕНАћжЪжаЃЌБэУїDTФмЙЛзЊдЫелЕўзДЬЌЕФЛѕЮяЁЃбаОПЗЂЯжЃЌAВПЗжЭЛБфПЩвдЯћГ§DTЕФРызгЭЈЕРЛюадЃЌЕЋЖдAВПЗжЕФзЊдЫМИКѕУЛгагАЯьЃЌЖјЦфЫћЭЛБфПЩвдзшжЙзЊдЫЃЌЕЋВЛЛсгАЯьЭЈЕРЛюадЁЃDTЕФФкЬхЬгвнГЪЯжЁАСПзгЁБЖЏСІбЇЃЌМДУПИіФкЬхЬгвнЪТМўЭЌЪБЯђАћНЌжаЪЭЗХ∼80ИіDTЗжзгЃЌЧвгыЯИАћЭтDTЕФХЈЖШЮоЙиЃЌЖјЭЈЙ§ПзЕРЕФDTЪЭЗХЪЧСЌајЕФ(МДвЛДЮЪЭЗХвЛИіDTЗжзг)ЁЃ
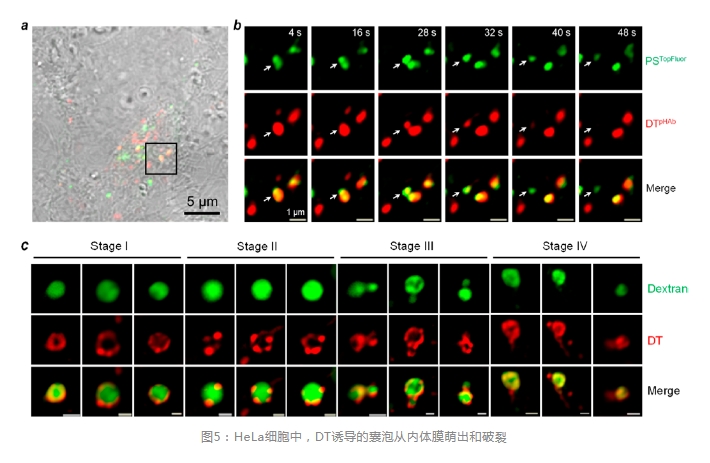
зюНќЃЌPeiЕШЗЂЯжDTЭЈЙ§VBCЛњжЦЬгРыФкЬхЁЃзїепгУpHAbЛђЫФМзЛљТоЕЄУї(TMR)БъМЧDTЃЌВЂЭЈЙ§ЛюЯИАћЙВОлНЙЯдЮЂОЕМрВтDTЕФАћФкзЊдЫЁЃDTдкHeLaЯИАћжагеЕМЧПСвЕФVBCВЂВњЩњгыCPPs/CPMsЯрЭЌЕФФкЬхФЄНсЙЙ(ЭМ5a,b,c)ЁЃР§ШчЃЌDTTMRЖЈЮЛгкФкЬхФЄЩЯЃЌзюГѕОљдШЗжВМгкФЄЩЯЃЌЫцКѓОлМЏГЩИЛКЌDTЕФжЌжЪгђЃЌетаЉжЌжЪгђЫцКѓвдаЁХнЕФаЮЪНУШГіВЂЭпНт(ЭМ5c)ЁЃгаШЄЕФЪЧЃЌвЛжжгЩГІГібЊадКЭжТВЁадДѓГІИЫОњВњЩњЕФН№ЪєЕААзУИNleCвВЭЈЙ§VBCЬгРыФкЬхЁЃгыABРрЯИОњЖОЫиВЛЭЌЃЌNleCгЩАќКЌ330ИіВаЛљЕФЕЅвЛДпЛЏНсЙЙгђзщГЩЃЌвдЦфЬьШЛНсЙЙНјШыЫожїЯИАћЁЃNleCЕФЦфНсЙЙКЌгаСНИіЖрМюЛљађСаЃЌетПЩФмЪЧЦфНјШыЯИАћЕФдвђЁЃШЛЖјЃЌЗжРыЕФУПИіЖрМюЛљађСаЖМВЛФмзїЮЊCPPЗЂЛгзїгУЃЌетгыЯИАћЩуШЁашвЊЭъећЕФ3DНсЙЙЪЧвЛжТЕФЁЃетаЉНсЙћБэУїЃЌЕААзжЪПчФкФЄзЊдЫМШВЛашвЊЫсгеЕМЕФЙЙЯѓБфЛЏЃЌвВВЛашвЊФЄВхШыЁЃвђДЫЃЌДцдквЛИіЮЪЬтЃКTНсЙЙгђЕФФЄВхШыКЭРызгДЋЕМЭЈЕРдкФкЬхЬгвнЙ§ГЬжаЗЂЛгЪВУДзїгУЃПзїепШЯЮЊЃЌTНсЙЙгђЕФФЄВхШыдіМгСЫЖОЫиЖдФкЬхФЄЕФНсКЯЧзКЭСІЃЌШЗБЃФкЬхжа80-360ИіЖОЫиЗжзгжаЕФДѓЖрЪ§гыФкЬхФЄНсКЯЃЌвдДйНјVBCЁЃетвЛЬиеїЖдгкдкМЋЕЭХЈЖШЯТ(ШчpM)ЗЂЛгЦфВЁРэЩњРэзїгУЕФЖОЫиПЩФмЪЧжСЙиживЊЕФЁЃРызгДЋЕМЭЈЕРПЩФмЪЧTНсЙЙгђВхШыЕФвЛИіЗжжЇЃЌЧвПЩФмУЛгаШЮКЮЩњЮябЇЙІФмЁЃ
ЕБЯИАћЭтЖОЫиХЈЖШдкpMЗЖЮЇЪБЃЌ80-360ИіЖОЫиЗжзгЪЧШчКЮОлМЏдкЕЅИіФкЬхжаДяЕН2-9ІЬMХЈЖШЕФФиЃПЪмЬхНщЕМЕФФкЭЬзїгУЪЙЖОЫиДгЯИАћЭтЛЗОГНјШыФкЬхДяЕНгавтвхЕФХЈЖШЃЌНјвЛВНЕФХЈЫѕПЩФмЭЈЙ§ФкЬхШкКЯРДЭъГЩЁЃвЛИіЕфаЭЕФВИШщЖЏЮяЯИАћгаЪ§АйИіФкЬхЃЌетаЉФкЬхЭЈЙ§ВЛЖЯЕФФвХнШкКЯКЭСбБфЯрЛЅСЌНгЁЃЫфШЛЕЅИіФкЬхзюГѕПЩФмВЛАќКЌгеЕМVBCЕФзюаЁЪ§СПЗжзгЃЌЕЋФкЬхЕФКсЯђШкКЯЃЌМгЩЯЖОЫиОлМЏЕНжЌжЪгђЃЌЛсж№НЅНЋЖОЫиЗжзгОлМЏГЩИќЩйЁЂИќДѓЕФФкЬхЃЌзюжеДяЕНVBCЕФЁАСПзгЁБМЖЁЃетвЛЧщПіПЩФмНтЪЭСЫжЎЧАЙлВьЕНЕФФкЬхЫсЛЏКЭDTЪЭЗХЕНЯИАћжЪжЎМфХЈЖШвРРЕадЕФЪБМфбгГй(МДдкНЯЕЭЕФDTХЈЖШЯТгаНЯГЄЕФбгГй)ЁЃетвВПЩФмНтЪЭЮЊЪВУДдкУЛгаШЮКЮЯИАћЕААзЕФЧщПіЯТ(ОЁЙмдкЯрЖдИпХЈЖШЕФ5−20ІЬM)ЃЌCPPsБОЩэОЭФмгеЕМGUVsВњЩњЧПСвЕФVBCЃЌЕЋдкФвХнНЛСЊКЭШкКЯжаЗЂЛгзїгУЕФHOPSИДКЯЬхЖдгкCPPsдкЬхФкЕФФкЬхЬгвнЪЧжСЙиживЊЕФЁЃ
ЦфЫћФЄДЉЭИЕААз
Г§СЫЯИОњЖОЫиЭтЃЌаэЖрЦфЫћЕФЯИОњКЭецКЫЕААзПЩвдЯђжЪФЄЛђФкЬхФЄЕФШЮвтЗНЯђзЊдЫЁЃР§ШчЃЌІС-synucleinЕФЯИАћМфДЋЕнгыХСН№ЩВЁЕФНјеЙгаЙиЃЌЖјPTEN-longСзЫсУИЕФЯИАћМфзЊдЫПЩвдЕїНкЪмЬхЯИАћжаЕФPI3KаХКХЁЃPeiЕШзюНќЗЂЯжЃЌНЋвЛИіЖЬЕФCPPађСа(ШчRRRRWWW)НгЕНВИШщЖЏЮяЕААзжЪ(ШчЕААзжЪРвАБЫсСзЫсУИ1BКЭрбпЪКЫмеСзЫсЛЏУИ)ЕФБэУцЛЗжаЪЙКѓепОпгаЯИАћЩјЭИадЁЃдкЯрЗДЕФЗНЯђЩЯЃЌаэЖрЯИОњКЭВИШщЖЏЮяЕФЕААзжЪдкЦфЬьШЛзДЬЌЯТЭЈЙ§ЗЧЙцЗЖЕФЗжУкЛњжЦДгАћНЌдЫЪфЕНжмжЪЛђАћЭтПеМфЁЃ
дкдКЫЩњЮяЁЂвЖТЬЬхКЭвЛаЉЯпСЃЬхжаЗЂЯжЕФTATЯЕЭГдЪаэелЕўЕФЕААзжЪПчФЄзЊдЫЁЃTATЯЕЭГдЫЪфЕФЕААзжЪЭЈГЃКЌгаИДдгЕФИЈвђзг(ШчРызг-СђДи)ЛђепЪЧЖрЕААзИДКЯЮяЕФзщГЩВПЗжЃЌПЩФмЪЧвЛжжБмУташвЊдкАћжЪЭтжиаТзщзАИДдгНсЙЙЕФЗНЪНЃЌВЂЧветжжзЊдЫУЛгаУїЯдЕФРызгаЙТЉЁЃецКЫЯИАћЕФUPSЯЕЭГЭЈЙ§жЪФЄЪфГіДѓСПЕФЮоСьЕМЕААзЃЌШчАзЯИАћНщЫи1ІТ(IL-1ІТ)МвзхЕФЯИАћвђзгЁЃЯИОњЫЦКѕвВгаРрЫЦЕФUPSЯЕЭГЁЃTATКЭUPSЯЕЭГ(ЭЈЙ§БъзМЕФSecЭООЖ)ЕФвЛИігХЕуЪЧЃЌЕААзжЪПЩвдвдвЛжжЪмЕїПиЕФЗНЪНПьЫйПчФЄдЫЪфЃЌетЖдВЮгыбзжЂЗДгІЕФЯИАћвђзгжСЙиживЊЁЃетаЉЕААзжЪЪЧШчКЮДЉЙ§ЯИАћФЄЕФЮЪЬтвЛжБЪЧвЛИіУеЭХЁЃ
ЩЯЪіЕААзжЪЭЈЙ§VBCзЊдЫДЉЙ§ЯИАћФЄгаСНИідвђЁЃЪзЯШЃЌГ§СЫVBCЭтЃЌЖдгкШЮКЮЛњжЦРДЫЕЃЌНЋВЛЭЌДѓаЁКЭРэЛЏаджЪЕФелЕўЕААззЊдЫЭЈЙ§ЯИАћФЄЖјВЛв§Ц№ДѓСПРызгаЙТЉЪЧЮоЗЈЯыЯѓЕФЃЛЦфДЮЃЌЩЯЪіДѓЖрЪ§ЕААзжЪЖМКЌгаФмЙЛгеЕМVBCЕФЖрМюЛљКЭЪшЫЎЛљађЁЃЯИАћЩјЭИадПЙЬх(ШчTMab4)дкЦфVLНсЙЙгђЕФ CDR3 ЛЗжаКЌгаЪшЫЎЛљађWYW(ЛђРрЫЦађСа)ЃЌвбБЛШЗЖЈЮЊЁАФкЬхЬгвнЛљађЁБЁЃЖдЦфађСаМьВтНсЙћБэУїЃЌПЙЬхдкVLНсЙЙгђЕФCDR1КЭCDR2ЛЗжавВКЌгаЖрМюЛљађСаЁЃIL-1ІТЕФГЩЪьКЭЗжУкашвЊcaspase-1ЕФМгЙЄЃЌЖјcaspase-1гжЪмбзжЂаЁЬхЕФЕїНкЁЃPro-IL-1ІТЕФЕШЕчЕуЮЊ4.6ЃЌCaspase-1ШЅГ§ИпЫсадN-ФЉЖЫ117ЮЛВаЛљКѓЃЌГЩЪьIL-1ІТЕФЕШЕчЕудіМгЮЊ8.8ЁЃДЫЭтЃЌЕААзЫЎНтМгЙЄБЉТЖСЫвЛИіC-ФЉЖЫЖрМюЛљађСаЃЌетБЛжЄУїЪЧIL-1ІТЗжУкЫљБиашЕФЁЃ
ЯИОњTATЛњжЦгЩШ§жжЕААзжЪзщГЩЃКTatAЁЂTatBКЭTatCЁЃзюЙиМќЕФГЩЗжTatAЪЧвЛжжаЁЗжзгФЄЕААзЃЌгЩЪшЫЎадІС-Тна§КЭСНЧзад(ЖрМюЛљ)ІС-Тна§зщГЩЁЃЪшЫЎТна§ПЩВхШыжЪФЄЃЌСНЧзадТна§ЦНаагкжЪФЄФквЖЃЌгыжЪФЄЯрЛЅзїгУЁЃTatBCЭЈЙ§ЕзЮяжаИпЖШБЃЪиЕФЫЋОЋАБЫсЛљађ(SRRxFLK)ЪЖБ№ЕзЮяЕААзЃЌЦфзЊдЫашвЊTatAЕФЙбОлзїгУЁЃTatAЭЈЙ§ДйНјVBCНщЕМЕзЮяЕААзЕФзЊдЫЃЌПЩФмЪЧдкTatBCКЭЕзЮяЕФЫЋОЋАБЫсЛљађЕФАяжњЯТНјааЕФЃЌЯжгаЮФЯзгыетвЛМйЩшЪЧвЛжТЕФЁЃР§ШчЃЌTatAВхШыжЌжЪЫЋЗжзгВуЛсЕМжТДѓЕФЕЅВуФвХнжаЕФИЦЛЦТЬЫи(вЛжжгЋЙтШОСЯ)ЁАСПЛЏЁБЁЂОжВПКЭднЪБЕФаЙТЉЁЃУПДЮдіМгЕААзжЪКѓЃЌгЋЙтЖМЛсДяЕНвЛИіаТЕФЦНЬЈЃЌжБЕНдіМгИќЖрЕФЕААзжЪКѓВХЛсНјвЛВНдіЧПЁЃдкУЛгаЕзЮяЕФЧщПіЯТЃЌTatABCОљдШЗжВМдкжЪФЄЩЯЃЛЕБЕзЮяНсКЯЪБЃЌTatABCОлМЏГЩЕЅИіЧјгђЃЌгыдкCPP12(ЭМ4)КЭDTгеЕМ(ЭМ5c)ЕФVBCжаЙлВьЕНЕФРрЫЦЁЃ
ВЁЖО
ЖдВЁЖОНјШыЯИАћЕФбаОПЭЌбљгажњгкЖдЩњЮяЗжзгАћФкзЊдЫЛњжЦЕФаТМћНтЁЃгаАќФЄЕФВЁЖОЭЈЙ§ЦфФЄгыФкЬхФЄШкКЯЖјЬгРыФкЬхЃЌЕЋЖдЮоАќФЄВЁЖОЬгРыФкЬхЕФЛњжЦСЫНтЩѕЩйЁЃвЛАуШЯЮЊЃЌЗЧАќФЄВЁЖОБиаыЦЦЛЕФкЬхФЄВХФмНјШыЯИАћжЪЁЃФПЧАвбОЗЂЯжСЫШ§РржївЊЕФЁАФЄШмНтЁБВЁЖОвђзг:СНадІСТна§НсЙЙгђ(ШчЯйВЁЖОЕААзVI)ЁЂШтЖЙоЂѕЃЛЏЕААз(ШчКєГІВЁЖОN-ШтЖЙоЂѕЃЛЏвТПЧЕААзІЬ1)КЭФЄжиЙЙУИНсЙЙгђ(ШчЯИаЁВЁЖОVP1ЕФСзжЌУИA2НсЙЙгђ)ЁЃФПЧАЛЙВЛЧхГўетаЉНсЙЙВЛЭЌЕФВЁЖОвђзгЪЧШчКЮЭъГЩЭЌбљЕФШЮЮёЕФЃКНЋжБОЖПЩФмЮЊ∼100 nmЧвЛљБОЭъећЕФВЁЖОСЃзгДгФкЬхЪЭЗХЕНАћНЌжаЁЃзїепШЯЮЊетШ§жжВЁЖОвђзгЖМЭЈЙ§геЕМVBCДйНјВЁЖОЕФФкЬхЬгвнЁЃ
ЖдЯйВЁЖОРДЫЕЃЌвТПЧЕААзVIЪЧВЁЖОФкЬхЬгвнЕФжївЊдвђЁЃWiethoffЕШНјвЛВНШЗЖЈЃЌЕААзVIЕФNЖЫгавЛИі20ИіАБЛљЫсЕФСНЧзадІС-Тна§ЃЌЫќдкЯйВЁЖОЮяжжжаИпЖШБЃЪиЃЌЪЧЕМжТФкЬхЬгвнЕФдвђЁЃетИіыФвдИпЧзКЭСІ(БэЙлKDЁж3ІЬM)НсКЯЕНGUVsЕФФкЬхФЄГЩЗжЩЯЃЌгеЕМФвХнЭфЧњЃЌВЂЪЙGUVЫщСбГЩИќаЁЕФФвХнЁЂЙмзДНсЙЙКЭыФ/жЌжЪОлМЏЬхЃЌетаЉЬиеїгыCPP12РрЫЦЁЃЯйВЁЖОНјШыФкЬхКѓЃЌЛсЪЭЗХЖрДя360ЗнПНБДЕФЕААзVIЃЌетаЉЕААзгыФкЬхФЄНсКЯЃЌВЂгеЕМзАдиВЁЖОЕФФвХнУШГіКЭЭпНтЁЃN-ШтЖЙоЂѕЃЛЏвТПЧЕААзІЬ1ИКд№КєГІЙТВЁЖОЕФФкЬхЬгвнЁЃИУЕААзЕФNЖЫ41ИіАБЛљЫсЦЌЖЮІЬ1Nзувдв§Ц№40 kDaЕФгва§ЬЧєћДгКьЯИАћжаЪЭЗХГіРДЁЃЪзЯШЃЌЭЈЙ§ВхШыЕНФкЬхФЄЃЌШтЖЙоЂѕЃЛљНЋВЁЖОЕААзАаЯђЕНФкЬхФЄЩЯЃЌВЂдіМгЦфгыФЄЕФНсКЯЧзКЭСІЁЃЦфДЮЃЌЖЬЕФѕЃЛљ(ШтЖЙоЂѕЃЛљгавЛИі14ЬМСД)ВхШыЧЛФкФЄВњЩње§ФЄЧњТЪ(ЭМ3c)ЃЌетЪЧУШГіОБВПЫљашвЊЕФЁЃІЬ1NЕФгрЯТВПЗжгыФкЬхФЄЕФЯрЛЅзїгУПЩФмв§Ц№ФЄЕФИКЧњТЪЁЃ
ВЁЖОPLA2ЪЧШчКЮгеЗЂVBCЕФФиЃПдчЦкФкЬхЕФЧЛФкФЄКЌгаЗсИЛЕФСзжЌѕЃЕЈМю(PC)ЃЌЦфГЩЗжгыжЪФЄЭтвЖЯрЫЦЁЃPCЕФЙЬгажЌжЪЧњТЪЮЊ∼0ЃЌгаРћгкВузДФЄЕФаЮГЩЁЃPCБЛPLA2ЫЎНтВњЩњШмбЊСзжЌѕЃЕЈМю(LPC)КЭжЌЗОЫсЁЃLPCгавЛИіДѓЕФМЋадЭЗЛљКЭвЛИіЕЅвЛЕФЬМЧтСДЃЌЕБЫќВхШыЕНжЌжЪЫЋВужаЪБЃЌЫќДйНјСЫФЄе§ЧњТЪ(ЭМ3c)ЁЃСэвЛЗНУцЃЌжЌЗОЫсЛсВњЩњИКЧњТЪЁЃвђДЫЃЌPLA2зїгУВњЩњЕФжЌжЪЗжзгЃЌжЇГжФкЬхФЄЩЯЭЌЪБаЮГЩе§ЭфЧњКЭИКЭфЧњЃЌетЪЧУШГіОБВПЫљашвЊЕФЁЃВЁЖОPLA2sдкЕзЮяЬивьадЩЯЪЧЛьдгЕФЃЌвВФмЫЎНтФкЬхФЄЩЯЗЂЯжЕФЦфЫћСзжЌЁЃФЄжиЫмУИЕФЪЙгУЫЦКѕЪЧВЁЖОЯИАћЩуШЁКЭЩњУќжмЦкЕФвЛжжГЃМћВпТдЃЌвђЮЊЯйВЁЖОРћгУЫожїЫсадЧЪСзжЌУИРДЪЕЯжПьЫйЕФАћНЌНјШыЁЃвЛаЉЯИОњЕААзЖОЫиЛЙРћгУСзжЌУИAЕФЛюадРДжиЫмЫожїЯИАћЕФжЪФЄЃЌвдЪЕЯжЯИАћНјШыЁЃ
КЯГЩвЉЮяЕнЫЭЯЕЭГ
ПЊЗЂЕФаэЖрШЫЙЄЯЕЭГФмЙЛНЋЩњЮяЗжзгЕнЫЭЕНВИШщЖЏЮяЯИАћжазїЮЊбаОПЙЄОпКЭжЮСЦЗНЗЈЁЃБОЮФНіЬжТлгУгкКЫЫсЕнЫЭЕФЖрОлЬхЁЂжЌИДКЯЮяКЭжЌжЪФЩУзСЃ(LNP)ЁЃЫфШЛЦфжавЛаЉЕнЫЭдиЬхдкСйДВЩЯШЁЕУСЫОоДѓГЩЙІЃЌШчгУLNPЕнЫЭSARSCoV-2ЕФmRNAвпУчЃЌЕЋЖдЫќУЧдЫзїЛњРэЕФРэНтУїЯджЭКѓЃЌетзшАСЫОпгаИпФкЬхЬгвнаЇТЪЕФЕнЫЭЙЄОпЕФЩшМЦКЭПЊЗЂЃЌЖјетЖдгкЪЧжЮСЦгІгУжСЙиживЊЁЃ
зюНќЃЌбаОПШЫдБРћгУЯШНјЕФЛюЯИАћЙВОлНЙЯдЮЂОЕММЪѕбаОПСЫЖрОлЬхЁЂжЌжЪЬхКЭLNPЕФФкЬхЬгвнЁЃur RehmanЕШЗЂЯжЃЌдкжЌжЪИДКЯЬхКЭЖрОлЬхНщЕМЕФsiRNAЕнЫЭЙ§ГЬжаЃЌКЫЫсКЭдиЬхЖМЪЧЭЛШЛДгФкЬхЪЭЗХГіРДЃЌЫцКѓКЫЫсдкЯИАћжЪКЭЯИАћКЫжабИЫйРЉЩЂ(ЭМ6)ЁЃЖдгкЖрОлЬхЖјбдЃЌДгФкЬхЙлВьЕНКЫЫсКЭдиЬхЕФЫВЪБКЭЭъећЕФХХГіЁЃетаЉЙлВьНсЙћБЛШЯЮЊЪЧжЪзгКЃУраЇгІЕФжБНгжЄОнЁЃWittrupЕШКѓРДЕФвЛЯюбаОПжЄЪЕСЫur RehmanЕШЕФаэЖрЗЂЯжЁЃШЛЖјЃЌWittrupЕШЗЂЯжгЮРыЕФsiRNAЃЌЖјВЛЪЧЭъећЕФжЌИДКЯЮяЛђLNPБЛЪЭЗХЕНАћНЌжаЃЌВЂЧвФкЬхЬгвнЪЧВЛЭъећЕФЃЌетБэУїФкЬхВЂУЛгаЭъШЋЦЦСбЁЃЫћУЧНјвЛВНЙлВьЕНЃЌдкаэЖрЧщПіЯТЃЌsiRNAЕФЪЭЗХгыЮЂаЁЕФАћжЪCa2+ЫВБфЗљЖШвЛжТЁЃ

PeiЖдur RehmanКЭWittrupЕФНсЙћ(вдМАЦфЫћЮФЯзЪ§Он)НјааЗжЮіЃЌЕУГіСЫСэвЛжжНтЪЭКЭНсТлЃЌМДКЯГЩЕнЫЭЯЕЭГЭЈЙ§геЕМVBCЬгРыФкЬхЁЃur RehmanЕШШЫЕФбаОПБэУїЃЌЖдгкУПвЛИіЦЦСбЕФФвХнЃЌИННќЭЈГЃЛсгаСэвЛИіФвХндкећИіЪЕбщЙ§ГЬжаБЃГжЭъећЁЃЪТЪЕЩЯЃЌЭМ6aжаЕФСНИіЯрСкЕФФвХн(Ек3ИіЭМЦЌжаЕФМ§ЭЗБъМЧ)зюГѕРДздЕЅИіФкЬх(ЭМ6a)ЁЃСэвЛжжНтЪЭжаЃЌдкЪЕбщЙ§ГЬжаБЃГжЭъКУЕФФвХнЪЧУШГіЪТМўКѓЕФЪЕМЪФкЬхЃЌЖјЦЦСбЕФЁАФкЬхЁБЪЧУШГіФвХнЃЌЫцКѓЭпНтЁЃWittrupЕШЙлВьЕНЕФЖрВНжшЁЂВПЗжsiRNAЪЭЗХПЩФмЪЧРДздЭЌвЛФкЬхКЭ/ЛђВЛЭЌФкЬхЕФЖрИіVBCЪТМўЁЃЯИАћФкЕФCa2+ЫВБфЪЧПЩвддЄЦкЕФЃЌвђЮЊУПДЮVBCЪТМўЖМЛсЕМжТаЁЕФФкЬхЬхЛ§(АќРЈCa2+РызгКЭШЮКЮВЛЯрЙиЕФЛѕЮя)ЪЭЗХЕНЯИАћжЪжаЁЃ
змНс
зїепЭЈЙ§ЪЕбщжЄУїСЫЯпадCPP(Tat)ЁЂЛЗзДCPP(CPP12)ЁЂЗЧыФРрCPM(CPM3)ЁЂABРрЯИОњЕААзЖОЫи(DT)ЁЂЕЅНсЙЙгђЕААзЖОЫи(NleC)ЕШ5жжНсЙЙВЛЭЌЕФЩњЮяЗжзгПЩЭЈЙ§геЕМVBCДгФкЬхжаЬгвнЕНАћНЌФкЃЌЯрЙиЮФЯзжЄОнБэУїЃЌЖрОлЬхЁЂжЌИДКЯЮяКЭLNPвВЪЧЭЈЙ§ЯрЭЌЕФЛњжЦЬгРыФкЬхЁЃ
ДЫЭтЃЌЦфЫћЯИОњКЭецКЫЕААзвдМАЮоАќФЄВЁЖОвВПЩвдЭЈЙ§VBCЛњжЦдкЯИАћФЄЩЯЕФСНИіЗНЯђзЊдЫЁЃживЊЕФЪЧЃЌVBCЛњжЦПЩвдЪЙаэЖрвдЧАРЇЛѓЧвУЌЖмЕФЙлВьНсЙћЕУвдЕїКЭЖјКЯРэЛЏЁЃзмжЎЃЌVBCЛњжЦЪЧвЛжжШЋаТЧвПЩФмЦеБщДцдкЕФФЄзЊдЫЛњжЦЃЌЦфЙІФмгывбжЊЕФБЛЖЏРЉЩЂКЭФмСПвРРЕЕФЗжУкЭООЖЪЧЦНааЕФЁЃШЛЖјЃЌVBCЛњжЦЪЧЗёЙуЗКЪЪгУгкВЛЭЌЕФЩњЮяЗжзг/ЯЕЭГЛЙашвЊНјвЛВНбаОПЃЌВЂНЋШЗжЄЕФЛњжЦбаОПНсЙћгІгУгкЩшМЦИќгааЇЕФвЉЮяЪфЫЭЯЕЭГЁЃ
ВЮПМЮФЯзЃК
DehuaPei.HowDo Biomolecules Cross the Cell Membrane? Acc. Chem. Res. 2022,55, 309-318.







