æ¼íÔȤë¾Æîøƒ, ¡Ô§Á, îŸøƒáÝ. ÑäŠáæåæÕæ¯ùÛủ¤çáöô¤ëøóÝ¡ñ§ñ´¥¯ûãØÔ涥êÆÎÆû[J]. ¡ÔñøæÆîÏÝ´,ýö¢¥öáüæ¢èåáÑêóÖ¢₤åÙöá
íˆØˆ
ÑäŠáæåæÕæ¯ùÛủ¤òúØ£øøÅôÅëçáàÚöÿøòýáêüȘù■ÆèÑäŠáë´¿»æåæÕæ¯Åö°èȘƒÔÆÅèºöÿ£ŸÅå¤ëèºöÿüÁàïÅå¡ÔÀÂØæÆÖèÒ¥óÆŠ¤ü°èØ奯Ñåëãý¢Çä¥ÊáÉ¢šùìüšÆÎçàÆéçÐȘù■åÖèºöÿاØˋÀÂñøö—¥šýãÀÂæÕø₤¿Ê°äçàêšÆ·ÆŤɡÔçáÆÎÆûú¯ƒ¯.݃öáø¼ØˆæɧÃêùöØûú§■áõâÇåÖÑäŠáæåæÕæ¯ùÛủ¤öô¤ëøóÝ¡ñ§ñ´îÅñÂñ§ûÌçá¿Êæ¼È˜ë˜òݧÕèÉêùÑäŠáæåæÕæ¯ùÛủ¤åÖØÔûÓ涥êñ§ûÌçáÇÇÅôÆÎÆûȘýÂä§äøêùÑäŠáæåæÕæ¯ùÛủ¤îŃ¢êšÆ·çáä¶í§¥¯îŃ¢ààçÐ.
ùÛủ¤åÖöØûúçáàí°È躣ŸøÅùÌÇ΢襫ȘàÓ¿«Ñ°ÀÂñ§¤ÀÂîÜ¡Áçà.ÆèÆÖù■òúØ£øø¡£¤˜ùÛçáöÿøò(ùÛ¤˜ê¢ë´°È¡ÔÇÿ90%Øåèü)Ș§Æ§■ÆÖàùäͤÉÑÁæÕø₤àÓ¡öåÁÀÂîÜú·ýÈêÏäÍçàȘù■åÖæÕø₤¿Ê°äÀÂØˋöÿçïùëÀÂåìèºØ§îÏçàêšÆ·ÆŤɡÔçáÆÎÆûú¯ƒ¯.¡ªƒïóðæÕ°è°èñøȘùÛủ¤¢èñøöˆ¡ÔñøæÆùÛủ¤¤ëÅÀñøæÆùÛủ¤È£Ñ½¡ªƒï°è§¤ñ§ò§È˜ù■Æø¢èñøöˆÆè¿ý¥Ü§£êˆçûç§çá¿ý¥ÜùÛủ¤¤ëÆèñú¿ý¥Ü¥■üÁ£Ëæ¼ÆûêÎѽ°èçáöÿâÚùÛủ¤.äšà£¡ÔñøæÆ£·íÔàù¿Ê¤ü°è¡ÔñøæÆ¢èë´¿»¿ý¥Ü§£êˆØý¢èØåë´¿»ñú¿ý¥Ü¥■æ¼ÆûêÎÅö°èùÛủ¤[1~12]ȘѽÅÀñøæÆø£áÉë´¿»ñú¿ý¥Ü¥■æ¼ÆûêÎæåæÕæ¯Åö°èùÛủ¤.¡ÔñøæÆùÛủ¤åÖàí°È躣Ÿ(ëùààäªçà)ÀÂéˋØç(øýöÿÝÈùÛ¥êçà)ÀÂèºöÿاîÏ(ñâí°ê˜çà)çàêšÆ·ƒªòçüøêùòç¥òÆÎÆû.ѽÅÀñøæÆùÛủ¤æ¼öˆØ£øøÅôÅëùÛủ¤È˜òú§■áõâÇ¢óîÅçáààçÐ.
ÅÀñøæÆùÛủ¤òúØ£øøÆèÅÀñøæÆ(ñøæÆê¢ë´°ÈçëÆÖ2000)ë´¿»æåæÕæ¯Ñ½°èçáùÛủ¤[13, 14].áɰ觤çáÅÀñøæÆ°óöˆ°è§¤Ø·æÆȘ°è§¤Ø·æÆë´¿»ñú¿ý¥Ü¥■æ¼ÆûȘàÓúã¥■ÀÂÎÅ-ÎÅæ¼ÆûÀÂòÒùÛæ¼ÆûÀÂø¼¢ëäÍüÁ£Ëæ¼ÆûÀÂí»¡¤çÓ¤èüÁ£Ëæ¼ÆûêÎØ奯éðö£¥■çàæåñÂçáÅö°èáÉåÖùÛàÉؤøÅöàÑ´ÇÌåÖçáà»ö˜ë½ôÓȘÇÆѽ¯■¿■ùÛñøæÆçàöÿøòÅö°èùÛủ¤.ÆèÆÖñú¿ý¥Ü¥■æ¼ÆûêÎòú¢èáÌÀ¢è¢ÄçáȘÅÀñøæÆùÛủ¤ëªëªüåüø°—¢èáÌÀ¢è¢Äçá°è§¤ÅÅöˆÈ˜òúØ£øøøúáÉçáùÛủ¤.°è§¤Ø·æÆë´°Èòú¡£¤˜úã¥■çáê§úæÅåñøæÆȘàÓäúîÉèºöÿ[15]ÀÂñ¥üÐåÆ£ñ£₤¤üöÿ[16]À¯ݣªùÃîÉèºöÿ[17]ÀÂÑÁŠá¥¯óðîÉèºöÿ[18~23]çà.óðøÅȘÑäŠáâÁ°è§¤Ø·æÆÆèÆÖóðꥤûçáèºöÿ£ŸÅå¤ëèºöÿüÁàïÅåÀÂØæÆÖèÒ¥ó¤ë¤ü°èÀÂÑåëãý¢Çä¥ÊçᢚùìüšÆÎÅåçàäÄÅåȘö■Ø»êùîÏò¾§Ó¿Ðñ¤çáîŃ¢ÅùàÊ.åÖ¿»àËçá20áõ¥ðȘ£ªÆÖÑäŠáçáÅÀñøæÆùÛủ¤åÖØˋöÿçïùë[24~27]ÀÂæÕø₤¿Ê°ä[28]ÀÂøæê—Øøøó[29~31]ÀÂñøö—¥šýã[32~34]¤ëØÔûÓ涥ê[35, 36]çàèºöÿاØˋêšÆ·üåüøêù¤É¤ûçáÆÎÆûú¯ƒ¯.
°È¥«çáÑäŠáùÛủ¤çá°è§¤ñ§ñ´¯■â´¥Æàà-âðàÇñ´ÀÂpHøç缧Öñ´ÀÂâŠæÆú¢Ñà¡áÝðñ´À°˜èª°è§¤ñ´ÀÂÆÅ£ºàÉ¥êøºàÉñ´çà[21, 23, 28, 37, 38].íãÅˋ°è§¤ñ§ñ´åÖÆÎÆûÆÖ£ŸÅåöÿøò¯■åÄòÝößñ´òçüøÑåóðößùÞ¯■åÄ.îŃ¢íÔ¢ˆñ°—ÑÁøøÆéê¥çá°è§¤ñ§ò§È˜àÓû¡ÇÔ£₤À¿ãííÀÂÅÀñøæÆÇÔ£₤ÀÂ篯棷¡ÔñøæÆäÚ¥Æöÿ¡´øºçà°è§¤ñ´[39~44].§■áõâÇȘöØûú¢öäãæÕØýñÂí¿êù¥¡øøèºöÿüÁàïÅåꥤûçáöô¤ë°è§¤ñ§ñ´È˜¯■â´û¡ÇÔ£₤ÀÂѱ귥■ÑüêîÀÂî¾£₤£¿åÙñÇÆÎç¼¢ÄØ奯§Òøºç¯¯æ-ÑÁŠáäÄØšÅå§Ã¤üêÎçà°è§¤ñ§ñ´.§ÒøºÆÖíãÅˋ°è§¤ñ§ñ´áÉòçüøÑäŠáùÛủ¤çá¢è¢ÄøóÝ¡¤ë¢èáÌç¼¢ÄȘùªçûç§çáùÛủ¤ØýØîƒÙåÖØˋöÿçïùëÀÂü¡¯«à»ö˜éÁî½ÀÂèºöÿ§ÓûÌ¢è¢Ä°è§¤ÀÂØÔûÓ涥êçàêšÆ·üåüøêù¤É¤ûçáÆÎÆûú¯ƒ¯.ÑäŠáùÛủ¤åÖØˋöÿçïùëÀÂü¡¯«éÁî½À¯ˋøÂØøøóçàêšÆ·çáÆÎÆûØîƒÙÆŧüÑÁçáæÜò—öáíôȘåÖ݃öáøÅȘöØûúøÄçÐäøôÜÑäŠáùÛủ¤åÖØÔûÓ涥êñ§ûÌçáÆÎÆû.
ÑäŠáùÛủ¤åÖØÔûÓ涥êñ§ûÌçáÆÎÆûòú§■¥¡áõçáÅôñÂüø.åÖüøǺØÔûÓ¿ÊØçøÅȘ篯æ¤ëÑÁŠáçàîúçË刢¿åÙÆèÆÖ¡■¤ûçá¯ýà¨ÅåÀÂçËØ£ÅåÀÂØæǵ¿ÌáÈøó嚤ëÇÂÇÌçàÆéçÐȘݣîŃ¢íÔ¤ëØÔûÓóµØç¿Ðñ¤îŃ¢.à£Ñ½È˜îúçËåˆØÔûÓÆèÆÖûãØÔåÙÅåçëȘëªëªößñ´Ø»óÞ£ºäÍýºèºæп£çáûãØÔÆÎÇÞȘíãØ£ý£æÐøóå¥êùóðåÖêìÇýèüçáÆÎÆû.Ø·ÇùȘîúçËåˆØÔûÓ°ÈÆŠûãØÔ涥ê¿ýë˜ò¿ÆûȘØåäáԣºäÍçáûãØÔÆÎÇÞ.åÖ§■¥¡òÛáõçáîŃ¢øÅȘÅÚÑÁáèûæýáêüȘàÓ§Õ¢æѱ₤¿ÒÀÂáèûæêÈæÆÀƒܤüöÿ§¤ò½À¡ÔñøæÆùÛủ¤çàÑ¥ØîƒÙÝ£°Âòåæ¼öˆûãØÔ涥ê[45~51].íãÅˋ涥êÆŠîúçËåˆØÔûÓêˆÆûáÉäáԢ¿äÍçöÑàȘç¨Çµý¢ñø涥êÇÌåÖ¯ýà¨ÅåýŸÀÂǵ¿ÌáÈøóÝ¡ößñ´òçüøÀÂÆŠ¢¿å١Ǥü¿ÊØí¡ÇåÆçàý£æÐ.ÑäŠáØæÆÖ¤ü°èúØèºöÿüÁàïÅå¡ÔȘÑäŠáæåæÕæ¯ùÛủ¤ÆÅë«°èöˆÆéê¥çáûãØÔ涥ê.åÖíãØ£îŃ¢êšÆ·È˜Collierǽêšçá¢öäãæÕ¢ˆí¿êùÇÇÅôÅåçáîŃ¢È˜ù«ûúñÂüøØ£Ñö¤˜Tü¡¯«ÝÚö£¤ëBü¡¯«ÝÚö£çáÑÁŠáæÕ毰èáèûæüùö˜¤µáÉ¿£Ø»óÞÅÀòµú¢êØçáûãØÔÆÎÇÞ[35]. Tirrellçàṳ̀µøÊû¼¤˜ÆÅØ£øøü¡¯«ÑƒÅåTü¡¯«ÝÚö£çáê§úæÅåæåæÕæ¯ÑÁŠáÅö°èçááèûæýáêüáÉ¿£åÖ£ŸäÍòçîÕøÅäáÔûãØÔÆÎÇÞ[52].à£Ñ½È˜íãÅˋñ§ñ´àåà£ÅÒ؈¯îT£·BÝÚö£ŠáÆŠæåæÕæ¯ÑÁŠá¿ý¥Ü꘧ÆóÞâÇ.öØûú柧■çáîŃ¢ñÂüøȘأâÁÑäŠáùÛủ¤¥·çËçÄöÿâÚ¯■¿■DNAÀÂ篯æÀ¢¿åÙŠáçàîúçËåˆØÔûÓƒëáÉ¿£Ø»óÞÅÀòµýºèºú¢êØçáäÍؤûãØÔ¤ëü¡¯«ûãØÔÆÎÇÞ.öØûúçáñÂüøáÉ¿£ëóÑ₤ÑäŠáæåæÕæ¯ùÛủ¤æ¼öˆØÔûÓ涥êçáòç¥òÆÎÆû.
݃öáø¼ØˆæɧÃêùöØûú¢öäãæÕ柧■åÖÑäŠáùÛủ¤çáöô¤ëøóÝ¡ñ§ñ´Ø奯ùÛủ¤ÆÎÆûÆÖûãØÔøöêóê§ñ§ûÌçáîŃ¢¿Êæ¼È˜ø¼ØˆñøöˆØåüô2¡—ý¢ñøý«ò—Ȥ(1)ÑäŠáæåæÕæ¯ùÛủ¤çáöô¤ëøóÝ¡ñ§ñ´¥¯óðÆÎÆûÈ£(2)ÑäŠáùÛủ¤æ¼öˆØÔûÓ涥êçáÆÎÆû.
1 ÑäŠáæåæÕæ¯ùÛủ¤çáöô¤ëøóÝ¡ñ§ñ´¥¯óðÆÎÆû
òçüøÑäŠáÆèàÉؤü·á»§¤æˆÝðçáýÔôåǵøô¢èñøöˆ2øøȤأòúÇ·óóÑäŠá°è§¤Ø·æÆçáê§úæÅåȘ¿¿ø±ùÛàÉÅåꥤûçá°è§¤Ø·æÆú¯äÍñøæÆȘࣤµë´¿»û¡¤ëÅÀñøæÆÇÔ£₤£₤îÏñÇÆÎ躰è°è§¤Ø·æÆ.åÖíã¡—¿»°äøÅȘñÇÆÎçûç§çá°è§¤Ø·æÆë´¿»ñú¿ý¥Ü¥■æ¼ÆûêÎæåæÕæ¯Åö°èáèûæ§Ã¿¿È˜¯■¿■ùÛñøæÆÅö°èùÛủ¤; ѱòúë´¿»äáÔÑäŠáæåæÕæ¯Åö°èçááèûæüùö˜øÛ¥ðçáüÁ£Ëæ¼ÆûȘò¿óðüÁ£Ë§£êˆòçüøÆèàÉؤü·á»§¤çá戣₤.ë´¿»ýÔôåأȘöØûúèÒ¥óêùû¡ÇÔ£₤ÀÂѱ귥■£¿åÙØ奯₤£¿åÙÇÔ£₤çà°è§¤ñ§ñ´È£ë´¿»ýÔôåѱȘöØûúèÒ¥óêù£ªÆÖ篯æ-ÑÁŠáäÄØšÅå§Ã¤üêÎçá°è§¤ñ§ñ´.
1.1 û¡ÇÔ£₤°è§¤ñ§ñ´
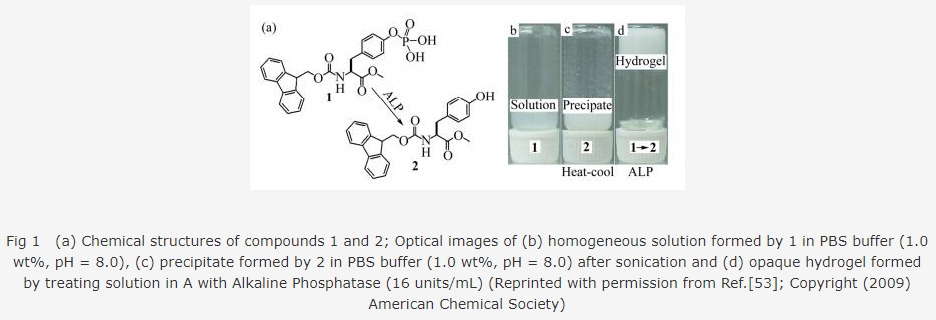
篯æçáêæùã₤¤ëàËêæùã₤åÖèºöÿäÍáÖòúØ£¡—øÄ؈çá缧Ö篯æ¿ÎáÉçáèºöÿ¿»°äȘ봰ÈñÂèºåÖ篯æçáâدÝùÃÀÂù¢¯Ýùäëùí¯ÝùÃçáýÁêÇýÅ£ªèü, åÖèºöÿäÍáÖ¿Ðñ¤ÇÌåÖ§¨ç¯¯æøòêæùã₤¤ëàËêæùã₤çáû¡.öØûú§¨òÒùÛçá°è§¤Ø·æÆ2øÅçáâدÝùÃêæùã₤[53]Șçû秧üöˆúæùÛçá°è§¤Ø·æÆú¯äÍ£₤¤üöÿ1(ë¥ 1(a)). 1¢èØåàÉÆÖùÛÅö°èƒªØ£çáàÉؤ(ë¥ 1(b)), ¥ÆàŠ¥ŸÅåêæùÃû¡(ALP)¤µÈ˜95%ØåèüêæùãªëéÝ£ùÛ§ãç¶È˜æˆ££°èòÒùÛ£₤¤üöÿ2Șê§íÔøÛ¥ð¥äѽ¿ýë˜æÕæ¯Åö°èùÛủ¤(ë¥ 1(d))ȘÆèÆְ觤طæÆ2ý£¤˜ÆŶ࣪£·íԯݣªÈ˜¡ûùÛủ¤åÖpHøç0 ~ 12.0ñÑöÏáÖÑ¥áÉöàÑ´ÇÌåÖ.£₤¤üöÿ2݃èÚáîàÉÆÖùÛȘ봿»°È¿Ìçá¥Æàà-âðàÇ£·pH缧Öçáñ§ñ´Ñ¥ößñ´àɧãȘø£áÉÅö°è°êçÚ(ë¥ 1(c)).ë´¿»Ø»àŠêæùãªëéȘýÂò¿ÆûàËêæùã₤¿»°ä¢Äøó°è§¤È˜òúØ£øøøóÝ¡òÒùÛ£₤¤üöÿùÛủ¤çáÅôýÔôåȘ봿»íãØ£ñ§ñ´È˜öØûú§¨ÅÚÑÁ¤ÉòÒùÛçᢿ¯ˋØˋöÿøóÝ¡°èêùùÛủ¤È˜üåø½äáÔêù¢¿¯ˋØˋöÿçáØˋÅϤëèºöÿâ«ÆûÑà[54~56].
1.2 ѱ귥■£¿åٰ觤ñ§ñ´
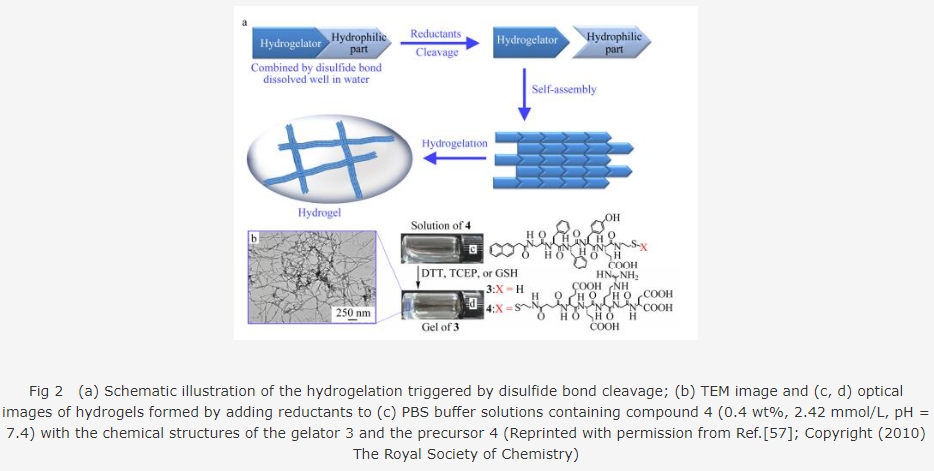
°»êùêæùã₤çáñ§ñ´È˜§¨ÑäŠá°è§¤Ø·æÆÆŠúæùÛÅåÑÁŠáüÁ꘧ÆȘØý¢èØåçûç§ùÛàÉÅåꥤûçá°è§¤ú¯äÍñøæÆ.°è§¤Ø·æÆÆŠúæùÛÑÁŠáøÛ¥ðë´¿»ØæÆÖÑü¢ˆçá£₤îÏ¥■üÁê˜È˜ë´¿»Çìñ£₤îÏ¥■çáÑüêîȘòëñé°—°è§¤Ø·æÆȘçûç§ùÛủ¤.öØûúØ·ÇùèÒ¥óêùѱ귥■£¿åٰ觤ñ§ñ´[57]ȘàÓë¥ 2(a)ùªòƒÈ˜§¨°è§¤Ø·æÆ(£₤¤üöÿ3)¤ëúæùÛÑÁŠáÅ·êÅÆûѱ귥■êǧÆçû称觤طæÆú¯äÍ(£₤¤üöÿ4)Șò¿Æûöô¤ëç᣿åÙ¥ê¥Ç¢è§¨Ñ±ê·¥■£¿åÙÑüêîȘàÓ¿àŠæ¡òŠá(GSH)Ș°è§¤Ø·æÆ£₤¤üöÿ3Ý£òëñé°—âÇȘÅö°èüÁ£Ë§£êˆçááèûæüùö˜ë½ôÓȘÅö°èùÛủ¤.íãøøñ§ñ´¢èåÖ37 ÀÌØ奯éÁî½£ªçàöÿøòÇÌåÖüôòçüøùÛủ¤çáøóݡȘÑåÆÖÑÁò»ØîÝ´çâ°—âÇçá°è§¤Ø·æÆØýÑ¥ƒÔÆÅóíÝÕçáòòÆûÅå. GSHòúØ£øøáÖåÇÅåçáü¡¯«áÖ¢¿î¾£₤¥êȘطÇùȘÆûGSHÇËñÂÑäŠáçáæåæÕæ¯Ñåü¡¯«ý££ÃýºèºÇµçáуÅå.Ø·ÇùȘíãøøë´¿»£¿åÙѱ귥■çá°è§¤ñ§ñ´òúØ£øøèºöÿüÁàïçáùÛủ¤øóÝ¡ñ§ñ´È˜åÖü¡¯«3DéÁî½ÀÂæÕø₤¿Ê°äÀÂØˋöÿǨçïçàîŃ¢êšÆ·áÉÆŤɤûçáÆÎÆûú¯ƒ¯[58, 59].
1.3 î¾£₤£¿åÙñÇÆÎçá¢èá̰觤ñ§ñ´
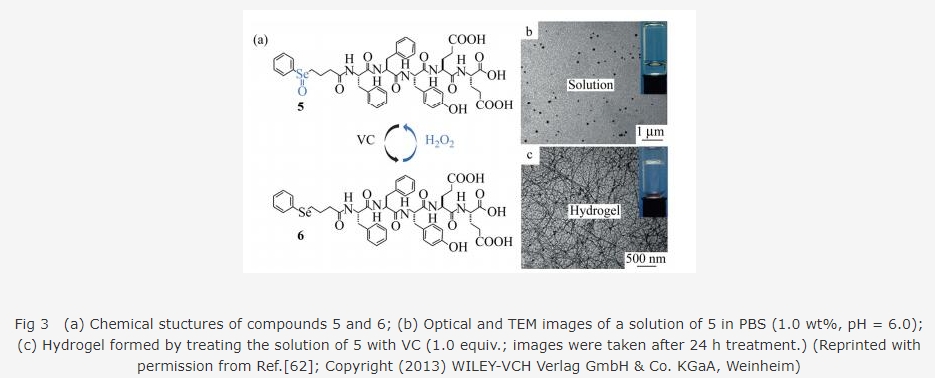
æåࣧÓøÅçáæåæÕæ¯äÍüç¤ÉÑÁòúÑ₤䘢èáÌçá, à£Ñ½ÇµÑÁò»ç¼¢ÄàÉؤ-§¤äÍøÛ¥ð戣£çáñ§ñ´(pH缧ÖÀÂöôÑàç¼¢ÄÀ°˜èªÀ¿ãíí¤ë£₤¤üöÿäÚ¥Æ)ý£áÉÝ£ÆÎÆûç§äÍáÖ.柧■ȘúÍ£ˆÇµîÏíéüÈ¢öäãæÕ¤ëÅÚ£ˆó§¢öäãæÕ¤ü°èêùüçêŤ˜ö½åˆùÄçáƒÜ¤üöÿ[60, 61], áÉ¿£ë´¿»î¾£₤£¿åÙñÇÆÎ缧ÖóðæåæÕæ¯çáÅåáÉȘ₤£¿åÙ¿»°äÆèö˜ù«û■C (vitamin CȘVC)¤ëù¨î¾ùÛ(H2O2)ç¼¢Ä.ë´¿»ÆŠù«ûú¤üæ¼È˜öØûúèÒ¥óý¤ü°èêù¤˜ÆÅö½îúÚ¢£ªëéçá£₤¤üöÿ5 (ë¥ 3)Șù■åÖùÛàÉؤøÅáÉÅö°èáèûæú·çá§Ã¿¿È˜àÓë¥ 3(a)ùªòƒÈ£¥ÆàŠVC¤µÈ˜ö½îúÚ¢£ªëéÝ££¿åÙȘ躰è£₤¤üöÿ6ȘóðùÛàÉÅå§ü£₤¤üöÿ5ýŸÈ˜æåæÕæ¯Åö°èáèûæüùö˜È˜§½Ñ½Åö°èùÛủ¤[62]ȘàÓë¥ 3(b)ùªòƒ.¡ûùÛủ¤åÖ¥ÆàŠù¨î¾ùÛ¿»¤µÆøáÉ戣£°èàÉؤȘåìÇö¥ÆàŠVC¤µÆø¢è£ø¡Ç°èùÛủ¤.íãøø§¤äÍ-ؤäÍøÛ¥ðçáüÁ£Ë戣£øêèì¢èØåîÙ£ñ3Çö. VC¤ëù¨î¾ùÛƒª¢èØååÖèºöÿäÍáÖ£ñƒ°ò¿ÆûȘ¡ûäÍüçÆÅë«åÖèºöÿäÍáÖòçüøàÉؤ-ủ¤¥ðçá¢èáÌîÙ£ñæˆÝð.
1.4 £ªÆÖ篯æ-ÑÁŠáäÄØšÅåüÁ£Ëæ¼Æûçá°è§¤ñ§ñ´
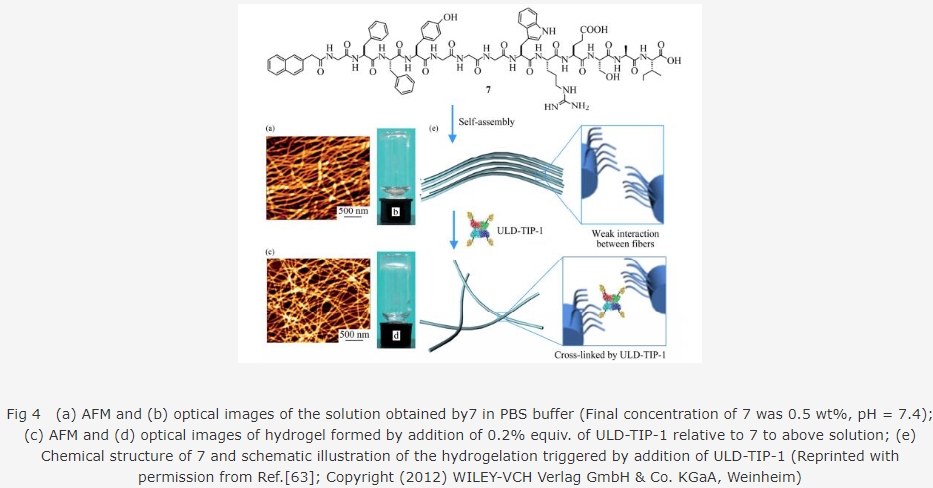
åÖæåæÕæ¯äÍüçøÅȘأÅˋÅÀñøæÆáÉ¿£æÕæ¯Åö°èáèûæüùö˜ÀÂáèû毶£·íÔáèûæú·çà§Ã¿¿È˜àÓ¿«íãÅˋáèûæ§Ã¿¿øÛ¥ðàÝñÎüÁ£Ëæ¼Æû£·íÔüÁ£Ëæ¼Æûú¢Ñà§üçë, ƒëø£áÉÅö°èñøèÂçáàÉؤȘýÂý£áÉÅö°èùÛủ¤.åÖíãøøäÍüçøÅȘ봿»å—ú¢áèûæ§Ã¿¿øÛ¥ðçáüÁ£Ëæ¼Æû¢èØåò¿áèûæ§Ã¿¿øÛ¥ðüÁ£Ë§£êˆÅö°èà»ö˜çáë½ôӧÿ¿È˜ÇÆѽÅö°èùÛủ¤.æþîÙíãøø¿Ìå·È˜öØûúèÒ¥óêùØ£øø£ªÆÖ篯æ-ÑÁŠáøÛ¥ðüÁ£Ëæ¼Æûçá°è§¤ñ§ñ´[63].öØûúüàèÒ¥óêùØ£¡—À¯ùáÝÜÀÝULD-TIP-1àÖ¤ü篯æȘóðøÅû¢Ø£¡—òøÝÜ¢èØåÆŠÑÁŠáÅ·êÅWRESAIäÄØšÅå§Ã¤ü.øÛ¤µèÒ¥óý¤ü°èêù¯■¤˜WRESAIÅ·êÅçáæåæÕæ¯ÑäŠá(£₤¤üöÿ7È˜ë¥ 4øÅùª£₤òƒ).¤üöÿ7åÖùÛàÉؤøÅáÉÅö°èáèûæüùö˜È˜ç¨òúÆèÆÖÅö°èçááèûæüùö˜øÛ¥ðàÝñÎæп£ú¢ÑàçáüÁ£Ëæ¼ÆûȘüùö˜øۥ𥡤¾û£Æŧ£êˆçá§ÖçÐ(ë¥ 4(a))Șò¿çûí«¡—äÍüç°òàÉؤæÇä˜(ë¥ 4(b)).åÖäÍüçøÅ¥ÆàŠULD-TIP-1篯æȘULD-TIP-1篯æçáÀ¯òøÝÜÀÝáÉÆŠý£ë˜üùö˜èüÝˋôÑ°—âÇçá-WRESAIÅ·êŧäüȘÇÆѽå—ú¢êùüùö˜øÛ¥ðçáüÁ£Ëæ¼Æû(ë¥ 4(c))ȘæŸøíÇìò¿êùùÛủ¤çáÅö°è(ë¥ 4(d)).òƒØãë¥(ë¥ 4(e))í¿òƒêùÑÁŠáüùö˜øÛ¥ðë´¿»ç¯¯æ§£êˆçá¿»°ä.ë´¿»ç¼¢Ä篯æçáꢣ·íÔ¡áÝðÑÁŠáÅ·êÅÇÆѽ¡áÝðƊ篯æçáüÁ£Ëæ¼ÆûêÎáɤɤûçáç¼¢Äùªçûç§ùÛủ¤çáêÎîÏÅåáÉ.íãøø°è§¤ñ§ñ´ÆÅøºÆÖøóÝ¡ÑÁ¿ÎáÉÑÁŠáæåæÕæ¯ùÛủ¤È˜åÖØˋöÿòëñéØ奯ü¡¯«à»ö˜éÁî½çàñ§ûÌÆÅꥤûÆÎÆûú¯ƒ¯[64, 65].
2 ÑäŠáùÛủ¤æ¼öˆØÔûÓ涥êçáÆÎÆû
2.1 æ¼öˆDNAØÔûÓçááèûæåÄäÍ
öˆêù¢ùñ±Ç¨ë°çᣟäÍýÀу£·¥¾£ŸýÀуæ¼öˆØÔûÓçáúÝåÖñÓüíȘDNAçàîúçËåˆØÔûÓæ¼öˆ§üöˆ¯ýà¨çáäÌǺóñòÉ秿Ðñ¤¿ÄæÂ.à£Ñ½È˜DNAü·ü¡¯«áÖçáçëæˆåùÅÏôòøóå¥êùóðÆÎÆûȘDNAØÔûÓÝÄÅŠÆŠåÄäÍüÁ£Ëæ¼Æû¿¿§´°èDNAǨçïüçë°¤µæÂèðýéáÉå—ú¢ûãØÔÆÎÇÞ.üøåÖ¢óîÏ¥ØûúØîƒÙ¿¿§´°—ÑÁøøÇ짽DNA¡ÔÅϧ½àŠý¡àÕÑ₤öÿü¡¯«çáǨçïüçë°È˜ç¨òúíãÅˋåÄäÍÇÌåÖü¡¯«ÑƒÅåú¢ÀÂDNAåÄê¢çëÀ¡ÇåÆçáøóÝ¡¿»°äç¥øôçáDNA£ŸÅå§ççëçààÝçÐøóå¥êùù■ûúçáêìÇýÆÎÆû.Ø·ÇùȘøóÝ¡Ø£øø¥à¯ýà¨Æø¡ÔÅÏçáDNAǨçïüçë°àåà£òúØ£¡—ä¶í§.
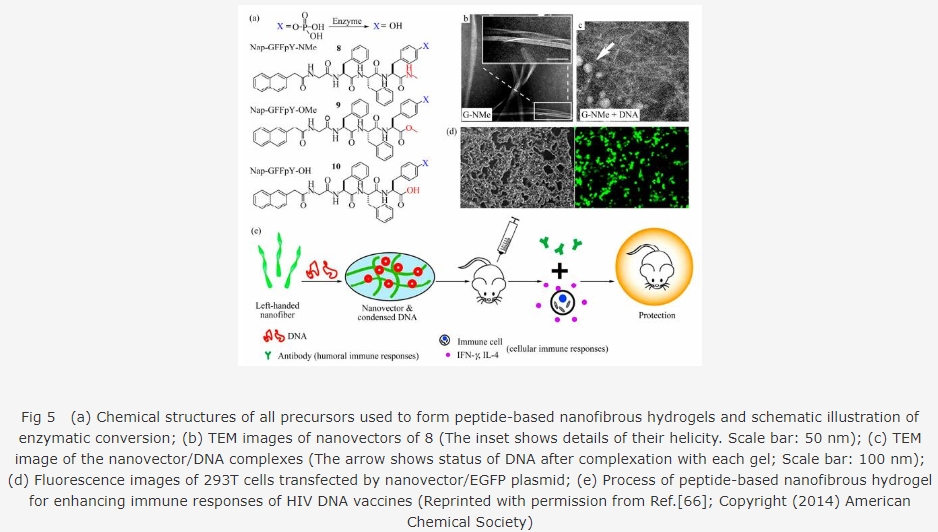
öØûúèÒ¥óýÂøóÝ¡êù3¡—§Ã¿¿âÁùóçáÑäŠáùÛủ¤Nap-GFFY-NMe (8), Nap-GFFY-OMe (9)¤ëNap-GFFY-OH (10)ȘýŸÝÞåÖÆÖÑÁŠáCÑù꘧Æçᣪëéý£ë˜È˜àÓë¥ 5(a)ùªòƒ. 3¡—ùÛủ¤ñøÝÞÆèóðÑåÆÎçáêæùã₤ú¯äÍñøæÆåÖ¥ŸÅåêæùÃû¡ÇÔ£₤üôøóÝ¡.òçîÕøÊû¼È˜8æåæÕæ¯Åö°èêùæµÅ»çáüùö˜§Ã¿¿È˜ò¿çûóðÅö°èçáùÛủ¤áÉ¿£é´ù¾DNAñøæÆýÂÝÈ£Êù■ûúûãÆÖ§ç§ã(ë¥ 5(b)¤ë5(c))Șë˜òÝÇ짽EGFP£ªØ·çáàÖ¤üøòêȧ½àŠý¡àÕÑ₤öÿü¡¯«øÅ(ë¥ 5(d)).¡ûùÛủ¤-¢¿å١ǤüöÿáÉ¿£üåø½äÃè»ØÔûÓHIV Env DNA (Ø£ÑöÝÁôŠHIV-1¯■áÊ篯ægp 145çáDNA) IgG¢¿äÍçöÑàçáäÃè»È˜úØë´¿»¥ÀáÖÀÂóÊüô¤ëƒýô—3øøûãØÔ§Æøøñ§ñ´ƒªáÉäáԣºäÍçáûãØÔÆÎÇÞ(ë¥ 5(e)).æ¼öˆDNAØÔûÓçáǨçïüçë°È˜¡ûùÛủ¤ƒÔÆÅøóÝ¡¿»°ä¥·çËÀ¡ԤèåÄê¢ÀÂÆéØšçáèºöÿüÁàïÅå¤ëèºöÿ¯ýà¨ÅåçàÆéçÐȘöˆåÊñâHIVçàýÀу¡ÅàƒçáDNAØÔûÓøóÝ¡äÿˋêùÅôçá¢èîÀýÔôå[66].
2.2 æ¼öˆç¯¯æâÁ¢¿åÙçá涥ê
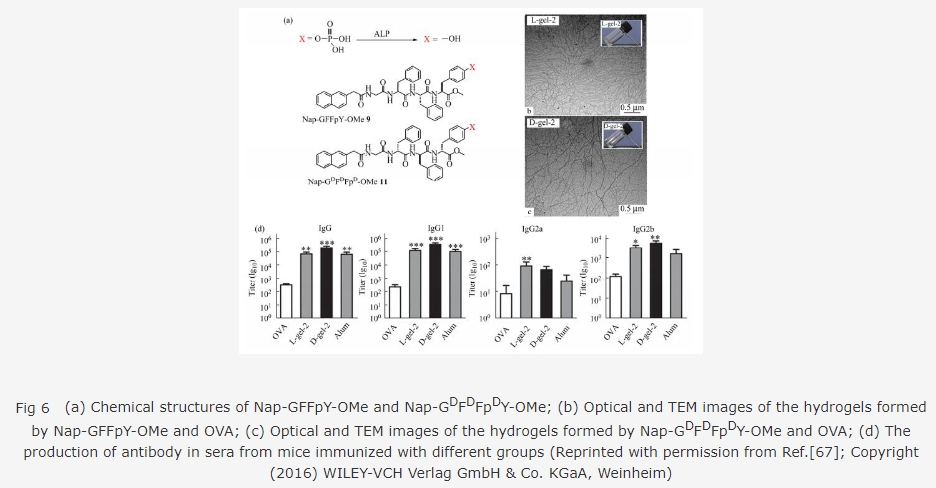
°»êùDNAØÔûÓØåëãȘ篯æØ奯ÑÁŠáçàîúçËö£ØÔûÓØýòúǨë°ØÔûÓçáäÌǺíÔȘù■ûúë˜îªÆÅûãØÔåÙÅåçëçáý£æÐ.Ø·ÇùöØûú§¨òÒùÛÑäŠá(ë¥ 6(a)ùªòƒ)ÆŠ¢¿åÙ篯æë´¿»ñú¿ý¥Ü¥■¿ýæÕæ¯Åö°èùÛủ¤È˜îŃ¢êùóðæ¼öˆç¯¯æâÁ¢¿åÙ涥êçáÅÏ¿«[67]
îÀàÀ°è§¤Ø·æÆNap-GFFY-OMe(9)Ø奯ù■ÑåÆÎçáD¿¿ÅëÅ·êÅ(11) (ë¥ 6(a)ùªòƒ)Ș봿»û¡ÇÔ£₤çáñ§ñ´ÆŠ¥ÎôîúÍ篯æ(ovalbuminȘOVA)¿ýæÕæ¯È˜ñøÝÞÅö°èêùL-gel¤ëD-gel (ë¥ 6(b)¤ë6(c)).§Ã¿«üåòƒÈ˜ÆŠôê涥êüÁÝàȘL-gel¤ëD-gelñøÝÞäáÔIgGýºê¢1.3ÝѤë3.8ÝÑȘüåø½äÃè»ÅÀòµäÍáÖçáûãØÔÆÎÇÞ, ѽúØD-gelÆŠL-gelüÁÝàȘäÃè»æ¼Æû¡■öˆû¼üå(ë¥ 6(d)).åÙØ·òúD¿¿ÅëçáÑÁŠáÑåäÍáÖçá篯æû¡ƒÔÆÅأѴçáçø¢¿êÎȘíãò¿çûù■ûúåÖäÍáÖÝàL¿¿ÅëçáÑÁŠá¡■¥ÆöàѴȘƒÔÆÅ¡■°ÊçáæÊê¶òÝ¥ð.°»êùäÃè»IgGçáçöÑàØåëãȘ2øø¿¿ÅëçáùÛủ¤£¿ƒÔÆÅÇ짽¢¿åÙåÖêɯë§Ãçá¡£¥₤ȘîÆ°Ê¢¿åÙåÖêɯë§ÃçáæÊê¶òÝ¥ðȘäáÔDCü¡¯«Ñ墿åÙçáèÐàÀê¢È˜Ç짽DCü¡¯«çá°èòš¤ëÇ짽èºñÂøÅÅáçáÅö°èçáæ¼Æû.êÚëã, D-geláÉÆÅÅÏçá¥Ê£Ÿü¡¯«ûãØÔȘíãÑåøæê—À¯˜æäýÀÀÂÝ«¡öçàøÄǵ¥ýýÀçáøöêóÅåØÔûÓçáÇÇøóØãØÍøÄǵ.ý£ë˜ÆÖØîƒÙÝ´çâç᧨æåæÕæ¯ÑÁŠáÆŠ¢¿åÙŠá¿ý¥Ü§Ã¤ü¤µæÕæ¯çáýÔôåȘöØûúèÒ¥óêùØ£øø¡■öˆñ§ÝÐÀ¡■öˆòçÆûçáòÒùÛÑäŠáÆŠ¢¿åÙ篯æë´¿»ñú¿ý¥Ü¥■¿ýæÕæ¯Åö°èáèûæüùö˜çáýÔôåȘÆÅâ«ÆÖóðöÇâÇçá¿ÊØç£₤èºýºÆŠêìÇýÆÎÆû.
2.3 D¿¿ÅëçáÑÁŠáùÛủ¤æ¼öˆáÉ¿£Çä¥ÊCD8+Tü¡¯«üšÆÎçáØÔûÓ涥ê
£ºäÍçáü¡¯«ûãØÔÆÎÇÞȘÆàóðòúCD8+ Tü¡¯«ûãØÔÆÎÇÞȘÑåûãØÔøöêóòÛñøøÄ؈ȘطöˆCD8+ Tü¡¯«ûãØÔÆÎÇÞòúáÉ¿£øݧÆèÝèùü¡ƒºÀÂýÀу¤ëøæê—ü¡¯«çáûãØÔ¿»°ä.ØîƒÙ£þçûFDAéºæ¥çáØÔûÓ涥êȘàÓôê涥ê¤ëÆëàÕ¥êMF59çàȘø£áÉ¿£å—ú¢£ºäÍçáäÍؤûãØÔÆÎÇÞȘѽ¥¨èìáÉ¿£ë˜òÝäáÔü¡¯«çáûãØÔÆÎÇÞ.á¢ú¯Ä§ÅÒ¢ˆñÂáÉ¿£Æí祣ºäÍýºèºü¡¯«ûãØÔÆÎÇÞȘÆàóðòúƒÔÆÅèÝèùæ¼ÆûçáCD8+ Tü¡¯«ûãØÔÆÎÇÞçáØÔûÓüçë°.
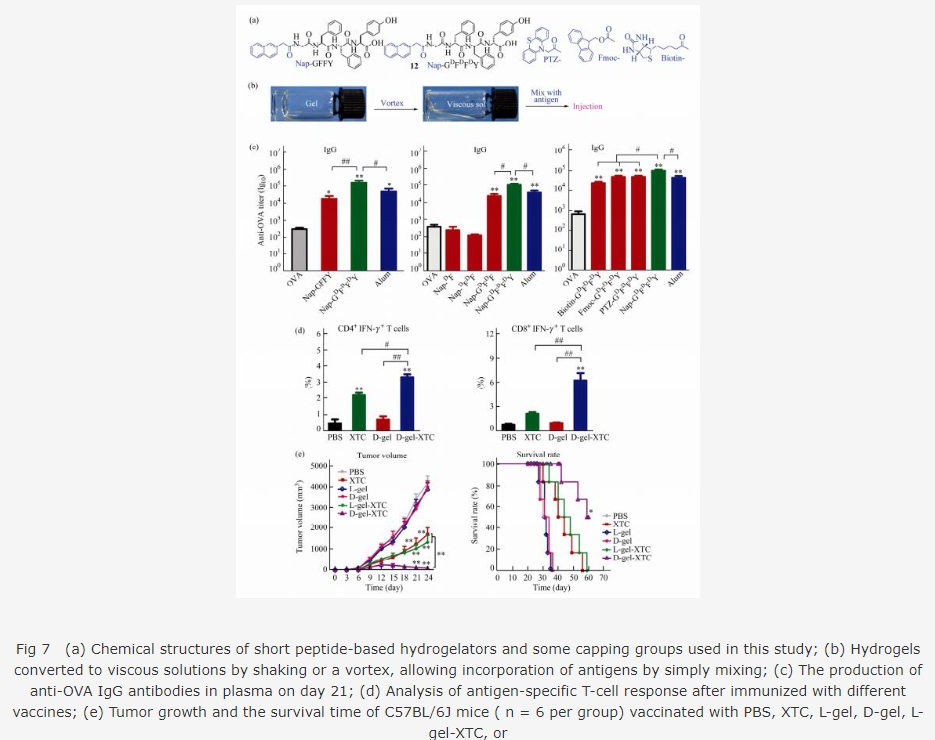
öˆêù§ãƒ—íã¡—öòäãȘöØûúè¡îÀêùüçêÅÑäŠáùÛủ¤È˜åÖäÍáÖëãóâ¿âóðäÃè»äÍؤûãØÔ¤ëü¡¯«ûãØÔçááÉêÎȘØåóÖ£þçûØ£øøáÉæ¼öˆøæê—ûãØÔøöêóçáùÛủ¤æ¶¥ê[68].òçîÕñÂüøȘ°è§¤Ø·æÆNap-GDFDFDY-OH(12) (ë¥ 7(a))Åö°èçáùÛủ¤ûãØÔÅÏ¿«æŸ¤û.¡ûùÛủ¤ÆŠûÞ£Ÿ¤µçáøæê—ü¡¯«¥·çËçáöÿâÚ£š¤üȘ¥Ç¢èøóÝ¡°èØÔûÓ-涥ê¡Ç¤üöÿ(ë¥ 7(b)).ÆŠóðù«ÑåííæÕØÔûÓüÁÝàȘò¿Æû¡û¡Ç¤üØÔûÓøó¥êûãØÔ¿»çáÅÀòµÈ˜IgG¢¿äÍçöÑàæŸú¢(ë¥ 7(c))ȘäÍáÖCD8+¤ëIFN-Îû+ù¨î¶ÅåTü¡¯«üåø½å—ÑÁ(ë¥ 7(d))ȘäÍáÖøæê—çû秡■¤ûçáØøøóȘÅÀòµèºÇÌóÖ¡■°Ê(ë¥ 7(e)).öØûúë˜òÝøÊû¼¡ûùÛủ¤òúØ£øøØæÆÖøóݡȘýÂúØáÉ¿£ë˜òÝ¥Êñ£ºäÍøÅäÍؤûãØÔ¤ëü¡¯«ûãØÔñÇÆÎçáØÔûÓ涥êȘåÖøæê—ûãØÔøöêóñ§û̃ÔÆÅ¥¨ÇµçáêìÇýÆÎÆûúÝáÉ.à£Ñ½È˜¡û涥ê¥Ê£ŸûãØÔüçë°ç᣺âÚÅÒ؈§½Ø£ý§èŸàŠîŃ¢.
2.4 ý£ë˜ôñƒÑç¼¢ÄçáæåæÕæ¯ÑäŠááèûæ§Ã¿¿ÑåØÔûÓ涥êçáƯüš
ë´¿»û¡ÇÔ£₤ôñƒÑ§½ÅÅæåæÕæ¯È˜ñÇÆÎçá£ñƒ°ñú°Èöô¤ëȘû£ÆŃÓêØçáöôÑàÝð£₤ȘæåæÕæ¯ñøæƧåÇÎÆÖ§üçëçááÉê¢æÇä˜È˜ñøæÆíþÑ₤§üÅÀȘطѽáÉ¿£ééêÅ°èåÖö¿Üèü¡■¥Æ¿Ìí«ÆÅÅ·çááèûæ§Ã¿¿.ѽ°È¿Ìçá¥Æàà-âðàÇñ§ñ´È˜¥ÆàवñøæÆåùÑ₤¤ëíþÑ₤ƒÓêØȘñøæÆ¿¿ÅëýŸØš§üǵȘåÖæÕæ¯òÝòóÝÄ£ÃÅö°èÅÚÑÁý£¿Ìå·çáééêÅȘçûç§çááèûæ§Ã¿¿ÆÅÅ·Ñà§üýŸ.íãøøÆÅÅ·ÑàçáýŸÝÞæŸøí£Ãç¥øôóðèºöÿ£ŸÅåçáýŸÝÞ.Ø·ÇùöØûúò¿Æû2øøôñƒÑç¼¢Äë˜Ø£ÑäŠá§½ÅÅæåæÕæ¯, ñøÝÞçûç§áèûæüùö˜¤ëáèûæú·È˜¢¥ýšêùù■ûúæ¼öˆØÔûÓ涥êçáûãØÔÅÏ¿«[69].
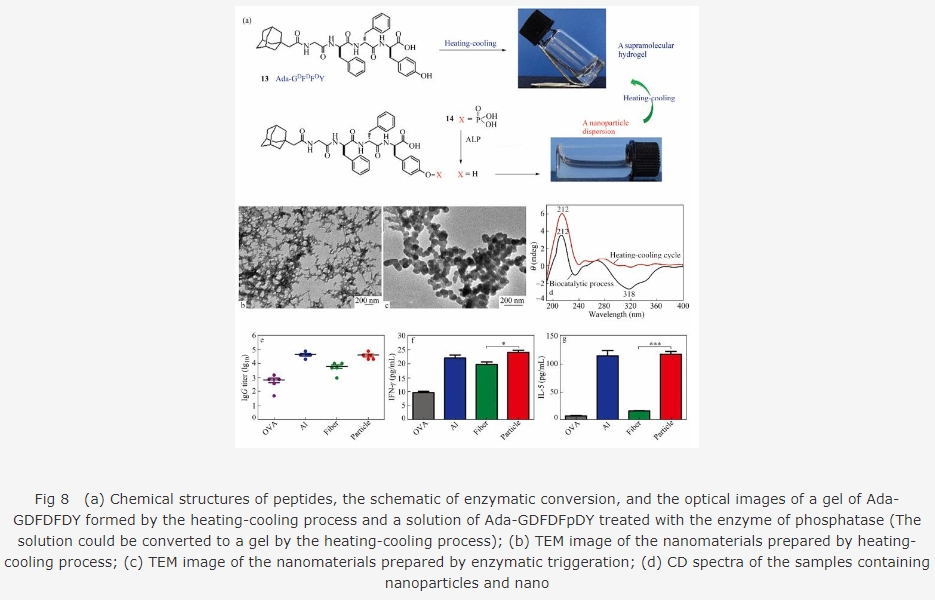
öØûúèÒ¥óêù2øøD¿¿ÅëçáæåæÕæ¯ÑÁŠáAda-GDFDFDY (13)¤ëAda-GDFDFpDY (14).ñøæÆ13ë´¿»¥Æàà-âðàÇçáñ§ñ´Åö°èáèûæüùö˜È˜Åö°èùÛủ¤(ë¥ 8(a)¤ë8(b))È£14åÖ¥ŸÅåêæùÃû¡çáÇÔ£₤üôæˆÝð°è13, æŸøíæåæÕæ¯Åö°èáèûæú·(ë¥ 8(a)¤ë8(c)). CD¤ëFTIR§Ã¿«üåòƒáèûæú·§Ã¿¿øÅçáñøæƃÔÆÅ¡■¥ÆÆÅÅ·çáÑÁŠá¿¿Åë(ë¥ 8(d)).§¨2øøÅöä˜çááèûæýáêüæ¼öˆæ¶¥êûãØÔÅÀòµÈ˜§Ã¿«üåòƒáèûæú·æÕIgGçöÑàòúáèûæüùö˜æÕçá6.5ÝÑ(ë¥ 8(e)).êÚëãȘäÍëãÇìDCsü¡¯«°èòšòçîÕüåòƒÈ˜áèûæú·Ýàáèûæüùö˜Çä¥ÊDCsü¡¯«ÝÚÇÿ¡■ÑÁçáü¡¯«Ø·æÆȘàÓIFN-ÎûÀÂIL-5ÀÂIL-6ÀÂTNF-Îêçà(ë¥ 8(f))ȘÝÚû¼áèûæú·Çä¥ÊäÍؤûãØÔ¤ëü¡¯«ûãØÔçááÉêΡ■ú¢.ë´¿»û¡ÇÔ£₤ôñƒÑç¼¢ÄÑÁŠáæåæÕæ¯áèûæ§Ã¿¿çáÆÅÅ·ÑàȘäÃè»ù■ûúæ¼öˆæ¶¥êçáÅÏ¿«È˜íãòúèÒ¥óáèûæýáêü涥êçáØ£øøÅôýÔôåȘöˆØÔûÓ涥êçáÆé£₤èÒ¥óäÿˋêù¡■ÑÁçáýÔôå.
3 æɧÃÆŠí¿ë«
ÑäŠáùÛủ¤ÆèÆÖèºöÿüÁàïÅå¤ûȘØæÆÖèÒ¥óÆŠøóÝ¡Ø奯Ñ₤䘢èáÌçáäÄÅåȘåÖèºöÿاØˋêšÆ·Ý£¿Ðñ¤çáîŃ¢.à£Ñ½È˜ÑäŠáùÛủ¤æŸøíòúñþáÉ¿£åÖòç¥ò躣ŸøÅí¥ÆÅØ£ü₤øÛçÄȘƊǨë°çá¡ÔñøæÆùÛủ¤çàÝà¥ÓȘ°èöˆý£¢è£·àÝçáèºöÿýáêüȘ£¿ÅÒ؈§½Ø£ý§ëÖƒ·óðäÄÅåȘíØç§úÀçÝçáÆÎÆûêšÆ·È˜ýÂÑåóð¯ýà¨Åå¢ˆí¿¡■öˆüçë°¤ëèŸàŠçáîŃ¢.§■áõâÇîŃ¢ñÂüøȘ봿»í«¤ü¡ÔñøæÆùÛủ¤£·íÔäڥơÔñøæÆÀÂ篯æçàèºöÿǵñøæÆáÉÆÅÅÏçáç¼¢ÄÑäŠáùÛủ¤çáêÎîÏú¢ÑàÀ°觤ÅåáÉÀÂèºöÿ£ŸÅåçà.ÑåíãâÁ¡Ç¤üÀÂåÆ£₤ùÛủ¤§½ÅÅèŸàŠä§ù¼§¨áÉí«¤üǵñøæÆÆŠÅÀñøæÆçáÆéòóȘëóÑ₤ÑäŠáùÛủ¤çáòç¥òÆÎÆû.
ÑäŠáùÛủ¤æ¼öˆØÔûÓ涥êñ§ûÌçáÆéòóòúǨë°ýáêüý£ƒÔÝ¡çá.ùÛủ¤çáäÄÅåò¿çûóðƊǨ밢¿åÙ(¥¾Ñƒ£·ûÞ£ŸçáýÀåÙäÍÀÂøæê—ü¡¯«çà)øÛ¥ð¢èØåë´¿»öÿâÚ£š¤ü¥·ÝÐçÄøóÝ¡°èûãØÔøó¥êÈ£ÑÁŠáæåæÕæ¯çáäÄÅåò¿çûóðÆŠ¯Š¢¿åÙ¿ýë˜æÕæ¯(篯æ¤ëÑÁŠáçà)ȘØå¥ÊñÂæŸÆéçáûãØÔñÇÆÎȘÇÿ秡■¤ûçáåÊñâØ奯øöêóÅÏ¿«.à£Ñ½È˜ÑäŠáùÛủ¤æ¼öˆæ¶¥êäáÔûãØÔüšÆÎç᣺âÚá¢ú¯£¿û£ÆÅ°èòšçáâÚôÜȘÅÒ؈¡■¥ÆèŸàŠçáîŃ¢È˜ýéáÉåÖêìÇýÆÎÆûñ§ûÌ¡■§½Ø£ý§.
ë´¿»ñÂí¿èºöÿüÁàïÅåꥤûçáÅôÅëøóݡ냃Ñ, ¢èØåò¿ÑÁŠáùÛủ¤æ—ç§ößùÞ¯■¿■ÆŠòëñ食ÅåöÿøòȘëÄ¢ÚóðÆÎÆûñ§ü·È˜ÆÎÆûÆÖæÕø₤¿Ê°äȘü¡¯«çáà»ö˜éÁî½çà.¡■øÄ؈çáòúȘîŃ¢ñÂüøȘ봿»Ñåý£ë˜°è§¤ôñƒÑçáîŃ¢È˜ÑÁŠáæåæÕæ¯çûç§çááèûæýáêüö¿ÜÅöûýØ奯ùÛủ¤çá¤õ¿ÜÅåøò£ÃòÉ称觤ôñƒÑçᥨǵƯüš[69~76].òæüàȘ봿»¥Æàà-âðàÇçàñ§ñ´çûç§çááèûæ§Ã¿¿¿Ìí«ÑàåÑåÑÅÀÆÖû¡ÇÔ£₤ñ§ñ´çûç§çááèûæ§Ã¿¿È£óðÇöȘû¡Ñ₤êÎîÏ£Ãüåø½Æ¯üšæåæÕæ¯ÑäŠáçá¢í¥ð¿¿Åë(Îê-ôïŻȘÎô-íÜç±È˜ö߿̃Úúºçà)È£ë˜òÝȘý£ë˜öôÑàüôû¡ÇÔ£₤çûç§çááèûæ§Ã¿¿£Ã°òüøýŸÝÞ¥¨Çµçá¤õ¿ÜÀÂö¿ܧÿ¿È˜§½Ñ½Æ¯üšíãÅˋáèûæ§Ã¿¿çáèºöÿîÏ¿ÎáÉ.öØûúüÁÅéȘ봿»°è§¤ôñƒÑØ奯û¡Ñ₤êÎîÏç¼¢ÄÑäŠáæåæÕ毧ÿ¿¤ë¿Îáɧ¨òúÑäŠáæåæÕæ¯ýáêüñÂí¿çáØ£¡—ÅôçáøÄ؈ñ§ü·.
ûãåÞèªû¼È¤ÝƒöáöˆÅÅØ秣ê¼îÏü¯È˜öáíôÝõæÂêùåÙæ¼íÔ¥¯°—ÇÎȘ¯Ìà´¿ÕåÙæ¼íÔùªÆÅȘàÓÆÅúøà´È˜¢èêˆüç胰»ÀÈ