ΓΕ÷–Ιζ“©―ß‘”÷ΨΓΖ2024ΡξΉς’ΏΘΚ¥όΡ»Θ§ Ζ―«ΨϋΘ§ΑΉΟτΘ§Άθ Λ’ΐΘ§ΕΓ“ΜΘΜ…¬Ές÷–“Ϋ“©¥σ―ß“©―ß‘ΚΘΜΩ’ΨϋΨϋ“Ϋ¥σ―ßΒΎ“ΜΗΫ τ“Ϋ‘Κ“©ΦΝΩΤΘΜΩ’ΨϋΨϋ“Ϋ¥σ―ß“©―ßœΒ
’Σ“ΣΘΚ÷– ύ…ώΨ≠œΒΆ≥Θ®centralnervous systemΘ§CNSΘ©Φ≤≤Γ―œ÷ΊΈΘΚΠ»ΥάύΒΡ…ζΟϋΫΓΩΒΘ§ΒΪ”…”Ύ―ΣΡ‘ΤΝ’œΘ®blood®CbrainbarrierΘ§BBBΘ©ΒΡ¥φ‘ΎΘ§»±ΖΠΫΪ“©Έο δΥΆΒΫ¥σΡ‘ΒΡ”––ßΦΦ θΘ§―œ÷Ί”ΑœλΤδœύΙΊ“©ΈοΒΡΩΣΖΔ≥…ΙΠ¬ Θ§÷¬ Ι’βάύΦ≤≤ΓΒΡ÷ΈΝΤ–ßΙϊΆυΆυ≤ΜΨΓ»γ»Υ“βΓΘ“ρ¥ΥΘ§Τ»«––η“Σ“Μ÷÷–¬ΦΦ θΫβΨω…œ ωΈ ΧβΓΘΡ‘Α–œρκΡ≈ΦΝΣ“©Έο”…Ρ‘Α–œρκΡΓΔΝ§Ϋ”ΜυΆ≈ΚΆ”––ß‘ΊΚ…’β»ΐ≤ΩΖ÷Ήι≥…Θ§Τδάϊ”Ο…ζΈοœύΙΊΒΡΡΎ‘¥–‘ΉΣ‘ΥΜζ÷Τ Ι…ζΈοΜν–‘Ζ÷Ή”ΆΗΙΐBBBΘ§≤ΔΒΫ¥οΡ‘ Β÷ Θ§“―≥…ΈΣ“Μ÷÷”–«ΑΨΑΒΡCNS“©Έο δΥΆœΒΆ≥ΓΘ±ΨΈΡΦρ“ΣΫι…ήΝΥΡ‘Α–œρκΡΓΔΝ§Ϋ”ΜυΆ≈ΓΔ”––ß‘ΊΚ…ΒΡ÷÷άύΦΑΧΊ’ςΒ»Θ§≤ΔΝ–ΨΌΝΥ“Μ–©≥ΘΦϊΒΡΡ‘Α–œρκΡ≈ΦΝΣ“©ΈοΘ§“‘ΦΑ¥Υάύ“©ΈοΟφΝΌΒΡΧτ’ΫΚΆΗΡΫχΒΡΖΫΖ®Θ§“‘ΤΎΈΣΚσ–χCNS“©ΈοΒΡ…ηΦΤΚΆΩΣΖΔΧαΙ©–¬ΥΦ¬ΖΓΘ
÷– ύ…ώΨ≠œΒΆ≥Θ®central nervous systemΘ§CNSΘ©Φ≤≤Γ « άΫγΖΕΈßΡΎΒΡ÷ς“ΣΫΓΩΒΈ Χβ÷°“ΜΘ§”»Τδ «Ρ‘Ήδ÷–ΓΔΡ‘Α©ΓΔ…ώΨ≠ΆΥ–––‘Φ≤≤ΓΒ»ΓΘΡΩ«ΑΘ§’β–©Φ≤≤ΓΜΙΟΜ”–––÷°”––ßΒΡ÷ΈΝΤΖΫΖ®Θ§ΨΩΤδ÷ς“Σ‘≠“ρ÷°“Μ «¥σΕύ ΐ“©ΈοΈόΖ®≥δΖ÷¥©Ιΐ―ΣΡ‘ΤΝ’œΘ®blood-brain barrierΘ§BBBΘ©ΓΘ“ρ¥ΥΘ§ΩΥΖΰ¥Υ…ζΈο’œΑ≠»‘»Μ «ΩΣΖΔCNS“©ΈοΒΡ÷ς“ΣΧτ’ΫΓΘBBBΒΡΜυ±ΨΉι≥…≤ΩΖ÷ «…ώΨ≠―ΣΙήΒΞ‘ΣΘ®neurovascular unitΘ§NVUΘ©Θ§÷ς“Σ”…Ρ‘ΟΪœΗ―ΣΙήΡΎΤΛœΗΑϊΚΆΡ‘–«–ΈΫΚ÷ œΗΑϊΙΙ≥…ΓΘ¥ΥΆβΘ§ΤδΥϊœΗΑϊ“≤”–÷ζ”ΎBBBΒΡ–Έ≥…ΚΆΈ§≥÷Θ§Αϋά®…ώΨ≠‘ΣΓΔ…ΌΆΜœΗΑϊΓΔ–ΓΫΚ÷ œΗΑϊΚΆΖ ¥σœΗΑϊΒ»ΓΘ»ΜΕχΘ§”κ¥φ‘Ύ”ΎCNSΆβΒΡ¥σΕύ ΐΤςΙΌ÷–ΒΡΗΏ…χΆΗ–‘¬ωΙήœΒΆ≥≤ΜΆ§Θ§BBB±μœ÷≥ωΗΏΒΡΩγΡΎΤΛΒγΉηΘ®transendothelial electrical resistanceΘ§TEERΘ©“‘ΦΑΒΆΒΡΉΣΑϊ¬ ΚΆœΗΑϊ≈‘…χΆΗ–‘ΓΘ―–ΨΩ±μΟςΘ§’βΕΦ «”…”ΎΫτΟήΝ§Ϋ”Θ®tight junctionΘ§TJΘ©ΒΑΑΉΗ¥ΚœΈοΙΙ≥…ΒΡΡΛΡΎΩ≈ΝΘ–Έ≥…ΒΡΝ¥Άχ¬γœύΕ‘”––ßΒΊΕ¬»ϊΝΥΡ‘ΈΔ―ΣΙήΡΎΤΛœΗΑϊΘ®cerebral microvascular endothelial cellΘ§BMECΘ©÷°ΦδΒΡœΗΑϊ≈‘Ά®¬ΖΓΘΗΟΫαΙΙΥδ»ΜΉη÷ΙΝΥ”–ΕΨΈο÷ Μρ≤Γ‘≠ΧεΫχ»κCNSΘ§ΒΪ“≤œ‘÷χœό÷ΤΝΥ÷ΈΝΤΚΆ’οΕœ“©ΈοΫχ»κ¥σΡ‘ΒΡΩ…Ρή–‘ΓΘ¥ΥΆβΘ§BBBΡΎΤΛœΗΑϊ÷–¥φ‘ΎΒΡATPΫαΚœΚ–ΉΣ‘ΥΧεΘ®ABCΉΣ‘ΥΧεΘ©ΫΪ“Μ–©Ω…Ρή¥©ΙΐBBBΒΡΜ·ΚœΈοΆβ≈≈ΜΊ―Σ“ΚΘ§Ϋχ“Μ≤Ϋœό÷ΤΝΥCNS÷–“©ΈοΚΆ≥…œώΧΫ’κΒΡΩ…”Ο–‘ΓΘ“ρ¥ΥΘ§÷Μ”–ΦΪ…Ό ΐΒΡΖ÷Ή”±Μ”––ßΒΊ δΥΆΒΫ¥σΡ‘ΓΘ
ΈΣΝΥΩΥΖΰœό÷Τ“©Έο δΥΆΒΫ¥σΡ‘ΒΡ…ζΈοΤΝ’œΘ§―–ΨΩ’Ώ“―Ψ≠≥Δ ‘ΩΣΖΔΝΥΕύ÷÷≤Ώ¬‘ΓΘΤδ÷–Θ§“Μ÷÷ΨΏ”–«ΑΨΑΒΡΗχ“©≤Ώ¬‘“ΐΤπΝΥ―–ΨΩ’ΏΟ«ΒΡΙψΖΚΙΊΉΔΓΘΗΟ≤Ώ¬‘ τ”Ύ“Μ÷÷Ζ««÷»κΗχ“©ΖΫ ΫΘ§“‘Ρ‘Α–œρκΡΉςΈΣ‘ΊΧεΘ§ΫΪ“©Έο“‘Μ·―ßΦϋΒΡΖΫ Ϋ”κΡ‘Α–œρκΡ≈ΦΝΣΘ§Ρ‘Α–œρκΡΩ…“‘¥©ΙΐBBBΘ§ΫΪ“©Έο¥χ»κΡ‘ Β÷ Θ§¥”Εχ¥οΒΫ÷ΈΝΤΒΡΡΩΒΡΓΘΤδΫαΙΙ”κΉς”ΟΜζ÷ΤΨυ”κΩΙΧε≈ΦΝΣ“©ΈοΘ®antibody drug conjugatesΘ§ADCΘ©œύΥΤΘ§ΨΏΧεΫαΙΙΦϊΆΦ1AΓΘ
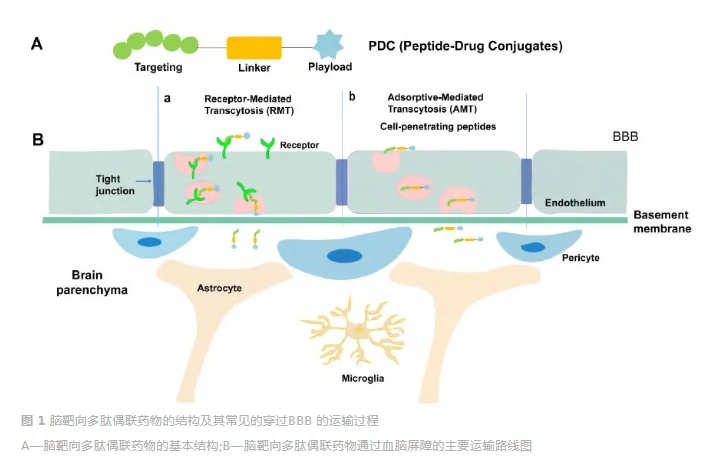
ΒΪ”κADCœύ±»Θ§Ρ‘Α–œρκΡ≈ΦΝΣ“©Έο”…”ΎΕύκΡΉ‘…μΒΡΧΊ–‘ΕχΨΏ”–Ζ÷Ή”ΝΩΗϋΒΆΘ§“Ή”Ύ¥σΙφΡΘΚœ≥…Θ§≥…±ΨΗϋΒΆΘ§¥©ΆΗBBBΡήΝΠΗϋΚΟ«“ΒΆΟβ“Ώ‘≠–‘Β»”≈ΒψΘ§Φϊ±μ1ΓΘ”…¥ΥΩ…ΦϊΘ§Ρ‘Α–œρκΡ≈ΦΝΣ“©Έο‘ΎΨΪΉΦ÷ΈΝΤ…œ“―±μœ÷≥ωΨό¥σ«±ΝΠΓΘ±ΨΈΡΫΪΕ‘Ρ‘Α–œρΕύκΡ≈ΦΝΣ“©ΈοΗςΫαΙΙΉςΦρΒΞΒΡΫι…ήΘ§≤ΔΉήΫα“Μ–©≥ΘΦϊΒΡΡ‘Α–œρΕύκΡ≈ΦΝΣ“©ΈοΘ§“‘ΦΑ¥Υάύ“©ΈοΟφΝΌΒΡΧτ’ΫΚΆΗΡΫχΒΡΖΫΖ®ΓΘ

1 Ρ‘Α–œρκΡ≈ΦΝΣ“©ΈοΒΡΫαΙΙ
1.1 Ρ‘Α–œρκΡ
Α–œρ≤ΩΖ÷‘ΎΡ‘Α–œρκΡ≈ΦΝΣ“©Έο÷–ΤπΉ≈÷ΝΙΊ÷Ί“ΣΒΡΉς”ΟΓΘ Ήœ»Θ§ΥϋΆ®ΙΐΕ‘“©ΈοΒΡ–ό ΈΘ§Ω…“‘ΗΡ±δ“©ΈοΒΡάμΜ·–‘÷ Θ§‘ωΦ”“©ΈοΒΡΈϋ ’ΘΜΤδ¥ΈΘ§ΥϋΩ…“‘ΫΪ“©Έο δΥΆΒΫ÷ΗΕ®≤ΩΈΜΘ§ΧαΗΏ―Γ‘ώ–‘Θ§ΫΒΒΆΕΨΗ±Ής”ΟΘ§‘ωΦ”ΝΤ–ßΓΘ”…¥ΥΩ…“‘Ω¥≥ωΘ§Ρ‘Α–œρκΡΕ‘“©ΈοΒΡΝΤ–ßΓΔ“©¥ζΕ·ΝΠ―ßΚΆ÷ΈΝΤ÷Η±ξΕΦ”–œ‘÷χ”ΑœλΓΘ“ρ¥ΥΘ§―Γ‘ώ“ΜΗωΚœ ΒΡΕύκΡ «÷ΝΙΊ÷Ί“ΣΒΡΓΘάμœκΒΡΡ‘Α–œρκΡ”ΠΨΏ”–Ϋœ«ΩΒΡΡΩ±ξΫαΚœ«ΉΚΆΝΠΓΔΗΏΈ»Ε®–‘ΓΔΒΆΟβ“Ώ‘≠–‘ΓΔΗΏ–ßΡΎΜ·ΚΆΫœ≥ΛΒΡ―ΣΫ§ΑκΥΞΤΎΒ»ΧΊΒψΓΘ
Ά®≥Θ―Γ‘ώΒΡΡ‘Α–œρκΡΈΣΑ–œρ¥σΡ‘ΡΎΧΊΕ® ήΧεΒΡΕύκΡΓΘ’βάύΕύκΡΩ…“‘Ά®Ιΐ ήΧεΫιΒΦΒΡΑϊΆΧΉς”ΟΘ®receptor-mediated transcytosisΘ§RMTΘ©ΧΊ“λ–‘…ψ»ΓΡ≥–©¥σΖ÷Ή”Θ§ΤδΨΏΧεΙΐ≥Χ»γΆΦ1BΥυ ΨΓΘ≥ΘΦϊΒΡΑ–œρ¥σΡ‘ΡΎΧΊΕ® ήΧεΒΡΕύκΡΦϊ±μ2ΓΘ

Ψί―–ΨΩΘ§“Μ÷÷’κΕ‘»ιœΌΑ©ΜΦ’ΏΑ©œΗΑϊΡ‘ΉΣ“Τ«ιΩωΒΡΡ‘Α–œρκΡ≈Φ“©ΈοANG4043“―Ψ≠±ΜΚœ≥…Θ§Φ¥Angiopep-2ΕύκΡ≈ΦΝΣ«ζΆΉ÷ιΒΞΩΙΓΘ«ζΆΉ÷ιΒΞΩΙΩ…“‘Α–œρ»Υ±μΤΛ…ζ≥Λ“ρΉ” ήΧε2Θ®human epidermal growth factor receptor-2Θ§HER2Θ©ΒΡΑϊΆβΫαΙΙ”ρΘ§ ΙHER2―τ–‘»ιœΌΑ©ΜΦ’ΏΒΡ…ζ¥φ¬ œ‘÷χΧαΗΏΓΘΒΪΒ±Α©œΗΑϊΉΣ“ΤΒΫ¥σΡ‘ΡΎ ±Θ§”…”ΎΤδΡ‘…χΆΗΡήΝΠ≤νΘ§ΥϋΨΆ»±ΖΠΝΤ–ßΓΘ“ρ¥ΥΘ§―–ΨΩ’Ώ―Γ‘ώΑ–œρΒΆΟήΕ»÷§ΒΑΑΉ ήΧεœύΙΊΒΑΑΉ1Θ®low-density lipoprotein receptor-related proteins1Θ§LRP1Θ©ΒΡΕύκΡAngiopep-2Θ§”κ«ζΆΉ÷ιΒΞΩΙ≈ΦΝΣΓΘLRP1 «ΒΆΟήΕ»÷§ΒΑΑΉΘ®Low Density LipoproteinΘ§LDLΘ© ήΧεΦ“ΉεΒΡ“Μ‘±Θ§‘ΎBBBΟΪœΗ―ΣΙήΡΎΤΛœΗΑϊ…œΗΏΕ»±μ¥οΘ§≤Δ“―±Μ÷ΛΟς‘ΎΡ‘ΟΪœΗ―ΣΙήΡΎΤΛœΗΑϊ÷–ΉΣ‘ΥΕύ÷÷≈δΧεΘ§Αϋά®»ιΧζΒΑΑΉΘ®lactoferrinΘ§LFΘ©ΓΔ‘Ί÷§ΒΑΑΉEΘ®apolipoprotein EΘ§ApoEΘ©ΚΆΠ¬-ΒμΖέ―υκΡΒ»ΓΘΗΟΕύκΡ≈ΦΝΣ“©ΈοΦ»±ΘΝτΝΥΕ‘HER2 ήΧεΒΡΧεΆβΫαΚœ«ΉΚΆΝΠΚΆΕ‘HER2―τ–‘BT-474»ιœΌΒΦΙήΑ©œΗΑϊΒΡΩΙ‘ω÷≥–ßΝΠΘ§”÷‘ωΦ”ΝΥΡ‘ΡΎΤΛœΗΑϊΒΡΈϋ ’ΓΘ¥ΥΆβΘ§≤βΝΩΨ±Ε·¬ωΡΎΒίΥΆΚσΒΡΡ‘±©¬ΕΥ°ΤΫΘ§ΖΔœ÷ΗΟΕύκΡ≈ΦΝΣΈο“‘1.6ΓΝ10-3mL/(gΓΛs)ΒΡΡ‘Ϋχ»κ¬ ¥©ΆΗ―ΣΡ‘ΤΝ’œΓΘΉνΚσΘ§‘ΎΡ‘ΡΎ“λ÷÷“Τ÷≤BT-474œΗΑϊΒΡ–Γ σΡΘ–Ά÷–Θ§±μΟςΗχ”ηANG4043÷ΈΝΤΚσΩ…Οςœ‘ΧαΗΏ…ζ¥φ¬ ΓΘΥυ“‘Θ§’βœν―–ΨΩ±μΟςAngiopepe-2”κΩΙHER2ΒΞΩΙΒΡΫαΚœΩ…“‘‘ωΦ”Ρ‘ΡΎΤΛœΗΑϊΒΡΈϋ ’“‘ΦΑBBBΒΡΆ®ΆΗ–‘ΓΘANG4043ΒΡ’β–©ΧΊ’ςΒΦ÷¬BT-474Ρ‘÷ΉΝω±©¬ΕΥ°ΤΫΫœΗΏΘ§Ω…“‘‘Ύ»Ϊ…μ÷ΈΝΤΚσ―”≥Λ…ζ¥φΤΎΓΘΦ»Άυ―–ΨΩ±μΟςΩώ»°≤Γ≤ΓΕΨΧ«κΡΘ®RVGΘ© «”…Ωώ»°≤Γ≤ΓΕΨGΒΑΑΉ÷–ΒΡ29ΗωΑ±ΜυΥαΉι≥…ΒΡΕύκΡΤ§ΕΈΓΘRVGκΡΉςΈΣΧΊ“λ–‘≈δΧεΘ§Ω… Ε±πΠΟ-ΜυΕΓΥαΘ®ΠΟ-aminobutyric acidΘ§GABAΘ©ΚΆ―ΧΦν““θΘΒ®Φν ήΧεΘ®nAchRΘ§Nicotinic acetylcholine receptorΘ©Θ§¥ΌΫχ≤ΓΕΨΉΣ‘Υ÷ΝCNSΓΘ“ρ¥ΥΘ§RVGκΡ≥Θ≥Θ”Ο”Ύ–ό Έ“©ΈοΒίΥΆœΒΆ≥Θ§“‘ΧαΗΏ“©ΈοΡ‘ΡΎΒίΥΆ–߬ ΓΘTHR «Ά®Ιΐ …ΨζΧε’Ι ΨΦΦ θ…Η―Γ≥ωΒΡ12ΨέΧεΕύκΡΘ§Ω…Ά®Ιΐ”κΉΣΧζΒΑΑΉ ήΧεΘ®TfRΘ©ΫαΚœΘ§ΆΗΙΐBBBΘ§‘Υ δΫπΡ…ΟΉΝΘΒΫ¥οCNSΓΘ’β–© ΐΨίΫχ“Μ≤Ϋ―ι÷ΛΝΥΡ‘Α–œρΕύκΡ“©Έο≈ΦΝΣ≤Ώ¬‘Ω…“‘ΉςΈΣ…ώΨ≠÷ΉΝω―ßΚΆΤδΥϊ÷– ύ…ώΨ≠…ώΨ≠œΒΆ≥Φ≤≤ΓΒΡ÷ΈΝΤ–¬ΖΫΖ®ΓΘ
Ρ≥–©œΗΑϊ¥©ΆΗκΡΘ®cell-penetrating peptidesΘ§CPPsΘ©“≤≥ΘΉςΈΣCNS“©ΈοΒΡΒίΥΆ‘ΊΧεΓΘCPPs÷Η“ΜΑψ≤Μ≥§Ιΐ30ΗωΑ±ΜυΥαΒΡΕύκΡΓΘΆ®≥Θ±μœ÷≥ω”–÷ζ”ΎΩγœΗΑϊΡΛΉΣ‘ΥΒΡΝΫ«Ή–‘ΚΆΨΜ’ΐΒγΚ…ΧΊ’ςΓΘΥϋΟ«ΫωΆ®Ιΐ”걩¬ΕΒΡœΗΑϊΡΛœύΜΞΉς”ΟΘ§±ψΩ…ΕάΝΔΒΊΫχ»κœΗΑϊΘ§ΤδΜζ÷ΤΩ…ΡήΈΣΈϋΗΫΫιΒΦΒΡΑϊΆΧΉς”ΟΘ®Adsorptive-mediated transcytosisΘ§AMTΘ©Θ§ΨΏΧεΙΐ≥Χ»γΆΦ1BΥυ ΨΓΘ’β «“Μ÷÷Ζ«ΧΊ“λ–‘ΑϊΆΧΉς”ΟΘ§”…Ρ≥–©¥σΖ÷Ή”ΒΡ¥χ’ΐΒγ≤ΩΖ÷”κΚ§”–“θάκΉ”ΗΈΥΊΒΑΑΉΕύΧ«ΒΡΡ‘ΡΎΤΛœΗΑϊ¥χΗΚΒγΒΡΡΛ÷°ΦδΒΡΨ≤ΒγœύΜΞΉς”Ο¥ΞΖΔΓΘ¥ΥΆβΘ§ΥϋΟ«”…”ΎΨΏ”–ΗΏœΗΑϊ…χΆΗ–‘ΚΆΒΆΟβ“Ώ‘≠–‘ΒΡΧΊΒψΘ§“≤±μœ÷≥ω≤Μ“άάΒ”Ύ ήΧεΒΡΧΊ’ςΓΘ’β“≤ «ΥϋΟ«±Μ»œΈΣ «Α≤»ΪΒΡΚΆΗΏ–ßΒΡ‘≠“ρΓΘΒΪ¥ΥάύΕύκΡΆυΆυ»±ΖΠ“ΜΕ®ΒΡ―Γ‘ώ–‘ΓΘ≥ΘΦϊΒΡœύΙΊœΗΑϊ¥©ΆΗκΡΦϊ±μ3ΓΘ

»γTATΕύκΡ «ά¥Ή‘»Υάύ“Ώ»±œί≤ΓΕΨ1–ΆΘ®human immunodeficiency virusΘ§HIV-1Θ©ΒΡΉΣ¬ΦΦΛΜνΈοTATΒΑΑΉΒΡΉΣΒΦΫαΙΙ”ρΓΘΥϋΩ…“‘≈ΦΝΣ“λ‘¥ΒΑΑΉ÷ ΜρΡ…ΟΉΝΘΒ»Θ§ ΙΤδΆΗΙΐBBBΓΘΝμΆβΘ§ΥϋΜΙΩ…“‘‘ΥΥΆΝΩΉ”Βψ¥©ΙΐBBBΒΫ¥οΡ‘ Β÷ ΓΘLiuΒ»‘Ύ‘ΊΜΖ±ϊ…≥–«ΒΡΡ…ΟΉΫΚ χ±μΟφ≈ΦΝΣTATΕύκΡΘ§ΫαΙϊœ‘ Ψ≈ΦΝΣTATΕύκΡΘ§Ω…“‘ ΙΗΟΫΚ χ¥©ΙΐBBBΘ§¥”Εχ‘ω«ΩΝΥ»Υ–«–ΈΫΚ÷ œΗΑϊΕ‘ΫΚ χΒΡ…ψ»ΓΓΘSynB1ΉςΈΣ“Μ÷÷ά¥Ή‘”ΎΩΙΨζκΡΒΑΑΉ1ΒΡ‘ΊΧε≤ΡΝœΘ§‘ΎΒίΥΆ“©ΈοΆΗΙΐBBBΖΫΟφ“―œ‘ Ψ≥ω“ΜΕ®”≈ ΤΓΘ”– Β―ι±μΟςSynB1‘Ύ≤Μ”ΑœλBBBΆξ’ϊ–‘ΒΡ«ιΩωœ¬Θ§Ω…“‘œ‘÷χ‘ω«Ω¥σΡ‘÷–ΒΡ¬πΖ»-6-ΤœΧ«»©ΥαθΞΘ®M6GΘ§Morphin-6-GlucuronidΘ©ΒΡΚ§ΝΩΓΘ
1.2 Ν§Ϋ”ΜυΆ≈
ΆξΟάΒΡΕύκΡ≈ΦΝΣ“©Έο÷Μ”–‘ΎΒΫ¥ο÷ΗΕ®≤ΩΈΜΚσ≤≈Μα ΆΖ≈“©ΈοΘ§ΕχΝ§Ϋ”ΜυΆ≈‘Ύ’βΖΫΟφœ‘ΒΟ”»ΈΣ÷Ί“ΣΓΘΦ¥“ΜΒ©ΕύκΡ≈ΦΝΣ“©ΈοΒΫ¥οΡΩ±ξΚσΘ§Ν§Ϋ”ΜυΆ≈±ΜΝ―ΫβΘ§“©Έο“‘Άξ»ΪΜν–‘Ή¥Χ§ ΆΖ≈ΓΘΥυ“‘Θ§Ν§Ϋ”ΜυΆ≈‘Ύ―≠ΜΖ ±±Ί–κΈ»Ε®Θ§”≈œ»‘ΎΡΩ±ξ≤ΩΈΜΝ―ΫβΘ§¥”Εχ»Ζ±ΘΉν¥σΦΝΝΩ“©ΈοΒΫ¥οΡΩ±ξΓΘ»ΜΕχΘ§¥σΕύ ΐΝ§Ϋ”ΜυΆ≈‘Ύ»Ϊ…μΗχ“©ΚσΘ§¥”Ϋχ»κ―Σ“ΚΡ«“ΜΩΧΩΣ ΦΨΆ±ΜΝ―ΫβΘ§Β±ΒΫ¥ο÷ΗΕ®≤ΩΈΜΚσΘ§Υυ Θ≤ΜΕύΒΡ“©Έο≤≈±ΜœΗΑϊΈϋ ’ΓΘ“ρ¥ΥΘ§…ηΦΤΕύκΡ≈ΦΝΣ“©Έο―Γ‘ώΝ§Ϋ”ΜυΆ≈ ±Θ§ΈΣ±ήΟβΗ…»≈ΕύκΡ”κΤδ ήΧεΒΡΫαΚœ«ΉΚΆΝΠΦΑ“©–ßΘ§–η“ΣΩΦ¬«ΒΫΤδΥυ‘ΎΒΡΈΔΜΖΨ≥Θ§»γΤδ≥ΛΕ»ΓΔΈ»Ε®–‘ΓΔ ΆΖ≈Μζ÷ΤΓΔΙΌΡήΆ≈ΓΔ«ΉΥ°–‘/ ηΥ°–‘ΚΆΤδΥϊΧΊ–‘ΓΘΡΩ«ΑΘ§ΕύκΡ≈ΦΝΣ“©ΈοΒΡΝ§Ϋ”ΜυΆ≈Ζ÷ΈΣΩ…Ν―ΫβΜυΆ≈ΚΆ≤ΜΩ…Ν―ΫβΜυΆ≈Θ®ΕΓΕΰθΘΝρΟ―ΓΔκΩΚΆ»ΐΏρΒ»Θ©ΝΫ¥σάύΓΘΩ…Ν―ΫβΜυΆ≈”÷Ζ÷ΈΣpHΟτΗ––ΆΘ®Υθ»©Θ§ΆΣΚΆΧΦΥαθΞΘ©ΓΔΟΗΟτΗ––ΆΘ®θΞΟΗΚΆθΘΑΖΟΗΓΔΑ±ΜυΦΉΥαθΞΘ©ΓΔ―θΜ·ΜΙ‘≠ΟτΗ––ΆΘ®ΕΰΝρΦϋΘ©»ΐ¥σάύΓΘ
‘ΎΕύκΡ≈ΦΝΣ“©Έο»Ϊ…μΗχ“©ΚσΘ§Ήν≤ΜΈ»Ε®ΒΡΈΜΒψ Ήœ»±ΜΝ―ΫβΘ§Τδ¥Έ «ΤδΥϊΈΜΒψΘ§Ήν÷’≥…ΈΣΑϋά®Έ¥ΗΡ–‘“©ΈοΓΔΨΏ”–≤ΩΖ÷Ν§Ϋ”ΜυΆ≈ΒΡ“©ΈοΜρ¥χ”–Ν§Ϋ”ΜυΆ≈ΒΡΑ±ΜυΥα‘ΎΡΎΒΡΜλΚœΈοΓΘΥδ»Μ‘ΎΑ–œρ÷ΈΝΤ“©ΈοΒΡΩΣΖΔ÷–Θ§Ω…Ν―ΫβΒΡΝ§Ϋ”ΜυΆ≈±»≤ΜΩ…Ν―ΫβΒΡΝ§Ϋ”ΜυΆ≈Ηϋ ή«ύμυΓΘΒΪ≤ΜΩ…Ν―ΫβΜυΆ≈ΨΏ”–≤ΜΜα“ρΆβ≤Ω¥ΧΦΛΕχ±ΜΝ―ΫβΘ®»γΜ·―ß”’ΒΦΒΡ¥ΧΦΛΘ©ΒΡ”≈ΒψΘ§“ρΕχ‘Ύ―≠ΜΖ÷–ΨΏ”–ΗϋΗΏΒΡΈ»Ε®–‘Θ§Ι ΤδΩ…Ρή≤ΜΜαœώΩ…Ν―ΫβΜυΆ≈Ρ«―υ‘Ύ―Σ“Κ÷–ΨΆ±ΜΝ―ΫβΘ§≤Δ‘ΎΒΫ¥οΡΩ±ξ≤ΩΈΜ÷°«Α‘Ύ―Σ“Κ÷–Ιΐ‘γ ΆΖ≈“Μ–©“©ΈοΓΘ“ρ¥ΥΘ§Ρ‘Α–œρΕύκΡΚΆ“©ΈοΒΡΨΏΧεΝ§Ϋ”ΖΫ ΫΘ§”ΠΗυΨί ΒΦ –η«σ»ΖΕ®ΓΘΡ‘ΫΚ÷ Νω «Ήν≥ΘΦϊΚΆΉν÷¬ΟϋΒΡ‘≠ΖΔ–‘Εώ–‘Ρ‘÷ΉΝωΓΘ”…”Ύ¥φ‘Ύ“©Έο»ήΫβ–‘≤νΓΔ»±ΖΠ÷ΉΝω―Γ‘ώ–‘ΓΔ¥©ΙΐBBBΒΡ…χΆΗ–‘≤νΓΔ“‘ΦΑΙψΖΚΒΡ÷ΉΝωΡΎΚΆ÷ΉΝωΦδ“λ÷ –‘Β»Φ§ ÷Έ ΧβΘ§¥σΕύ ΐ÷ΈΝΤ‘ΎΝΌ¥≤…œΆυΆυ“‘ ßΑήΗφ÷’ΓΘΒΪ“Μ÷÷÷Μ‘ΎCNS÷–±μ¥οΒΡœΗΑϊΆβΜυ÷ Θ®extracellular matrixΘ§ECMΘ©Χ«ΒΑΑΉΘ§≥ΤΈΣbrevicanΘ®BcanΘ©Θ§±ΜΖΔœ÷‘ΎΡ‘ΫΚ÷ Νω÷–±μœ÷ΈΣ…œΒςΘ§≤Δ”κ÷ΉΝω«÷œ°–‘ΚΆ«÷œ°–‘‘ωΦ””–ΙΊΓΘΤδ±Μ≥ΤΈΣdg-BcanΒΡ»ΞΧ«ΜυΜ·―«–ΆΫω‘Ύ»ΥάύΗΏΦΕ±πΫΚ÷ ΝωΘ®Αϋά®ΫΚ÷ ΝωΘ©Ήι÷·―υ±Ψ÷–ΖΔœ÷Θ§≤Δ‘Ύ’ϊΗω÷ΉΝωΉι÷·÷–±μ¥ο≥ω÷ΉΝωΧΊ“λ–‘ΚΆ“Μ÷¬–‘ΓΘ’β«ΩΒςΝΥΤδΉςΈΣ“Μ÷÷–¬–ΆΫΚ÷ ΝωΧΊ“λ–‘±ξΦ«Έο“ρΕχΨΏ”–ΩΣΖΔ–¬ΒΡΑ–œρ“©ΈοΒΡ«±ΝΠΓΘ”Ύ «Θ§―–ΨΩ’Ώ…Η―ΓΝΥ“ΜΗωΟϊΈΣBTP-7Α–œρκΡΘ§ΗΟκΡ‘Ύ―Σ«ε÷–Έ»Ε®Θ§Ω…“‘¥©ΙΐBBBΘ§ΧΊ“λ–‘ΫαΚœdg-BcanΓΘ”Ύ «Θ§ΨΆΫΪΗΟΕύκΡ”κœ≤ ςΦνΘ®camptothecinΘ§CPTΘ©Ά®ΙΐΕΰΝρΦϋ≈ΦΝΣΘ§ΒΟΒΫΕύκΡ≈ΦΝΣ“©ΈοBTP-7-CPTΓΘ Β―ιΫαΙϊ±μΟςΘ§ΗΟΕύκΡ≈ΦΝΣ“©Έο‘ΎΧεΆβΕ‘ΜΦ’Ώ‘¥–‘Ρ‘ΫΚ÷ ΝωΗ…œΗΑϊ±μœ÷≥ω“÷÷ΤΉς”ΟΘ§‘Ύ»Υ‘¥–‘Ρ‘ΫΚ÷ Νω¬≠ΡΎ“λ÷÷“Τ÷≤Θ®patient-derived tumor xenograftΘ§PDXΘ©–Γ σΡΘ–Ά÷–‘ωΦ”ΝΥΕ‘÷ΉΝω≤ΩΈΜΒΡ“©Έο δΥΆΓΘΕχ«“Θ§”κΫΓΩΒΡ‘Ήι÷·œύ±»Θ§ΗΟΕύκΡ≈ΦΝΣ“©ΈοΜΙ‘ω«ΩΝΥ÷ΉΝωΕΨ–‘Θ§≤Δ―”≥ΛΝΥΕ·ΈοΒΡ…ζ¥φΤΎΓΘΒΪΗΟΜ·ΚœΈο»‘¥φ‘Ύ“Μ–©≤ΜΉψΘ§Υδ»ΜΧλ»ΜBTP-7‘Ύ»Υ―Σ«ε÷–Έ»Ε®≥§Ιΐ12–Γ ±Θ§ΒΪBTP-7-CPTΕύκΡ≈ΦΝΣ“©Έο‘Ύ1–Γ ±ΡΎΆξ»ΪΫΒΫβΘ§’β±μΟς‘ΎΜΙΈ¥ΒΫ¥ο÷ΉΝω≤ΩΈΜ ±Θ§―Σ“Κ÷–ΒΡΕΰΝρΦϋΚήΩ…Ρή“―Ψ≠±ΜΝ―ΫβΓΘ“ρ¥ΥΘ§–η“ΣΧαΗΏΗΟΜ·ΚœΈο‘Ύ―Σ“Κ÷–ΒΡΝ§Ϋ”ΜυΆ≈ΒΡΈ»Ε®–‘ΓΘ
1.3 ”––ß‘ΊΚ…
Ρ‘Α–œρκΡ≈ΦΝΣ“©Έο÷–ΒΡ”––ß‘ΊΚ…Θ§≤Μ÷ΜΨ÷œό”Ύ÷ΈΝΤ“©ΈοΘ§ΜΙΩ…“‘ «‘λ”ΑΦΝΓΘΫΪ“©Έο”κΡ‘Α–œρΕύκΡ≈ΦΝΣΚσΘ§Ω…“‘ΗΡ±δ“©ΈοΒΡάμΜ·–‘÷ Θ§»γ»ήΫβΕ»ΓΔ―Γ‘ώ–‘ΚΆΑκΥΞΤΎΒ»Θ§ Ι“©ΈοΨΏ”–―Γ‘ώ–‘Θ§Ω…“‘ΧαΗΏ‘≠±Ψ“©ΈοΒΡΝΤ–ßΘ§Φθ…ΌΕΨΗ±Ής”ΟΘ§ΗΡ…Τ»ήΫβΕ»Θ§‘ωΦ”Έϋ ’ΓΘ
“‘÷ΈΝΤΡ‘ΫΚ÷ ΝωΈΣάΐΘ§≥Θ”ΟΒΡ «¥ΪΆ≥ΒΡΜ·ΝΤ“©ΈοΘ§»γΉœ…Φ¥ΦΘ®paclitaxelΘ§PTXΘ©ΓΔCPTΜρΑΔΟΙΥΊΘ®doxorubicinΘ§DOXΘ©Β»ΓΘΤδ÷ς“Σ «Ά®ΙΐΗς÷÷Μζ÷Τά¥Ήη÷ΙΑ©œΗΑϊΒΡ”–ΥΩΖ÷Ν―Μρ¥ΌΫχœΗΑϊΒρΆωΘ§¥”Εχ¥οΒΫ÷ΈΝΤΡΩΒΡΓΘ’βάύ“©ΈοΥδ»Μ”–“ΜΕ®ΒΡΝΤ–ßΘ§ΒΪ“≤”–“ΜΕ®ΒΡ»±ΒψΘ§»γΕΨΗ±Ής”Ο¥σΓΔ»ήΫβΕ»≤νΓΘ―Γ‘ώΚœ ΒΡΡ‘Α–œρκΡ≈ΦΝΣΨΆΩ…“‘ΫβΨω’β–©Έ ΧβΓΘ―–ΨΩ’ΏΗυΨίΗΟ≤Ώ¬‘…ηΦΤΝΥPTX≈ΦΝΣΥΪΙΠΡήκΡSynB3ΚΆ–ρΝ–ΈΣPVGLIGΒΡΜυ÷ Ϋπ τΒΑΑΉΟΗ2Θ®Matrix metalloproteinase-2Θ§MMP-2Θ©ΟτΗ–κΡΘ§”Ο”ΎΡ‘ΫΚ÷ ΝωΒΡ÷ΈΝΤΓΘ Β―ιΫαΙϊ±μΟςΘ§1Θ©SynB3-PVGLIG-PTX”κMMP-2±μœ÷≥ωΫœ«ΩΒΡ«ΉΚΆΝΠΘ§ΥϋΩ…“‘Ά®ΙΐΨέΚœ–Έ≥…¥χ’ΐΒγΚ…ΒΡΧΊ βΫαΙΙά¥ΧαΗΏΥ°»ή–‘ΘΜ2Θ©MMP-2Ν―ΫβΚσΘ§SynB3-PVGLIG-PTXΩ…ΩΊ÷Τ ΆΖ≈PTXΘ§’β±μΟςSynB3-PVGLIG-PTXΕ‘ΫΚ÷ ΝωœΗΑϊΨΏ”–ΧΊ“λ–‘ΒΡœΗΑϊΕΨ–‘ΘΜ3Θ©SynB3-PVGLIG-PTX‘ΎΧεΡΎΆβΨυΡή”––ß“÷÷ΤΫΚ÷ ΝωœΗΑϊΒΡ‘ω÷≥ΓΔ«®“ΤΚΆ«÷œ°ΓΘ¥ΥΆβΘ§SynB3-PVGLIG-PTXΒΡ“÷÷Τ¬ œ‘÷χΗΏ”Ύ―τ–‘“©ΧφΡΣΏρΑΖ(TemozolomideΘ§TMZ)ΚΆPTXΘΜ4Θ©ΝΣΚœ Ι”ΟMMP-2ΟτΗ–ΒΡΕύκΡΚΆCPPsΘ®SynB3Θ©Θ§Φ»‘ω«ΩΝΥBBB…χΆΗ–‘Θ§”÷ΧαΗΏΝΥSynB3-PVGLG-PTXΒΡΫΚ÷ ΝωΑ–œρ–ß”ΠΘ§ Ι“©Έο‘Ύ÷ΈΝΤΤΎΦδΨΏ”–ΒΆ≤ΜΝΦΖ¥”ΠΒΡΗΏΩΙ÷ΉΝωΜν–‘ΓΘ≥ΐ¥Υ÷°ΆβΘ§Ρ‘Α–œρκΡ≈ΦΝΣ“©ΈοΜΙΩ…“‘”Ο”Ύœρ÷ΉΝωœΗΑϊ¥ΪΒί–ΓΗ…»≈RNAΘ®siRNAΘ©ΓΘ“ΜΒ©±ΜΑ–œρΘ§siRNAΩ…“‘“÷÷ΤΖ≠“κΚΆΥφΚσΒΡΒΑΑΉ÷ Κœ≥…ΓΘ’β÷÷ΫαΚœ≤Ώ¬‘Θ§ΜΙ”–÷ζ”ΎΕ‘ΩΙΡΆ“©–‘ΓΘ
ΒΪ»γΙϊΡήΙΜ Ι”Ο≤ΜΆ§ΒΡ≥…œώΖΫ ΫΕ‘ΖΔ≤Γ≤ΩΈΜΒΡΫαΙΙΙΠΡή≥…œώΘ§»ΖΕ®≤Γ±δ≤ΩΈΜΚΆΉ¥Χ§Θ§ΨΆΩ…“‘ΗϋΦ”ΨΪΉΦΒΊ’οΕœΚΆ÷ΈΝΤΦ≤≤ΓΓΘάΐ»γΟάΙζ ≥ΤΖΚΆ“©ΈοΙήάμΨ÷Θ®Food And Drug AdministrationΘ§FDAΘ©≈ζΉΦΒΡ ΉΗωΚ§Ζ≈…δ–‘ΚΥΥΊΒΡΕύκΡ≈ΦΝΣ“©Έο111In-DTPA-OctreotideΘ®octrescanΘ©Θ§”Ο”Ύ÷ΈΝΤ…ώΨ≠ΡΎΖ÷ΟΎ÷ΉΝωΓΘ»ΜΕχΘ§―–ΨΩ±μΟςΑ¬«ζκΡΘ®octreotideΘ©…®ΟηΕ‘÷ΈΝΤ÷ΉΝωΒΡΉς”Ο”–œόΘ§“ρ¥ΥΗΟ“©ΈοΨΆ÷ς“Σ”Ο”Ύ’οΕœΓΘΕχ¥σΡ‘ΒΡΫαΙΙΚΆΙΠΡήΗϋΈΣΗ¥‘”Θ§»γΙϊΡήΕ‘Τδ≥…œώΙέ≤λ≤Γάμ…ζάμΉ¥Χ§Θ§Ω…“‘¥οΒΫΗϋΚΟΒΡ÷ΈΝΤ–ßΙϊΓΘΫϋΡξά¥ΈΣΝΥΆ§ ±ΫβΨω“©ΈοΕ®ΈΜΓΔ“©Έο ΆΖ≈ΚΆ“©ΈοΝΤ–ßΒΡœύΙΊΈ ΧβΘ§“―Ψ≠ΧΫΥςΝΥΫΪ“©ΈοΚΆœ‘œώΦΝΉιΚœ‘ΎΖ÷Ή”ΜρΡ…ΟΉΦΕΤΫΧ®…œΒΡΕύ≥…Ζ÷ΫαΙΙΘ§≥ΤΈΣ÷ΈΝΤ’οΕœΦΝΓΘ’β÷÷ΖΫΖ®Θ§”–Άϊœ‘÷χΗΡ…Τ÷ΈΝΤ–ßΙϊ«ΖΦ―ΒΡΡ‘≤ΩΦ≤≤ΓΘ§»γΧεΡΎΖ÷Ή”…ώΨ≠≥…œώΒ»ΓΘBen WoodsΒ»…ηΦΤΝΥ[[99mTcO4]−CPepH3]Η¥ΚœΈοΘ§PepH3ΕύκΡΈΣΡ‘Α–œρκΡΘ§CPepH3ΈΣΩΆΧεΘ§99mTcO4Ζ≈…δ–‘±ξΦ«ΈΣ÷ςΧεΓΘ―–ΨΩ±μΟςΘ§ΗΟΗ¥ΚœΈοΡήΙΜ¥©ΙΐBBBΘ§ΤδΡ‘ΜΐάέΝΩΗΏ”ΎΤδΥϊ”Ο”ΎΡ‘Α–œρ¥ΪΒίΒΡκΡΓΘCPepH3ΫαΙΙ≥ ΝΐΉ¥ΫαΙΙΘ§ΗΟΝΐΉ¥÷ßΦήΩ…“‘ Ι”Ο≤ΜΆ§ΒΡΦΦ θΫχ––’ΐΫΜ≥…œώΘ§»γΈΣ’ΐΒγΉ”ΖΔ…δΕœ≤ψ…®Οη≥…œώ θΘ®Positron Emission TomographyΘ§PETΘ©…ηΦΤΒΡΩΆΧεΝΐΚΆΈΣ¥≈Ι≤’ώ≥…œώΘ®magnetic resonance imagingΘ§MRIΘ©…ηΦΤΒΡ÷ςΧεΝΐΒ»ΓΘΆ§―υΘ§’β–©≥§Ζ÷Ή”Ϋπ τΜυΫαΙΙΒΡΦαΙΧ–‘ΚΆΡΘΩιΜ·Ήι≥…Ω…“‘“ΐ»κΑ–œρ≤ΩΖ÷Θ§»γΕύκΡΜρΩΙΧεΒ»ΓΘΡΩ«ΑΘ§ΗΟ Β―ι “’ΐ‘ΎΧΫΥς Βœ÷ΨΏ”–≤ΜΆ§ΙΠΡήΒΡ“λ÷ ΝΐΘ§Ά§ ±ΖβΉΑΩΙΑ©“©Έο‘ΎΡΎΘ§»γΥ≥≤§Β»ΓΘ
2≥ΘΦϊΒΡΡ‘Α–œρκΡ≈ΦΝΣ“©Έο
2.1 ANG1005(GRN1005)
ANG1005 «”…“ΜΖ÷Ή”Angiopep-2ΕύκΡΚΆ»ΐΖ÷Ή”ΒΡPTXΆ®ΙΐΩ…Ν―ΫβΒΡγζγξθΘθΞ≈ΦΝΣΕχ≥…ΒΡΘ§Angiopep-2“‘LRP-1ΈΣΑ–ΒψΘ§ ΙΤ䥩Ιΐ―Σ-Ρ‘ΦΙ“ΚΤΝ’œΘ®Blood-Cerebrospinal fluid BarrierΘ§BCBΘ©ΚΆBBBΘ§Ϋχ»κ÷ΉΝωœΗΑϊΘ§‘Ύ÷ΉΝωœΗΑϊ÷–Ν―Ϋβ≥ωPTX“‘ΖΔΜ”ΤδΩΙ÷ΉΝωΜν–‘ΓΘ‘≠ΈΜΡ‘ΙύΉΔ Β―ιœ‘ ΨΘ§ANG1005Ϋχ»κ¥σΡ‘ΒΡΝΩ±»PTXΗϋ¥σΘ§≤Δ«“Ω…“‘»ΤΙΐBBB…œΒΡP-Χ«ΒΑΑΉΘ®P-glycoproteinΘ§P-gpΘ©ΓΘΧεΆβ Β―ι÷ΛΟςANG1005Ε‘»ΥάύΑ©œΗΑϊ÷ξΒΡΩΙ÷ΉΝω–ßΝΠ”κPTXœύΥΤΘΜΧεΡΎ Β―ι÷ΛΟςANG1005Ε‘»Υ÷ΉΝω“λ÷÷“Τ÷≤ΒΡ“÷÷ΤΉς”Ο±»PTXΗϋ”––ßΘ§Ω…œ‘÷χΧαΗΏΡ‘ΡΎ÷≤»κU87MGΫΚ÷ ΡΗœΗΑϊΝωœΗΑϊΜρNCI-H460ΖΈΑ©œΗΑϊΒΡ–Γ σΒΡ¥φΜν¬ ΓΘ‘ΎIΤΎ―–ΨΩ÷–Θ§ΒΞ¥ΈΨ≤¬ωΉΔ…δΗΟΕύκΡ≈ΦΝΣ“©ΈοΘ§‘Ύ3-6–Γ ±Κσ«–≥ΐΒΡΗ¥ΖΔ–‘ΫΚ÷ Νω÷–Ω…“‘Φλ≤βΒΫ÷ΈΝΤ≈®Ε»ΒΡANG1005Θ§’βΈΣΤδΆ®ΙΐBBBΉΣ‘ΥΚΆ÷ΉΝω…χΆΗΧαΙ©ΝΥ”–ΝΠ÷ΛΨίΓΘ‘ΎΗ¥ΖΔ–‘»ιœΌΑ©Ρ‘ΉΣΘ®brain metastases from breast cancerΘ§BCBMΘ©ΓΔΑιΜρ≤ΜΑι”–»μΡ‘ΡΛΑ©÷ΔΘ®leptomeningeal carcinomatosis subsetΘ§LMCΘ©ΒΡIIΤΎΝΌ¥≤―–ΨΩ÷–Θ§ANG1005ΟΩ3÷ήΨ≤¬ωΉΔ…δ600mg/m2Θ§77%¬≠ΡΎΚΆ86%¬≠ΆβΜΦ’ΏΜώ“φΘ§÷ς“Σ±μœ÷ΈΣ≤Γ«ιΈ»Ε®ΜρΗϋΚΟΘΜ‘Ύ»μΡ‘ΡΛΑ©÷Δ÷–Θ§79%ΒΡΜΦ’Ώ¬≠ΡΎΦ≤≤ΓΒΟΒΫΩΊ÷ΤΘ§ΙάΦΤ÷–ΈΜΉή…ζ¥φΤΎΈΣ8.0Ηω‘¬Θ®95%÷Ο–≈«χΦδΘ§5.4~9.4Ηω‘¬Θ©ΓΘ“ΜœνΉΔ≤αΚ≈ΈΣNCT03613181ΒΡIIIΤΎΝΌ¥≤ ‘―ι’ΐ‘ΎΫχ––÷–Θ§ΡΩΒΡ «Ιέ≤λ”κ“Ϋ…ζ―Γ‘ώΒΡΉνΦ―“©Έοœύ±»Θ§ANG1005 «ΖώΩ…“‘―”≥Λ–¬Ϋϋ’οΕœΈΣLMC≤Δ‘χ÷ΈΝΤΙΐΡ‘ΉΣ“ΤΒΡHER2“θ–‘»ιœΌΑ©ΜΦ’ΏΒΡ…ζ¥φΤΎΓΘ
2.2 DA-TP10
≈ΝΫπ…≠≤ΓΘ®Parkinson's diseaseΘ§PDΘ© «“Μ÷÷≥ΘΦϊΒΡΫχ–––‘…ώΨ≠ΆΥ–––‘Φ≤≤ΓΘ§ΒΪ÷ΈΝΤ–ßΙϊ≤Δ≤ΜΆξ»ΪΝν»Υ¬ζ“βΓΘΡΩ«ΑPD÷ΈΝΤΒΡ÷ς“ΣΡ―Βψ÷°“Μ «“©ΈοBBB…χΆΗ–‘Ϋœ≤νΓΘ―–ΨΩ’Ώ…ηΦΤ―Γ”ΟœΗΑϊ¥©ΆΗκΡTP10ΉςΈΣ“©Έο‘ΊΧεΘ§≤…”ΟΓΑclickΓ±Ζ¥”ΠΘ§≈ΦΝΣΕύΑΆΑΖΘ®DopamineΘ§DAΘ©ΓΘ Β―ιΫαΙϊ±μΟςΘ§ΗΟΕύκΡ≈ΦΝΣ“©ΈοΨΏ”–±»DAΗϋΚΟΒΡ“©¥ζΕ·ΝΠ―ßΚΆ“©–ß―ß–‘ΡήΓΘΥϋΩ…¥©ΙΐBBBΘ§Ϋχ»κΡ‘Ήι÷·Θ§Ε‘Ευ≤ηΖ”-O-ΦΉΜυΉΣ“ΤΟΗΒΡO-ΦΉΜυΜ·Ζ¥”ΠΒΡΟτΗ––‘ΫœΒΆΘ§…θ÷ΝΒΆ”ΎDAΘ§Ε‘ΕύΑΆΑΖ1–Ά ήΧεΘ®dopamine receptor1Θ§D1Θ©ΚΆΕύΑΆΑΖ2–Ά ήΧεΘ®dopamine receptor2Θ§D2Θ© ήΧεΒΡ«ΉΚΆΝΠΫœΗΏΘ§»γ‘ΎD1 ήΧεΒΡ«ιΩωœ¬Θ§‘ΕΗΏ”ΎDAΓΘ‘Ύ“©Έο”’ΒΦΒΡPDΝΌ¥≤«ΑΕ·ΈοΡΘ–Ά÷–Θ§”κΉσ–ΐΕύΑΆΘ®L-DOPAΘ©œύ±»Θ§ΩΙ≈ΝΫπ…≠Μν–‘ΗϋΟςœ‘ΓΘ“ρ¥ΥΘ§÷ΈΝΤPDΒΡ“©Έο”κCPPsΒΡΫαΚœΩ…ΡήΜα≥…ΈΣ“Μ÷÷÷ΈΝΤPDΒΡ–¬≤Ώ¬‘ΓΘ
2.3 M6G-Ang
M6G‘ΎΡ‘ΡΎΉΔ…δΚσΒΡ’ρΆ¥–ßΙϊ±»¬πΖ»ΗΏ50±ΕΓΘ»ΜΕχΘ§M6GΒΡΡ‘¥©ΆΗ–‘Οςœ‘ΒΆ”Ύ¬πΖ»Θ§¥”Εχ”ΑœλΝΥΤδΝΤ–ßΓΘ“ρ¥ΥΘ§…ηΦΤΝΥM6G-AngΕύκΡ≈ΦΝΣ“©ΈοΘ§Φ¥1ΗωAngiopep-2ΕύκΡΆ®ΙΐΕΰΝρΦϋ≈ΦΝΣ3ΗωM6GΓΘ Β―ι÷ΛΟςΘ§Ψ≤¬ωΉΔ…δΜρΤΛœ¬ΉΔ…δAn2-M6GΕύκΡ≈ΦΝΣ“©ΈοΘ§”κM6GΓΔ¬πΖ»ΒΞΧεœύ±»Θ§M6G-Ang‘ωΦ”ΝΥBBBΆ®ΆΗ–‘Θ§Τδ±»Ά§Β»ΦΝΝΩΒΡ¬πΖ»ΜρM6GΨΏ”–Ηϋ¥σΓΔΗϋ≥÷ΨΟΒΡ’ρΆ¥Μν–‘Θ§«“An2-M6G±μœ÷≥ωΦθ…Ό±ψΟΊΗ±Ής”ΟΒΡ”≈ΒψΓΘ’β–©ΫαΙϊ±μΟς Ι”ΟΡ‘Α–œρΕύκΡ‘ΊΧεΉςΈΣ“Μ÷÷–¬–ΆΒΡΆΗΙΐBBBΒΡΦΦ θΘ§Ω…”Π”Ο”ΎCNSΦ≤≤ΓΒΡ÷ΈΝΤΓΘ
3ΡΩ«ΑΡ‘Α–œρκΡ≈ΦΝΣ“©ΈοΟφΝΌΒΡΧτ’ΫΦΑΗΡΫχΖΫΖ®
ΨΓΙήΡ‘Α–œρκΡ≈ΦΝΣ“©Έο”–ΚήΕύ”≈ΒψΘ§ΒΪ»‘¥φ‘Ύ“Μ–©Ψ÷œό–‘ΓΘ”…”ΎΤδΖ÷Ή”ΝΩΫœ…ζΈο¥σΖ÷Ή”ΒΆΘ§Έ»Ε®–‘Ϋœ≤νΘ§…ω‘ύΩ…ΩλΥΌ«ε≥ΐΘ§ΑκΥΞΤΎΚΆ―≠ΜΖ÷ήΤΎΫœΕΧΘ§Ω…ΡήΒΦ÷¬“©ΈοΝΤ–ß”–œόΓΘ¥ΥΆβΘ§“ρΈΣΈΗ≥ΠΒά”–Εύ÷÷ΟΗάύΘ§Μα ΙΕύκΡ‘ΎΈΗ≥ΠΒάΡΎΫΒΫβΘ§Ι ¥Υάύ“©Έο≤Μ ΚœΩΎΖΰΗχ“©Θ§≥Θ”ΟΒΡΗχ“©ΖΫ Ϋ «Ψ≤¬ωΉΔ…δΘ§÷¬ ΙΜΦ’Ώ“ά¥”–‘≤νΓΘΡΩ«ΑΘ§―–ΨΩ’Ώ“≤Ά®Ιΐ≤ΜΆ§ΒΡΦΦ θά¥ΩΥΖΰ’β–©Χτ’ΫΓΘ
3.1 Ε‘ΕύκΡΉ‘…μΫαΙΙΒΡ–ό Έ
ΡΩ«ΑΘ§―–ΨΩ’Ώ≥Θ≤…”ΟΜΖΜ·κΡΘ®ΆΖΈ≤ΜΖΜ·ΓΔΕΰΝρΦϋΜΖΜ·Β»Θ©ΓΔΡβκΡΓΔΕ© ικΡΓΔbicycle≤Ώ¬‘ΓΔ”ΟD-Α±ΜυΥα¥ζΧφL-Α±ΜυΥαΒ»Θ§‘ω«ΩΕύκΡΒΡΈ»Ε®–‘Θ§“‘¥Υά¥―”≥ΛΑκΥΞΤΎΓΘRAP12κΡά¥‘¥”Ύ ήΧεœύΙΊΒΑΑΉ(receptor associated proteinΘ§RAP)ΒΡΈΔ–ΆΜ·Θ§”κLRP-1ΨΏ”–ΫαΚœ«ΉΚΆΝΠΓΘ»ΜΕχΘ§Β±ΤδΆ―άκΈ»Ε®ΒΑΑΉΜΖΨ≥ ±Θ§RAP12±μœ÷≥ω»θΒΡΠΝ-¬ί–ΐΤ§ΕΈΓΘΩΦ¬«ΒΫΠΝ-¬ί–ΐΫαΙΙ «ΗΟκΡ÷–ΫιΒΦ≈δΧε- ήΧεœύΜΞΉς”ΟΒΡ≥ΘΦϊΫαΙΙΜυ–ρΘ§―–ΨΩ’Ώάϊ”ΟκΡΈ«ΚœΤςΦΦ θΚœ≥…ΝΥΕ© ικΡstapled RAP12Θ®ST-RAP12Θ©ΓΘΨ≠―ι÷ΛΘ§”κRAP12œύ±»Θ§”≈Μ·ΚσΒΡST-RAP12ΨΏ”–ΗϋΗΏΒΡΠΝ-¬ί–ΐΚ§ΝΩΓΔ”κLRP-1ΒΡΫαΚœ«ΉΚΆΝΠΚΆ―Σ«εΈ»Ε®–‘ΓΘ¥ΥΆβΘ§ST-RAP12±μœ÷≥ωΕ‘bEnd.3œΗΑϊΓΔU87ΫΚ÷ ΝωœΗΑϊΚΆ»ΥΤξΨ≤¬ωΡΎΤΛœΗΑϊΘ®human umbilical vein endothelial cellsΘ§HUVECΘ©ΡΎΜ·‘ω«ΩΓΘΕχ«“Θ§ST-RAP12‘ΎΧεΆβΩΥΖΰBBBΚΆ―ΣΡ‘÷ΉΝωΤΝ’œΘ®blood®Cbrain tumorbarrierΘ§BBTBΘ©ΒΡΡήΝΠ“≤‘ω«ΩΝΥΓΘΫχ“Μ≤Ϋ”Π”ΟST-RAP12κΡ–ό ΈΗΏΖ÷Ή”≤ΡΝœΘ§ΙΙΫ®ST-RAP12ΫΚ χΓΘ Β―ιΫαΙϊ±μΟςΘ§ΗΟΫΚ χ‘ΎΧεΡΎΆβΩ…“‘”––ߥ©ΆΗBBB/BBTB≤ΔΑ–œρΫΚ÷ ΝωΓΘ¥ΥΆβΘ§ST-RAP12ΫΚ χΡή”––ßΒΊœρΫΚ÷ Νω¥ΪΒίPTXΘ§―”≥ΛΫΚ÷ ΝωΚ…Νω–Γ σΒΡ…ζ¥φ ±ΦδΘ§“÷÷Τ÷ΉΝω―ΣΙή…ζ≥…Θ§”’ΒΦΫΚ÷ ΝωœΗΑϊΒρΆωΘ§ΨΏ”–Οςœ‘ΒΡΩΙΫΚ÷ ΝωΉς”ΟΓΘ¥Π”ΎΝΌ¥≤ ‘―ιΫΉΕΈΒΡBT1718Θ§ «”…ΥΪΜΖκΡΆ®ΙΐΩ…Ν―ΫβΒΡΕΰΝρΦϋ”κΟάΒ«ΥΊΘ®mertansineΘ§DM1Θ©≈ΦΝΣΒΟΒΫΒΡΓΘΥΪΜΖκΡΩ…“‘ΧΊ“λ–‘ΫαΚœΡΛ–Ά1Μυ÷ Ϋπ τΒΑΑΉΟΗΘ®MT1-MMPΘ©Θ§MT1-MMP‘Ύ»ιœΌΑ©ΓΔΖΈΑ©ΓΔ¬―≥≤Α©ΓΔΫα≥ΠΑ©Β»Εώ–‘÷ΉΝω÷–Ιΐ±μ¥οΓΘ”κADCœύ±»Θ§BT1718Ζ÷Ή”ΝΩΒΆΘ§Ζ÷≤ΦΝΦΚΟΘ§Ω…ΩλΥΌ¥©ΆΗ≤ΔΓΑ…±ΥάΓ±÷ΉΝωœΗΑϊΘ§Ε‘ΆμΤΎ ΒΧεΝω”–÷ΈΝΤΉς”ΟΓΘ“―”–¥σΝΩ―–ΨΩ±μΟςAngiopep-2–ό ΈΒΡΡ…ΟΉ‘ΊΧεœ‘÷χ‘ωΦ”ΝΥΡ‘Ζ÷≤ΦΓΘWeiΒ»ΙΙΫ®ΝΥAngiopep-2ΒΡΖ¥œρ“λΙΙΧεΘ§ΟϋΟϊΈΣDAngiopep-2Θ§Ϋ®ΝΔΝΥΡ‘Α–œρ“©Έο δΥΆœΒΆ≥ΓΘΥδ»Μ‘ΎΧεΆβ Β―ι÷–Θ§DAngiopep-2±Μ¥σΡ‘ΟΪœΗ―ΣΙήΡΎΤΛœΗΑϊ…ψ»ΓΒΡ–ß¬ ±»LAngiopep-2ΒΆΘ§ΒΪΥϋ±μœ÷≥ωΝΥ‘ω«ΩΒΡΈ»Ε®–‘Θ§≤Δ«“–ό ΈΚσΒΡΫΚ χ±»LAngiopep-2–ό ΈΚσΒΡΫΚ χ‘Ύ’ΐ≥ΘΒΡ¥σΡ‘ΚΆ¬≠ΡΎΫΚ÷ ΡΗœΗΑϊΝωœΗΑϊ÷–ΨΏ”–ΗϋΗΏΒΡΖ÷≤ΦΓΘ
3.2 ”κΜ·―ߥσΖ÷Ή”ΒΡΫαΚœ–ό Έ
ΕύκΡΒΡΒγΚ…“≤”κ“©Έο«ε≥ΐ¬ ”–ΙΊΓΘ¥χΗΚΒγΚ…ΒΡΕύκΡ–ρΝ–±»¥χ’ΐΒγΚ…ΒΡ”–Ηϋ≥ΛΒΡΑκΥΞΤΎΘ§’β «“ρΈΣ…ω–Γ«ρΡΎΡΛ…œ“θάκΉ”ΒγΚ…ΒΡ¥φ‘Ύœό÷ΤΝΥΡρ“Κ÷–“θάκΉ”Μ·ΚœΈοΒΡΙΐ¬ΥΓΘ¥ΥΆβΘ§ΜΙΩ…Ά®Ιΐ‘ωΦ”ΕύκΡΒΡ¥σ–ΓΚΆ―ΣΫ§ΒΑΑΉΫαΚœΘ§“‘Ζά÷ΙΫαΚœΈοΆ®Ιΐ…ω‘ύ±ΜΙΐ¬Υ≥ωά¥ΓΘ”–“Μ÷÷≤Ώ¬‘ «ΫΪΨέ““Εΰ¥ΦΘ®polyethylene glycolΘ§PEGΘ©”κΡ‘Α–œρκΡ“©Έο≈ΦΝΣΘ§Ω…“‘―”≥ΛΑκΥΞΤΎΓΘPEGΒΡΙΧ”––‘÷ ΙΤδ≥…ΈΣΗΡ–‘ΒΡάμœκΚρ―Γ≤ΡΝœΘΚ±ψ“ΥΓΔ«ΉΥ°ΓΔ…ζΈοœύ»ί–‘ΓΔΖ«Οβ“Ώ‘≠–‘ΓΘΥϋ «ΉνΙψΖΚ Ι”ΟΒΡΖ«Χλ»ΜΨέΚœΈο÷°“ΜΘ§”Ο”Ύ‘ωΦ”κΡΒΡ»ήΫβΕ»ΓΔΫΒΒΆΟβ“ΏΖ¥”ΠΚΆΧαΗΏκΡΒΡ…ζΈοάϊ”ΟΕ»ΓΘPEGΨέΚœΈοΖ÷Ή”÷–ΒΡΟΩΗω―θ‘≠Ή”ΕΦΡήΫαΚœΝΫΒΫ»ΐΗωΥ°Ζ÷Ή”Θ§’β―υΜα¥σ¥σ‘ωΦ”ΗΫΉ≈‘ΎΤδ…œΒΡΜ·ΚœΈοΒΡ÷ ΝΩΚΆ»ήΫβΕ»ΓΘFDA“≤≈ζΉΦΝΥΕύ÷÷Ψέ““Εΰ¥ΦΜ·ΒΑΑΉ÷ Θ§»γPEG-≈ΘœΌή’Ά―Α±ΟΗΚΆPEG-ΠΝ-Η…»≈ΥΊΒ»ΓΘΒΪΖ÷Ή”ΝΩ÷Ν…ΌΈΣ30kDaΨέ““Εΰ¥ΦΜ·ΒΡΕύκΡΜαΒΦ÷¬Τδ‘ΎΗς÷÷ΤςΙΌ÷–ΒΡΩ’≈ίΜ·Θ§»γ…ω‘ύΓΔΗΈ‘ύΓΔΤΔ‘ύΓΔΙ«ΥηΒ»ΓΘ“ρ¥ΥΘ§PEGΧλ»ΜΧφ¥ζΤΖ±ΜΩΣΖΔ≥ωά¥ΓΘΉνΆΜ≥ωΒΡΧφ¥ζΤΖ «PASylationΚΆXTENΓΘXTEN «”…±ϊΑ±ΥαΘ®AΘ©ΓΔΙ»Α±ΥαΘ®EΘ©ΓΔΗ Α±ΥαΘ®GΘ©ΓΔΗ§Α±ΥαΘ®PΘ©ΓΔΥΩΑ±ΥαΘ®SΘ©ΚΆΥ’Α±ΥαΘ®TΘ©’βΝυ÷÷Μ·―ßΈ»Ε®Α±ΜυΥαΒΡΖ«÷ΊΗ¥ΥφΜζΤ§ΕΈΉι≥…ΒΡ“≈¥Ϊ»ΎΚœΕύκΡΓΘ’β–©Α±ΜυΥαΒΡ―Γ‘ώ «Μυ”Ύ±ήΟβΩ…Ρή”ΑœλΒΑΑΉ÷ »ήΫβΕ»ΓΔΜν–‘ΜρΈ»Ε®–‘‘≠‘ρΓΘΑ§»ϊΡ«κΡ”κXTEN≈ΦΝΣΩ…œ‘÷χΗΡ…ΤκΡΒΡ“©¥ζΕ·ΝΠ―ßΘ§ΫΪΤδ‘Ύ¥σ σΓΔ–Γ σΜρΚοΉ”ΧεΡΎΒΡΑκΥΞΤΎΖ÷±π―”≥Λ65ΓΔ71Μρ125±ΕΓΘPASylationΜ· «÷ΗΗ§Α±ΥαΘ®PΘ©ΓΔ±ϊΑ±ΥαΘ®AΘ©ΚΆΥΩΑ±ΥαΘ®SΘ©ΒΡΨέΚœΈοΓΘ”…’β–©Α±ΜυΥαΉι≥…ΒΡΨέΚœΈο±Μ»œΈΣΕ‘κΡΒΡΥ°ΝΠΕ·Χ§ΧεΜΐ”κPEG”–άύΥΤΒΡ”ΑœλΘ§≤Δ«“ «Ω……ζΈοΫΒΫβΒΡΘ§“―Ψ≠≥…ΙΠ”Π”Ο”Ύ≥§Ιΐ10÷÷ΒΡΒΎ“Μ¥ζ…ζΈο÷ΤΦΝΘ§Αϋά®»Υάύ…ζ≥ΛΦΛΥΊΓΔ ίΥΊΓΔ¥ΌΚλœΗΑϊ…ζ≥…ΥΊΓΔΑ§»ϊΡ«κΡΓΔΡρΥαΟΗΚΆΡΐ―Σ“ρΉ”Β»ΓΘ
3.3 ΦΝ–Ά–ό Έ
ΈΗ≥ΠΒάΒΡ…ζάμΜζΡήΉηΑ≠ΝΥ¥σΕύ ΐΩΎΖΰΒΑΑΉ÷ ÷ΤΦΝΒΡΝΌ¥≤ΉΣΜ·ΓΘΈΗ÷–Κ§”–¥ΧΦΛ–‘ΒΡΥαΚΆΟΗΘ§ΈΣΝΥ»Ζ±Θ“©ΈοΖΔΜ”Ής”ΟΘ§±Ί–κ±ΘΜΛΤδΚΆ¥ΪΒί‘ΊΧε≤Μ ή”ΑœλΓΘ”–“Μ–©ΖΫΖ®Ω…“‘ΧαΗΏΕύκΡάύ“©ΈοΒΡΩΎΖΰ…ζΈοάϊ”ΟΕ»Θ§»γ Ι”ΟΡΆΥαΆΩ≤ψΓΔ≥ΠΒάΟΗ“÷÷ΤΦΝΓΔ’≥“Κ¥©ΆΗκΡΚΆ…χΆΗ‘ω«ΩΦΝΒ»ΓΘLamson Β»―–ΨΩΖΔœ÷<100nmΒΡ“θάκΉ”Ρ…ΟΉΩ≈ΝΘΩ…“‘≥δΒ±ΈοάμΜ·―ß…χΆΗ‘ω«ΩΦΝΘ§¥ΌΫχΒΑΑΉ÷ ΒΡΩΎΖΰ δΥΆΓΘ–η“ΣΉΔ“βΒΡ «Θ§’βάοΟη ωΒΡΡ…ΟΉΩ≈ΝΘ≤Μ «Ά®ΙΐΉςΈΣ‘Υ δ‘ΊΧε“ΤΕ·¥©Ιΐ≥Π…œΤΛΘ§Εχ «Ά®ΙΐΫαΚœ≥Π±μΟφΒΡ ήΧεΫιΒΦΫτΟήΝ§Ϋ”ΒΡΩΣΖ≈Θ§Φ¥Ρ…ΟΉΩ≈ΝΘΆ®ΙΐΫαΚœ’ϊΚœΥΊΚΆΦΛΜνΦΓ«ρΒΑΑΉ«αΝ¥ΦΛΟΗΘ®myosin-light-chain kinaseΘ§MLCKΘ©‘ωΦ”≥ΠΒάΆ®ΆΗ–‘Θ§«“’β÷÷Ής”Ο «Ω…ΡφΒΡΘ§≤ΜΜαΒΦ÷¬≥ΠΉι÷·ΜΒΥάΜρ―Ή÷ΔΓΘ¥ΥΆβΘ§ Ι”ΟΥαΈ»Ε®ΆΩ≤ψΘ§ «Ά®Ιΐ‘Ύ±μΟφΆΩ…œpHΟτΗ–ΒΡ≥ΠΒάΨέΚœΈοά¥ Βœ÷ΒΡΘ§’β÷÷ΨέΚœΈο÷Μ”–‘Ύ¥οΒΫ≥ΠΒάΗϋ÷––‘ΒΡpH÷Β ±≤≈Μα»ήΫβΘ§ΒΦ÷¬ΆΩ≤ψΤΤΝ―ΚΆΑϋΙϋΈο ΆΖ≈ΓΘ
4–ΓΫα
”…”ΎBBBΒΡ¥φ‘ΎΘ§ΖΔœ÷ΚΆΩΣΖΔ–¬ΒΡ÷ΈΝΤΗς÷÷CNSΦ≤≤Γ”––ß“©Έο «Ζ«≥ΘΨΏ”–Χτ’Ϋ–‘ΒΡΓΘΡ‘Α–œρκΡ≈ΦΝΣ“©ΈοΉςΈΣ“Μ÷÷Ζ««÷»κ–‘“©Έο δΥΆœΒΆ≥Θ§Ω…“‘ΆΗΙΐBBBΘ§ΫΪ“©Έο¥χ»κΡ‘ Β÷ ΓΘ”κADCœύ±»Θ§ΒΆΖ÷Ή”÷ ΝΩΒΡΡ‘Α–œρκΡ≈ΦΝΣ“©ΈοΩ…Ρή”–ΗΏ…χΆΗ–‘Θ§ΗΏ–ßΒΡœΗΑϊ‘Υ δΘ§ΒΆΟβ“Ώ‘≠–‘Θ§“‘ΦΑΗϋ»ί“ΉΒΡΚœ≥…ΚΆ¥ΩΜ·ΓΘ’β ΙΒΟΥϋ≥…ΈΣΦΧADCΚσΘ§Α–œρΗχ“©Νλ”ρ”÷“Μ―–ΨΩ»»ΒψΓΘ”ΑœλΡ‘Α–œρκΡ≈ΦΝΣ“©Έο≥…ΈΣ÷ΈΝΤCNSΦ≤≤Γ”––ß“©ΈοΒΡ“ρΥΊ”–ΘΚΔΌ“©Έο‘ΥΥΆΒΫ¥σΡ‘ΒΡ–ß¬ ΘΜΔΎΡ‘ΡΎ“©ΈοΒΡΖ÷≤Φ«ιΩωΘΜΔέ”––ß“©ΈοΒΡ ΆΖ≈ΚΆΡ‘ΡΎΒΡ–νΜΐΝΩΘΜΔή”κ“©Έο ΆΖ≈ΚΆΧεΡΎΈ»Ε®–‘”–ΙΊΒΡΝ§Ϋ”ΜυΆ≈ΒΡ―Γ‘ώΘΜΔί ήΧε±ΞΚΆ–‘Β»ΓΘ“ρ¥ΥΘ§Ρ‘Α–œρκΡ≈ΦΝΣ“©ΈοΗς≤ΩΖ÷ΒΡ―Γ‘ώΚΆ…ηΦΤ”»ΈΣ÷Ί“ΣΓΘ
ΒΪ”…”ΎΕύκΡΒΡΧΊ–‘Θ§“≤ ΙΤδ”Π”Ο ήΒΫ“ΜΕ®ΒΡœό÷ΤΓΘΡΩ«ΑΘ§―–ΨΩ’Ώ“≤ΖΔΟςΝΥ–μΕύ–¬ΦΦ θΘ§”Οά¥ΩΥΖΰ’β–©»±ΒψΘ§»γΕ‘ΤδΫαΙΙ–ό ΈΓΔ”κ…ζΈο¥σΖ÷Ή”≈ΦΝΣΚΆΦΝ–Ά–ό ΈΒ»ΓΘΥφΉ≈œύΙΊΦΦ θΒΡΖΔ’ΙΘ§»γά¥Ή‘ …ΨζΧεΓΔΫΆΡΗ’Ι ΨΓΔ »…ώΨ≠≤ΓΕΨΚΆΗ…œΗΑϊΒΡκΡΩβΒΡ–¬–Ά…Η―ΓΤΫΧ®“‘ΦΑΜυ”ΎΧΊΕ®Α–ΒψΒΡΦΤΥψΜζΡΘΡβ…ηΦΤΘ§―–ΨΩ’ΏΫΪΩΣΖΔ≥ωΗϋΚΟΒΡBBB―Γ‘ώ–‘ΓΔΗϋΗΏΒΡΉΣ‘ΥΡήΝΠΓΔΗϋ«ΩΒΡ¥ζ–ΜΈ»Ε®–‘ΒΡΡ‘Α–œρκΡΓΘœύ–≈‘ΎΈ¥ά¥Ρ‘Α–œρκΡ≈ΦΝΣ“©Έο δΥΆœΒΆ≥Ω…“‘»ΓΒΟ Β÷ –‘Ϋχ’ΙΘ§‘ΎCNSΦ≤≤Γ÷ΈΝΤ÷–ΖΔΜ”ΤδΕάΧΊ”≈ ΤΓΘ
Οβ‘π…υΟςΘΚ±ΨΈΡΈΣ––“ΒΫΜΝς―ßœΑΘ§Αφ»®Ιι‘≠Ής’ΏΦΑ‘≠‘”÷ΨΥυ”–Θ§»γ”–«÷»®Θ§Ω…ΝΣœΒ…Ψ≥ΐΓΘΈΡ’¬±ξΉΔ”–Ής’ΏΦΑΈΡ’¬≥ω¥ΠΘ§»γ–η‘ΡΕΝ‘≠ΈΡΦΑ≤ΈΩΦΈΡœΉΘ§Ω…‘ΡΕΝ‘≠‘”÷ΨΓΘ





